制冷剂水合物由主体水分子和客体制冷剂分子在一定温度和压力条件下形成的非化学计量的笼形晶体化合物。制冷剂水合物作为蓄冷介质,具有比水更高的蓄冷密度和比冰更低的蓄冷能耗,在常压下HCFC–141b (CH3CCl2F)能够在8.4 ℃与水形成Ⅱ型水合物,相变潜热为344 kJ·kg-1,是空调系统非常有前途的相变蓄冷材料[1-2]。提高水合物生成速率和实际储冷量是水合物应用于蓄冷的关键。因此,研究者对如何促进水合物的生成进行了大量研究。相比之下,利用物理促进方法,比如搅拌[3]、喷雾[4]、鼓泡[5]和磁场[6]等方法均存在能耗大和运行费用高等缺点。利用四丁基溴化铵(TBAB) [7]、四氢呋喃(THF) [8]等热力学促进剂能降低水合物形成压力,促进水合物生成;利用相变材料[9-10]、纳米粒子[11-12]、多孔介质[13-14]和表面活性剂[15-22]等添加剂能不同程度上提高两相接触面积、强化传热和增加成核点,从而促进水合物快速生成。马鸿凯等[16-17]研究了十二烷基硫酸钠(SDS)、Tween80和司盘80(Span80)等表面活性剂对HCFC–141b水合物生成诱导时间的影响,发现表面活性剂提高了制冷剂相和水相接触面积,添加w = 2% Tween80诱导HCFC–141b水合物生成的效果最好。李璞等[21]利用表面活性剂吐温20和大豆卵磷脂复配制得的HCFC–141b微乳液,提高了HCFC–141b与水的互溶度和相界面,促进水合物的大量生成。李娜等[12]在其基础上又加入铜和三氧化二铝纳米粒子,强化了流体的传热性能,促进水合物快速大量生成。梁坤峰等[19]利用X射线衍射(XRD)分析了HCFC–141b水合物晶体构型为Ⅱ型,并且认为HCFC–141b的加入量能影响受分子扩散与晶体成核及生成相互制约的结晶微环境。可见,提高两相接触面积可以促进HCFC–141b水合物的生成,表面活性剂的加入可以不同程度上使制冷剂相和水相混合均匀。目前,各种表面活性剂促进气体(甲烷和二氧化碳等)水合物生成的机理多有报道,但是促进HCFC–141b水合物生成机理的研究较少,因此,研究表面活性剂对水合物生成促进效果以及探究水合物生成机理尤为重要。
本文选取不同类型表面活性剂AEO–9、AES和Tween80,研究其类型和浓度对HCFC–141b水合物的生成诱导时间、生成速率和蓄冷量的影响,探究促进HCFC–141b水合物快速生成的有效途径,为制冷剂水合物作为蓄冷介质的工业化应用提供参考。
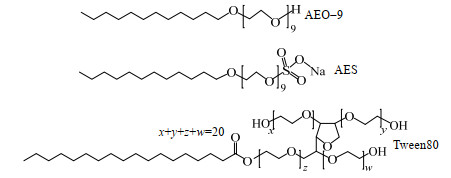
2 实验部分 2.1 实验材料HCFC–141b (≥ 99.5%)由浙江中龙制冷剂有限公司生产;Tween80为分析纯,由无锡市晶科化工有限公司生产;AEO–9 (≥ 99%)和AES (≥ 70%)均由青岛优索化学科技有限公司生产;4N高纯无氧铜丝(≥99.9%)直径0.3 mm,长度30 cm,绕成螺旋丝状;蒸馏水实验室自制。实验所用3种表面活性剂分子结构见图 1。
|
图 1 实验所用表面活性剂分子结构 Fig.1 Molecular structures of surfactants used in this work |
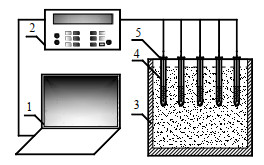
实验系统包括水合物形成装置和分解装置两部分。水合物形成装置主要由低温恒温槽、数据采集系统、计算机、水合物形成容器等构成(图 2)。水合物分解装置主要由自制的保温箱和真空保温瓶等构成。低温恒温槽(THD–2015)控制精度为±0.1 ℃,控温范围–20~99 ℃,温度波动值为±0.05 ℃;温度由T型热电偶测量,测量精度±0.1 ℃,温度保存到Agilent–34970A数据采集器系统中;水合物形成容器为长200 mm、直径20 mm的玻璃试管。
|
图 2 水合物形成实验装置 Fig.2 Schematic diagram of experimental setup for hydrate formation 1. computer 2. data collector 3. low temperature bath 4. glass test tube 5. silicone plug |
首先进行HCFC–141b乳液的配制。用电子天平(BSA224S,精度为±0.1 mg)称取一定量的水和表面活性剂分别加入到量杯中,用高速搅拌器(XFJ300–S)以10 000 r·min-1的转速搅拌5 min;再称取一定量的HCFC–141b (HCFC–141b与水为理想质量比1:2.62)缓慢地滴加到表面活性剂和水的混合液中,继续搅拌10 min,形成乳液,然后将制备好的乳液倒进试管中,密封待用。
预先将低温恒温槽的温度恒定到12 ℃,将装有乳液的试管插入热电偶后放入恒温水槽中,开启数据采集器,设置水槽温度到实验温度,形成水合物。本文水合物诱导时间测定是从温度降至HCFC–141b水合物相平衡温度(8.4 ℃)到体系内温度开始出现上升的时间段,由于HCFC–141b水合物生成存在随机性和不确定性,所以每个体系均进行多次重复实验。实验体系见表 1。
|
|
表 1 实验体系 Table 1 Experimental parameters |
水合物形成后,实验温度再稳定2 h,然后将装有水合物的试管快速放入自制保温箱的保温瓶中,温水与水合物进行换热直至水合物分解实验完成。实验过程中每20 s记录一次数据。
2.4 理论分析利用混合量热法[23]测量水合物的蓄冷量。根据能量守恒定律,温水的放热量等于水合物的蓄冷量与玻璃试管、轻质硅胶塞、热电偶吸收的热量和混合过程中损失的热量之和,计算式为:
| $ Q_{\mathrm{H}}=Q_{\mathrm{S}}+Q_{\mathrm{G}}+Q_{\mathrm{p}}+Q_{\mathrm{C}}+Q_{\mathrm{L}} $ | (1) |
式中,QH为温水的放热量,kJ。QS为水合物的蓄冷量,kJ。QG、QP和QC分别为玻璃试管、轻质硅胶塞和热电偶吸收的热量,kJ。QL为混合过程中损失的热量,kJ。由于实验所用保温瓶和外置保温箱的保温性能良好,实验过程中损失热量很小,所以忽略QL。轻质硅胶塞和热电偶吸收的热量也很小,QP和QC同样可以忽略。
温水放热量的计算式为:
| $ Q_{\mathrm{H}}=c_{\mathrm{w} 2} m_{\mathrm{w} 2}\left(T_{\mathrm{f}}-T_{\mathrm{a}}\right) $ | (2) |
式中,cw2是温水的比热容,kJ·kg-1·K-1。mw2是温水的质量,kg。Tf和Ta分别是初始温水和平衡后水合物的温度,℃。
玻璃试管吸收的热量为:
| $ Q_{\mathrm{G}}=c_{\mathrm{g}} m_{\mathrm{g}}\left(T_{\mathrm{a}}-T_{\mathrm{b}}\right) $ | (3) |
式中,cg是玻璃试管的比热容,kJ·kg-1·K-1。mg分别是玻璃试管的质量,kg。Tb是初始水合物的温度,℃。
假定体系中HCFC–141b全部生成水合物,且水合物在混合加热过程全部分解。水合物蓄冷量QS包括分解前水合物的温差显热、水合物的相变潜热、分解后水和HCFC–141b的温差显热和表面活性剂的温差显热,计算公式为:
| $ Q_{\mathrm{S}}=c_{\mathrm{h}} m_{\mathrm{h}}\left(T_{\mathrm{h}}-T_{\mathrm{b}}\right)+m_{\mathrm{h}} \Delta H_{\mathrm{h}}+\left(c_{\mathrm{w} 1} m_{\mathrm{w} 1}+c_{\mathrm{r}} m_{\mathrm{r}}\right)\left(T_{\mathrm{a}}-T_{\mathrm{h}}\right)+c_{\mathrm{A}} m_{\mathrm{A}}\left(T_{\mathrm{a}}-T_{\mathrm{b}}\right) $ | (4) |
式中,ch、cw1、cr和cA分别为水合物、水合物分解产生的水、HCFC–141b和表面活性剂的比热容,kJ·kg-1·K-1。Th为水合物的分解温度,℃。mh、mw1、mf和mA分别为水合物、水合物分解产生的水、HCFC–141b和表面活性剂的质量,kg。ΔHh为单位质量水合物的蓄冷量,kJ·kg-1。由于AEO–9所占含量很小,所以其温差显热也忽略。
根据式(1)~(4),可以计算出单位质量水合物的蓄冷量ΔHh为:
| $ \Delta H_{\mathrm{h}}=\frac{c_{\mathrm{w} 2} m_{\mathrm{w} 2}\left(T_{\mathrm{a}}-T_{\mathrm{f}}\right)-c_{\mathrm{h}} m_{\mathrm{h}}\left(T_{\mathrm{h}}-T_{\mathrm{b}}\right)-\left(c_{\mathrm{w} 1} m_{\mathrm{w} 1}+c_{\mathrm{r}} m_{\mathrm{r}}\right)\left(T_{\mathrm{a}}-T_{\mathrm{h}}\right)-c_{\mathrm{g}} m_{\mathrm{g}}\left(T_{\mathrm{a}}-T_{\mathrm{b}}\right)}{m_{\mathrm{h}}} $ | (5) |
水合物的平均生成速率vh定义为1 kg水合物生成过程中平均每分钟放出的热量,计算式为:
| $ v_{\mathrm{h}}=\frac{\Delta H_{\mathrm{h}}}{\Delta t} $ | (6) |
式中,Δt为水合物从生成开始到结束的时间,min。vh为水合物平均生成速率,kJ·kg-1·min-1。
3 结果与讨论 3.1 表面活性剂对水合物形成诱导时间的影响 3.1.1 AEO–9/AES浓度对水合物形成诱导时间的影响诱导时间定义为温度降至水合物相平衡温度到成核放热开始的时间[24]。水合物形成持续时间定义为体系成核放热到体系温度和实验温度相同的时间。平均诱导时间为几组平行实验下水合物形成诱导时间的平均值,诱导时间的标准方差用来衡量水合物形成稳定性的参考值,标准方差值越小,说明水合物成核随机性越小。表 2列出了各体系水合物形成诱导时间和形成持续时间。
|
|
表 2 水合物生成诱导时间和持续时间 Table 2 Induction time and duration of hydrate formation |
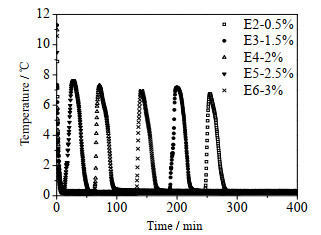
实验E1~E6研究了添加w = 0%~3%的AEO–9对水合物形成诱导时间的影响(图 3)。在静态条件下,纯制冷剂水合物很难形成,在实验过程中HCFC–141b没有形成水合物,纯水中表面活性剂的添加促进了水合物形成。随着AEO–9浓度的增大水合物生成的诱导时间表现出先减少后增大的特征,添加2.5%的AEO–9时水合物生成的诱导时间最短,平均诱导时间为63 min,诱导时间标准方差也最小,此时水合物形成的随机性小。低浓度的AEO–9没有达到胶束浓度,不能完全将HCFC–141b溶于水中,此时水合物成核机会少,诱导时间长;而高浓度的AEO–9会使得乳液易于分层,造成破乳,不利于水合物生成。
|
图 3 AEO–9促进水合物生成 Fig.3 Hydrate formation promoted by AEO–9 |
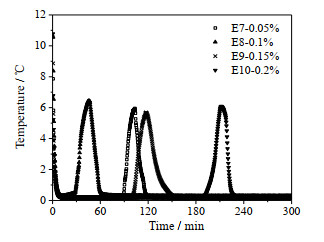
实验E1和E7~E10研究了AES浓度对水合物生成的影响(图 4)。实验过程发现单独添加AES时水合体系稳定性较差,易于分层,水合物的生成率较低。阴离子型表面活性剂促进水合物形成的机理主要是吸附,所以在研究AES促进水合物生成的体系中加入螺旋的4N高纯无氧铜丝,增加AES在铜丝表面的吸附能力,提高水合物生成率。实验研究了添加w = 0.05%~0.2%的AES对水合物形成诱导时间的影响,结果表明AES的添加量也存在一个最佳浓度,0.1%的AES水合物平均生成诱导时间最短为67 min,诱导时间标准方差35.26,这时水合体系的随机性较低。低浓度的AES乳化能力比不上AEO–9,乳液易分层,且其在铜丝表面吸附能力也不够,水合物成核机会较少;高浓度的AES乳液不够稳定,易于沉降,不利水合物生成。
|
图 4 AES促进水合物生成 Fig.4 Hydrate formation promoted by AES |
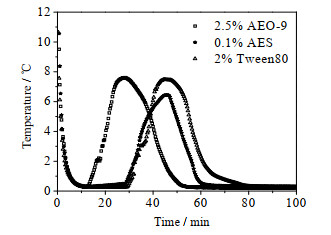
实验E5、E8和E11研究了不同表面活性剂在最佳添加量条件下对水合物生成的影响(图 5)。w = 2%的Tween80为课题组前期研究得到的最优浓度[17]。可见添加2.5% AEO–9对HCFC–141b水合物生成诱导时间的促进效果最好,并且从图中可以明显看出Tween80和AEO–9体系中温升曲线所包括的面积比AES体系要大,也就是说Tween80和AEO–9体系的HCFC–141b水合物蓄冷量更大。
|
图 5 不同表面活性剂促进水合物生成 Fig.5 Hydrate formation promoted by different surfactants |
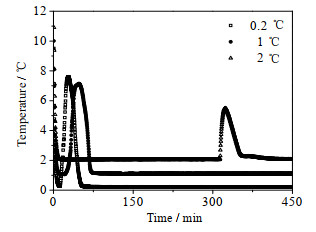
HCFC–141b水合物的过冷度为实验温度与HCFC–141b水合物相平衡温度的差值。实验E5、E12和E13研究了过冷度对水合物生成的影响(图 6)。过冷度对HCFC–141b水合物生成的影响很大,过冷度越大,对水合物生成的促进效果越好。表 2中E5的诱导时间标准方差最小,说明过冷度越大,水合物生成的随机性越小。水合物生成过程中,温度是很重要的参数,原因是温度越低,体系中分子运动越弱,水分子形成的水簇稳定,从而促进水合物晶核的形成和生长。
|
图 6 过冷度对水合物生成的影响 Fig.6 Effects of subcooling on hydrate formation |
首先对水合物蓄冷量测量装置的可靠性进行了验证实验,通过对比冰的相变潜热实验值与理论值的差确定。CRC化学物理手册中冰的融化热值为333.55 kJ·kg-1 [25],表 3所得的冰相变潜热值与其误差在5%以内,装置可靠性较好。但是测量值均小于理论值,出现这样的原因有两点:1.保温装置保温性能虽然很好,其仍会从环境中吸收部分热量,使得最后平衡温度偏高;2.在将试管置入保温装置的过程中,试管吸收了部分环境热量,导致最后平衡温度偏高,造成实验计算的相变潜热值也相应偏小。
|
|
表 3 冰相变潜热计算参数与结果 Table 3 Calculation parameters and results of ice phase change latent heats |
表 4列出了添加不同浓度的AEO–9后HCFC–141b水合物蓄冷量的测量结果。随着AEO–9浓度提高,HCFC–141b水合物蓄冷量先增大后减小,原因是更高浓度的表面活性剂易导致乳液破乳沉降,水合物生成而产生的水合物膜阻碍水分子和HCFC–141b分子接触,不利于水合物蓄冷量提高。添加2.5%的AEO–9体系中水合物的平均蓄冷量最大,平均蓄冷量约为167.74 kJ·kg-1,此值相当于将1 kg纯水升高40 ℃所需的热量,可见添加AEO–9后对水合物的蓄冷量效果显著。
|
|
表 4 各AEO-9浓度下水合物蓄冷量 Table 4 Hydrate storage capacities of samples prepared at different AEO–9 concentrations |
表 5列出了添加不同最佳浓度表面活性剂后HCFC–141b水合物蓄冷量的测量结果。可见,添加2% Tween80的体系,水合物的平均蓄冷量最大,平均蓄冷量约为202.73 kJ·kg-1,虽然AEO–9更有利于水合物成核,但Tween80更有利于提高HCFC–141b水合物蓄冷量。由于非离子表面活性剂Tween80和AEO–9在水中不电离,能将HCFC–141b很好地乳化在水中,乳液保持稳定而不易分层,因此水合物生长得很密实。而对于阴离子表面活性剂AES,在水中电离为正价的钠离子和带阴离子的疏水基团,乳液不稳定,易分层,造成添加非离子表面活性剂的体系比添加阴离子表面活性剂的体系蓄冷量高
|
|
表 5 表面活性剂对水合物蓄冷量的影响 Table 5 Effects of surfactants on hydrate storage capacity |
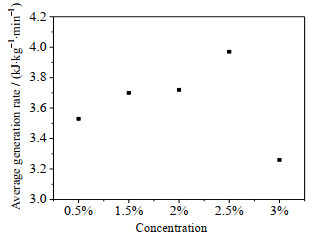
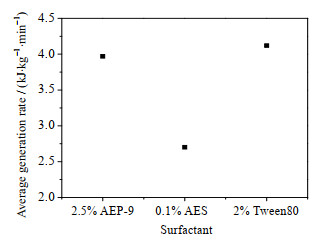
根据式(6)计算得到了添加不同浓度AEO–9下HCFC–141b水合物的生成速率(图 7),可见添加2.5% AEO–9的水合物平均生成速率最高为3.97 kJ·kg-1·min-1。图 8为添加不同最佳浓度表面活性剂下水合物生成速率,添加2% Tween80的水合物平均生成速率最高为4.12 kJ·kg-1min-1,添加0.1% AES的水合物平均生成速率最低为2.70 kJ·kg-1·min-1。
|
图 7 添加不同AEO–9浓度下水合物生成速率 Fig.7 Hydrate formation rates at different AEO–9 concentrations |
|
图 8 添加最佳浓度表面活性剂下水合物生成速率 Fig.8 Hydrate formation rates at different optimum concentrations of surfactants |
图 9为不同表面活性剂最佳浓度作用下的水合物生成图像,从图中可见,分别添加2% Tween80和2.5% AEO–9的试管(a)和(c),水合物呈现乳白色,均匀且密实;添加0.1% AES的试管(b),明显可见靠近铜丝周围呈现亮白色状水合物,而远离铜丝呈现浅白色状水合物,生成水合物多小孔,造成这样的原因是AES在水合物中的不均匀分布,靠近铜丝附近的AES发生吸附造成生成水合物比较密实呈现更亮白的颜色。

|
图 9 添加最佳浓度表面活性剂体系水合物生成图像 Fig.9 Hydrate formation profiles under the optimum surfactant concentrations |
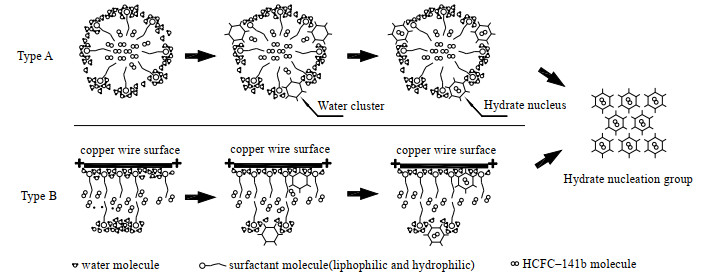
图 10形象地描述了不同表面活性剂促进HCFC–141b水合物生成的机理。对于非离子表面活性剂Tween80和AEO–9,其作用机理主要为胶束理论[26-28],即图 10中的Type A。首先表面活性剂溶解在水中,在达到胶束浓度时,表面活性剂的疏水基指向乳液的内部,亲水基指向外侧的水,HCFC–141b分子为非极性分子溶于胶束的内部。在低温条件下,处于表面活性剂亲水基侧的水首先会形成水簇,水簇为水合物晶核形成做前期准备,由于HCFC–141b分子在胶束内外的浓度差,在微弱的范德华力作用下进入水簇空腔形成水合物晶核,晶核再以其结构为模板在空间上生长扩张。对于离子型表面活性剂AES,其作用机理主要为吸附理论[18, 29-30],即图 10中的Type B。首先AES在水中溶解方式是电离成带正价的钠和带负价的疏水基团,铜丝表面带正电荷,带阴离子的疏水基团会在铜丝表面发生吸附,疏水基团的亲水基指向铜丝表面,疏水基指向乳液内部,此时金属表面疏水。随着吸附量增加,会形成如图所示的双层吸附,水簇首先在水分子聚集处形成,水合物晶核随之会形成,因为表面活性剂的吸附作用,晶核能够在铜丝表面营造出多孔介质环境,在毛细效应作用下,同样最终会有大量的水合物晶核形成,得到具有宏观规模的水合物晶体。
|
图 10 表面活性剂促进HCFC–141b水合物生成机理 Fig.10 Mechanism of HCFC–141b hydrate formation promoted by surfactants |
在静态条件下,研究了3种表面活性剂AEO–9、Tween80和AES促进HCFC–141b水合物生成过程,最有利于缩短水合物形成诱导时间的浓度分别为w = 2.5%、2%和0.1%。AES促进水合物形成效果最差,AEO-9有利于水合物成核,而Tween80更有利于提高水合物生长速度和蓄冷量。随着AEO–9浓度增加,水合物蓄冷量先增大后减小,最大蓄冷量为167.74 kJ·kg-1。添加2.5% AEO–9、0.1% AES和2% Tween80对应HCFC–141b水合物的蓄冷量分别为167.74、122.47和202.73 kJ·kg-1,水合物平均生长速率分别为3.97、2.70和4.12 kJ·kg-1·min-1,Tween80表现出较好的水合物生长促进效果,更有利于HCFC–141b水合物蓄冷应用。结合宏观实验观察,对不同表面活性剂促进HCFC–141b水合物生成的机理分析,非离子表面活性剂AEO–9和Tween80促进水合物生成的机理为胶束浓度理论,而阴离子表面活性剂AES则是吸附作用。
| [1] |
AKIYA T, SHIMAZAKI T, OOWA M, et al. Formation conditions of clathrates between HFC alternative refrigerants and water[J]. International Journal of Thermophysics, 1999, 20(6): 1753-1763. DOI:10.1023/A:1022614114505 |
| [2] |
张奕, 舒碧芬. R141b和R142b水合结晶动力学特性实验研究[J]. 兰州理工大学学报, 2003, 29(1): 57-60. ZHANG Y, SHU B F. Experimental study of kinetic characteristics of phase change of R141b and R142b hydrates[J]. Journal of Lanzhou University of Technology, 2003, 29(1): 57-60. DOI:10.3969/j.issn.1673-5196.2003.01.016 |
| [3] |
刘妮, 李菊, 陈伟军, 等. 机械强化制备二氧化碳水合物的特性研究[J]. 中国电机工程学报, 2011, 31(2): 51-54. LIU N, LI J, CHEN W J, et al. Performance investigations on CO2 hydrate production with stirring[J]. Proceedings of the CSEE, 2011, 31(2): 51-54. |
| [4] |
LI G, LIU D P, XIE Y M, et al. Study on effect factors for CO2 hydrate rapid formation in a water-spraying apparatus[J]. Energy & Fuels, 2010, 24(8): 4590-4597. |
| [5] |
吕秋楠, 宋永臣, 李小森. 鼓泡器中环戊烷-甲烷-盐水体系水合物的生成动力学[J]. 化工进展, 2016, 35(12): 3777-3782. LV Q N, SONG Y C, LI X S. Formation kinetics of cyclopentane-methane hydrate in NaCl solution with a bubbling equipment[J]. Chemical Industry and Engineering Progress, 2016, 35(12): 3777-3782. |
| [6] |
刘勇, 郭开华, 梁德青, 等. 在磁场作用下HCFC-141b制冷剂气体水合物的生成过程[J]. 中国科学(B辑化学), 2003, 33(1): 89-96. LIU Y, GUO K H, LIANG D Q, et al. Formation process of HCFC-141b refrigerant gas hydrate under magnetic field[J]. Chinese Science (B Science Chemistry), 2003, 33(1): 89-96. |
| [7] |
臧小亚, 梁德青, 吴能友. 不同浓度TBAB半笼型水合物法分离沼气中CO2过程的研究[J]. 高校化学工程学报, 2016, 30(6): 1241-1248. ZANG X Y, LIANG D Q, WU N Y. CO2 removal from simulated biogas using semi-clathrate hydrates of different concentration tetra-n-butyl ammonium bromide aqueous solutions[J]. Journal of Chemical Engineering of Chinese Universities, 2016, 30(6): 1241-1248. DOI:10.3969/j.issn.1003-9015.2016.06.002 |
| [8] |
陈广印, 孙强, 郭绪强, 等. 水合物法连续分离煤层气实验研究[J]. 高校化学工程学报, 2013, 27(4): 561-566. CHEN G Y, SUN Q, GUO X Q, et al. Experimental study on the continuous separation process of coal bed methane via forming hydrate[J]. Journal of Chemical Engineering of Chinese Universities, 2013, 27(4): 561-566. DOI:10.3969/j.issn.1003-9015.2013.04.003 |
| [9] |
朱明贵, 孙志高, 杨明明, 等. 有机相变材料促进HCFC-141b水合物生成实验[J]. 化工进展, 2017, 36(4): 1265-1269. ZHU M G, SUN Z G, YANG M M, et al. Experimental study on promoting HCFC-141b hydrate formation with organic phase change materials[J]. Chemical Industry and Engineering Progress, 2017, 36(4): 1265-1269. |
| [10] |
SONG X F, XIN F, YAN H C, et al. Intensification and kinetics of methane hydrate formation under heat removal by phase change of n-tetradecane[J]. AIChE Journal, 2015, 61(10): 3441-3450. DOI:10.1002/aic.14867 |
| [11] |
RAHMATI A M, MANTEGHIAN M, PAHLAVANZADEH H. Experimental and theoretical investigation of methane hydrate induction time in the presence of triangular silver nanoparticles[J]. Chemical Engineering Research & Design, 2017, 120: 325-332. |
| [12] |
李娜, 马振魁. 利用纳米粒子强化微乳液体系HCFC141b水合物的生成[J]. 科学通报, 2011, 56(22): 1846-1853. LI N, MA Z K. Nano-particle enhanced formation of HCFC141b gas hydrate in a microemulsion system[J]. Chinese Science Bulletin, 2011, 56(22): 1846-1853. |
| [13] |
王春龙, 翟盼盼, 冯荣, 等. 多孔介质水合物中储存二氧化碳的实验研究[J]. 工程热物理学报, 2012, 33(4): 616-618. WANG C L, ZHAI P P, FENG R, et al. Experimental study on carbon dioxide storage in porous media hydrates[J]. Journal of Engineering Thermophysics, 2012, 33(4): 616-618. |
| [14] |
ZHAO Y S, ZHAO J Z, WEI G L, et al. Semi-clathrate hydrate process of methane in porous media-microporous materials of 5A-type zeolites[J]. Fuel, 2018, 220: 185-191. DOI:10.1016/j.fuel.2018.01.067 |
| [15] |
李清平, 陈光进, 罗虎, 等. 十二烷基硫酸钠(SDS)对甲烷水合物膜生长动力学的影响[J]. 高校化学工程学报, 2008, 22(2): 210-215. LI Q P, CHEN G J, LUO H, et al. Influence of sodium dodecyl sulfate (SDS) on film growth kinetics of methane hydrate[J]. Journal of Chemical Engineering of Chinese Universities, 2008, 22(2): 210-215. DOI:10.3321/j.issn:1003-9015.2008.02.006 |
| [16] |
马鸿凯, 孙志高, 焦丽君, 等. 添加剂对静态条件下HCFC-141b水合物生成的促进作用[J]. 制冷学报, 2016, 37(1): 101-105. MA H K, SUN Z G, JIAO L J, et al. Promoting effects of additives on HCFC-141b hydrate formation in quiescent systems[J]. Journal of Refrigeration, 2016, 37(1): 101-105. DOI:10.3969/j.issn.0253-4339.2016.01.101 |
| [17] |
马鸿凯, 孙志高, 蔡伟, 等. HCFC-141b水合物静态生成促进技术的试验研究[J]. 流体机械, 2016, 44(1): 66-70. MA H K, SUN Z G, CAI W, et al. Experimental study on promot technology of HCFC-141b hydration formation in quiescent system[J]. Journal of Fluid Mechanics, 2016, 44(1): 66-70. DOI:10.3969/j.issn.1005-0329.2016.01.014 |
| [18] |
李文昭, 潘振, 马贵阳, 等. 表面活性剂吸附对促进甲烷水合物生成效果的影响[J]. 化工学报, 2017, 68(4): 1542-1549. LI W H, PAN Z, MA G Y, et al. Promotion effects of surfactant adsorption on formation of methane hydrates[J]. CIESC Journal, 2017, 68(4): 1542-1549. |
| [19] |
梁坤峰, 袁争印, 王林, 等. R141b气体水合物的晶体结构与结晶特性分析[J]. 高校化学工程学报, 2017, 31(6): 1293-1300. LIANG K F, YUAN Z Y, WANG L, et al. Analysis of crystal structure and crystallization characteristics of R141b gas hydrate[J]. Journal of Chemical Engineering of Chinese Universities, 2017, 31(6): 1293-1300. |
| [20] |
JIANG L L, LI A R, XU J F, et al. Effects of SDS and SDBS on CO2 hydrate formation, induction time, storage capacity and stability at 274.15 K and 5.0 MPa[J]. Chemistry Select, 2016, 1(19): 6111-6114. |
| [21] |
李璞, 张龙明, 覃小焕, 等. 微乳液中R141b水合物快速生成实验研究[J]. 工程热物理学报, 2014, 35(12): 2358-2362. LI P, ZHANG L M, QIN X H, et al. Experimental study on fast formation of R141b hydrate in microemulsion[J]. Journal of Engineering Thermophysics, 2014, 35(12): 2358-2362. |
| [22] |
MITARAI M, KISHIMOTO M, SUH D, et al. Surfactant effects on the crystal growth of clathrate hydrate at the interface of water and hydrophobic-guest liquid[J]. Crystal Growth & Design, 2015, 15(2): 812-821. |
| [23] |
张龙明, 李璞, 李娜, 等. 混合量热法测定水合物浆体蓄冷密度[J]. 制冷学报, 2014, 35(6): 47-52. ZHANG L M, LI P, LI N, et al. Determination of hydrate slurry's cold-storage density with mixing calorimetry method[J]. Journal of Refrigeration, 2014, 35(6): 47-52. DOI:10.3969/j.issn.0253-4339.2014.06.008 |
| [24] |
KACIEV D. Nucleation:Basic theory with applications[M]. Oxford: Butterworth Heinemann, 2000.
|
| [25] |
JOHN R. Handbook of chemistry and physics[M]. 99th ed. Boca Raton: CRC Press/Taylor & Francis FL, 2018.
|
| [26] |
ZHONG Y, ROGERS R E. Surfactant effects on gas hydrate formation[J]. Chemical Engineering Science, 2000, 55(19): 4175-4187. DOI:10.1016/S0009-2509(00)00072-5 |
| [27] |
李玉星, 朱超, 王武昌. 表面活性剂促进CO2水合物生成的实验及动力学模型[J]. 石油化工, 2012, 41(6): 699-703. LI Y X, ZHU C, WANG W C. Promoting effects of surfactants on carbon dioxide hydrate formation and the kinetics[J]. Petrochemicals, 2012, 41(6): 699-703. DOI:10.3969/j.issn.1000-8144.2012.06.015 |
| [28] |
KHURANA M, YIN Z Y, LINGA P. A review of clathrate hydrate nucleation[J]. ACS Sustainable Chemistry & Engineering, 2017, 5(12): 11176-11203. |
| [29] |
ZHANG R, SOMASUNDARAN P. Advances in adsorption of surfactants and their mixtures at solid/solution interfaces[J]. Advances in Colloid & Interface Science, 2006, 123/124/125/126: 213-229. |
| [30] |
BOTIMER J D, DUNNRANKIN D, TABOREK P. Evidence for immobile transitional state of water in methane clathrate hydrates grown from surfactant solutions[J]. Chemical Engineering Science, 2016, 142(3): 89-96. |




