近年来随着煤化工和石油化工产业产能的提升,其副产物C10重芳烃的产量也迅速增加。重芳烃中含量较多的四甲苯是一类十分重要的化工原料,具有均四甲苯、连四甲苯、偏四甲苯3种同分异构体。均四甲苯常见的生产方法是萃取精馏与冷冻结晶,而均四甲苯与连四甲苯、偏四甲苯之间的分离研究还较少[1]。且由于物理和化学性质非常接近,四甲苯同分异构体的分离较为困难,制约着C10重芳烃的高效利用。
金属-有机骨架材料(MOFs)是一类新兴的有机-无机杂化晶体材料,具有种类多、功能性强、孔隙率和比表面积大、孔道尺寸高度可调、稳定性强等优点[2-3]。国内外学者对MOFs材料在液相中的吸附分离,尤其是同分异构体的分离进行了较多的研究,比如杨玉茜[4]选用MIL-53(Cr)吸附分离二甲苯同分异构体,发现吸附剂对邻二甲苯的吸附远大于另2种同分异构体,具有良好的选择性,可用于二甲苯同分异构体的分离。基于四甲苯与二甲苯的结构与性质的类似性,本研究提出将MOFs材料用于四甲苯同分异构体的分离,重点研究了均四甲苯(DR)与连四甲苯(PR)在UIO-66-NH2上的吸附行为,包括吸附动力学与热力学研究,并获得了相关参数。
2 实验材料与方法 2.1 实验试剂正己烷、均四甲苯、连四甲苯和N,N-二甲基甲酰胺由阿达玛斯试剂有限公司提供;四氯化锆和2-氨基对苯二甲酸购于上海迈瑞尔化学技术有限公司;活性炭、21AE、40Q和三菱HP20由卓然环保科技有限公司提供。
2.2 实验仪器电热恒温鼓风干燥箱(中仪国科科技有限公司),真空干燥箱(中仪国科科技有限公司),气相色谱仪(浙江福立仪器有限公司),X-射线多晶衍射仪(德国布鲁克AXS有限公司),比表面积和孔径分布(美国麦克仪器公司)。
2.3 MOFs的合成 2.3.1 ZIF-8称取2-甲基咪唑,在搅拌下溶解于甲醇中。称取适量的六水合硝酸锌和无水甲酸钠并加入甲醇溶液中。在超声下完全溶解后,转移至内衬聚四氟乙烯的高压水热反应釜中。在一定温度下反应一段时间后,将反应釜冷却至室温后进行离心处理(10 000 r⋅min−1),所得固体在80 ℃下干燥6 h,而后在150 ℃下真空干燥3 h,得到ZIF-8样品。
2.3.2 UIO-66-NH2称取2-氨基对苯二甲酸与四氯化锆,在搅拌下按照物质的量比2:2:1:76配制2-氨基对苯二甲酸、盐酸、四氯化锆、N,N-二甲基甲酰胺的混合溶液。将其转移到内衬聚四氟乙烯的高压水热反应釜中,180 ℃下反应24 h后,将反应釜冷却至室温,经离心机离心(6 000 r⋅min−1)后用乙醇和N,N-二甲基甲酰胺各洗涤3次,在90 ℃下真空干燥得到UIO-66-NH2样品。
2.3.3 MIL-53(Cr)称取对苯二甲酸和九水合硝酸铬,在搅拌下溶解于去离子水中。称取适量的氢氟酸并加入溶液中,转移至内衬聚四氟乙烯的高压水热反应釜中。220 ℃下反应3 d后将反应釜冷却至室温,经离心(6 000 r⋅min−1)得到固体产物。依次用N,N-二甲基甲酰胺和乙醇各淋洗3次,干燥一段时间后在300 ℃的马弗炉中煅烧12 h,得到MIL-53(Cr)样品。
2.4 吸附量的计算采用气相色谱进行样品组成分析,色谱仪柱温升温程序为:初始温度为80 ℃,以5 ℃⋅min−1的速率升至120 ℃,恒温停留2 min,再以30 ℃⋅min−1的速率升至180 ℃。根据气相色谱分析计算吸附量,计算公式如式(1):
| $ {Q_t} = \frac{{({w_0} - w') \times {m_1} \times {1_{}}000}}{{{m_2}}} $ | (1) |
式中:Qt为吸附进行时间t后的吸附量,mg⋅g−1;w0为吸附前DR或PR在溶液中的质量分数;w′为吸附后DR或PR在溶液中的质量分数;m1为溶液的质量,g;m2为加入吸附剂的质量,g。
2.5 吸附动力学研究 2.5.1 实验研究在真空干燥箱中将合成的UIO-66-NH2在165 ℃下活化过夜。配制50 mL 0.1 mol⋅L−1(或0.3 mol⋅L−1)的DR(或PR)正己烷溶液,加入0.3 g吸附剂。将溶液放入恒温磁力搅拌槽中,在25 ℃下进行吸附。每隔一定时间用滴管吸取1 mL上层液体至离心管中离心后,用针管吸取适量上层清液,经微滤后用气相色谱分析四甲苯浓度。
2.5.2 数据关联分别采用准一级、准二级和颗粒内扩散模型对动力学实验数据进行拟合。
(a) 准一级动力学模型
该模型假设外部传质是吸附过程的速率控制步骤,从而简化了多孔颗粒内非稳态扩散的公式[5]。具体速率方程如式(2):
| $ \frac{\mathrm{d} Q}{\mathrm{~d} t}=k_1\left(Q_{\mathrm{e}}-Q\right)$ | (2) |
式中:Qe与Q分别为吸附平衡时的吸附量和取样时的吸附量,mg⋅g−1;t为时间,h;k1为准一级动力学模型参数,g⋅mg−1⋅h−1。对该方程积分可得线性方程式(3):
| $\ln \left(Q_{\mathrm{e}}-Q\right)=\ln Q_{\mathrm{e}}-k_1 t$ | (3) |
ln (Qe−Q)~t为线性关系,由斜率可得准一级动力学模型参数,由截距可得平衡吸附量[5-6]。
(b) 准二级动力学模型
该模型假设吸附剂的表面反应是吸附过程的速率控制步骤[7],具体速率方程如式(4):
| $\frac{\mathrm{d} Q}{\mathrm{~d} t}=k_2\left(Q_{\mathrm{e}}-Q\right)^2$ | (4) |
式中:k2为准二级动力学模型参数,g⋅mg−1⋅h−1。对该方程积分可得线性方程式(5):
| $ \frac{t}{Q}=\frac{t}{Q_{\mathrm{e}}}+\frac{1}{k_2 Q_{\mathrm{e}}^2} $ | (5) |
t⋅Q−1~t是线性关系,由斜率得到平衡吸附量,由截距得到准二级动力学方程系数[8]。
(c) 颗粒内扩散模型
该模型假设吸附质在颗粒内部的扩散为吸附过程的速率控制步骤[9],具体速率方程如式(6):
| $ Q=k_3 t^{0.5}+c $ | (6) |
式中:k3为颗粒内扩散模型参数,g⋅mg−1⋅h−1;c为涉及厚度与边界层的常数,mg⋅g−1。Q~t0.5为线性关系,由斜率可得颗粒内扩散系数[10]。
2.6 吸附热力学研究 2.6.1 实验研究将合成的UIO-66-NH2在真空干燥箱、165 ℃下活化过夜。依次配制5 mL 0.1、0.2、0.3、0.4、0.5 mol⋅L−1的DR(或PR)正己烷溶液,并加入0.5 g吸附剂。将溶液置于恒温磁力搅拌槽中,在25 ℃下吸附6 h。用滴管吸取1 mL上层液体至离心管中离心后,用针管吸取适量上层清液,经微滤后用气相色谱分析四甲苯浓度。改变温度(35和45 ℃),其他条件不变,重复上述实验。
2.6.2 数据关联分别采用Langmuir与Freundlich 2个模型对热力学实验数据进行拟合。
(a) Langmuir模型
该模型常用于描述单层吸附[11],其方程如式(7):
| $ Q_{\mathrm{e}}=\frac{Q_{\mathrm{m}} K_{\mathrm{L}} c_{\mathrm{e}}}{1+K_{\mathrm{L}} c_{\mathrm{e}}}$ | (7) |
式中:Qm为吸附剂达到饱和时的吸附量,mg⋅g−1;ce为达到吸附平衡时四甲苯的溶液浓度,mol⋅L−1;KL为Langmuir模型参数。对式(7)进行线性化处理可得式(8):
| $ \frac{c_{\mathrm{e}}}{Q_{\mathrm{e}}}=\frac{1}{K_{\mathrm{L}} Q_{\mathrm{m}}}+\frac{c_{\mathrm{e}}}{Q_{\mathrm{m}}} $ | (8) |
ce⋅Qe−1对ce呈线性关系,由斜率可得饱和吸附量,由截距可得Langmuir模型参数[12]。
(b) Freundlich模型
该模型用于描述多层吸附过程,其方程如式(9):
| $ Q_{\mathrm{e}}=K_{\mathrm{F}} c_{\mathrm{e}}^{n^{-1}}$ | (9) |
式中:KF为Freundlich模型参数;n−1为吸附指数,该指数较小时(小于1)吸附较为容易,较大时(大于2),吸附较为困难[13]。对式(9)两边取对数可得式(10):
| $ \lg \;\;Q_{\mathrm{e}}=\lg K_{\mathrm{F}}+\frac{1}{n} \lg c_{\mathrm{e}} $ | (10) |
lg Qe~lg ce为线性关系,斜率为吸附指数,截距为Freundlich模型参数的对数[14]。
2.6.3 参数计算(a) 吉布斯自由能
根据过程吉布斯自由能的变化能够判断吸附过程能否自发进行[15]。具体计算式如式(11):
| $ \Delta G^0=-R T \ln K_{\mathrm{c}}^0 $ | (11) |
式中:
(b) 焓变
焓变是一个过程前后焓的增加量,常用于判断吸附过程是吸热还是放热[17]。具体计算式如式(12):
| $ \ln c_{\mathrm{e}}=\ln k_0+\frac{\Delta H^0}{R T} $ | (12) |
式中:
(c) 熵变
熵反应了体系的混乱程度,熵变是一个过程前后熵的增加量[18],具体计算式如式(13):
| $ \ln K_{\mathrm{c}}^0=\frac{\Delta S^0}{R}-\frac{\Delta H^0}{R T} $ | (13) |
式中:
将合成的UIO-66-NH2在真空干燥箱、165 ℃下活化过夜。依次配制5 mL 0.03、0.05、0.1、0.2、0.3、0.4、0.5 mol⋅L−1的DR/PR混合溶液,并加入0.5 g吸附剂。将溶液放入恒温磁力搅拌槽中,在25 ℃下进行吸附,6 h后取出。用滴管吸取1 mL上层液体至离心管中离心后,用针管吸取适量上层清液,经微滤后用气相色谱分析四甲苯浓度。改变温度(35和45 ℃),其他条件不变,重复上述实验。
2.8 动态穿透实验用正己烷浸泡UIO-66-NH2过夜,采用湿法填料将吸附剂移入一根内径1.0 cm,长度15 cm,且上下装有0.015 mm筛网的层析柱中,以1 mL⋅min−1速率用正己烷冲洗柱子2 h,使吸附剂装填充实。以1 mL⋅min−1速率泵入0.05 mol⋅L−1 DR/PR混合溶液,从第1滴溶液流出开始,每间隔1 min取样1次,直至柱子被溶液中有效组分完全穿透,取样结束。采用气相色谱分析从穿透开始到穿透结束时所有样品的浓度变化。改变DR/PR混合溶液浓度(0.1 mol⋅L−1),其他条件不变,重复上述实验。
2.9 再生性能研究对吸附剂进行循环利用,首先将吸附过四甲苯的吸附剂用正己烷浸泡洗涤3次后离心,在70 ℃烘箱干燥,放入真空干燥箱中165 ℃真空干燥12 h,得到的UIO-66-NH2继续用于吸附实验。上述步骤重复进行3次,根据相邻2次吸附量的变化,评价吸附剂再生性能和稳定性。
3 结果与讨论 3.1 吸附剂的初筛筛选了UIO-66-NH2、MIL-53(Cr)、ZIF-83种MOFs材料以及三菱HP20、活性炭、40Q、21AE 4种多孔材料对DR-PR溶液(wDR =15%,wPR =85%)进行静态吸附实验,并计算吸附量,结果如表1所示。其中,UIO-66-NH2、MIL-53(Cr)、ZIF-8 3种MOFs材料通过溶剂热法制备获得,三菱HP20、活性炭、40Q、21AE 4种多孔材料为市售产品。
|
|
表 1 吸附剂对DR与PR的吸附量 Table 1 Adsorption capacities of different adsorbents for DR and PR |
由表1可见,不同吸附剂的吸附量有较大差异,这可能是因为7种吸附剂的比表面积,孔隙率和极性不同;3种MOFs材料中,UIO-66-NH2对DR与PR的吸附量差距最大,达到了53.24 mg⋅g−1,具有良好的选择性吸附性能,这可能是由于PR极性高于DR,UIO-66-NH2骨架与极性分子PR之间存在较强的相互作用,使得吸附剂对PR的吸附量明显高于对DR的吸附量。选定UIO-66-NH2为吸附剂,对其吸附四甲苯过程进一步研究。
3.2 UIO-66-NH2的表征分别采用扫描电子显微镜、X射线粉末衍射与BET吸附法对合成材料进行表征。
合成所得的UIO-66-NH2的XRD图谱在各波峰的位置、大小、强度等方面,与文献中的图谱基本符合[19],确定本研究合成的材料为UIO-66-NH2;由扫描电镜图谱,合成的UIO-66-NH2的颗粒呈不规则形状;由孔径分布表征结果,UIO-66-NH2孔尺寸主要分布在1.8~8.5 nm;由合成材料77.3 K下N2吸附脱附曲线,通过BET方程计算出材料比表面积为695.4 m2⋅g−1。
与萃取精馏和冷冻结晶相比,采用MOFs材料分离DR和PR具有成本低,流程简单,产品纯度和收率高等优点。研究选用UIO-66-NH2作为吸附剂,与其他MOFs材料和常见吸附剂相比,具有合成简单,比表面积大,吸附量大,选择性好等优点。
3.3 吸附动力学研究 3.3.1 吸附动力学曲线在25 ℃、不同初始浓度下,进行静态吸附实验,吸附动力学曲线如图1所示。
|
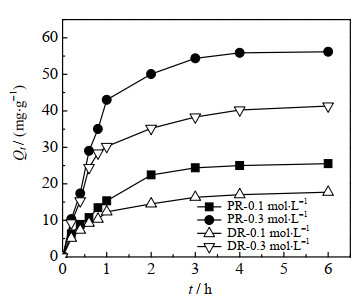
图 1 25 ℃下不同初始浓度DR和PR在UIO-66-NH2上的吸附动力学曲线 Fig.1 Adsorption kinetics of UIO-66-NH2 for DR and PR with different initial concentrations at 25 ℃ |
由图1可见,UIO-66-NH2对DR与PR的吸附量最初随时间延长迅速增加,3 h后吸附动力学曲线趋于平缓,6 h后吸附基本达到平衡;当初始浓度相同时,PR的吸附量大于DR,说明UIO-66-NH2具有较好的DR/PR选择性吸附性能;当初始浓度由0.1增至0.3 mol⋅L−1时,PR的平衡吸附量由25.53增至56.16 mg⋅g−1,DR的平衡吸附量也从17.74增至41.32 mg⋅g−1,说明UIO-66-NH2对DR和PR的吸附量随初始浓度的增大而增大。
3.3.2 动力学数据关联选用准一级、准二级和颗粒内扩散3个模型对动力学实验数据进行拟合。
(a) 准一级动力学模型
分别计算取样时和吸附平衡时的吸附量,以ln (Qe−Q)为纵坐标、t为横坐标作图,得到拟合数据与相关系数。由计算可得,采用准一级动力学方程拟合时,相关系数在0.68~0.96,ln (Qe−Q)与t的线性关系较弱,所以UIO-66-NH2对DR和PR的吸附动力学不适合用准一级动力学模型进行拟合。
(b) 准二级动力学模型
分别计算取样时和吸附平衡时的吸附量,以t⋅Q−1为纵坐标,t为横坐标作图。计算得到的拟合数据与相关系数如表2所示。
|
|
表 2 DR和PR在UIO-66-NH2上吸附的准二级动力学方程拟合参数 Table 2 Fitting parameters of pseudo second order kinetic equation for DR and PR adsorption on UIO-66-NH2 |
由表2可见,对动力学实验数据采用准二级动力学模型拟合的相关系数均大于0.98,t⋅Q−1与t呈线性关系,说明准二级动力学模型能较好地描述DR与PR在UIO-66-NH2上的吸附过程;初始浓度相同时,PR的准二级动力学方程系数小于DR,但PR的平衡吸附量大于DR,说明UIO-66-NH2对DR与PR具有较高的选择性吸附;当初始浓度上升时,DR与PR的准二级动力学方程系数均减小,平衡吸附量均增大。
(c) 颗粒内扩散模型
采用气相色谱仪分析样品,并计算取样时的吸附量,以Q对t0.5作图,得到拟合数据和相关系数。由计算可得,选用颗粒内扩散模型拟合动力学实验数据时,相关系数在0.80~0.92,Q~t0.5线性关系较弱,所以颗粒内扩散模型不适用于描述UIO-66-NH2对DR和PR的吸附过程。
3.4 吸附热力学 3.4.1 吸附等温线在25、35、45 ℃下进行静态吸附实验,研究DR与PR的平衡吸附量与初始浓度的关系,不同温度下UIO-66-NH2吸附DR和PR的平衡吸附量与初始浓度关系,如图2所示。
|
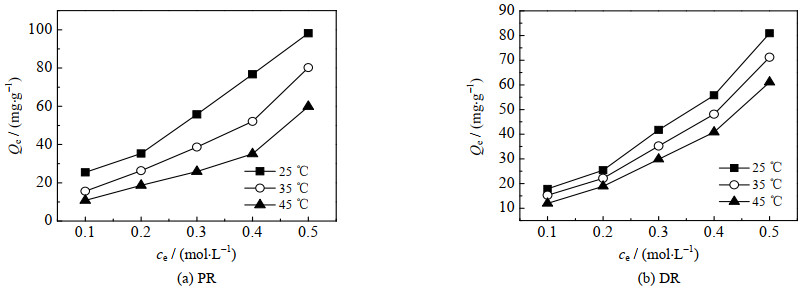
图 2 不同温度下UIO-66-NH2吸附等温线 Fig.2 Adsorption isotherms of PR and DR on UIO-66-NH2 at different temperatures |
由图2可见,当温度上升时,DR与PR的平衡吸附量减少,例如初始浓度为0.5 mol⋅L−1时,随着温度由25升至45 ℃,PR的平衡吸附量由98.16降至59.87 mg⋅g−1,DR的平衡吸附量由80.91降至61.07 mg⋅g−1。推测UIO-66-NH2吸附DR与PR的过程是放热过程,升高温度不利于吸附。而在相同的温度与初始浓度下,PR的平衡吸附量大于DR,再次说明了UIO-66-NH2对DR/PR优良的吸附选择性,将UIO-66-NH2应用于DR与PR的分离是可行的。
3.4.2 吸附等温线拟合分别采用Langmuir与Freundlich方程对热力学实验数据进行拟合。
(a) Langmuir方程
采用气相色谱仪分析样品并计算平衡吸附量Qe。作图得到拟合数据和相关系数。由计算可得,当采用Langmuir模型对实验数据进行拟合时相关系数均小于0.05,ce·Qe−1与ce之间线性关系较差,说明不适合采用Langmuir模型描述。
(b) Freundlich方程
通过实验数据计算得到平衡吸附量Qe,并以lg Qe为纵坐标,lg ce为横坐标作图,计算得到的拟合数据和相关系数见表3。
|
|
表 3 DR和PR在UIO-66-NH2上吸附的Freundlich等温线拟合参数 Table 3 Freundlich isotherm fitting parameters of DR and PR adsorption on UIO-66-NH2 |
由表3可见,采用Freundlich模型拟合的相关系数均大于0.9,lg Qe与lg ce呈线性关系,说明UIO-66-NH2吸附DR和PR的等温线可用Freundlich模型拟合。同时DR与PR的模型系数KF均大于90,吸附指数n−1均小于1,吸附较为容易。
3.4.3 热力学参数选用式(11)与式(13)计算吸附过程的吉布斯自由能、焓变和熵变。先采用Freundlich等温线模型拟合热力学实验数据,通过模型参数与吸附指数计算得到标准热力学平衡常数,进而得到吉布斯自由能。再以ln Kc0为纵坐标,以T−1为横坐标作图,通过斜率得到焓变,通过截距得到熵变,所得拟合数据和相关系数见表4。
|
|
表 4 DR和PR在UIO-66-NH2上吸附的热力学参数 Table 4 Thermodynamic parameters of DR and PR adsorption on UIO-66-NH2 |
由表4可见,DR与PR的吉布斯自由能、焓变和熵变均小于零。吉布斯自由能小于零,表明吸附过程能自发进行;PR与DR的焓变分别为−46.24与−16.61 kJ⋅mol−1,均小于零,表明DR与PR的吸附均为放热过程,温度降低有利于吸附过程进行,这与吸附量随温度的增大而减小是相符合的;UIO-66-NH2吸附PR与DR的熵变分别为−106.79和−11.85 J⋅mol−1⋅K−1,均小于零,表明吸附过程熵减少,即吸附质更有规律地整齐排列在吸附剂表面,混乱度减小。
3.5 竞争吸附选用式(1)计算竞争吸附实验中UIO-66-NH2对DR与PR的吸附量,计算各工况下的吸附分离系数,结果见表5,不同温度下UIO-66-NH2吸附DR与PR的平衡吸附量及选择性αPR,DR与初始浓度关系如图3所示。
|
|
表 5 DR和PR在UIO-66-NH2上的吸附分离系数 Table 5 Separation coefficients of DR and PR using UIO-66-NH2 as the adsorbent |
|
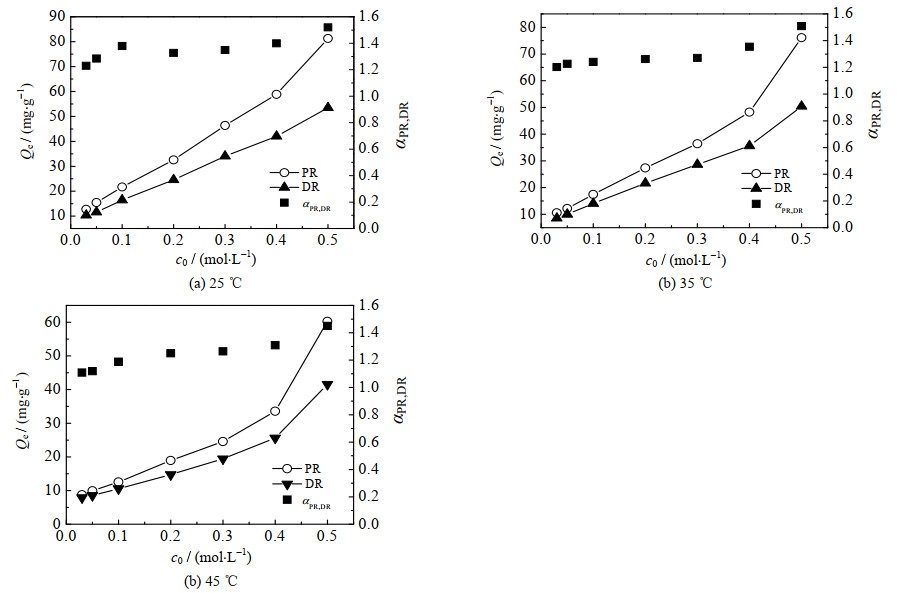
图 3 UIO-66-NH2对DR与PR的二组分竞争性吸附实验 Fig.3 Results of competitive adsorption of DR and PR on UIO-66-NH2 |
由表5可见,3个温度下DR与PR在UIO-66-NH2上的吸附分离系数均大于1.1,温度越高,分离系数越小,这与DR和PR的吸附过程放热相符合;在同一温度下,分离系数随初始浓度的增大而增大。
3.6 穿透曲线流出液中DR与PR浓度随时间变化的曲线如图4所示。
|
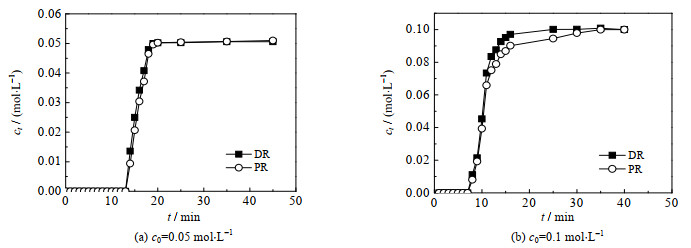
图 4 UIO-66-NH2吸附DR/PR的穿透曲线 Fig.4 Breakthrough curves of DR/PR on UIO-66-NH2 |
虽然DR和PR流出时间相似,但流出液中DR浓度大于PR,主要是因为UIO-66-NH2对PR有更强的吸附性;最后两组分均达到溶液的初始浓度。对比0.05、0.1 mol⋅L−1的DR/PR穿透曲线图,得出浓度升高,DR和PR的穿透时间都变短。
由以上研究,DR与PR在UIO-66-NH2上的吸附为放热过程,平衡吸附量随温度的增大而减小;初始浓度增大时,平衡吸附量与吸附分离系数都增大。所以低温、高初始浓度对吸附分离有利。
3.7 再生性能以连四甲苯的平衡吸附量为指标,研究4个周期内吸附剂的重复使用性能。在后3个吸附周期中,UIO-66-NH2对PR的平衡吸附量依次为第1周期的93.42%、87.31%、80.19%。相邻2个周期内,UIO-66-NH2的吸附量下降7% 左右,这可能是由于上一周期孔道结构内吸附的PR分子未被完全脱除。
4 结论针对四甲苯同分异构体的分离,研究了DR与PR在UIO-66-NH2上的吸附过程,主要结论如下:
(1) 吸附剂的制备与筛选。以DR与PR吸附量的差异为依据,分析3种MOFs材料和4种多孔材料的吸附,确定UIO-66-NH2为吸附剂。通过溶剂热法制备UIO-66-NH2,并采用扫描电子显微镜、X射线粉末衍射以及BET吸附法对材料进行表征,验证合成所得材料为UIO-66-NH2,且呈不规则形状,孔径集中在1.8~8.5 nm,比表面积为695.4 m2⋅g−1。
(2) DR和PR在UIO-66-NH2的吸附动力学研究。考察了不同浓度DR与PR在UIO-66-NH2上吸附量与吸附时间的关系,确定平衡时间为6 h,且平衡吸附量随初始浓度的增大而增大。分别采用准一级、准二级和颗粒内扩散3个动力学模型对实验数据进行拟合,其中准二级动力学模型的关联结果较优,相关系数大于0.98。
(3) DR和PR在UIO-66-NH2的吸附热力学研究。考察了温度对吸附量的影响,发现温度上升平衡吸附量降低。研究了UIO-66-NH2吸附DR与PR的等温线,分别选用Langmuir与Freundlich方程对实验数据进行拟合,其中Freundlich方程的关联结果较优,相关系数均大于0.9,同时DR与PR的模型参数KF均大于90,吸附指数n−1均小于1,吸附较为容易。在此基础上计算了吸附过程的热力学参数,DR的吉布斯自由能为−14.55 kJ⋅mol−1(298.15 K)、−13.02 kJ⋅mol−1(308.15 K)、−12.43 kJ⋅mol−1(318.15 K),焓变为−46.24 kJ⋅mol−1,熵变为−106.79 J⋅mol−1⋅K−1;PR的吉布斯自由能为−13.06 kJ⋅mol−1 (298.15 K)、−12.99 kJ⋅mol−1 (308.15 K)、−12.82 kJ⋅mol−1 (318.15 K),焓变为−16.61 kJ⋅mol−1,熵变为−11.85 J⋅mol−1⋅K−1。
(4) 竞争吸附、动态吸附及吸附剂的再生。3个温度下UIO-66-NH2吸附DR与PR的分离系数均大于1.1;动态吸附后的穿透曲线表明UIO-66-NH2有良好的选择性;经过4个吸附周期后UIO-66-NH2对PR的平衡吸附量可以达到初次吸附平衡吸附量的80.19%,说明该吸附剂的重复使用性能较好。
本研究结果可为C10重芳烃中四甲苯同分异构体的吸附分离提供依据。
| [1] |
李竞草, 吴冬霞, 常丽萍, 等. 疏水性金属-有机骨架材料的研究进展[J]. 化工进展, 2020, 39(1): 224-232. LI J C, WU D X, CHANG L P, et al. Research progress of hydrophobic metal-organic framework materials[J]. Chemical Industry and Engineering Progress, 2020, 39(1): 224-232. |
| [2] |
HARUN K, MERT P H, SAFIYYE K, et al. Improving CO2 separation performance of MIL-53(Al) by incorporating 1-n-butyl-3-methylimidazolium methyl sulfate[J]. Energy Technology, 2019, 7(7): 1-9. |
| [3] |
SUN Y X, JIA X M, HUANG H L, et al. Solvent-free mechanochemical route for the construction of ionic liquid and mixed-metal MOF composites for synergistic CO2 fixation[J]. Journal of Materials Chemistry, 2020, 8(6): 3180-3185. DOI:10.1039/C9TA10409G |
| [4] |
杨玉茜. 金属-有机骨架材料吸附分离二甲苯异构体的研究 [D]. 天津: 天津大学, 2018. YANG Y Q. Study on adsorptive separation of xylene isomers by metal-organic framework materials [D]. Tianjin: Tianjin University, 2018. |
| [5] |
LI J, WANG X X, ZHAO G X, et al. Metal-organic framework-based materials superior adsorbents for the capture of toxic and radioactive metal ions[J]. Chemical Society Reviews, 2018, 47(7): 2322-2356. DOI:10.1039/C7CS00543A |
| [6] |
LIU M S, WANG J, YANG Q F, et al. Patulin removal from apple juice using a novel cysteine-functionalized metal-organic framework adsorbent[J]. Food Chemistry, 2019, 270(1): 1-9. |
| [7] |
IOANNIS S, MOHAMED E, GUILLAUME M. Highly tunable sulfur hexafluoride separation by interpenetration control in metal organic frameworks[J]. Microporous & Mesoporous Materials, 2019, 281: 44-49. |
| [8] |
魏伟, 夏炎. 功能化金属有机骨架材料在放射性离子检测中的应用[J]. 大学化学, 2020, 35(12): 192-200. WEI W, XIA Y. Application of functionalized metal-organic frameworks in radioactive ions detection[J]. University Chemistry, 2020, 35(12): 192-200. |
| [9] |
刘璇, 崔颖娜, 尹静梅, 等. 金属有机骨架材料在吸附脱硫领域的应用[J]. 化工进展, 2020, 39(8): 3163-3176. LIU X, CUI Y N, YIN J M, et al. Application of metal-organic frameworks materials in adsorptive desulfurization[J]. Chemical Industry and Engineering Progress, 2020, 39(8): 3163-3176. |
| [10] |
杨磊, 吴宇静, 吴选军, 等. 面向C4烯烃混合物吸附分离的真实金属-有机骨架材料高通量筛选[J]. 化学学报, 2021, 79(4): 520-524. YANG L, WU Y J, WU X J, et al. High-throughput screening of real metal-organic frameworks for adsorption separation of C4 olefins[J]. Acta Chimica Sinica, 2021, 79(4): 520-524. |
| [11] |
KONNERTH H, MATSAGAR B M, MARTIN H G, et al. Metal-organic framework (MOF)-derived catalysts for fine chemical production[J]. Coordination Chemistry Reviews, 2020, 416(8): 926-937. |
| [12] |
AMARAJOTHI D, ABDULLAH M, HERMENEGILDO G. Metal-organic frameworks as multifunctional solid catalysts[J]. Trends in Chemistry, 2020, 2(5): 454-466. DOI:10.1016/j.trechm.2020.02.004 |
| [13] |
吴厚晓, 陈永伟, 梁俊杰, 等. CH4/C2H6/C3H8在MOF-505@5GO上吸附相平衡和选择性[J]. 化工学报, 2018, 69(4): 1500-1507. WU H X, CHEN Y W, LIANG J J, et al. Adsorption isotherms and selectivity of CH4/C2H6/C3H8 on MOF-505@5GO[J]. CIESC Journal, 2018, 69(4): 1500-1507. |
| [14] |
LIU C, QIAO J, ZHANG X, et al. Bimetallic MOF-derived porous CoNi/C nanocomposites with ultra-wide band microwave absorption properties[J]. New Journal of Chemistry, 2019, 43(42): 16546-16554. DOI:10.1039/C9NJ04115J |
| [15] |
TIAN H L, ZHANG M Z, JIN G X, et al. Cu-MOF chemodynamic nanoplatform via modulating glutathione and H2O2 in tumor microenvironment for amplified cancer therapy[J]. Journal of Colloid and Interface Science, 2021, 587: 358-366. DOI:10.1016/j.jcis.2020.12.028 |
| [16] |
BEHNAZ H, MAJID R, HAMED R B, et al. Ultra-sensitive molecularly imprinted electrochemical sensor for patulin detection based on a novel assembling strategy using Au@Cu-MOF/N-GQDs[J]. Sensors and Actuators B:Chemical, 2020, 318: 145-154. |
| [17] |
XU Y, XU J L, BAI C P, et al. A facile strategy for fabricating AgI-MIL-53(Fe) composites: superior interfacial contact and enhanced visible light photocatalytic performance[J]. New Journal of Chemistry, 2018, 42(5): 3799-3807. DOI:10.1039/C8NJ00417J |
| [18] |
MAO M, WU X X, HU Y, et al. Charge storage mechanism of MOF-derived Mn2O3 as high performance cathode of aqueous zinc-ion batteries[J]. Journal of Energy Chemistry, 2020, 52(1): 277-283. |
| [19] |
武卓敏, 石勇, 李春艳, 等. 双金属MOF-74-CoMn催化剂的制备及其CO选择性催化还原技术应用[J]. 化学学报, 2019, 77(8): 758-764. WU Z M, SHI Y, LI C Y, et al. Synthesis of bimetallic MOF-74-CoMn catalyst and its application in selective catalytic reduction of NO with CO[J]. Acta Chimica Sinica, 2019, 77(8): 758-764. |




