挥发性有机化合物(volatile organic compounds,VOCs)是指在常温下沸点在50~260 ℃的各种有机化合物[1],主要来源于建筑行业、石油冶炼、汽车尾气以及人类动植物的日常活动等[2-3]。高的挥发性有机物会引起人体过敏、恶心、头晕和头痛。因此,最大限度地减少挥发性有机物的排放是至关重要的。处理VOCs的方法包括吸收法[4]、吸附法[5-9]、冷凝法[10]、直接燃烧法[11]、催化燃烧法[12-14]、光催化法[15]和膜分离法[16]等。其中,吸附法操作简单,操作成本低廉,能耗要求低,并且能通过吸脱附重复使用。吸附法能否起到良好的效果通常与吸附剂的性能有关,常用的吸附剂有黏土[5]、分子筛[6]、碳材料[7]以及金属有机骨架材料(metal organic framework,MOF)[8]等。其中碳纳米管(carbon nanotubes,CNTs)作为碳材料的一种,自1991年日本的Iijima发现以来[17],一度成为各行业的热门。CNT具有良好的导电导热性能、较高的机械强度、较高的比表面积和吸附容量以及其易改性的性质使其具有作为一般吸附剂的特点。VOCs在CNT上的吸附机理主要是物理吸附,同时有轻微的化学反应在碳纳米管表面官能团与VOC分子之间发生[18-19]。CNT石墨层表面表现出良好的疏水性和一致性,这使其与有机化合物有强相互作用,有利于吸附进行[20]。但由于碳纳米管之间存在着范德华力,并具有很大的比表面积及长径比,导致碳纳米管很容易团聚。因此在将CNT应用于吸附的过程中,常常导致床层压降过大,不利于传质的进行[21]。常用的解决方法是将CNT负载在大孔材料上,如一些结构化载体和整体式载体,这能使得床层压降显著降低,并提高传质传热效率 [22]。膨胀珍珠岩作为一种大孔材料,热力学性质稳定且具有开放的孔隙度,非常适合作为生长碳纳米管的载体[23]。膨胀珍珠岩主要应用于建筑行业,在应用的过程中往往容易产生小粒径的膨胀珍珠岩颗粒。这些颗粒难于处理且对环境造成了很大的污染。以膨胀珍珠岩为载体,在其表面合成碳纳米管,既可以解决碳纳米管在吸附过程中压降过大的问题,也可以解决小粒径膨胀珍珠岩造成的环境污染问题。本研究以樟脑作为廉价碳源,通过化学气相沉积法(CVD)在膨胀珍珠岩表面生长碳纳米管以合成膨胀珍珠岩碳纳米管膜(carbon nanotubes/expanded perlite,CNTs/Perlite)梯度孔复合材料,旨在将CNT优异的吸附性能和膨胀珍珠岩高孔隙率、高稳定性等性质相结合,以研究合成CNTs/Perlite的最佳工艺条件和甲苯基于CNTs/Perlite复合材料与颗粒型CNT构成的结构化固定床上的吸附透过行为。
2 实验(材料与方法) 2.1 实验材料膨胀珍珠岩(粒径0.160~0.212 mm,工业级),河南信阳平桥中原珍珠岩有限公司;无水乙醇(分析纯),广州化学试剂厂;天然樟脑(化学纯),上海阿拉丁生化科技股份有限公司;二茂铁(化学纯),上海阿拉丁生化科技股份有限公司;高纯氮气(>99.999%),广州盛盈气体有限公司;高纯氢气(>99.999%),广州盛盈气体有限公司;干燥空气(21%O2+N2),广州盛盈气体有限公司;六水合硝酸钴(分析纯),天津科密欧化学有限公司;硝酸铁(分析纯),广州化学试剂厂;甲苯(分析纯),广州化学试剂厂。百分数为体积分数。
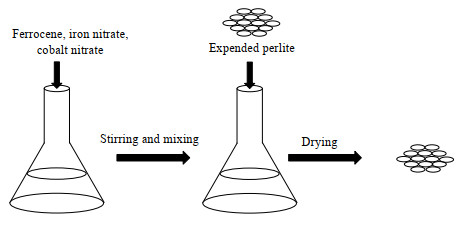
2.2 CNTs/Perlite复合材料的制备 2.2.1 膨胀珍珠岩的预处理膨胀珍珠岩的预处理过程如图1所示。将少量的二茂铁、硝酸铁和硝酸钴与适量的乙醇混合,用磁力搅拌器搅拌15 min使其混合均匀。称取一定量的膨胀珍珠岩加入搅拌后的溶液中,并用80 ℃水浴加热将溶剂挥发蒸干,得到的溶质即为预处理后的膨胀珍珠岩。
|
图 1 膨胀珍珠岩预处理流程图 Fig.1 Flow chart of pretreatment for expanded perlite |
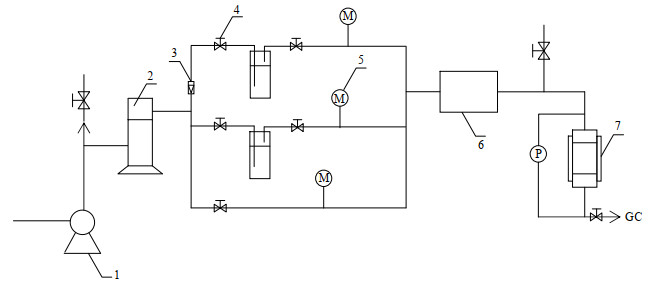
采用化学气相沉积法制备CNTs/Perlite,制备过程在OTF-1200X管式炉中完成,过程采用二段加热法,如图2所示。预处理过的膨胀珍珠岩盛于瓷舟中放置在高温区中央,樟脑作为碳源盛于另一瓷舟放置于管式炉前段,加热方式为恒温加热圈。准备完毕后,通入250 mL⋅min−1的N2 0.5 h左右,以排除反应炉内空气。膨胀珍珠岩作为载体在高温区以10 ℃⋅min−1恒定速率升至指定温度;在该温度下预热10 min后开启加热圈,使其以20 ℃⋅min−1的升温速率升至200 ℃并保持固定的时间。樟脑在200 ℃下升华为樟脑蒸气,进入高温反应区后在膨胀珍珠岩表面生成碳纳米管。本实验将从樟脑用量(1、2和3 g)、生长温度(600、700、800、900和1 000 ℃)和生长时间(30、40和50 min) 3个方面考察CNTs/Perlite复合材料的合成工艺。

|
图 2 CVD法制备CNTs/Perlite的实验流程装置图 Fig.2 Experimental procedure of CNTs/Perlite preparation via CVD 1. nitrogen bottle 2. valve 3. gas mixing chamber 4. pressure gauge 5. heating belt 6. camphor 7. perlite 8. water bath 9. vacuum pump |
采用S-3700N扫描电子显微镜对材料的微观形貌以及结构进行观测,操作电压为10~15 kV。测试前需要将样品干燥处理,并喷金使其具有导电性。
2.3.2 热重分析仪(TG)采用STA449C综合热分析仪对材料的热稳定性与化学成分进行测试。测试前将样品放入干燥箱烘干1 h,待去除吸附在样品表面的水分后,取5~10 mg样品置于坩埚中。工作条件:N2为吹扫气,O2为工作氛围,升温速率为10 ℃⋅min−1,升温范围为30~800 ℃。
2.3.3 拉曼光谱(Raman)采用HYJ Lab RAM Aramis激光共聚焦显微拉曼光谱仪对材料表面碳纳米管的石墨化程度、结晶度及表面缺陷程度进行测试。测试前无需对材料进行处理。
2.4 吸附性能评价甲苯在基于CNT颗粒与CNTs/Perlite构成的结构化固定床上的吸附动力学实验流程与装置如图3所示,装置由电脑控制。气路分成空气和甲苯蒸气两路,空气泵输送空气进入装有液体甲苯的鼓泡器中,通过鼓泡获得甲苯蒸气。两路气体进入气体混合室中混合均匀,用铝箔袋收集后通过Agilent7890A气相色谱测定其体积分数,所使用的色谱柱型号为HP-5。固定床进口气体体积分数通过调节各路气体流量来控制。达到固定床目标气体出口体积分数之后每隔5 min收集一次通过结构化固定床的气体进行测试。将固定床进口和出口气体体积分数分别记为ϕ0和ϕ。以t(甲苯气体出口体积分数ϕ对应的时间,min)为横坐标、ϕ/ϕ0为纵坐标作图,得到甲苯在结构化固定床上的吸附透过曲线。甲苯的色谱分析条件:H2流量为35 mL⋅min−1,N2流量为30 mL⋅min−1,干燥空气流量为375 mL⋅min−1,进样口温度为150 ℃,炉温为160 ℃,FID检测器温度为200 ℃,分流比为100:1。
|
图 3 甲苯在基于CNTs/Perlite结构化固定床上的吸附透过实验流程装置图 Fig.3 Experimental procedure of toluene adsorption and permeation on a structured fixed bed based on CNTs/Perlite 1. vacuum pump 2.drying column 3. rotameter flowmeter 4. valve 5. mass flow controller 6.mixing chamber 7. fixed bed |
本研究将考察不同甲苯体积流量(200、300和400 mL⋅min−1),不同甲苯入口体积分数(500×10−6、1 000×10−6和1 500×10−6)及不同结构化固定床(0.5 cm CNT+1.5 cm CNTs/Perlite、1 cm CNT+1 cm CNTs/Perlite、1.5 cm CNT+0.5 cm CNTs/Perlite以及2 cm CNT)对甲苯吸附透过曲线的影响。
2.5 理论模型 2.5.1 无效床层厚度评价结构化固定床的吸附性能,除了考察吸附透过曲线,结构化固定床的床层利用率也是重要的评判标准之一。无效床层厚度Lub指的是传质床层的无效床层的厚度,无效床层厚度越低,代表床层的利用率越高,其表达式由柯林斯[24]计算得出,如式(1)所示:
| $ L_{\mathrm{ub}}=\left(1-\frac{t_{\mathrm{b}}}{t^*}\right) L $ | (1) |
式中:L为固定床床层长度,m;tb为透过点时间,min;t*通过透过曲线计算得到,表达式为
| $ t^*=\int_0^{\infty}\left(1-\frac{\varphi}{\varphi_0}\right) \mathrm{d} t$ | (2) |
对于对称的吸附透过曲线,t*为当ϕ /ϕ 0等于0.5时所对应的时间。
此外,床层利用率∆Z可由无效床层厚度计算获得
| $ \Delta Z=\left(1-\frac{L_{\mathrm{ub}}}{L}\right) \times 100 \% $ | (3) |
该模型是Yoon和Nelson提出的关于描述固定床吸附的动力学模型,其假定吸附质分子吸附概率的衰减率与其吸附概率和透过概率成正比[25]。Yoon-Nelson能够准确地预测吸附剂的吸附透过曲线,这在工业生产中意义重大。Yoon-Nelson模型的表达式为
| $ t = \tau + \frac{1}{{k'}}\ln \frac{\varphi }{{{\varphi _0} - \varphi }} $ | (4) |
式中:τ为50% 透过时间,min;k′为速率常数,min−1;实验过程中可测得t、ϕ和ϕ0,以ln [ϕ/(ϕ0−ϕ)]为纵坐标对t作图,拟合直线的斜率和截距可以得到k′和τ。
3 结果与讨论 3.1 不同樟脑用量的影响 3.1.1 SEM首先在生长温度为800 ℃、合成时间为40 min的条件下考察前驱体(樟脑)用量对CNTs/Perlite梯度孔吸附剂形貌结构的影响,结果如图4所示。在图4中,(a)、(b)、(c)分别为樟脑用量为1、2、3 g所合成的样品。随着前驱体樟脑的用量增加(1、2、3 g),珍珠岩表面的碳纳米管覆盖率和生长密度显著提高(如图4(a)、(b)、(c)所示),但是随着樟脑用量继续增加,碳纳米管的生长密度提升不明显,并且CNTs/Perlite中无定型碳的数量有所增加。在目前已知的研究中,碳溶剂化、扩散、沉淀(carbon solvation,diffusion,precipitation,CSPD)模型是一种较为合理的碳纳米管生长机制模型,主要分为3个步骤[26]:(1)碳的溶剂化;(2)碳的扩散;(3)碳的沉淀。樟脑用量的提高加快了单位时间内碳溶剂化的速率,从而提高了反应区中樟脑的蒸气压[27],进而碳纳米管的产率也有所提高。过高的樟脑用量会导致催化碳纳米管生长的活性位点数量相对不足,多余的樟脑热分解后形成无定型碳沉积在衬底上[27-28]。因此珍珠岩上Fe和Co活性位点的数目与樟脑用量之间的平衡对于碳纳米管的生长十分重要。

|
图 4 不同樟脑用量生长CNTs/Perlite的SEM图 Fig.4 SEM images of CNTs/Perlite grown with different amounts of camphor |
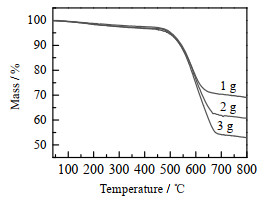
通过热重分析仪测试了不同樟脑用量对于CNTs/Perlite热稳定性的影响,图5为不同樟脑用量生长CNTs/Perlite的TG热重曲线。由图5可以看出,3条曲线的失重温度均为505 ℃左右,这表明樟脑的用量对于CNTs/Perlite的热稳定性无明显影响。从图5中观察得知,CNTs/Perlite的失重率分别为30% (1 g)、38% (2 g)和47% (3 g)。樟脑用量的提高会增加单位时间内进入反应炉中碳物种的量,有更多的碳自由基沉积在催化剂颗粒上,从而形成碳纳米管。因此CNT的产率会随着樟脑用量而增加,这与文献报道一致[29]。
|
图 5 不同樟脑用量生长CNTs/Perlite的热重分析图 Fig.5 TG analysis of CNTs/Perlite grown with different amounts of camphor |
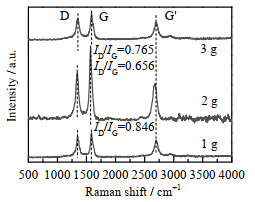
采用Raman光谱研究了不同樟脑用量对生成碳纳米管的缺陷程度、石墨化程度及有序性的影响,结果如图6所示。从图6可以看出,不同樟脑用量生长的CNTs/Perlite均在1 350,1 590和2 700 cm−1左右的位置产生了碳纳米管的特征峰。其中1 350 cm−1的D峰对应的是CNT中残留无组织的石墨结构,1 590 cm−1的G峰对应的是石墨E2g伸缩模式的分裂[30]。D峰与G峰的峰强之比ID/IG越低代表碳纳米管质量越高[31],从图中得知,随着樟脑用量从1 g增加到3 g,ID/IG从最初的0.765降低到0.656再升高至0.846,呈现出先下降后上升的趋势,其中樟脑用量为2 g时ID/IG最低,为0.656,表明其缺陷程度最低,生成碳纳米管的石墨化质量最高。综上所述,在合成CNTs/Perlite的实验中,最合适的樟脑用量为2 g。
|
图 6 不同樟脑用量生长CNTs/Perlite的Raman光谱图 Fig.6 Raman spectra of CNTs/Perlite grown with different amounts of camphor |
在樟脑用量为2 g、生长时间为40 min的条件下考察了不同生长温度对于碳纳米管生长形貌的影响,结果如图7所示。

|
图 7 不同温度下生长CNTs/Perlite的SEM图 Fig.7 SEM images of CNTs/Perlite grown at different temperatures |
由图7得知,在生长温度为600和700 ℃时,碳纳米管的覆盖率,生长密度以及生长长度都较低。当温度上升到800 ℃时,碳纳米管的覆盖率生长密度和生长长度有了显著的提高,而当温度进一步提高(900,1 000 ℃)时,碳纳米管的曲率变小,直径增加,逐渐转为石墨片状结构[32]。碳纳米管的生长主要依赖于金属粒子的催化作用[33]。金属催化剂在低于碳氢化学物自发热分解的温度下将其分解形成碳和氢,形成的碳自由基会在金属粒子中经历沉积、扩散、沉淀等一系列过程,而碳自由基在经历这些过程中的速率除了和金属催化剂本身的碳溶性有关,还与生长温度有关[34-35]。在低温下,碳的扩散速率较慢,碳溶性较低,因此碳纳米管的生长速率会较为缓慢(如图7(a)、(b)所示)。温度过高时,碳在金属催化剂中的扩散速率较快,单位时间内碳在金属表面沉积的量也更多,因此会生成直径更大管壁更厚的碳纳米管,同时产生曲率半径较大、石墨化程度较高的碳纳米纤维以及石墨层[36](如图7(e)所示)。相比于低温条件下的碳纳米管(如图7(a)、(b)、(c)所示),高温条件下的碳纳米管也更容易断裂(如图7(d)、(e)所示),同时碳热分解的速率也会更快从而产生更多的无定型碳[37]。
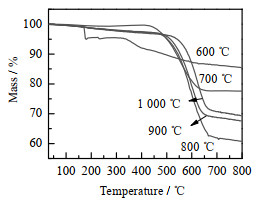
3.2.2 TG热重通过热重分析仪测试了不同生长温度对于CNTs/Perlite热稳定性的影响,结果如图8所示。从图8可以看出,生长温度从600到1 000 ℃,CNTs/Perlite的失重温度分别为300、430、500、520和550 ℃,其中600 ℃下合成的CNTs/Perlite失重温度较低,仅为300 ℃,一般来说无定型碳的失重温度在500 ℃以下[38],这表明在生长温度为600、700 ℃时,碳物种转化成无定形碳的数量较多,但随着生长温度的上升,CNTs/Perlite的失重温度逐渐向高温区移动。研究表明,纳米碳结构的氧化温度与碳材料的结晶度有关,高结晶度的纳米碳热稳定性强[39],因此高温下生成的结晶度良好的碳纳米管及石墨层等具有更强的热稳定性。从失重率来看,生长温度600~1 000 ℃的失重率分别为13%、22%、38%、32% 和29%,总体呈现出先增加后减小的趋势,因为提高温度能增加碳纳米管的生长速率,但同时碳沉淀的速率也更快了,使得其容易在催化剂表面形成石墨层,当石墨层完全包裹住金属催化剂时,碳纳米管生长停止。所以温度过高也可能导致催化剂过早失活,降低碳纳米管的产率。
|
图 8 不同生长温度下CNTs/Perlite的TG热重分析图 Fig.8 TG analysis of CNTs/Perlite at different temperatures |
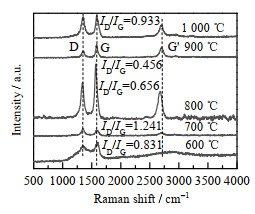
通过拉曼光谱研究不同生长温度对于CNTs/Perlite缺陷程度的影响,结果如图9所示。从图9中可以观察到,不同生长温度的CNTs/Perlite均在1 350、1 590和2 700 cm−1左右的位置分别产生了碳纳米管的D、G及G′等特征峰。其中生长温度为600 ℃时生长的碳纳米管较少,导致其峰型不规则,峰之间的分离程度较低。而在其他生长温度下,随着温度的提高,ID/IG先减小后增加,表明较高温度有利于生成缺陷较少的碳纳米管,但是过高的温度,也可能破坏碳纳米管的结构,生成无定型碳。结合之前的SEM和TG可得出结论,800 ℃为本实验中碳纳米管的最适生长温度。
|
图 9 不同生长温度下CNT/Perlite的Raman光谱图 Fig.9 Raman spectra of CNT/Perlite at different temperatures |
在生长温度为800 ℃、樟脑用量为2 g的条件下考察了不同生长时间对于CNTs/Perlite生长形貌的影响,图10显示了不同生长时间下生长CNTs/Perlite的SEM形貌图。

|
图 10 不同生长时间生长CNTs/Perlite的SEM图 Fig.10 SEM images of CNTs/Perlite grown at different times |
从图10(a)、(b)、(c)中可以看出,在30、40和50 min的碳纳米管覆盖率和生长密度均较高,结合(a)、(b)、(c)不难发现,30 min的生长时间得到的CNTs/Perlite碳纳米管管长较短且形状呈螺旋状和锯齿状,而40和50 min均得到管长较长、中空圆筒状的碳纳米管。结果表明,在一定的时间内,碳纳米管的生长长度与时间呈正比[40]。同时,较长的生长时间有利于为碳源和催化剂提供足够的接触时间,从而让碳源催化分解完全,形成较为完整的碳纳米管,同时生长时间的增加也减少无定型碳的数量,得到了比较好的碳纳米管晶型结构[41]。
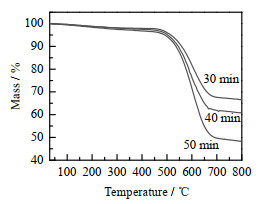
3.3.2 TG热重通过TG热重曲线分析不同生长时间对CNTs/Perlite的稳定性的影响结果如图11所示。从图11中可以看出,3条不同生长时间的曲线失重温度均在500 ℃左右,说明生长时间对CNTs/Perlite的热稳定性影响不大。而随着生长时间的延长,CNTs/Perlite的失重率也在增加,30、40和50 min CNTs/Perlite的失重率分别为34%、38% 和53%,这也说明碳纳米管的产率也是随着生长时间的延长而提高,与SEM中CNT生长密度所呈现的规律一致。
|
图 11 不同生长时间生长CNTs/Perlite的TG热重分析图 Fig.11 TG analysis of CNTs/Perlite grown at different times |
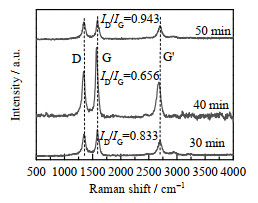
通过Raman光谱研究生长时间对CNTs/Perlite缺陷程度的影响,结果如图12所示。从图12中可以看出,在不同生长时间下合成的CNTs/Perlite均出现碳纳米管的特征峰。并且随着生长时间的延长,ID/IG先下降后上升,表明生长的碳纳米管缺陷程度呈现先提高后下降的趋势。较长的生长时间有利于为碳源和催化剂提供足够的接触时间,形成石墨化较好的碳纳米管。但随着生长时间不断延长,催化剂会被表面沉积的碳逐渐包裹失去活性。失去催化剂的催化分解,碳氢化合物将以自发热分解的形式转化为无定型碳等其他碳物质,因此使得整体碳纳米管的石墨化程度下降[28]。在Raman光谱中表现为ID/IG先下降后上升,即与本实验结果一致。结合以上表征,40 min为本研究合成CNTs/Perlite的最佳生长时间。
|
图 12 不同生长时间生长CNTs/Perlite的Raman光谱图 Fig.12 Raman spectra of CNTs/Perlite grown at different times |
采用BET和MIP压汞法测试了膨胀珍珠岩和CNTs/Perlite 的孔结构和比表面积。从表1中可以看出,通过CVD法在膨胀珍珠岩上负载碳纳米管膜,样品的比表面积由0.057增加到18.69 m2⋅g−1,而负载CNT后的样品孔隙率仍然有83.05%,平均孔径为597.8 nm,属于大孔材料。大孔材料的引入能够显著地降低床层压降,提高VOC基于吸附剂上的传质速率和接触效率[42]。
|
|
表 1 CNTs/Perlite 和膨胀珍珠岩的孔结构与比表面积 Table 1 Pore structure and specific surface areas of CNTs/Perlite and expanded perlite |
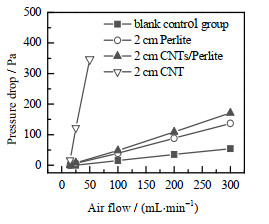
考察了不同结构床层的压降,其结果如图13所示。2 cm Perlite的床层结构压降远小于同流速下CNT的压降,并且Perlite在负载CNT后,压降上升程度很小,这表明CNTs/Perlite作为一种梯度孔材料可以有效降低床层压降。
|
图 13 各结构床层在不同流速下的压降变化曲线图 Fig.13 Pressure drop curves of each structural bed at different flow rates |
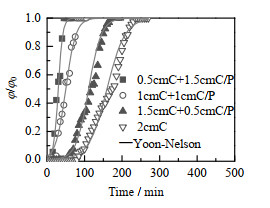
吸附透过曲线常作为评价吸附剂的标准,本研究分别设计了不同结构化的床层(0.5 cm CNT+1.5 cm CNTs/Perlite、1 cm CNT+1 cm CNTs/Perlite、1.5 cm CNT+0.5 cm CNTs/Perlite以及2 cm CNT),在甲苯体积分数为1 500×10−6、流量为200 mL⋅min−1的条件下,测定了甲苯在各结构化床层上的吸附透过曲线,结果如图14所示,图中,C为CNT,C/P为CNTs/Perlite。其中1.5 cm CNT+0.5 cm CNTs/Perlite和2 cm CNT的固定床床层吸附透过时间远大于其他2种,表明CNT的吸附容量是要高于CNTs/Perlite。但随着CNTs/Perlite厚度的增加,吸附透过曲线的斜率呈现上升的趋势,这说明CNTs/Perlite的梯度孔结构有利于传质发生[43],适当引入大孔结构能够有效地提高流体的接触效率及扩散速率,从而降低传质阻力。因此合理地调控CNTs/Perlite与CNT的比例有利于提高床层的吸附效率。结合以上实验结果,1.5 cm CNT和0.5 cm CNTs/Perlite组成的结构化床层为本实验的最佳吸附床层。
|
图 14 不同床层结构的甲苯吸附透过曲线 Fig.14 Breakthrough curves of toluene with different bed structures (flow rate 200 mL⋅min−1, toluene concentration 1 500 cm3×m−3) |
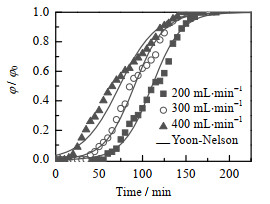
考察了在甲苯体积分数为1 500×10−6时,不同流量(200、300和400 mL⋅min−1)下的甲苯在1.5 cm CNT+0.5 cm CNTs/Perlite结构化固定床层的吸附透过曲线,结果如图15所示。可以看出,随着气体流量的增大,甲苯的吸附透过时间明显缩短,这可以理解为单位时间内床层吸附甲苯的量是一定的,气体流量的增大增加了单位时间内进入床层甲苯气体的量,从而使得吸附透过时间提前[44-45]。而斜率的减小表明床层传质阻力增加,在较大的气体流量下,气体的扩散速率下降,使得传质效率降低。
|
图 15 不同流量下的甲苯吸附透过曲线 Fig.15 Breakthrough curves of toluene at different flow rates (bed 1.5 cm CNT+0.5 cm CNTs/Perlite, toluene volume fraction 1 500 cm3⋅m−3) |
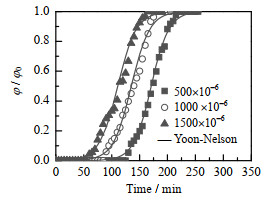
探讨了在甲苯气体流量为200 mL⋅min−1下,不同甲苯体积分数(500×10−6、1 000×10−6和1 500×10−6)下的甲苯在1.5 cm CNT+0.5 cm CNTs/Perlite的结构化固定床层上的吸附透过曲线。如图16所示,随着甲苯体积分数的增加,甲苯吸附透过曲线明显缩短,这同样可以理解为甲苯体积分数的增大增加了单位时间内进入床层甲苯气体的量,而结构化固定床层的吸附容量为一定的,所以导致吸附透过曲线前移[46]。甲苯体积分数增加时,吸附透过曲线的斜率并没有因体积分数的改变而发生太大的变化。这证明该结构化固定床层的传质效率高,具有较好的吸附性能。
|
图 16 不同体积分数下的甲苯吸附透过曲线 Fig.16 Breakthrough curves of toluene at different volume fractions (bed 1.5 cm CNT+0.5 cm CNTs/Perlite, flow rate 200 mL⋅min−1 |
根据2.5.1节中式(1)、(2)、(3)计算出的不同结构化床层的无效床层厚度及床层利用率等参数如表2所示,0.5 cm CNT+1.5 cm CNTs/Perlite、1 cm CNT+1 cm CNTs/Perlite、1.5 cm CNT+0.5 cm CNTs/Perlite以及2 cm CNT的无效床层厚度分别为0.889、0.959、0.984和1.028 cm,床层利用率分别为55.6%、52.1%、50.8% 和48.6%,可以看出,随着CNTs/Perlite比例的增加,结构化床层的无效层厚度在减小且床层利用率有明显提高,这表明CNTs/Perlite能有效提高甲苯气体的传质效率。
|
|
表 2 不同结构化床层的无效层厚度 Table 2 Lub of different structured beds |
在选定了最优结构化床层之后,进一步研究了结构化床层(0.5 cm CNT+1.5 cm CNTs/Perlite)对于不同入口浓度和流量甲苯气体吸附的无效层厚度及床层利用率。如表3所示,甲苯气体流量分别为200、300、400 mL⋅min−1时,其无效层厚度和床层利用率分别为0.984、1.045、1.446 cm和50.8%、47.8%、27.7%,其中400 mL⋅min−1下的床层利用率比200 mL⋅min−1下降了23.1%。原因可以归结为较高的流量导致甲苯气体的停留时间缩短,不利于吸附过程传质的进行。因此较低的流量更有利于甲苯气体的吸附。而甲苯体积分数分别为500×10−6、1 000×10−6、1 500×10−6时,其床层无效层厚度和利用率分别为0.520、0.662、0.984 cm和74.0%、66.9%、50.8%,床层利用率呈现降低的趋势。
|
|
表 3 不同条件下固定床床层的无效层厚度 Table 3 Lub of fixed bed under different conditions |
根据2.5.2节中式(4)计算各条件下的Yoon-Nelson模型参数。不同固定床床层吸附甲苯的Yoon-Nelson模型参数如表4所示,0.5 cm CNT+1.5 cm CNTs/Perlite、1 cm CNT+1 cm CNTs/Perlite、1.5 cm CNT+0.5 cm CNTs/Perlite以及2 cm CNT的k′分别为0.166 5、0.074 3、0.059 6、0.041 6 min−1,根据Yoon-Nelson模型理论[25],k′的数值与吸附透过曲线的斜率成正相关,这与之前实验得到的结论一致。并且随着CNTs/Perlite的减小、50% 吸附透过时间τ延长,这也与吸附透过曲线所呈现的结果一致。
|
|
表 4 不同固定床床层结构甲苯吸附的Yoon-Nelson模型参数 Table 4 Parameters of Yoon-Nelson model for toluene adsorption in different fixed bed structures |
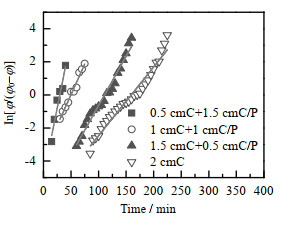
根据实验数据对吸附透过曲线进行了拟合,不同固定床床层的吸附透过曲线拟合如图17所示,结合表3中的线性回归相关系数R2,可以发现所有的R2均大于0.93,这表明Yoon-Nelson模型能够比较准确地预测甲苯在固定床床层上的吸附实验。将Yoon-Nelson模型应用于不同条件下的固定床床层吸附甲苯的吸附透过曲线,结果如表5、6所示,在200、300、400 mL⋅min−1的甲苯气体流量下,1.5 cm CNT+0.5 cm CNTs/Perlite的固定床床层对甲苯的吸附速率常数分别为0.059 6、0.058 5、0.047 2 min−1,50% 透过时间τ分别为110.9、90.6、73.5 min。流量越低的情况下,其吸附速率常数越大,且透过时间越长。这与实验结果一致。
|
图 17 甲苯在不同固定吸附床上的Yoon-Nelson线性拟合图 Fig.17 Yoon-Nelson linear fitting diagram of toluene on different fixed adsorption beds |
|
|
表 5 不同流量下甲苯吸附的Yoon-Nelson模型参数 Table 5 Parameters of Yoon-Nelson model for toluene adsorption at different flow rates |
|
|
表 6 不同体积分数下甲苯吸附的Yoon-Nelson模型参数 Table 6 Parameters of Yoon-Nelson model for toluene adsorption at different volume fractions |
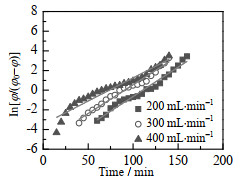
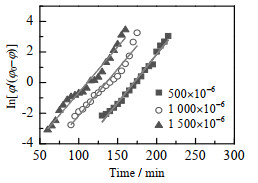
表5中线性回归方程的相关系数R2均大于0.93,并且图18中Yoon-Nelson线性回归曲线与实验所得的吸附透过曲线拟合较好,这说明在不同的甲苯流量下Yoon-Nelson模型能够准确地预测甲苯在固定床床层上的吸附实验。在500×10−6、1 000×10−6、1 500×10−6的甲苯入口体积分数下,1.5 cm CNT+0.5 cm CNTs/Perlite的固定床层对甲苯的吸附速率常数分别为0.063 1、0.060 8、0.059 6 min−1,50% 透过时间分别为170.8、135.4、110.9 min。其变化的趋势均与实验结果一致。并且结合表6中的相关系数R2均大于0.93和图19中的Yoon-Nelson线性回归曲线拟合较好的事实,表明在不同的甲苯入口体积分数下,Yoon-Nelson模型能准确地预测甲苯在固定床床层上的吸附实验。
|
图 18 不同流量的甲苯在固定吸附床上的Yoon-Nelson线性拟合图 Fig.18 Yoon-Nelson linear fitting diagram of toluene with different flow rates on fixed adsorption bed |
|
图 19 不同入口体积分数的甲苯在固定吸附床上的Yoon-Nelson线性拟合图 Fig.19 Yoon-Nelson linear fitting diagram of toluene with different inlet volume fractions on fixed adsorption bed |
以樟脑为前驱体,采用化学气相沉积法成功在膨胀珍珠岩表面生长了碳纳米管,合成出一种新型的CNTs/Perlite梯度孔复合材料,并探究了不同合成条件对复合材料的影响规律。实验表明,在生长温度为800 ℃、生长时间为40 min、樟脑用量为2 g时,合成的CNT生长密度较高、热稳定性较强、表面缺陷结构最少。甲苯吸附实验于最佳工艺下合成的CNTs/Perlite复合材料与颗粒型CNT组成的结构化固定床上进行。结果表明,随着CNTs/Perlite与颗粒CNT比例的增加,吸附透过时间有所缩短。LUB计算结果表明,在床层厚度为2 cm、甲苯流量为200 mL⋅min−1、入口甲苯气体体积分数为1 500×10−6的条件下,与颗粒型碳纳米管床层相比,结构化固定床层(1.5 cm CNT+0.5 cm CNTs/Perlite)的无效床层厚度由1.028 cm降低为0.984 cm,床层利用率从48.6% 提高为50.8%。Yoon-Nelson模型拟合数据所有线性回归方程得到的相关系数R2均大于0.93,表明Yoon-Nelson模型在本实验中具有较高的准确性。
| [1] |
ZAVYALOVA U, NIGROVSKI B, POLLOK K, et al. Gel-combustion synthesis of nanocrystalline spinel catalysts for VOCs elimination[J]. Applied Catalysis B:Environmental, 2008, 83(3/4): 221-228. |
| [2] |
王欢, 王亚男. 公共场所中挥发性有机化合物的检测分析[J]. 中国城乡企业卫生, 2017, 32(10): 144-145. WANG H, WANG Y N, et al. Detection and analysis of volatile organic compounds in public places[J]. Chinese Journal of Urban and Rural Areas of Hygiene, 2017, 32(10): 144-145. |
| [3] |
BARLETTA B, MEINARDI S, SHERWOOD ROWLAND F, et al. Volatile organic compounds in 43 Chinese cities[J]. Atmospheric Environment, 2005, 39(32): 5979-5990. DOI:10.1016/j.atmosenv.2005.06.029 |
| [4] |
MOURA L, MOUFAWAD T, FERREIRA M, et al. Deep eutectic solvents as green absorbents of volatile organic pollutants[J]. Environmental Chemistry Letters, 2017, 15(4): 747-753. DOI:10.1007/s10311-017-0654-y |
| [5] |
DENG L, YUAN P, LIU D, et al. Effects of microstructure of clay minerals, montmorillonite, kaolinite and halloysite, on their benzene adsorption behaviors[J]. Applied Clay Science, 2017, 143: 184-191. DOI:10.1016/j.clay.2017.03.035 |
| [6] |
NIEN K C, CHANG F T, CHANG M B. Adsorption of mesitylene via mesoporous adsorbents[J]. Journal of the Air & Waste Management Association, 2017, 67(12): 1319-1327. |
| [7] |
YANG X, YI H, TANG X, et al. Behaviors and kinetics of toluene adsorption-desorption on activated carbons with varying pore structure[J]. Journal of Environmental Sciences, 2018, 67: 104-114. DOI:10.1016/j.jes.2017.06.032 |
| [8] |
ZHOU L, ZHANG X, CHEN Y. Facile synthesis of Al-fumarate metal–organic framework nano-flakes and their highly selective adsorption of volatile organic compounds[J]. Materials Letters, 2017, 197: 224-227. DOI:10.1016/j.matlet.2017.01.120 |
| [9] |
OZTURK B, YILMAZ D. Absorptive removal of volatile organic compounds from flue gas streams[J]. Process Safety and Environmental Protection, 2006, 84(5): 391-398. DOI:10.1205/psep05003 |
| [10] |
GUPTA V K, VERMA N. Removal of volatile organic compounds by cryogenic condensation followed by adsorption[J]. Chemical Engineering Science, 2002, 57(14): 2679-2696. DOI:10.1016/S0009-2509(02)00158-6 |
| [11] |
VANDER VAART D R, VATVUK W M, WEHE A H. Thermal and catalytic incinerators for the control of VOCs[J]. Journal of the Air & Waste Management Association, 1991, 41(1): 92-98. |
| [12] |
PAPAEFTHIMIOU P, IOANNIDES T, VERYKIOS X E. Catalytic incineration of volatile organic compounds present in industrial waste streams[J]. Applied Thermal Engineering, 1998, 18(11): 1005-1012. DOI:10.1016/S1359-4311(98)00021-0 |
| [13] |
KONSOLAKIS M, CARABINEIRO S A C, TAVARES P B, et al. Redox properties and VOC oxidation activity of Cu catalysts supported on Ce1−xSmxOδ mixed oxides[J]. Journal of Hazardous Materials, 2013, 261: 512-521. DOI:10.1016/j.jhazmat.2013.08.016 |
| [14] |
ABBASI Z, HAGHIGHI M, FATEHIFAR E, et al. Synthesis and physicochemical characterizations of nanostructured Pt/Al2O3–CeO2 catalysts for total oxidation of VOCs[J]. Journal of Hazardous Materials, 2011, 186(2/3): 1445-1454. |
| [15] |
DEMEESTERE K, DEWULF J, VAN LANGENHOVE H. Heterogeneous photocatalysis as an advanced oxidation process for the abatement of chlorinated, monocyclic aromatic and sulfurous volatile organic compounds in air: State of the art[J]. Critical Reviews in Environmental Science and Technology, 2007, 37(6): 489-538. DOI:10.1080/10643380600966467 |
| [16] |
PARMAR G R, RAO N N. Emerging control technologies for volatile organic compounds[J]. Critical Reviews in Environmental Science and Technology, 2008, 39(1): 41-78. DOI:10.1080/10643380701413658 |
| [17] |
IIJIMA S. Helical microtubules of graphitic carbon[J]. Nature, 1991, 354(6348): 56-58. DOI:10.1038/354056a0 |
| [18] |
SHIH Y, LI M. Adsorption of selected volatile organic vapors on multiwall carbon nanotubes[J]. Journal of Hazardous Materials, 2008, 154(1/2/3): 21-28. |
| [19] |
CHEN W, DUAN L, ZHU D. Adsorption of polar and nonpolar organic chemicals to carbon nanotubes[J]. Environmental Science & Technology, 2007, 41(24): 8295-8300. |
| [20] |
YAN Y, PENG L, LI R, et al. Concentration, ozone formation potential and source analysis of volatile organic compounds (VOCs) in a thermal power station centralized area: A study in Shuozhou, China[J]. Environmental Pollution, 2017, 223: 295-304. DOI:10.1016/j.envpol.2017.01.026 |
| [21] |
ZHAO X, LV L, PAN B, et al. Polymer-supported nanocomposites for environmental application: A review[J]. Chemical Engineering Journal, 2011, 170(2/3): 381-394. |
| [22] |
YANG Y, ZHANG H, YAN Y. Synthesis of carbon nanotube on stainless steel microfibrous composite—Comparison of direct and indirect growth and its application in fixed bed m-cresol adsorption[J]. Chemical Engineering Research and Design, 2018, 139: 162-173. DOI:10.1016/j.cherd.2018.09.027 |
| [23] |
PILATOS G, SAMOUHOS M, ANGELOPOULOS P, et al. Carbon nanotubes growth on expanded perlite particles via CVD method: The influence of the substrate morphology[J]. Chemical Engineering Journal, 2016, 291: 106-114. DOI:10.1016/j.cej.2016.01.112 |
| [24] |
COLLINS J J. The LUB/equilibrium section concept for fixed-bed adsorption: Proceeding of the Chemical Engineering Progress Symposium Serials [C]. New York: American Institute of Chemical Engineers, 1967, 63(74): 31-35.
|
| [25] |
YOON Y H, NELSON J H. Application of gas adsorption kinetics I. A theoretical model for respirator cartridge service life[J]. The American Civil The American Industrial Hygiene Association Journal, 1984, 45(8): 517-524. |
| [26] |
VANDER WAL R L, HALL L J. Carbon nanotube synthesis upon stainless steel meshes[J]. Carbon, 2003, 41(4): 659-672. DOI:10.1016/S0008-6223(02)00369-X |
| [27] |
KUMAR M, ANDO Y. Controlling the diameter distribution of carbon nanotubes grown from camphor on a zeolite support[J]. Carbon, 2005, 43(3): 533-540. DOI:10.1016/j.carbon.2004.10.014 |
| [28] |
LI X, CI L, KAR S, et al. Densified aligned carbon nanotube films via vapor phase infiltration of carbon[J]. Carbon, 2007, 45(4): 847-851. DOI:10.1016/j.carbon.2006.11.010 |
| [29] |
黄浩鑫, 张会平, 鄢瑛. NCNTs/PSSF微纤复合催化剂的制备及在苯酚降解中的应用[J]. 工程科学与技术, 2019, 51(6): 44-53. HUANG H X, ZHANG H P, YAN Y. Preparation of NCNTs/PSSF microfiber composite catalyst and its application in phenol degradation[J]. Engineering Science and Technology, 2019, 51(6): 44-53. |
| [30] |
BELIN T, EPRON F. Characterization methods of carbon nanotubes: A review[J]. Materials Science and Engineering:B, 2005, 119(2): 105-118. DOI:10.1016/j.mseb.2005.02.046 |
| [31] |
DRESSELHAUS M S, DRESSELHAUS G, SAITO R, et al. Raman spectroscopy of carbon nanotubes[J]. Physics Reports, 2005, 409(2): 47-99. DOI:10.1016/j.physrep.2004.10.006 |
| [32] |
SHINDE S M, KANO E, KALITA G, et al. Grain structures of nitrogen-doped graphene synthesized by solid source-based chemical vapor deposition[J]. Carbon, 2016, 96: 448-453. DOI:10.1016/j.carbon.2015.09.086 |
| [33] |
MOISALA A N A G K. The role of metal nanoparticles in the catalytic production of single-walled carbon nanotubes—A review[J]. Journal of Physics:Condensed Matter, 2003, 15(42): S3011. DOI:10.1088/0953-8984/15/42/003 |
| [34] |
KUMAR M, ANDO Y. Chemical vapor deposition of carbon nanotubes: A review on growth mechanism and mass production[J]. Journal of Nanoscience and Nanotechnology, 2010, 10(6): 3739-3758. DOI:10.1166/jnn.2010.2939 |
| [35] |
KUMAR M, ANDO Y. Single-wall and multi-wall carbon nanotubes from camphor—a botanical hydrocarbon[J]. Diamond and Related Materials, 2003, 12(10/11): 1845-1850. |
| [36] |
MUSSO S, PORRO S, ROVERE M, et al. Fluid dynamic analysis of gas flow in a thermal-CVD system designed for growth of carbon nanotubes[J]. Journal of Crystal Growth, 2008, 310(2): 477-483. DOI:10.1016/j.jcrysgro.2007.10.064 |
| [37] |
YANG Y, ZHANG H, YAN Y. Synthesis of CNTs on stainless steel microfibrous composite by CVD: Effect of synthesis condition on carbon nanotube growth and structure[J]. Composites Part B:Engineering, 2019, 160: 369-383. DOI:10.1016/j.compositesb.2018.12.100 |
| [38] |
HORDY N, MENDOZA-GONZALEZ N, COULOMBE S, et al. The effect of carbon input on the morphology and attachment of carbon nanotubes grown directly from stainless steel[J]. Carbon, 2013, 63: 348-357. DOI:10.1016/j.carbon.2013.06.089 |
| [39] |
AWADALLAH A E, ABOUL-ENEIN A A, KANDIL U F, et al. Facile and large-scale synthesis of high quality few-layered graphene nano-platelets via methane decomposition over unsupported iron family catalysts[J]. Materials Chemistry and Physics, 2017, 191: 75-85. DOI:10.1016/j.matchemphys.2017.01.007 |
| [40] |
PAL S K, TALAPATRA S, KAR S, et al. Time and temperature dependence of multi-walled carbon nanotube growth on inconel 600[J]. Nanotechnology, 2008, 19(4): 45610. DOI:10.1088/0957-4484/19/04/045610 |
| [41] |
CHEKIN F, RAOOF J, BAGHERI S, et al. Fabrication of chitosan-multiwall carbon nanotube nanocomposite containing ferri/ferrocyanide: Application for simultaneous detection of d-penicillamine and tryptophanb[J]. Journal of the Chinese Chemical Society (Taipei), 2012, 59(11): 1461-1467. DOI:10.1002/jccs.201200138 |
| [42] |
WAHID S, TATARCHUK B J. Catalytic material with enhanced contacting efficiency for volatile organic compound removal at ultrashort contact time[J]. Industrial & Engineering Chemistry Research, 2013, 52(44): 15494-15503. |
| [43] |
CHEN H, ZHANG H, YAN Y. Preparation and characterization of a novel gradient porous ZSM-5 zeolite membrane/PSSF composite and its application for toluene adsorption[J]. Chemical Engineering Journal, 2012, 209: 372-378. DOI:10.1016/j.cej.2012.08.020 |
| [44] |
PARK S, CHOI B, LEE J. Breakthrough data analysis of adsorption of toluene vapor in a fixed-bed of granular activated carbon[J]. Separation Science and Technology, 2007, 42(10): 2221-2233. DOI:10.1080/01496390701444105 |
| [45] |
AMARI A, CHLENDI M, GANNOUNI A, et al. Experimental and theoretical studies of VOC adsorption on acid-activated bentonite in a fixed-bed adsorber[J]. Industrial & Engineering Chemistry Research, 2010, 49(22): 11587-11593. |
| [46] |
CHEN H, ZHANG H, YAN Y. Adsorption dynamics of toluene in structured fixed bed with ZSM-5 membrane/PSSF composites[J]. Chemical Engineering Journal, 2013, 228: 336-344. DOI:10.1016/j.cej.2013.04.102 |




