2. 浙江大学衢州研究院,浙江 衢州 324000
2. Institute of Zhejiang University-Quzhou, Quzhou 324000, China
手性是生命的基础内在特性,人体本身也是一个手性环境。这使得一种手性药物的两种对映体在人体内通常在药理活性,代谢速率和毒性等方面存在较大差异[1-2]。因此,如何获取单一光学纯度的手性药物一直是医药化学工业中的研究热点[3-4]。
目前,单一对映体主要通过不对称合成和消旋体拆分两种方式获得。不对称合成是获得单一光学纯化合物的重要方法,但其通常需要复杂的合成过程和较高的成本,费时费力[5-6]。因此,许多非天然手性药物仍需通过各种拆分方法获得,如结晶拆分法[7],动力学拆分法[8-9],色谱拆分法[10-11],膜拆分法[12]等。其中,手性液液萃取法是利用液液萃取方法进行对映体分离的技术,其能耗低,设备简单,操作条件温和,易于连续化规模化生产,是具有良好工业应用前景的一种方法[13-15]。在手性液液萃取技术中,关键在于高立体选择性的手性拆分剂[16]。目前,常用的手性选择剂多为环糊精类,酒石酸衍生物类,冠醚类等[17]。手性离子液体是离子液体中重要的一类,其具备离子液体蒸气压低,热稳定性好,溶解性强等特性,且拥有良好的手性识别能力。近来,手性离子液体大量用在分离领域研究,尤其在对映体拆分方面[18-21]。因此,将手性离子液体作为药物对映体的拆分剂是值得考虑的。
另一方面,当只用一种手性选择剂进行拆分时,单相手性识别系统的效率相对较低。于是双相识别手性液液萃取(BRCE)最先被TANG等[22]开发出来。BRCE是通过在水相和油相分别添加亲水性手性拆分剂和亲油性手性拆分剂,在两相中分别优先识别不同的对映体的萃取分离技术。对比于只添加单一萃取剂,双相手性识别体系同时结合了亲水性和亲油性两种手性选择剂的识别能力,能在一定程度上改善分离效果,提高选择性系数[17, 23]。
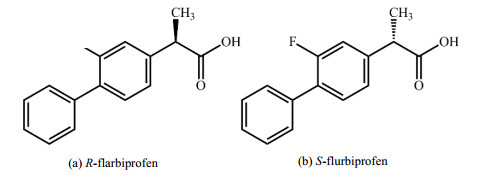
氟比洛芬,化学名(±)-2-(2-氟-4-联苯基)-丙酸(图 1),是临床上常用的非甾体抗炎类手性药,药效优于布洛芬和阿司匹林。其S型对映体对于类风湿性关节炎和骨关节炎有很好的治疗效果,而R型对映体却几乎没有效果并有一定毒副作用[24-25]。近来发现R型对映体则对于海尔默兹病有一定疗效,还可以抑制肿瘤生长和缓解疼痛[26-27]。TANG等[28]以环糊精衍生物和酒石酸酯为拆分剂研究了氟比洛芬对映体的传统双相识别液液萃取手性拆分,筛选了萃取剂种类,优化了萃取剂浓度,药物浓度,pH,温度等条件,5 ℃下选择性达1.24。CHEN等[29]建立了乙醇水溶液/硫酸铵水溶液双水相体系,并以酒石酸酯和L-色氨酸为拆分剂分离了氟比洛芬对映体,取得了良好的拆分效果。但由于其较为复杂的分离体系,较长的相分离时间且添加了一定的无机盐(硫酸铵),对后续药品分离及萃取剂回收利用不利。本课题组[30]也筛选了多种手性离子液体作为萃取剂,单相识别分离了氟比洛芬对映体。优化条件下,手性拆分剂[Bmim][L-Trp]在25 ℃分配系数为21.1和25.5,选择性系数约为1.20,相对较低,有待进一步提高。
|
图 1 R-氟比洛芬和S-氟比洛芬的结构图 Fig.1 The structures of R-flurbiprofen and S-flurbiprofen |
本文基于本组之前的研究工作[30],以[Bmim][L-Trp]和酒石酸酯为萃取剂开发了双相识别手性液液萃取体系并用于氟比洛芬对映体的分离。考察酒石酸酯种类及浓度,药物浓度,有机溶剂种类,pH,温度等因素对于萃取过程的影响,并通过反萃取过程进行了手性离子液体的循环回用研究。
2 实验部分 2.1 实验试剂氟比洛芬消旋体(分析纯,99%,百灵威科技有限公司);氟比洛芬标准品(色谱级,99.8%,中国食品药品检定研究院);R-氟比洛芬(98%,百灵威科技有限公司);正己烷(色谱纯,95%,Sigma-Aldrich化学有限公司);乙醇(色谱纯,99.8%,阿拉丁生化科技有限公司);三氟乙酸(色谱纯,99.5%,阿拉丁生化科技有限公司);1-丁基-3-甲基咪唑L-色氨酸([Bmim][L-Trp]) (分析纯,97%,上海成捷化学有限公司);D-和L-酒石酸酯均按照文献中方法由实验室合成得到[31-32],纯度 > 95%;其他试剂均为分析纯,购买自国药集团化学试剂有限公司。
2.2 实验过程(1) 萃取过程
配置一定pH的0.3 mol·L-1磷酸盐缓冲溶液,与10% (体积比)的甲醇混合改善氟比洛芬在水相的溶解性。加入一定量的氟比洛芬消旋体和0.02 mol·L-1的[BMIM][L-trp]得到水相。将一定量的酒石酸酯衍生物溶解于纯的脂肪醇或卤代烃溶剂中得到油相。将3 mL的水相和3 mL油相混合于10 mL的离心管中,在恒温水浴振荡器中200 r·min-1转速下震荡,直到平衡。静置约15 min,待完全相分离后,取少量油相进行HPLC检测。水相对映体浓度可由物料衡算得到。
(2) 反萃取过程
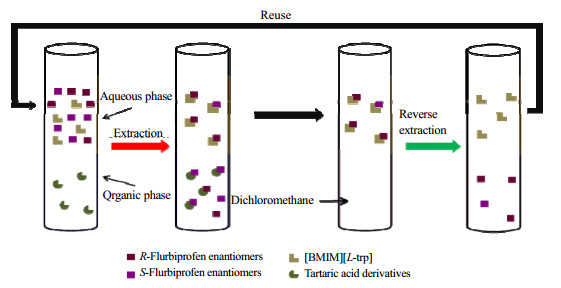
分离萃取后的水相,与等体积的二氯甲烷混合,在25 ℃下恒温震荡约2 h。静置15 min直到相分离,分离上层含[BMIM][L-trp]的水相,调节pH后可再次用于萃取过程。过程示意图如图 2所示。
|
图 2 实验过程示意图 Fig.2 Schematic diagram of the experimental process |
油相中氟比洛芬对映体的浓度通过带有紫外检测器的高效液相色谱系统(Agilent 1260 Infinity II)检测。色谱柱为CHIRALPAK IG (5 μm, 4.6 mm× 250 mm),柱温20 ℃,检测波长为254 nm。流动相为w(三氟乙酸) = 0.1%的正己烷:乙醇= 95:5 (体积比),进样量为20 μL,流量为1 mL·min-1。两对映体的峰可基线分离,且通过单对映体标准品检验,R-氟比洛芬保留时间少于S-氟比洛芬。
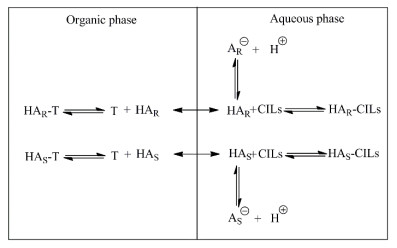
2.4 实验原理萃取平衡及反应机理如图 3所示。平衡机理主要包含3部分,氟比洛芬分子在两相间的物理分配平衡,氟比洛芬在水相的溶解平衡,氟比洛芬与手性选择剂形成络合物的络合平衡。这里由于氢键、静电作用、范德华力、位阻作用等,氟比洛芬对映体与两种手性选择剂共形成四种非对映异构体,依据其自由能的差异而实现分离。
对映体在平衡状态的分配系数K和选择性系数α是描述系统萃取效率的重要参数。本研究中可由以下各式求得:
|
图 3 氟比洛芬萃取机理 Fig.3 Mechanism of flurbiprofen extraction HAR and HAS: R-flurbiprofen and S-flurbiprofen molecules AR-and A: R-flurbiprofen and S-flurbiprofen ionics T and CILs: tartaric acid derivatives and chiral ionic liquids |
| $ {K_{\rm{S}}} = \frac{{{C_{{\rm{O}}, {\rm{S}}}}}}{{{C_{{\rm{W}}, {\rm{S}}}}}} $ | (1) |
| $ {K_{\rm{R}}} = \frac{{{C_{{\rm{O}}, R}}}}{{{C_{{\rm{W}}, R}}}} $ | (2) |
| $ \alpha = \frac{{{K_{\rm{S}}}}}{{{K_{\rm{R}}}}} $ | (3) |
其中CO, S和CW, S分别代表S-氟比洛芬在油相和水相中的浓度,CO, R和CW, R分别代表R-氟比洛芬在油相和水相中的浓度,KS和KR分别代表S-氟比洛芬和R-氟比洛芬的分配系数。α为体系的操作选择性系数,其上限是内在选择性系数,也就是生成络合物的比值。
3 实验结果与讨论 3.1 筛选酒石酸酯种类基于先前氟比洛芬单相识别萃取的研究工作[30],选择[BMIM][L-trp]作为水相萃取剂,浓度为0.02 mol·L-1。酒石酸酯作为油相萃取剂,考察种类及烷基链长度的影响,结果如表 1所示。从表 1可以看出,在单相识别的基础上,油相中添加酒石酸酯后,两种氟比洛芬对映体的分配系数均有上升,这是由于酒石酸酯与氟比洛芬分子间的相互作用所致。当D-酒石酸酯用作手性萃取剂时,体系选择性系数有明显增加,而选择L-酒石酸酯时选择性则有一定程度的降低,表明D-酒石酸酯对于S-氟比洛芬有较好的识别作用而L-酒石酸酯则优先识别R-氟比洛芬。对比不同D-酒石酸酯的实验结果可以看出,随烷基链增长选择性系数持续增加,D-酒石酸二辛酯分离效果最好,被用来作为本研究合适的油相萃取剂。
|
|
表 1 酒石酸酯对分配系数和选择性系数的影响 Table 1 Effects of tartaric esters on distribution coefficients and enantioselectivity |
从单相识别到双相识别,加入D-酒石酸二辛酯后,选择性系数由1.21增加至1.30,双相识别萃取体系大大提升了对映体的拆分效果。
3.2 有机溶剂的影响以0.02 mol·L-1的[BMIM][L-trp]为水相萃取剂和0.3 mol·L-1的D-酒石酸二辛酯为油相萃取剂,考察不同有机溶剂种类对于氟比洛芬分配行为的影响,结果如表 2所示。可以看到,当正癸醇和正辛醇用作有机溶剂时,选择性系数较低,这是由于[BMIM][L-trp]在长链脂肪醇中有轻微的溶解。二氯甲烷和氯仿用作有机溶剂时,虽然选择性系数较好,但分配系数过大,这对于实际生产是非常不利的。综合考虑选择性系数和分配系数,选择二氯乙烷作为合适的有机溶剂。
|
|
表 2 有机溶剂种类对分配系数和选择性系数的影响 Table 2 Effects of organic solvents on distribution coefficients and enantioselectivity |
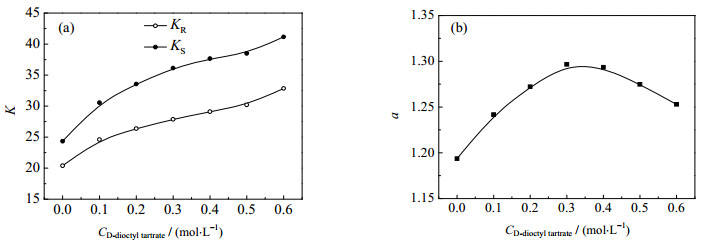
实验配置含0.1到0.6 mol·L-1不同浓度D-酒石酸二辛酯的油相,用于氟比洛芬双相识别拆分过程,考察其对于氟比洛芬萃取分离效果的影响,结果如图 4所示。从图 4可以看出,两种对映体的分配系数都随D-酒石酸二辛酯浓度的增加而上升,这是因为D-酒石酸二辛酯和氟比洛芬对映体通过多种分子间作用力相互作用生成了非对映体络合物,增加了氟比洛芬在油相的溶解度,提高了分配系数。选择性系数则随着D-酒石酸二辛酯浓度的增加先上升后下降,在0.3 mol·L-1处达到最大值。这是因为适量的D-酒石酸二辛酯会增加非对映体络合物浓度,增强识别作用,但过量的手性识别剂会与氟比洛芬对映体非选择性结合,削弱了手性识别作用,造成选择性系数的下降。
|
图 4 D-酒石酸二辛酯浓度对分配系数(a)和选择性系数(b)的影响 Fig.4 Effects of D-dioctyl tartrate concentrations on distribution coefficients (a) and enantioselectivity (b) |
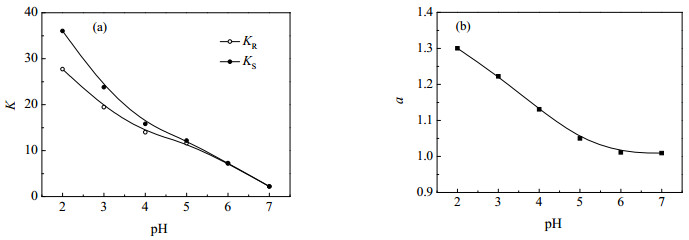
缓冲溶液的pH是萃取过程的重要影响因素,实验配置了pH 2~7的0.3 mol·L-1的磷酸盐缓冲溶液,并用于氟比洛芬的双相识别萃取,结果如图 5所示。从图 5可见,pH值能显著影响氟比洛芬在两相的分配和选择性,两种对映体的分配系数和选择性系数都随着pH的升高而急剧下降,这点与只含[BMIM][L-trp]的单相识别体系十分类似。因为pH能影响氟比洛芬分子在水相中的形态和溶解度,而两种手性选择剂对分子态的氟比洛芬有较强的识别能力[28]。因此,较低的pH是有利于萃取过程的。本实验优化的pH选为2.0。
|
图 5 pH值对分配系数(a)和选择性系数(b)的影响 Fig.5 Effects of pH on distribution coefficients (a) and enantioselectivity (b) CD-Dioctyl tartrate = 0.3 mol·L-1, C[BMIM][L-trp] = 0.02 mol·L-1, Cflurbiprofen = 50 μg·mL-1, 25 ℃, solvent: ClCH2CH2Cl |
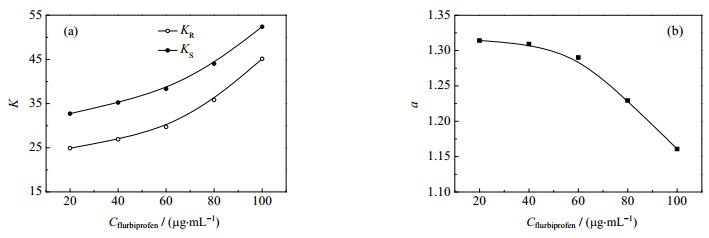
初始加入氟比洛芬消旋体的量代表萃取体系的处理能力且能影响生成非对映体络合物的浓度,影响选择性,因此,配置氟比洛芬浓度20~100 μg·mL-1的多个双相识别萃取体系,萃取结果列于图 6。与单相识别类似,受限于氟比洛芬在水相的溶解度,当初始氟比洛芬浓度上升时,分配系数单调增加,而选择性下降。在初始氟比洛芬浓度较低时,选择性系数下降缓慢,初始浓度60 μg·mL-1时仍能保持1.30左右。但在较高的初始浓度下,由于非选择作用的增强,选择性是相对较差的。为了便于对比,本实验选择50 μg·mL-1作为合适的氟比洛芬初始浓度。
|
图 6 初始氟比洛芬消旋体浓度对分配系数(a)和选择性系数(b)的影响 Fig.6 Effects of initial racemic flurbiprofen concentrations on distribution coefficients (a) and enantioselectivity (b) CD-Dioctyl tartrate = 0.3 mol·L-1, C[BMIM][L-trp] = 0.02 mol·L-1, pH = 2.0, 25 ℃, solvent: ClCH2CH2Cl |
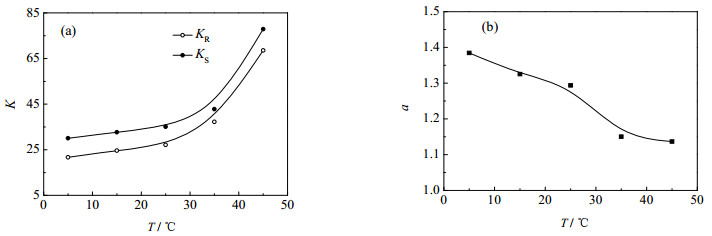
温度是萃取过程的重要参数,双相手性识别萃取体系在5~45 ℃的萃取效果如图 7所示。随着温度的增加,分配系数迅速上升,尤其在较高的温度区域;而选择性系数则逐渐下降。在5 ℃下,体系选择性系数能达到1.38;在室温附近,仍能保持在1.30以上。随着萃取温度的进一步增加,选择性系数快速下降,这是由于在较高温度下手性选择剂和药物对映体间的相互作用大大降低了。总体来说,双相识别手性萃取在低温下显示了良好的分离效果并且在室温附近保持了不错的拆分能力。
|
图 7 萃取温度对分配系数(a)和选择性系数(b)的影响 Fig.7 Effects of temperatures on distribution coefficients (a) and enantioselectivity (b) |
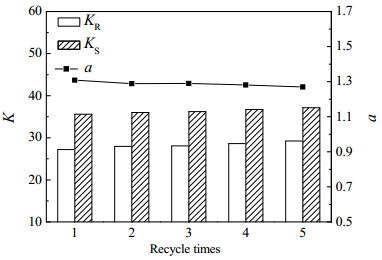
本研究利用回用整个水相的反萃取过程实现手性离子液体的回收再利用,无需经过分离纯化。综合考虑溶剂的毒性和反萃取率,使用分配系数更高的二氯甲烷替代二氯乙烷作为反萃取有机溶剂。HPLC分析结果显示反萃取后水相氟比洛芬浓度低于0.2 μg·mL-1,反萃取率高达98%。再生的水相5次循环回用结果如图 8所示。在重复使用水相5次后,分配系数略微增加,体系选择性系数仍保持在1.25以上。与初始水相相比,循环使用的水相与含D-酒石酸二辛酯的油相组成的双相识别萃取系统,仍然显示了良好的协同萃取效果。
|
图 8 水相循环次数对分配系数和选择性系数的影响 Fig.8 Distribution coefficients and enantioselectivity of flurbiprofen after different recycle usages CD-Dioctyl tartrate = 0.3 mol·L-1, C[BMIM][L-trp] = 0.02 mol·L-1, Cflurbiprofen = 50 μg·mL-1; pH = 2.0, 25 ℃; solvent: ClCH2CH2Cl |
(1) 合成的8种酒石酸酯对于氟比洛芬均有一定识别作用,其中D-酒石酸酯类优先识别S-氟比洛芬对映体,D-酒石酸二辛酯作为油相萃取剂与[BMIM][L-trp]具有最好的协同萃取效果。
(2) 在二氯乙烷为溶剂,D-酒石酸二辛酯浓度0.3 mol·L-1,氟比洛芬初始浓度50 μg·mL-1,pH = 2.0,5 ℃时,体系选择性系数达到1.38,在室温附近仍能保持在1.30以上。相比于单相识别,双相识别手性液液萃取选择性系数得到明显改善。
(3) 通过反萃取过程实现了手性离子液体的循环回用,再生的水相仍然具有良好的拆分效果。
(4) 本研究为更多手性药物的双相识别手性液液萃取系统的开发提供了参考。进一步提高氟比洛芬浓度和选择性系数,研究多级萃取分离过程是后续需要考虑的内容。
| [1] |
HUTT A J, TAN S C. Drug chirality and its clinical significance[J]. Drugs, 1996, 52: 1-12. |
| [2] |
AGRANAT I, CANER H, CALDWELL A. Putting chirality to work:The strategy of chiral switches[J]. Nature Reviews Drug Discovery, 2002, 1(10): 753-768. DOI:10.1038/nrd915 |
| [3] |
BROOKS W H, GUIDA W C, DANIEL K G. The significance of chirality in drug design and development[J]. Current Topics in Medicinal Chemistry, 2011, 11(7): 760-770. DOI:10.2174/156802611795165098 |
| [4] |
KASPRZYK-HORDERN B. Pharmacologically active compounds in the environment and their chirality[J]. Chemical Society Reviews, 2010, 39(11): 4466-4503. DOI:10.1039/c000408c |
| [5] |
SOLANO D M, HOYOS P, HERNAIZ M J, et al. Industrial biotransformations in the synthesis of building blocks leading to enantiopure drugs[J]. Bioresource Technology, 2012, 115: 196-207. DOI:10.1016/j.biortech.2011.11.131 |
| [6] |
HAWKINS J M, WATSON T J N. Asymmetric catalysis in the pharmaceutical industry[J]. Angewandte Chemie-International Edition, 2004, 43(25): 3224-3228. DOI:10.1002/anie.200330072 |
| [7] |
LU Y H, WANG X J, CHING C B. Application of preferential crystallization for different types of racemic compounds[J]. Industrial & Engineering Chemistry Research, 2009, 48(15): 7266-7275. |
| [8] |
MURATA T, KAWANISHI T, SEKIGUCHI A, et al. Kinetic resolution of racemic 2-hydroxyamides using a diphenylacetyl component as an acyl source and a chiral acyl-transfer catalyst[J]. Molecules, 2018, 23(8): 2003. DOI:10.3390/molecules23082003 |
| [9] |
SIKORA A, SIODMIAK T, MARSZALL M P. Kinetic resolution of profens by enantioselective esterification catalyzed by candida antarctica and candida rugosa lipases[J]. Chirality, 2014, 26(10): 663-669. DOI:10.1002/chir.22362 |
| [10] |
WARD T J, BAKER B A. Chiral separations[J]. Analytical Chemistry, 2008, 80(12): 4363-4372. DOI:10.1021/ac800662y |
| [11] |
李晨亮, 张毅军, 赵富强, 等. 奎宁叔丁基氨基甲酸酯衍生物手性整体柱的制备及应用[J]. 高校化学工程学报, 2018, 32(5): 1210-1216. LI C L, ZHANG Y J, ZHAO F Q, et al. Preparation and application of a chiral monolithic column made of quininetert-butylcarbamoyl derivatives[J]. Journal of Chemical Engineering of Chinese Universities, 2018, 32(5): 1210-1216. DOI:10.3969/j.issn.1003-9015.2018.00.016 |
| [12] |
HIGUCHI A, TAMAI M, KO Y A, et al. Polymeric membranes for chiral separation of pharmaceuticals and chemicals[J]. Polymer Reviews, 2010, 50(2): 113-143. DOI:10.1080/15583721003698853 |
| [13] |
TANG K W, ZHANG P L, PAN C Y, et al. Equilibrium studies on enantioselective extraction of oxybutynin enantiomers by hydrophilic beta-cyclodextrin derivatives[J]. AIChE Journal, 2011, 57(11): 3027-3036. DOI:10.1002/aic.12513 |
| [14] |
SCHUUR B, VERKUIJL B J V, MINNAARD A J, et al. Chiral separation by enantioselective liquid-liquid extraction[J]. Organic & Biomolecular Chemistry, 2011, 9(1): 36-51. |
| [15] |
张维阳, 崔兴, 蒋淑娴, 等. L-酒石酸二乙酯萃取拆分氧氟沙星对映体的研究[J]. 高校化学工程学报, 2017, 31(4): 769-775. ZHANG W Y, CUI X, JIANG S X, et al. Enantiseparation of ofloxacin enantimers via diethyl l-tartrate extraction[J]. Journal of Chemical Engineering of Chinese Universities, 2017, 31(4): 769-775. DOI:10.3969/j.issn.1003-9015.2017.04.003 |
| [16] |
黄钰清, 鲍宗必, 邢华斌, 等. 手性萃取剂与液-液萃取拆分对映体技术研究进展[J]. 化工进展, 2015, 34(12): 4324-4332. HUANG Y Q, BAO Z B, XING H B, et al. Chiral extractants and enantioselective liquid-liquid extraction[J]. Chemical Industry and Engineering Progress, 2015, 34(12): 4324-4332. |
| [17] |
HUANG X Y, QUAN K J, PEI D, et al. The development of biphasic chiral recognition in chiral separation[J]. Chirality, 2018, 30(8): 974-981. DOI:10.1002/chir.22975 |
| [18] |
崔兴, 于飞, 朱海, 等. 手性离子液体拆分对映体技术研究进展[J]. 高校化学工程学报, 2016, 30(6): 1229-1240. CUI X, YU F, ZHU H, et al. Review on enantioseparation using chiral ionic liquids[J]. Journal of Chemical Engineering of Chinese Universities, 2016, 30(6): 1229-1240. |
| [19] |
DING Q, CUI X, XU G H, et al. Quantum chemistry calculation aided design of chiral ionic liquid-based extraction system for amlodipine separation[J]. AIChE Journal, 2018, 64(11): 4080-4088. DOI:10.1002/aic.16372 |
| [20] |
KIMARU I W, MORRIS L, VASSILIOU J, et al. Synthesis and evaluation of L-phenylalanine ester-based chiral ionic liquids for GC stationary phase ability[J]. Journal of Molecular Liquids, 2017, 237: 193-200. DOI:10.1016/j.molliq.2017.04.079 |
| [21] |
练伟平, 崔兴, 丁琦, 等. 1-丁基-3-甲基咪唑L-色氨酸萃取拆分酮洛芬对映体的研究[J]. 高校化学工程学报, 2018, 32(5): 1147-1152. LIAN W P, CUI X, DING Q, et al. Enantioseparation of ketoprofen enantiomers with 1-butyl-3-methylimidazole l-tryptophan extraction[J]. Journal of Chemical Engineering of Chinese Universities, 2018, 32(5): 1147-1152. DOI:10.3969/j.issn.1003-9015.2018.05.021 |
| [22] |
TANG K W, YI J M, HUANG K L, et al. Biphasic recognition chiral extraction:A novel method for separation of mandelic acid enantiomers[J]. Chirality, 2009, 21(3): 390-395. DOI:10.1002/chir.20601 |
| [23] |
TANG K W, SONG L T, LIU Y B, et al. Enantioselective partitioning of 2-phenylpropionic acid enantiomers in a biphasic recognition chiral extraction system[J]. Chemical Engineering Journal, 2012, 180: 293-298. DOI:10.1016/j.cej.2011.11.065 |
| [24] |
BROGDEN R N, HEEL R C, SPEIGHT T M, et al. Fenbufen-A review of its pharmacological properties and therapeutic use in rheumatic diseases and acute pain[J]. Drugs, 198, 21(1): 1-22. |
| [25] |
WECHTER W J, BIGORNIA A E, MURRAY E D, et al. Rac-flurbiprofen is more ulcerogenic than its (S)-enantiomer[J]. Chirality, 1993, 5(7): 492-494. DOI:10.1002/chir.530050703 |
| [26] |
GEERTS H. Drug evaluation:(R)-flurbiprofen-An enantiomer of flurbiprofen for the treatment of alzheimer's disease[J]. Drugs, 2007, 10(2): 121-133. |
| [27] |
ZEMSKOVA M, WECHTER W, BASHKIROVA S, et al. Gene expression profiling in R-flurbiprofen-treated prostate cancer:R-flurbiprofen regulates prostate stem cell antigen through activation of akt kinase[J]. Biochemical Pharmacology, 2006, 72(10): 1257-1267. DOI:10.1016/j.bcp.2006.07.028 |
| [28] |
TANG K W, SONG L T, LIU Y B, et al. Separation of flurbiprofen enantiomers by biphasic recognition chiral extraction[J]. Chemical Engineering Journal, 2010, 158(3): 411-417. DOI:10.1016/j.cej.2010.01.009 |
| [29] |
CHEN Z, ZHANG W, WANG L P, et al. Enantioseparation of racemic flurbiprofen by aqueous two-phase extraction with binary chiral selectors of L-dioctyl tartrate and L-tryptophan[J]. Chirality, 2015, 27(9): 650-657. DOI:10.1002/chir.22481 |
| [30] |
CUI X, DING Q, SHAN R N, et al. Enantioseparation of flurbiprofen enantiomers using chiral ionic liquids by liquid-liquid extraction[J]. Chirality, 2019, 31(6): 457-467. DOI:10.1002/chir.23071 |
| [31] |
HELDIN E, LINDNER K J, PETTERSSON C, et al. Tartaric acid-derivatives as chiral selectors in liquid-chromatography[J]. Chromatographia, 1991, 32(9-10): 407-416. DOI:10.1007/BF02327970 |
| [32] |
刘斌, 赵建强, 周鸣强. 酒石酸酯化物的合成与应用研究进展[J]. 合成化学, 2016, 24(3): 266-276. LIU B, ZHAO J Q, ZHOU M Q. Research progress of synthesis and applications of tartaric esters[J]. Chinese Journal of Synthetic Chemistry, 2016, 24(3): 266-276. |




