2. 美国奥本大学 化学工程学院,阿拉巴马奥本 36849
2. Department of Chemical Engineering, Auburn University, Auburn 36849, USA
硫化物燃烧后会生成SOx,不仅腐蚀汽车发动机,还会造成环境污染,危害人体健康。随着环境污染的日趋严重,环保法规也日益严格。世界各国对于燃油中的硫含量提出了严格的要求[1~3],美国环境保护署规定,汽油中硫含量不超过30 μg·g-1[4],欧盟国家要求汽油中的硫含量小于10 μg·g-1[5]。2013年底中国发布的国V车用汽油标准,规定汽油中硫含量不高于10 μg·g-1 [6]。此外,清洁能源生产系统燃料电池对硫含量要求更加严苛[7, 8]。加氢脱硫是目前被广泛采用的燃油脱硫精制技术,能有效脱除燃油中的小分子硫化物,如硫醇、硫醚和二硫化物。但是油品中噻吩类硫化物及其衍生物具有极高的稳定性,在高温(> 400℃)、高压(氢分压 > 3.0 MPa)下难以被加氢脱除[9, 10]。传统的加氢脱硫工艺难以达到低硫燃料油标准,较难实现燃料油的深度脱硫。因此吸附脱硫[11, 12]、氧化脱硫[13]和生物脱硫[14]等非氢脱硫技术近年迅速发展,有望取代现有的加氢脱硫。其中吸附脱硫的操作条件温和,不需要高温、高压,同时也不用H2作为载气,不改变油品性质,成为目前受关注的深度脱硫技术。现阶段,吸附脱硫技术还处于研究阶段,硫化物选择性较差、吸附性能和再生性能低是目前吸附脱硫存在的主要问题。吸附工艺的优化以及吸附机理的研究成为选择性吸附脱硫的主要研究方向。
TiO2是一种性能优越的光催化材料,被广泛用于光催化氧化脱硫中。有机硫化物在TiO2催化剂表面上发生光催化氧化反应[15]。同时,TiO2也是一种常见的脱硫吸附剂,其表面端羟基与有机硫化物进行π耦合, 从而实现硫化物的吸附分离[16]。因此如何提高TiO2吸附剂表面活性端羟基的数量是提升其脱硫性能的关键。本研究在传统吸附脱硫工艺的基础上,首次将紫外光引入动态吸附脱硫过程中,创新开发出光辅助吸附脱硫技术,现阶段并未有相关研究及文献报道。本研究以TiO2为吸附剂,考察此新型脱硫技术对TiO2吸附剂的性能影响,再通过原位红外(in-situ IR)和X射线光电子能谱(XPS)对光辅助吸附脱硫机理进行研究。
2 实验方法 2.1 原料及试剂锐钛型二氧化钛TiO2 (ST61120) (3. 2 mm,Saint-Gobain Norpro公司);硝酸银AgNO3 (分析纯,Alfa Aesar有限公司);苯并噻吩benzothiophene (分析纯,Alfa Aesar化学有限公司产品);正辛烷n-octane (分析纯,Acros Organics公司)。
2.2 吸附剂的制备及模拟燃料油配置称取一定量的二氧化钛原料研磨、筛分,得到850~1400 μm的TiO2颗粒,之后置于烘箱内110℃干燥6 h以上得到干燥TiO2颗粒。再置于管式炉中,在空气气氛下于450℃煅烧2 h,然后冷却至室温,得到TiO2吸附剂。
选择苯并噻吩代表燃料油中含硫化合物,正辛烷代表烃类化合物,配置硫质量浓度比为0.35%的模拟燃料油MF-1。同时为了考察水分子对于吸附剂性能的影响,将蒸馏水加入模拟燃料油中配置成水质量分数为0.1%的含水模拟燃料油MF-2。
2.3 紫外灯设备紧凑式紫外灯UVL-21 (4 W,365 nm)、紫外灯UVL-28 (8 W,365 nm)及UVX-36型辐射计均购于UVP公司。UVL-21紫外灯放置于吸附脱硫固定床反应器两侧,距离UVL-21紫外灯1 cm处的紫外光强度为1.8~2.0 mW·cm-2。UVL-28紫外灯放置于XPS的快速进样室,进样室内的紫外光强度为1.2 mW·cm-2。
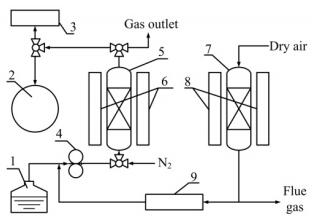
2.4 固定床吸附脱硫实验在常温常压下,采用固定床反应器进行吸附脱硫实验,反应器内径为16 mm、长62 mm的石英管。10.0 g吸附剂装填于反应器底部,两端填满石英棉。将两盏UVL-21紫外光灯置于固定床反应器两侧。吸附脱硫固定床与高温再生装置如图 1所示。关闭紫外灯,向固定床通入干燥高纯N2吹扫床层1 h,之后用进料泵在0.5 mL·min-1流量下抽取模拟燃料油(空速为2 h-1),使其自下而上的通过吸附床层开始传统吸附脱硫实验。
|
图 1 光辅助吸附脱硫及热再生装置 Fig.1 Schematic diagram of the photo-assisted sulfur adsorption setup and the thermal regeneration unit 1. fuel container 2. auto-sampler 3. product container 4. peristaltic pump 5. adsorbent bed 6. UV lamp 7. tube furnace 8. heater 9. condenser |
对于光辅助吸附脱硫实验,在进料泵抽取模拟燃料油的同时打开反应器两侧的紫外灯,进行光辅助穿透实验。在床层出口处定时收集模拟燃料油样品,采用ANTEK公司9000S型硫分析仪检测样品中硫含量,并绘制脱硫穿透曲线。将固定床出口处模拟燃料油的硫质量分数高于0.0035%时作为穿透点,计算得到穿透吸附硫容量。通过研究固定床穿透曲线,分析并计算吸附剂的最大吸附硫容量。
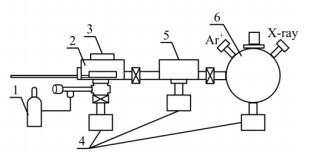
2.5 机理表征采用Kratos公司AXIS Ultra DLD型XPS光电子能谱仪(Al Ka射线,通能20 eV),用C1s = 284. 6 eV为基准进行结合能校正,表征紫外光对TiO2表面活性官能团的影响。将TiO2吸附剂置于XPS样品台上,当真空度优于10-8 Torr后,对样品进行紫外光照射处理,之后将样品移至分析室进行XPS表征,分析室真空度优于10-9 Torr。XPS光电子能谱仪装置见图 2。
|
图 2 X射线光电子能谱装置 Fig.2 Scheme of XPS equipped with UV lamp 1. N2 gas cylinder 2. load lock 3. UV lamp 4. vacuum system 5.sample treatment chamber (STC) 6. sample analysis chamber (SAC) |
采用Nicolet公司IR 100型傅里叶变换红外光谱仪表征紫外光和水分子对TiO2表面活性基团的影响。将TiO2样品薄片装入ZnSe窗片的红外吸收池并通入干燥空气加热至200℃恒温1 h,之后在N2下冷却至室温。高真空状态(100 mTorr)下考察紫外光及水分子对于TiO2表面活性羟基的影响。测定范围是4000~400 cm-1,扫描次数为32次,分辨率为4 cm-1。
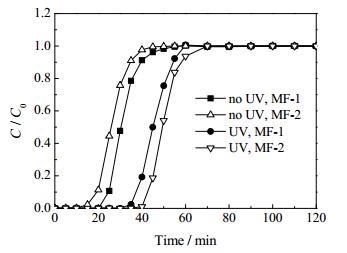
3 结果与讨论 3.1 光辅助吸附脱硫工艺常温常压下,通过固定床吸附实验考察光辅助吸附脱硫工艺下TiO2吸附剂对于模拟燃料油MF-1的吸附性能,以穿透时间对流出液中硫含量C和初始浓度C0的比值C/C0作图,得到传统吸附脱硫及光辅助吸附脱硫条件下TiO2的穿透曲线,如图 3所示。根据穿透曲线计算出TiO2吸附剂在传统吸附脱硫技术及光辅助吸附脱硫下的硫容量。从图 3的穿透曲线可以看出:在传统吸附脱硫条件下,TiO2吸附剂很快达到穿透点,其穿透吸附硫容量仅为2.45 mg S·g-1,而饱和吸附硫容量也只有3.90 mg S·g-1;在光辅助吸附脱硫条件下,TiO2的穿透吸附硫容量为4.05 mg S·g-1,同时最大吸附硫容量也增至5.63 mg S·g-1。结果显示光辅助吸附脱硫技术显著提高了TiO2吸附剂的脱硫性能。利用气相色谱-脉冲光度检测器(GC-PFPD)分析对比模拟燃料油初始样品,传统吸附脱硫中流出液及光辅助吸附脱硫中流出液。模拟燃料油中的苯并噻吩在紫外光照射下未发生光催化氧化反应,因此光辅助吸附脱硫不同于其他光催化氧化脱硫,是一种全新高效的吸附脱硫技术。
|
图 3 在传统及光辅助吸附脱硫工艺下使用模拟燃料油MF-1和MF-2得到的TiO2吸附穿透曲线 Fig.3 Breakthrough curves of MF-1 and MF-2 obtained under traditional and UV-assisted adsorptive desulfurization techniques |
许多研究表示燃料油中的水分会降低酸性吸附剂的硫容量[17],现分别考察传统和光辅助吸附脱硫工艺下含水模拟燃料油MF-2对于TiO2吸附脱硫性能的影响。从图 3及表 1的数据及可以看出,在传统吸附脱硫过程中,水分子大大降低了TiO2的脱硫性能。在光辅助吸附脱硫条件下,使用含水模拟燃料油MF-2,TiO2吸附剂的脱硫能力最大。可能原因是:(1)在无紫外光的条件下,水分子会与TiO2表面的活性羟基形成氢键,减少吸附剂表面的脱硫基团。(2) H2O分子和苯并噻吩分子在TiO2吸附剂上竞争吸附,使得吸附剂的脱硫性能降低。(3)在紫外光下,水分子与TiO2表面的氧空穴发生反应,生成了更多的活性端羟基,因此提高了TiO2吸附剂的脱硫性能。同时,实验结果也表明光辅助脱硫工艺很好地解决了含水燃料油对于吸附剂的负面影响。
|
|
表 1 TiO2在传统吸附脱硫及光辅助吸附脱硫中使用MF-1和MF-2的硫容量 Table 1 Sulfur capacities (MF-1 and MF-2) of TiO2 studied with traditional and UV-assisted adsorptive desulfurization techniques |
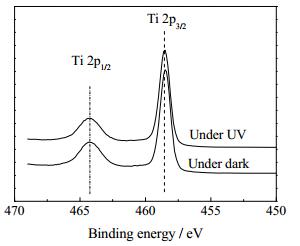
在真空、室温条件下,表征紫外光对TiO2吸附剂表面活性羟基的影响。TiO2吸附剂在无光和有紫外光处理下的Ti2p和O1s的XPS谱见图 4、图 5 (已去除污染碳信号)。从图 4可以看出,对于无紫外光处理样品和紫外光处理样品,出现了两个峰,分别对应于Ti2p1/2和Ti2p3/2。其中Ti2p1/2的结合能为464. 3 eV,Ti2p3/2的结合能为458. 5 eV,表明钛主要以Ti4+的形态存在,没有Ti3+出现[18, 19]。从图 4可以看出,在光辅助吸附脱硫条件下,结合能峰的位置和强度均未发生变化,与无光照条件下基本相同,可以认为紫外光条件不影响Ti4+的价态。
|
图 4 TiO2吸附剂在无紫外光和有紫外光条件下的 Ti 2p XPS谱图 Fig.4 High resolution XPS spectra of Ti 2p for TiO2 samples treated with and without UV |
|
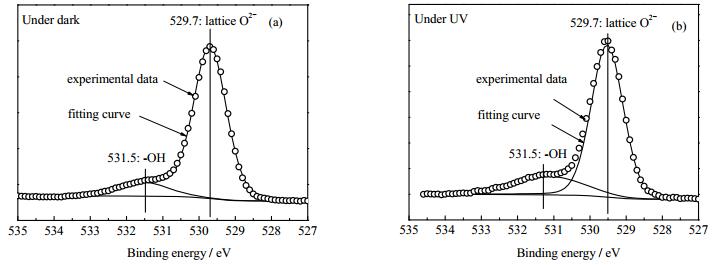
图 5 TiO2吸附剂在无紫外光和有紫外光条件下的O1s XPS谱图 Fig.5 O1s XPS spectra of TiO2 treated with and without UV |
图 5(a)和(b)分别为无光条件和有紫外光照射下TiO2的O1s XPS谱。在两种处理条件下,TiO2均出现两个峰,结合能为529. 7和531. 5 eV,分别对应于晶格O2-以及表面羟基-OH[20~23]。对比图 5(a)和(b)可以看出,在紫外光照射下,各峰的结合能不变,并未发生位置偏移,证明O的价态不受紫外光的影响。
但是从表 2的数据可以看出,-OH/O2-的面积比发生了改变,在无光条件下,此面积比数值为0.13,而经过紫外光照射后,面积比增加至0.25,提高了大约一倍。XPS结果说明:TiO2吸附剂在紫外光辅助条件下能形成更多的羟基基团,从而提高TiO2吸附剂的脱硫性能。
|
|
表 2 紫外光对于TiO2的Ti2p和O1s XPS结合能及-OH/O2-面积比的影响 Table 2 Effects of UV on Ti2p and O1s binding energy (TiO2) and –OH/O2- area ratios |
用原位红外in-situ IR对光辅助吸附脱硫机理进行研究,分别考察紫外光及水分子对TiO2样品表面活性脱硫羟基的影响。研究表明紫外光在ZnSe窗片内不发生光催化反应,因此不考虑紫外光对红外吸收池的影响[24]。图 6为在不同条件下TiO2吸附剂的红外谱图。
|
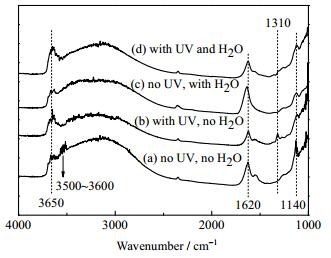
图 6 TiO2在不同条件下的原位红外吸收光谱 Fig.6 In-situ IR spectra (under absorbance mode) of TiO2 treated under different conditions |
由图 6(a)可知,在无紫外光及无水的条件下,3650 cm-1显著的吸收峰为孤立羟基的伸缩振动,说明TiO2吸附剂上本身含有一定量的活性端羟基Ti(Ⅳ)-OH [25, 26]。在3500~3600 cm-1处的吸收峰则归属于桥羟基或氢键羟基,稳定性差,且不具备脱硫活性[27, 28]。而在1620 cm-1的强特征吸收峰为分子态水的弯曲震动吸收峰,说明有大量的水分子吸附于TiO2表面[29, 30]。这说明TiO2吸附剂本身具有一定的吸附脱硫性能,但是其硫容量并不高。从图 6(b)可以看出,在紫外光下,TiO2并未出现新的红外吸收峰,它与无光条件下的TiO2谱图相似。对比图 6(a)和(b)的红外谱图发现,紫外光条件下,TiO2吸附剂表面的化学吸附水分子(1650 cm-1)及桥羟基(3500~3600 cm-1)数量大大减少,而活性端羟基(3650 cm-1)数量则明显增加,端羟基能与有机硫化物进行π耦合[16]。因此TiO2吸附剂在紫外光辅助吸附条件下的硫容量得到显著提高,这也与之前XPS得出的结论一致。图 6(c)为无光条件下通入水分子后TiO2吸附剂的红外光谱谱图。与图 6(a)对比发现,化学吸附水分子的特征吸收峰(1620 cm-1)强度显著增强,Ti(Ⅳ)-OH的特征吸收峰(3650 cm-1)强度稍有减弱,同时TiO2上几乎没有桥羟基的吸收峰(3500~3600 cm-1),说明水分子与大部分桥联羟基以及部分自由羟基以氢键相结合。可见在无紫外光情况下,燃料油中的水分子会使得TiO2吸附剂失去一部分活性脱硫中心,从而降低其脱硫能力。图 6(d)为在紫外光条件下水分子在TiO2吸附剂上的红外光谱谱图。对比图 6(c)和(d)可以看出,在紫外光下,化学吸附态的水分子数量明显减少,同时活性脱硫基团Ti(Ⅳ)-OH吸收峰强度增加。另外,图 6(d)中TiO2在3650 cm-1的特征吸收峰达到最强。这说明光辅助脱硫不仅能有效阻止水分子降低TiO2吸附剂的硫容量,而且紫外光和水分子的共同作用还能进一步提高TiO2表面的活性脱硫羟基数量。因此,光辅助吸附脱硫技术不仅提高了TiO2吸附剂的脱硫性能,还妥善解决了含水燃料油对吸附剂的影响。
4 结论(1) 将紫外光引入动态吸附脱硫工艺,开发出新型光辅助吸附脱硫工艺,是一种全新高效的深度脱硫技术。
(2) 光辅助吸附脱硫将TiO2吸附剂在传统吸附脱硫条件下的性能提高了近1倍,还解决了含水燃料油对于吸附剂的负面影响。
(3) 光辅助吸附脱硫与传统吸附脱硫条件下的TiO2吸附剂相比,具有较少的化学吸附水分子和更多的活性脱硫羟基Ti(Ⅳ)-OH,因此脱硫性能更佳。
| [1] | Srivastava V C. An evaluation of desulfurization technologies for sulfur removal from liquid fuels[J]. RSC Advances , 2012, 2(3): 759-783. DOI:10.1039/C1RA00309G. |
| [2] | Song C S. An overview of new approaches to deep desulfurization for ultra-clean gasoline, diesel fuel and jet fuel[J]. Catalysis Today , 2003, 86(1-4): 211-263. DOI:10.1016/S0920-5861(03)00412-7. |
| [3] | Babich I V, Moulijn J A. Science and technology of novel processes for deep desulfurization of oil refinery streams:a review[J]. Fuel , 2003, 82(6): 607-631. DOI:10.1016/S0016-2361(02)00324-1. |
| [4] | Stanislaus A, Marafi A, Rana M S. Recent advances in the science and technology of ultra low sulfur diesel (ULSD) production[J]. Catalysis Today , 2010, 153(1-2): 1-68. DOI:10.1016/j.cattod.2010.05.011. |
| [5] | ZHOU Wei(周威), XU Wan-zhen(徐婉珍), HUANG Wei-hong(黄卫红), et al. Advance in adsorptive desulfurization(吸附脱硫研究进展)[J]. Environmental Science & Technology(环境科学与技术) , 2012, 35(1): 122-128. |
| [6] | WANG Yun-fang(王云芳), YIN Feng-li(尹风利), SHI De-qing(史德清), et al. Progress in deep desulfurization for vehicle fuel oil by adsorption(车用燃料油吸附法深度脱硫技术进展)[J]. Petrochemical Technology(石油化工) , 2006, 35(1): 94-99. |
| [7] | Katikaneni S, Gaffney A M, Song C S. Fuel processing for fuel cell applications[J]. Catalysis Today , 2002, 77(1-2): 1-2. DOI:10.1016/S0920-5861(02)00229-8. |
| [8] | Song C S. Fuel processing for low-temperature and high-temperature fuel cells:challenges, and opportunities for sustainable development in the 21st century[J]. Catalysis Today , 2002, 77(1-2): 17-49. DOI:10.1016/S0920-5861(02)00231-6. |
| [9] | Shafi R, Hutchings G J. Hydrodesulfurization of hindered dibenzothiophenes:an overview[J]. Catalysis Today , 2000, 59(3-4): 423-442. DOI:10.1016/S0920-5861(00)00308-4. |
| [10] | Girgis M J, Gates B C. Reactivities, reaction networks, and kinetics in high-pressure catalytic hydroprocessing[J]. Industrial & Engineering Chemistry Research , 1991, 30(9): 2021-2058. |
| [11] | Hernandez-Maldonado A J, Yang R T. Desulfurization of transportation fuels by adsorption[J]. Catalysis Reviews, Science and Engineering , 2004, 46(2): 111-150. DOI:10.1081/CR-200032697. |
| [12] | SHI Xue-mei(时雪梅), LIU Ming(刘民), GUO Xin-wen(郭新闻), et al. Investigation of adsorption desulfurization of gasoline by AgY and AgMgY adsorbents(AgY和AgMgY吸附剂吸附脱硫性能的考察)[J]. Modern Chemical Industry(现代化工) , 2011, 31(8): 50-53. |
| [13] | Sundararaman R, Song C S. Catalytic oxidative desulfurization of diesel fuels using air in a two-step approach[J]. Industrial & Engineering Chemistry Research , 2014, 53(5): 1890-1899. |
| [14] | Boniek D, Figueiredo D, Dos Santos A F B, et al. Biodesulfurization:a mini review about the immediate search for the future technology[J]. Clean Technologies and Environmental Policy , 2015, 17(1): 29-37. DOI:10.1007/s10098-014-0812-x. |
| [15] | Wang L, Cai H J, Li S Z, et al. Ultra-deep removal of thiophene compounds in diesel oil over catalyst TiO2/Ni-ZSM-5 assisted by ultraviolet irradiating[J]. Fuel , 2013, 105(2): 752-756. |
| [16] | Nair S, Hussain A H M, Tatarchuk B J. The role of surface acidity in adsorption of aromatic sulfur heterocycles from fuels[J]. Fuel , 2013, 105(2): 695-704. |
| [17] | Kulkarni A P, Muggli D S. The effect of water on the acidity of TiO2 and sulfated titania[J]. Applied Catalysis A:General , 2006, 302(2): 274-282. DOI:10.1016/j.apcata.2006.01.033. |
| [18] | Kumar P M, Badrinarayanan S, Sastry M. Nanocrystalline TiO2 studied by optical, FTIR and X-ray photoelectron spectroscopy:correlation to presence of surface states[J]. Thin Solid Films , 2000, 358(1-2): 122-130. DOI:10.1016/S0040-6090(99)00722-1. |
| [19] | XUE Qin(薛琴), GUAN Yu-jiang(管玉江), WANG Zi-bo(王子波), et al. Preparation of nitrogen doped TiO2 nanotube arrays and its visible light responsive photocatalytic properties(N掺杂TiO2纳米管阵列的制备及可见光光催化性能研究)[J]. ActaChimicaSinica(化学学报) , 2010, 68(16): 1603-1608. |
| [20] | Erdem B, Hunsicker R A, Simmons G W, et al. XPS and FTIR surface characterization of TiO2 particles used in polymer encapsulation[J]. Langmuir , 2001, 17(9): 2664-2669. DOI:10.1021/la0015213. |
| [21] | Simmons G W, Beard B C. Characterization of acid-base properties of the hydrated oxides on iron and titanium metal-surfaces[J]. Journal of Physical Chemistry , 1987, 91(5): 1143-1148. DOI:10.1021/j100289a025. |
| [22] | Ohtsu N, Masahashi N, Mizukoshi Y, et al. Hydrocarbon decomposition on a hydrophilic TiO2 surface by UV irradiation:spectral and quantitative analysis using in-situ XPS technique[J]. Langmuir , 2009, 25(19): 11586-11591. DOI:10.1021/la901505m. |
| [23] | Lampimaki M, Schreiber S, Zelenay V, et al. Exploring the environmental photochemistry on the TiO2(110) surface in situ by near ambient pressure X-ray photoelectron spectroscopy[J]. Journal of Physical Chemistry C , 2015, 119(13): 7076-7085. DOI:10.1021/jp511340n. |
| [24] | Nakamura R, Imanishi A, Murakoshi K, et al. In situ FTIR studies of primary intermediates of photocatalytic reactions on nanocrystalline TiO2 films in contact with aqueous solutions[J]. Journal of the American Chemical Society , 2003, 125(24): 7443-7450. DOI:10.1021/ja029503q. |
| [25] | Szczepankiewicz S H, Colussi A J, Hoffmann M R. Infrared spectra of photoinduced species on hydroxylated titania surfaces[J]. Journal of Physical Chemistry B , 2000, 104(42): 9842-9850. DOI:10.1021/jp0007890. |
| [26] | Hadjiivanov K I, Klissurski D G. Surface chemistry of titania (anatase) and titania-supported catalysts[J]. Chemical Society Reviews , 1996, 25(1): 61-69. DOI:10.1039/cs9962500061. |
| [27] | Deiana C, Fois E, Coluccia S, et al. Surface structure of TiO2 P25 nanoparticles:infrared study of hydroxy groups on coordinative defect sites[J]. Journal of Physical Chemistry C , 2010, 114(49): 21531-21538. DOI:10.1021/jp107671k. |
| [28] | LIN Hua-xiang(林华香), WANG Xu-xu(王绪绪), FU Xian-zhi(付贤智). Properties and distribution of the surface hydroxyl groups of TiO2(TiO2表面羟基及其性质)[J]. Progress in Chemistry(化学进展) , 2007, 19(5): 665-670. |
| [29] | Panayotov D A, Yates J T. Depletion of conduction band electrons in TiO2 by water, chemisorption:IR spectroscopic studies of the independence of Ti-OH frequencies on electron concentration[J]. Chemical Physics Letters , 2005, 410(1-3): 11-17. DOI:10.1016/j.cplett.2005.03.146. |
| [30] | Bezrodna T, Puchkovska G, Shymanovska V, et al. IR-analysis of H-bonded H2O on the pure TiO2 surface[J]. Journal of Molecular Structure , 2004, 700(1-3): 175-181. DOI:10.1016/j.molstruc.2003.12.057. |




