棕榈酸异丙酯作为一种重要的化工产品在日常生活中发挥着重要作用[1, 2],而近年来棕榈酸异丙酯因具备生物柴油的特性再次引起人们的关注[3, 4]。文献报道的棕榈酸异丙酯的合成方法主要有酰氯法[5]、离子交换树脂法、直接酯化法[6]、棕榈油-甲醇法[6],在工业上广泛应用的是直接酯化法。该反应是可逆反应,其反应器流出物的主要成分是棕榈酸异丙酯、水和未反应完全的异丙醇或棕榈酸。如何纯化棕榈酸异丙酯,回收异丙醇或棕榈酸以便于循环使用是工业应用中必须解决的实际问题。井强山[7]提出直接酯化法制备棕榈酸异丙酯过程中,利用苯(或甲苯)-异丙醇-水三相混合物组成恒沸剂带出水,反应产物后处理先用水洗再用10%(wt)Na2CO3溶液洗涤未反应完全的棕榈酸,然后用清水洗涤至中性,进行常压蒸馏,蒸出苯或甲苯以循环利用,剩余物(粗酯)进行减压蒸馏,得到精酯。刘群[6]提出用4A分子筛吸附脱水技术合成棕榈酸异丙酯,常压下回收过量的异丙醇,中和、水洗、常压脱水,得到无色透明液体,即为精酯。耿再新、白银鸽[8~11]提出的“两步法”合成生物柴油组分脂肪酸酯专利技术,即脂肪酸经酰氯化、醇解生产脂肪酸酯,反应原理如下:
| $\begin{array}{l} {{\rm{R}}^1} - {\rm{COOH}} + {\rm{SOC}}{{\rm{l}}_2} \to {{\rm{R}}^1} - {\rm{COCl}} + {\rm{S}}{{\rm{O}}_2} + {\rm{HCl}}\\ {{\rm{R}}^1} - {\rm{COCl}} + {{\rm{R}}^2} - {\rm{OH}} \to {{\rm{R}}^1} - {\rm{COO}}{{\rm{R}}^2} + {\rm{HCl}} \end{array}$ |
在该合成方法基础上,以棕榈酸、氯化亚砜、异丙醇为原料,进行棕榈酸异丙酯的合成。由于反应生成物中酸性气体的残存,以及原料异丙醇和氯化亚砜的过量,使得产品中除了含有酸性无机物外,还含有过量的异丙醇和氯化亚砜等,工艺上需要对反应器中出来的粗产品进行纯化。异丙醇与水互溶,而棕榈酸异丙酯不溶于水,尽管异丙醇与棕榈酸甲酯的沸点差异较大,可用精馏的方法加以回收,但考虑到氯化亚砜和酸性无机物不易去除,故需要采用水洗技术对粗品进行提纯。针对此工艺选用水作为溶剂,用萃取分离技术提纯棕榈酸异丙酯,目前棕榈酸异丙酯+异丙醇+水三元物系的液液平衡数据尚无文献报道,因而,本研究用平衡法[13, 14]测定了该常压下棕榈酸异丙酯+异丙醇+水三元物系的液液相平衡数据,并用NRTL模型和UNIQUAC模型进行模拟关联实验数据[15~24],得到三元二组分之间的相互作用参数,为产物棕榈酸异丙酯分离提纯的过程设计和流程模拟提供基础数据。
2 实验材料和方法 2.1 实验药品与仪器棕榈酸异丙酯(上海晶纯生化科技股份有限公司),异丙醇和正硅酸乙酯(天津科密欧化学试剂有限公司),甲苯(洛阳吴华化学试剂有限公司),以上化学试剂皆为市售分析纯。水(去离子水,自制)。
LRY-Ⅱ型低温水浴仪(郑州市化工制冷研究所),XK78-1型磁力搅拌器(姜堰市新康医疗器械有限公司),BS-110-S型分析天平(北京赛多利斯天平有限公司),THZ-98A型恒温振荡箱(上海一恒科技有限公司),GC900型气相色谱仪(上海科创色谱仪器有限公司)。
2.2 分析条件棕榈酸异丙酯的定量分析方法为气相色谱内标法。分析条件:SE-54毛细管柱(30 m×0.53 mm×1 μm),流量40 mL⋅min-1,载气柱前压:0.4 MPa,氢气流量:20 mL⋅min-1,程序升温,柱温初温90℃,保持2 min,以30℃⋅min-1升至280℃,保持1 min,汽化室温度:240℃,检测器温度:280℃。进样量2 μL。分析用溶剂和内标物分别是甲苯和正硅酸乙酯。
2.3 实验过程配制一系列已知不同组成的三元混合物于碘量瓶中,将碘量瓶置于恒温振荡箱中,充分振荡2 h后确保液液两相达到平衡,在恒温振荡箱中静置分层8 h。用针筒注射器分别抽取上、下两相的样品5 mL于容量瓶中,在精密电子天平(±0.00001)上精确称取质量,并用甲苯定容到10 mL,分别加入相同量(0.2 mL)的正硅酸乙酯,按照2.2节的分析方法测定样品中棕榈酸异丙酯、异丙醇和水的质量分数,得到三元体系的液液相平衡数据。
2.4 液液相平衡数据的关联模型 2.4.1 NRTL模型NRTL模型是基于局部组成概念、混合溶液非随机性等的考虑下,得出的活度系数模型关联式[18~21],主要适用于极性与非极性混合物,强非理想混合物和部分互溶体系。NRTL模型的表达式如式(1) ~ (2)所示。
| $\ln {\gamma _i} = \frac{{\sum\limits_j {{\tau _{ji}}{G_{ji}}{x_j}} }}{{\sum\limits_k {{G_{ki}}{x_k}} }} + \sum\limits_j {\frac{{{G_{ij}}{x_j}}}{{{G_{kj}}{x_k}}}} \left[ {{\tau _{ij}} - \frac{{\sum\limits_l {{\tau _{lj}}{G_{lj}}{x_l}} }}{{\sum\limits_k {{G_{kj}}{x_k}} }}} \right]$ | (1) |
其中:
| ${\tau _{ji}} = \frac{{{g_{ji}} - {g_{ii}}}}{{RT}},{G_{ji}} = \exp \left( { - {\alpha _{ji}}{\tau _{ji}}} \right),{\alpha _{ji}} = {\alpha _{ij}}$ | (2) |
式中,gij为i、j两组分间的互相作用能量参数;αij是与混合物非自由度相关、组元之间的可调性常数或非随机参数;τij或(gji-gii)为二元相互作用参数或称模型参数。本文采用NRTL模型模拟过程中,三个体系的非随机参数α均取固定值0.3。
2.4.2 UNIQUAC模型UNIQUAC[20~22]也是基于局部组成概念,并基于双液模型而提出的活度系数模型关联式。UNIQUAC模型适用于不完全互溶体系,同时适用于完全互溶体系。UNIQUAC活度系数模型表达式如式(3)~(4)所示。
| $\ln {\gamma _i} = \ln \frac{{{\varphi _i}}}{{{x_i}}} + \left( {\frac{Z}{2}} \right){q_i}\ln \frac{{{\theta _i}}}{{{\varphi _i}}} + {l_i} - \frac{{{\varphi _i}}}{{{x_i}}}\sum\limits_j {{x_j}} {l_j}{\rm{ }} - {q_i}\ln \left( {\sum\limits_j {{\theta _j}{\tau _{ji}}} } \right) + {q_i} - {q_i}\sum\limits_j {\frac{{{\theta _j}{\tau _{ij}}}}{{\sum\limits_k {{\theta _k}{\tau _{kj}}} }}} $ | (3) |
其中:
| ${l_i} = \frac{Z}{2}\left( {{r_i} - {q_i}} \right) - \left( {{r_i} - 1} \right),{\theta _i} = \frac{{{q_i}{x_i}}}{{\sum\limits_j {{q_j}{x_j}} }},{\varphi _i} = \frac{{{r_i}{x_i}}}{{\sum\limits_j {{r_j}{x_j}} }},{\tau _{ji}} = \exp \left( { - \frac{{{u_{ji}} - {u_{ii}}}}{{RT}}} \right)$ | (4) |
式中,θi和φi是纯物质i的平均面积分数和体积分数;ri和qi是纯物质参数,其值根据分子的Van De Waals体积和表面积算出;Z为晶格配位数,取为10;uij是分子i-j的相互作用能,但uij≠uji,可由实验值确定。
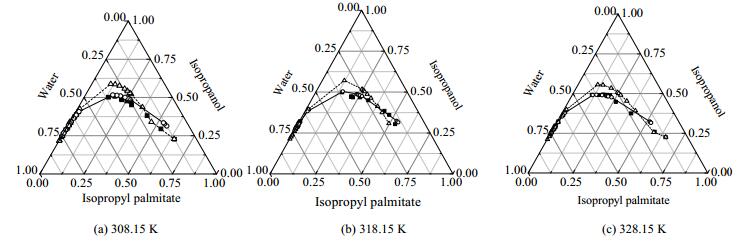
3 实验结果与讨论 3.1 液液相平衡数据的测定在常压下,测定了308.15、318.15、328.15 K棕榈酸异丙酯+异丙醇+水三元物系的液液相平衡曲线,见图 1所示。从图 1中可以看出,在308.15~328.15 K,随着温度的升高,液液相平衡线变化不大。
|
图 1 棕榈酸异丙酯+异丙醇+水三元体系液液平衡相图 Fig.1 LLE phase diagram for the isopropyl palmitate+ isopropanol+ water system ■ experimental data ┈△┈ calculation data by NRTL —○— calculation data by UNIQUAC |
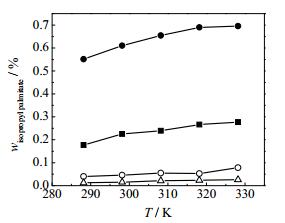
由图 2可知,随着异丙醇与水的质量百分比的比值减小,棕榈酸异丙酯在混合溶剂中的质量分数受温度的影响较小,当醇水比值小于2(m异丙醇:m水=65%:35%)时,其质量分数变化趋势非常小,几乎不受温度的影响。而在同一温度下,随着溶剂中异丙醇质量分数的减小,水质量分数的增加,棕榈酸异丙酯在混合溶剂中的质量分数呈下降趋势。“两步法”合成生物柴油组分脂肪酸酯专利技术用萃取分离技术提纯棕榈酸异丙酯,其醇水比值一般都小于2,故在常温下用水洗技术对棕榈酸异丙酯粗品进行提纯分离是可行的。
|
图 2 在不同比例的异丙醇和水体系中的棕榈酸异丙酯浓度随温度的变化 Fig.2 Solubility of isopropyl palmitate as a function of temperature in solvents with different isopropanol and water ratios ● 85%:15% ■ 75%:25% ○ 65%:35% △ 55%:45% |
液液相平衡数据受温度的影响较小,当温度变化范围不大时,可以将其视为不变。因此,本实验的模拟可将308.15、318.15和328.15 K三个温度下的液液相平衡数据作为一个大样本一同进行回归计算,得到该三元体系中各个二组分的相互作用参数。
通过Aspen Plus软件,用NRTL模型和UNIQUAC模型对实验数据进行回归,得到该三元体系的二元相互作用参数。目标函数表达式如式(5)所示:
| $OF = \min \sum\limits_i {\sum\limits_j {\sum\limits_k {\left( {x_{ijk}^{\exp } - x_{ijk}^{{\rm{cal}}}} \right)} } } $ | (5) |
用相对误差RD和平均相对误差ARD来描述模型预测的计算值和实验值之间的偏差。RD、ARD的表达式分别为式(6)和(7)。
| $RD = \left| {\frac{{{x_{i,\exp }} - {x_{i,{\rm{cal}}}}}}{{{x_{i,\exp }}}}} \right| \times 100\% $ | (6) |
| $ARD = \frac{1}{n}\sum\limits_{i = 1}^n {\left| {\frac{{{x_{i,\exp }} - {x_{i,{\rm{cal}}}}}}{{{x_{i,\exp }}}}} \right|} \times 100\% $ | (7) |
式中:xijkexp, xijkcal分别为组分摩尔分数的实验值和计算值,i、j、k分别代表组分、相数和连结线;n为连结线的数目。
用NRTL模型和UNIQUAC模型对实验数据进行关联,所得的二元交互作用参数见表 1。NRTL模型和UNIQUAC模型计算得到的棕榈酸异丙酯(1)+异丙醇(2)+水(3)液液平衡曲线,见图 1所示。该三元体系的液液平衡实验值与计算值的结果见表 2和表 3。比较两模型的ARD,发现UNIQUAC模型的ARD值均比NRTL的ARD值要小,说明UNIQUAC模型比NRTL模型的关联性更好。就UNIQUAC模型关联结果来看,在有机相中,对棕榈酸异丙酯、异丙醇和水而言,它们的ARD值分别为10.30%、8.10%和10.34%;在水相中,则分别为3.28%、3.08%和1.34%。由此表明,运用回归得到的UNIQUAC参数对该三元相平衡数据进行预测是能够满足工程计算的要求的。
| 表 1 NRTL、UNQUAC模型参数回归结果 Table 1 Parameters of NRTL and UNIQUAC models |
| 表 2 NRTL模型的计算值及与实验值的比较结果 Table 2 Comparison of experimental and calculated data of NRTL model |
| 表 3 UNIQUAC模型的计算值及与实验值的比较结果 Table 3 Comparison of experimental and calculated data of UNIQUAC model |
(1) 用平衡法测定了常压下308.15~328.15 K,棕榈酸异丙酯+异丙醇+水三元体系的液液相平衡数据,实验数据表明液液相平衡数据受温度的影响较小,当温度变化范围不大时,可以将其视为不变。
(2) 利用Aspen Plus软件对该三元体系用NRTL、UNIQUAC模型进行关联,结果表明用UNIQUAC模型的计算值与实验值的误差小于NRTL模型,UNIQUAC模型关联的参数能够满足工程计算的要求。
符号说明:
| [1] | Chin S Y, Ahmad A L, Mohamed A R, et al. Characterization and activity of zinc acetate complex supported over functionalized silica as a catalyst for the production of isopropyl palmitate[J]. Applied Catalysis A , 2006, 297(1): 8-17. DOI:10.1016/j.apcata.2005.08.034. |
| [2] | Kee C Y, Hassan M, Ramachandran K B. Studies on the kinetics of isopropyl palmitate synthesis in packed bed bioreactor using immobilized lipase[J]. Artificial Cells, Blood Substitutes, and Immobilization Biotechnology , 1999, 27(5-6): 393-8. DOI:10.3109/10731199909117709. |
| [3] | FU Li-li(付丽丽), JIANG Deng-gao(蒋登高). Thermodynamic analysis of isopropyl palmitate synthesis(棕榈酸异丙酯合成反应的热力学分析)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报) , 2016, 30(2): 398-403. |
| [4] | FU Li-li(付丽丽), JIANG Deng-gao(蒋登高), ZHOU Cai-rong(周彩荣). Determination of thermodynamic parameters of isopropyl palmitate synthesis(棕榈酸异丙酯反应体系热力学参数的测定)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报) , 2017. |
| [5] | WANG Xiao-chun(王晓春), GAO Jia-jun(高甲君), ZHANG Xin-chun(张新春). Synthesis of isopropyl palmitate and application in cosmetics(棕榈酸异丙酯的合成及在化妆品中的应用)[J]. Sichuan Daily Chemical(四川日化) , 1993, 9(4): 26. |
| [6] | BU Wen-juan(卜文娟), GENG Quan-hua(耿全华), RUAN Fu-chang(阮复昌). Development on synthesis and application of isopropyl palmitate(棕榈酸异丙酯的合成研究进展)[J]. Flavor Fragrance Cosmetics(香料香精化妆品) , 2010, 8(6): 49-52. |
| [7] | JING Qiang-shan(井强山), WANG Zhen-hai(王振海), WANG Shen-dian(王慎典). Inquire into the technology of palmitic acid isopropyl ester prepared by direct esterification method(直接酯化法制备棕榈酸异丙酯工艺路线探讨)[J]. Journal of Xinyang Teachers College (Natural Science Edition)(信阳师范学院学报(自然科学版)) , 1998, 11(3): 291-293. |
| [8] | LIU Qun(刘群), DING Bin(丁斌), HAO Feng-ling(郝凤岭), et al. Study on green synthesis process of isopropyl palmitate(棕榈酸异丙酯的绿色合成工艺研究)[J]. Chemical World(化学世界) , 2015, 56(10): 609-613. |
| [9] | GENG Zai-xin(耿再新), ZHANG Miao-juan(张苗娟), JIANG Deng-gao(蒋登高). Synthesis Method of biodiesel(一种生物柴油合成方法) : CN, 101538487A[P]. 2009-09-23. |
| [10] | BAI Ying-ge(白银鸽). Continuous process of two-step biodiesel production(两步法合成生物柴油连续化生产工艺研究) [D]. Zhengzhou(郑州) : Zhengzhou University(郑州大学), 2010. http://cdmd.cnki.com.cn/Article/CDMD-10459-1014392983.htm |
| [11] | GENG Zai-xin(耿再新), ZHANG Miao-juan(张苗娟), FU Li-li(付丽丽), et al. A novel non-catalytic method for synthesizing biodiesel at ordinary temperature(常温非催化合成生物柴油研究)[J]. Chemical World(化学世界) , 2012, 54(4): 36-38. |
| [12] | LIU Yuan-yuan(刘源源), PENG Yang-feng(彭阳峰), ZHAO Hong-liang(赵红亮), et al. Measurement and correlation of liquid-liquid equilibrium data for methyl lactate-dichloromethane-water(乳酸甲酯-二氯甲烷-水三元液液平衡数据的测定及关联)[J]. Chemical Engineering(China)(化学工程) , 2013, 41(12): 43-47. |
| [13] | JIAO Zhen(焦真), MA Shao-ling(马少玲), WANG Bing(王兵), et al. Correlation and prediction of liquid-liquid phase equilibrium of ionic-alcohol-water systems with NRTL equation(用NRTL方程关联和预测离子液体-醇-水体系的液液相平衡)[J]. CIESC Journal(化工学报) , 2006, 57(12): 2801-2805. |
| [14] | YANG Chu-fen(杨楚芬), QIAN Yu(钱宇), ZHANG Li-juan(章莉娟), et al. Measurement and correlation of liquid-liquid equilibrium data for methyl isobutyl ketone-water-phenol ternary system(甲基异丁基酮-水-苯酚三元物系液液相平衡数据的测定与关联)[J]. CIESC Journal(化工学报) , 2007, 58(4): 805-809. |
| [15] | CHEN Ying(陈莹), LIU Chang-jian(刘昌见). Determination and correlation of liquid-liquid equilibrium data for toluene-n-hexene-dimethyl sulfoxide system(甲苯-正己烯-二甲基亚砜液-液平衡数据的测定与关联)[J]. CIESC Journal(化工学报) , 2013, 64(3): 814-819. |
| [16] | ZHUANG Zhi-hai(庄志海), ZHANG Jian-qiang(张建强), LIU Dian-hua(刘殿华). Liquid-liquid equilibrium study for polyoxymethylene dimethyl ethers+ water+ n-hexane ternary system(聚甲氧基二甲醚+水+正己烷三元体系的液液相平衡研究)[J]. CIESC Journal(化工学报) , 2016, 67(3): 1-9. |
| [17] | SHEN Z P, WANG Q B, CHENL H, et al. Liquid-liquid equilibria for ternary systems water+ acetic acid+1, 2, 4-trimethylbenzene and water+ acetic acid+1, 3, 5-trimethylbenzene at (303.2-343.2)K[J]. Fluid Phase Equilibria , 2016, 414: 48-54. DOI:10.1016/j.fluid.2016.01.005. |
| [18] | Niklas S, Anne F, ErikV H, et al. Liquid-liquid equilibrium in binary and ternary mixtures containing formaldehyde, water, methanol, methylal, and poly (oxymethylene) dimethyl ethers[J]. Fluid Phase Equilibria , 2016, 425: 127-135. DOI:10.1016/j.fluid.2016.05.017. |
| [19] | Omarua , FarouqS M, Mohamed K H K, et al. Measurements and prediction of ternary liquid-liquid equilibria for mixtures of IL + sulfur compound + hexadecane[J]. Fluid Phase Equilibria , 2016, 421: 16-23. DOI:10.1016/j.fluid.2016.03.014. |
| [20] | Younas D, Solomon G, Brian J N, et al. Multicomponent phase behavior predictions using QSPR-generalized NRTL and UNIQUAC models[J]. Fluid Phase Equilibria , 2016, 409: 318-326. DOI:10.1016/j.fluid.2015.10.009. |
| [21] | LIU Xiao-jing(刘晓静). Measurement and correlation of liquid-liquid equilibrium data for the ternary dicholomethane + water +N, N-dimethylacetamide system(二氯甲烷-水-N, N-二甲基乙酰胺体系液液平衡数据的测定与关联) [D]. Changchun (长春): Changchun University of Technology(长春工业大学), 2015. |
| [22] | MA Pei-sheng(马沛生). Chemical engineering thermodynamics(化工热力学教程)[M].Beijing(北京): Higher Education Press(高等教育出版社), 2011: 89-93. |
| [23] | Prausnitz J M, Lichtenthaler R N, Azevedo E G. Molecular thermodynamics of fluid-phase equilibria (流体相平衡的分子热力学)[M]. LU Xiao-hua(陆小华), LIU Hong-lai(刘洪来). trans. 3rd ed. Beijing (北京): Chemical Industry Press(化学工业出版社), 2005: 156-178. |
| [24] | Abrams D S, Prausnitz J M. Statistical thermodynamics of liquid mixtures:A new expression for Gibbs energy of partly or completely miscible system[J]. AJChE Journal , 1975, 21(1): 116-128. |




