2. 浙江大学衢州研究院, 浙江 衢州 324000
2. Institute of Zhejiang University-Quzhou, Quzhou 324000, China
稀土元素因独特的物化性质,在化工、电子、航天航空和新能源等众多领域中被广泛应用[1-4],已成为一种重要战略资源。稀土开采困难且伴随严重环境污染[5-6],随着稀土储量不断减少和需求量不断增大,从废弃稀土产品中回收稀土金属成为应对稀土供应风险和减轻环境负荷的良策[7-8]。
钕铁硼作为常见稀土永磁材料,凭借优异的永磁体性能被广泛应用于航空航天、风力发电、医疗器械等领域[9-10]。钕铁硼中铁、钕和硼的质量分数一般为50%~60%、25%~30% 和1%,Al、Ga、Co等作为添加剂以改善钕铁硼耐热性、磁性或腐蚀性能[11-12]。但由于工艺和设备的问题,钕铁硼生产过程中不可避免会产生约25% 的废料,其中稀土元素约占33%[13],造成了严重的污染和浪费。稀土资源的供应压力和钕铁硼废料中潜在的巨大价值,使钕铁硼废料中稀有元素的回收利用得到越来越多学者的重视[14-16]。
钕铁硼废料结构稳定坚实,在弱酸下金属离子的浸出极为缓慢,研磨时还会产生电火花,存在较大的安全隐患,因此金属离子的浸出成为钕铁硼废料回收工艺的关键步骤和难点。目前国内对钕铁硼废料的回收主要依靠湿法工艺,一般借助高温、高压、强酸[16-19]浸出金属离子,虽然处理量大,但焙烧能耗高、尾气排放量大,且会产生大量酸性废水,产生二次污染,与减轻稀土开采环境负荷的初衷相背。电化学阳极氧化技术无需进行消磁、研磨等前处理,可在温和条件下浸出金属离子,避免高温焙烧,减少酸性废水排放,绿色环保,逐渐成为钕铁硼废料回收新的研究热点。Venkatesan等[20]采用氯化钠-盐酸溶液浸出金属离子,电解浸出液使铁氧化物沉淀,再用草酸将钕沉淀。兰超群[21]利用湿法分离得到稀土氧化物和含铁酸液,采用电沉积技术回收浸出液中的铁。以上工艺虽均采用了电化学技术,但仍需酸泡以浸出金属离子,工艺复杂成本高。Makarova等[22-23]使用硫酸-草酸体系作为浸出液,利用静电吸引原理在阴极沉积稀土草酸盐,但该工艺需要持续补充草酸,否则纯度将大幅下降。
相比其他电化学工艺,本研究以钕铁硼废料作为阳极,使用较廉价易得的硫酸钠代替强酸作为电解液,通过阳极氧化直接浸出钕铁硼废料中的金属离子,金属离子在电解液中形成无定形疏松多孔的混合氢氧化物沉淀,分离沉淀后电解液可循环重复使用。该工艺流程短,操作简单,可以避免强酸的使用,能耗低,且反应器等无需防腐,是一项绿色的钕铁硼浸出工艺。
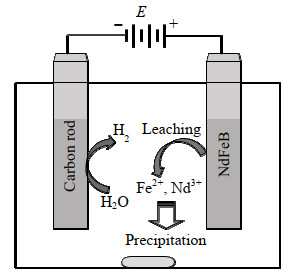
2 实验部分实验中所用的钕铁硼废料依次用无水乙醇和去离子水清洗3次,60 ℃烘箱中烘干,称重后备用。阳极氧化实验以钕铁硼废料为阳极,石墨棒为阴极,电解液为不同浓度和pH值的硫酸钠溶液,在转速为300 r⋅min−1水浴中电解。电解过程如图 1所示,阴极上电解水产生氢气,钕铁硼阳极中的钕和铁失去电子后变成离子进入溶液中,最终与OH−结合形成沉淀被分离,具体反应见式(1)~(3)。
|
图 1 阳极氧化反应示意图 Fig.1 Diagram of anodic oxidation reaction |
阳极:
| ${\rm{Fe}} \to {\rm{F}}{{\rm{e}}^{2 + }} + 2{{\rm{e}}^ - }\;\;\;\;\;{E_0} = + {\rm{0}}{\rm{.447}}\;{\rm{V}} $ | (1) |
| $ {\rm{Nd}} \to {\rm{N}}{{\rm{d}}^{3 + }} + 3{{\rm{e}}^ - }\;\;\;\;\;{E_0} = + 2.3{\rm{23}}\;{\rm{V}} $ | (2) |
阴极:
| $ 2{{\rm{H}}^ + } + 2{{\rm{e}}^ - } \to {{\rm{H}}_{\rm{2}}}\;\;\;\;\;{E_0} = {\rm{0}}\;{\rm{V}}$ | (3) |
式中:E0为标准电极电势。
每次测定电解前后钕铁硼质量,以钕铁硼阳极的减重评价浸出速率,实验重复3次取平均值,计算公式见式(4)。电解后进行离心、过滤、清洗、干燥,得到最终固体沉淀产物。采用扫描电镜(SEM)、X射线衍射仪(XRD)、X射线能谱仪(EDS)分析样品表面的微观结构、成分和元素分布。XRD采用Cu靶辐射,参数为:入射线波长λ=0.154 1 nm,管电压为40 kV,管电流为40 mA,衍射角范围2θ为10°~80°。固体沉淀产物在60 ℃烘干后称重,采用离子体发射光谱仪(ICP)测定其中的钕和铁质量分数并分别计算回收率,如式(5)~(6)所示。
| $ {\text{Leaching rate (mg}} \cdot {\text{mi}}{{\text{n}}^{ - 1}}{\text{) = }}\frac{{60({m_0} - {m_t})}}{t} $ | (4) |
| $ {\text{ Recovery rate (Nd ) = }}\frac{{w \times m}}{{{m_0} - {m_t}}} \times \frac{{{M_r}(N{d_2}F{e_{14}}B)}}{{2{M_r}(Nd)}} \times 100\% $ | (5) |
| $ {\text{ Recovery rate (Fe ) = }}\frac{{w \times m}}{{{m_0} - {m_t}}} \times \frac{{{M_r}(N{d_2}F{e_{14}}B)}}{{14{M_r}(Fe)}} \times 100\% $ | (6) |
式中:m0和mt分别为钕铁硼废料的初始质量和电解时间t后的质量,mg;m为沉淀产物的质量,mg;w为沉淀产物中Nd或Fe的质量分数;Mr(Nd)和Mr(Fe)分别为Nd和Fe的相对分子质量;Mr(Nd2Fe14B)为Nd2Fe14B的相对分子质量。
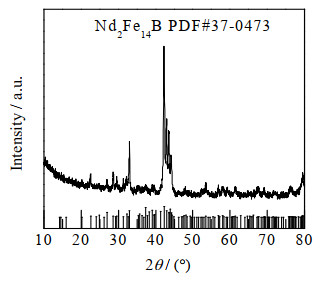
3 结果与讨论 3.1 钕铁硼废料的形貌组成分析采用SEM、EDS和XRD对钕铁硼废料进行分析,其微观形貌和晶体结构如图 2、3所示。由图 2(a)可见,钕铁硼废料为表面粗糙的块状结构。EDS结果表明废料中含有Nd、Fe元素,且在表面均匀分布。由图 3可见,钕铁硼废料的XRD图谱出现明显的峰,与Nd2Fe14B的XRD标准晶体结构(PDF#37-0473)相符。

|
图 2 钕铁硼废料的SEM和元素分布图 Fig.2 SEM and EDX mapping images of Nd2Fe14B waste |
|
图 3 钕铁硼废料的XRD图 Fig.3 XRD pattern of Nd2Fe14B waste |
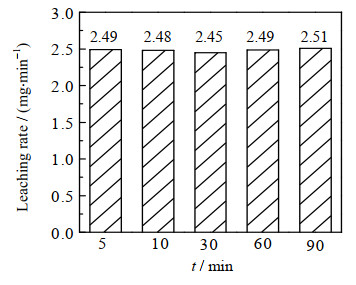
为考察电解时间对浸出速率的影响,测定不同电解时间下的阳极浸出速率,实验以浓度c(Na2SO4)=0.2 mol⋅L−1的Na2SO4为电解液,温度20 ℃,电压2.5 V,结果如图 4所示。电解时间t为5、10、30、60、90 min时,浸出速率分别为2.49、2.48、2.45、2.49、2.51 mg⋅min−1,即电解时间对浸出效率无明显影响。考虑实验和误差,电解时间设为10 min。
|
图 4 不同电解时间下的浸出速率 Fig.4 Leaching rates at different electrolytic times |
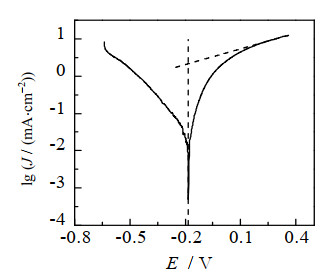
钕铁硼的动电位极化曲线如图 5所示,图中E为参考标准零电位的极化电位,J为阳极电流密度。由图 5可知,阳极电流密度随极化电位的增大而增大,即浸出速度随电位变正而逐渐增大,且极化曲线无明显的钝化区,其中自腐蚀电位为−0.183 V,自腐蚀电流为4.314 mA⋅cm−2。为了探究电解电压对浸出速率的影响,对不同电压下的阳极氧化浸出速率进行了测定,结果如图 6所示,图中U为电解电压。实验电解液是浓度为0.2 mol⋅L−1的Na2SO4,反应温度20 ℃。
|
图 5 钕铁硼的动电位极化曲线 Fig.5 Potentiodynamic polarization curve of NdFeB |

|
图 6 不同电解电压下的浸出速率 Fig.6 Leaching rates at |
由图 6可知,电解施加的电压越高,浸出速率越快,可近似为正比关系。电压的增大促使阳极钕铁硼废料中金属元素失去电子,形成离子进入溶液。根据法拉第定律,反应转移的电荷量与电量成正比,在电解过程中电流几乎保持不变,因此浸出速率正比于电解电压。考虑到电解的能耗和后续实验,电压为2.5 V时,阳极氧化的浸出速率较高,是较为适宜的反应条件。
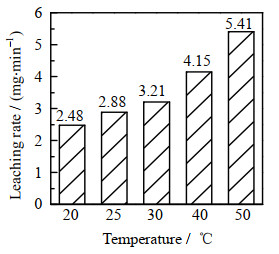
3.4 温度对浸出速率的影响在电解电压为2.5 V、Na2SO4电解液浓度为0.2 mol⋅L−1的条件下,分别测定温度在20、25、30、40、50 ℃水浴下的浸出速率,考察温度对阳极氧化行为的影响,结果如图 7所示。在实验温度范围内,随着温度的升高,浸出速率逐渐增加。但同时,温度较高也会促进如下反应[24-25]的发生:
| $ 4{\text{Fe(OH}}{{\text{)}}_{\text{2}}}{\text{ + }}{{\text{O}}_{\text{2}}}{\text{ + 2}}{{\text{H}}_{\text{2}}}{\text{O}} \to {\text{4Fe(OH}}{{\text{)}}_3} $ | (7) |
| $ {\text{3Fe(OH}}{{\text{)}}_{\text{2}}} \to {\text{F}}{{\text{e}}_{\text{3}}}{{\text{O}}_{\text{4}}}{\text{ + }}{{\text{H}}_{\text{2}}}{\text{ + 2}}{{\text{H}}_{\text{2}}}{\text{O}} $ | (8) |
|
图 7 不同温度下的浸出速率 Fig.7 Leaching rates at different temperatures |
高温下反应时观察到红色沉淀明显增多,说明升温会推动反应式(7)~(8)发生。而在20 ℃时只观察到蓝绿色沉淀,说明沉淀中氢氧化亚铁和氢氧化钕的含量较高,红棕色的氢氧化铁和氧化铁的含量较低。此外,高温对电解体系的阴极也有一定的影响,会提高阴极反应析出氢气的速率,从而降低整个反应的反应电阻,提高金属离子浸出速率。综上所述,考虑高温能耗和浸出速率,25 ℃下的浸出速率已满足需求,后续实验在25 ℃下进行。
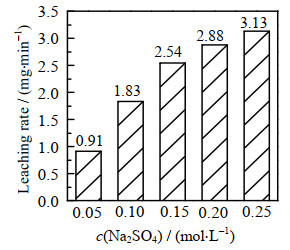
3.5 电解质浓度对浸出速率的影响不同的酸溶液作为电解液时,电解钕铁硼的电化学行为不同。硼酸和草酸为弱酸,超过一定电压后会形成钝化效应;而硫酸、硝酸、盐酸的电化学表现相似,在相同的电压下,电流大小:盐酸 > 硫酸 > 硝酸。由于氯离子在反应过程中会生成氯气,从环保和动力学角度考虑,本研究选择硫酸根作为电解质阴离子。电解过程中温度25 ℃,电解电压2.5 V,分别以c(Na2SO4)=0.05、0.10、0.15、0.20、0.25 mol⋅L−1的硫酸钠溶液为电解液,研究电解质浓度对浸出速率的影响,结果如图 8所示。
|
图 8 不同硫酸钠溶液浓度下的浸出速率 Fig.8 Leaching rates at different electrolytes and concentrations |
由图 8可见,随着电解液中硫酸钠浓度逐渐增大,浸出速率也逐渐增大,但增幅减小。这是由于电解质浓度增加提高了溶液电导率,溶液电阻产生的能耗降低,而电解质浓度较高时,电解质浓度不再是限制浸出速率的主要因素。综合考虑,后续实验选取c(Na2SO4)=0.2 mol⋅L−1的硫酸钠溶液作为电解液。
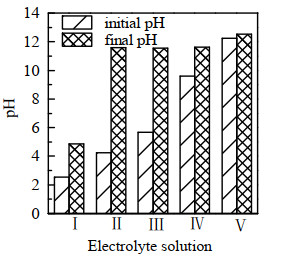
3.6 初始pH值对浸出速率和回收率的影响为考察电解液初始pH对阳极氧化浸出速率的影响,在浓度为0.2 mol⋅L−1的Na2SO4溶液的基础上分别配制了含10−2 mol⋅L−1 H2SO4、10−4 mol⋅L−1 H2SO4、无、10−4 mol⋅L−1 NaOH和10−2 mol⋅L−1 NaOH的电解液,分别记为I、II、III、IV、V(pH分别为2.55、4.25、5.67、9.6、12.23),电解电压为2.5 V,水浴25 ℃,结果如图 9所示。由图可知,5种电解液下的浸出速率没有显著差别,说明在pH=2~12内,电解液的初始pH值对浸出速率基本没有影响。这是因为在pH > 2时,钕铁硼的酸溶效果无法体现。另一方面,阳极氧化浸出金属元素的原理是通过施加电压使金属失去电子,变为离子进入电解质溶液,而不是通过酸溶浸出金属离子。电解液始末pH如图 10所示,由图可知,不同电解液的pH在阳极氧化后都有一定的升高。这是因为反应过程中阴极消耗H+生成H2,使电解液的pH值在电解后增大。

|
图 9 不同初始pH电解液下的浸出速率 Fig.9 Leaching rates in electrolytes with different initial pH |
|
图 10 不同电解质溶液中的始末pH Fig.10 Initial and final pH in different electrolyte solutions |
过低的pH值对Fe离子和Nd离子的沉淀有较大的抑制作用,因此需要对不同pH电解液中金属离子的回收率进行分析。如图 11所示,电解液I中Fe和Nd的回收率(75.2% 和44.2%)明显低于其他4组电解液的回收率,而其他4组无明显差别(II、III、IV、V中Fe和Nd的回收率分别为96.3% 和93%、96.1% 和94.6%、95.9% 和94.0%、95.3% 和94.8%)。当pH低至1[26]时,溶液中将不产生絮状沉淀物,铁和钕以离子形式存在于电解液中,不利于金属离子的回收,因此电解液的pH值不宜过低。综合浸出速率和回收率的分析,硫酸钠电解液可不额外调节pH值,此时的钕铁硼的浸出速率为2.88 mg⋅min−1,Fe和Nd的回收率分别为96.1% 和94.6%。

|
图 11 不同初始pH电解液中钕和铁的回收率 Fig.11 Recovery rates of Nd and Fe in electrolytes with different initial pH |
利用SEM和EDS进一步对浸出产物进行分析,分别如图 12和表 1所示。由图 12可知,所得产物为无定形结构,相比原钕铁硼废料坚实的结构,其表面疏松多孔,有利于后续分离。从元素分布结果可看出产物中Nd、Fe、O均匀分布。由表 1可知,Fe与Nd的物质的量比约为7:1,与Nd2Fe14B的比例相符,因此Fe和Nd均匀浸出。为分析产物组成,对60 ℃烘干和800 ℃煅烧2 h的产物进行XRD分析,如图 13所示。从图可得,60 ℃烘干的产物中主要为Fe(OH)3、Nd(OH)3及少量Fe2O3,800 ℃煅烧后全部转变为Fe2O3和Nd2O3。

|
图 12 回收产物的扫描电子显微镜图像和O、Nd、Fe元素的分布图 Fig.12 SEM and O, Nd, Fe element mapping images of recovered products |
|
|
表 1 钕铁硼废料的EDS分析 Table 1 EDS analysis of NdFeB waste |

|
图 13 60 ℃烘干和800 ℃煅烧后回收产物的XRD图 Fig.13 XRD patterns of the recovered products after drying at 60 ℃ and calcination at 800 ℃ |
为进一步分析电化学阳极氧化技术浸出工艺的应用价值,在优化参数的基础上进行工艺放大实验,其中电解液为1 L 0.2 mol⋅L−1 Na2SO4溶液,电解电压2.5 V,温度25 ℃,电解时间2 h。实验过程照片如图 14所示,电解时钕和铁离子浸出并沉淀,静置后沉在烧杯底部,分离沉淀后的电解液可循环利用。电解前后钕铁硼的质量分别为4.714 g和4.236 6 g。电能消耗以处理每千克钕铁硼的能耗表示,计算公式如下:
| $ Q{\text{ = }}\frac{{U\int {I{\text{d}}t} }}{{{3\;}600({m_0} - {m_t})}} \;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\text{(9)#}$ |

|
图 14 放大实验不同时间的光学照片 Fig.14 Optical photos taken at different times in the pilot experiment |
式中:Q为每千克钕铁硼能耗,kW⋅h;I为电化学工作站实时记录的电流,A。
计算得能耗Q=1.74 kW⋅h,相比其他钕铁硼浸出工艺,电化学阳极氧化技术能耗低,更绿色环保。
4 结论本研究利用SEM、EDS和XRD分析钕铁硼废料的表面形貌和晶体结构,通过阳极氧化技术直接浸出钕铁硼废料中的稀土元素和铁元素,研究不同电解条件对钕铁硼的阳极氧化动力学行为的影响,并通过SEM和EDS对回收产物的微观形貌和组成进行分析。
(1) 金属离子的浸出速率随电压、温度、硫酸钠浓度提高而增大,电解时间对浸出速率无明显影响,综合可操作性和能耗考虑,最适合条件:电解电压为2.5 V,反应温度为25 ℃,电解液采用浓度为0.2 mol⋅L−1的硫酸钠。
(2) 在pH为2~12时,电解液的初始pH值对阳极氧化的浸出速率几乎没有影响,但过低pH值会抑制铁和钕离子的沉淀,降低钕铁硼废料的回收率。当电解液pH < 1时,将不产生沉淀。因此硫酸钠溶液可无需使用酸或碱调节pH值直接用作电解液。
(3) 在最合适条件下,钕铁硼废料的浸出速率为2.88 mg⋅min−1,Fe和Nd的回收率分别为96.1% 和94.6%,Q=1.74 kW⋅h。本方法的回收产物成分主要为铁和钕的氢氧化物,相比原钕铁硼废料坚实的结构,无定形疏松多孔的结构更有利于后续金属元素的分离回收。
(4) 与现有钕铁硼浸出工艺相比,本研究采用的阳极氧化技术操作简单,能耗低,可在较温和条件下浸出金属离子,且电解液可在分离回收沉淀后循环利用,是一项绿色环保的钕铁硼浸出工艺。
| [1] |
黄小卫, 李红卫, 王彩凤, 等. 我国稀土工业发展现状及进展[J]. 稀有金属, 2007, 31(3): 279-288. HUANG X W, LI H W, WANG C F, et al. Present situation and development of rare earth industry in China[J]. Chinese Journal of Rare Metals, 2007, 31(3): 279-288. DOI:10.3969/j.issn.0258-7076.2007.03.002 |
| [2] |
KIM J S, JYOTHI R K, LEE J Y. Status and preparation technology of rare earth materials[M]. New York: John Wiley & Sons Inc, 2013.
|
| [3] |
SHEN L, WU N, ZHONG S, et al. Overview on China's rare earth industry restructuring and regulation restructuring and regulation reforms[J]. Journal of Resources Ecology, 2017, 8(3): 213-222. DOI:10.5814/j.issn.1674-764x.2017.03.001 |
| [4] |
BIEDERMANN R P. China's rare earth sector-between domestic consolidation and global hegemony[J]. International Journal of Emerging Markets, 2014, 2(9): 276-293. |
| [5] |
FENG J, ZHOU F, CHI R. , et al. Effect of a novel compound on leaching process of weathered crust elution deposited rare earth ore[J]. Minerals Engineering, 2018, 129: 63-70. DOI:10.1016/j.mineng.2018.09.018 |
| [6] |
卞玉洋. 从钕铁硼废料中回收稀土元素的新工艺研究[D]. 上海: 上海大学, 2016. BIAN Y Y. Development of novel processes on the recovery of rare earth elements from NdFeB-based permanent magnet waste [D]. Shanghai: Shanghai University, 2016. |
| [7] |
张所续, 马朋林. 美国稀土研究及政策对我国的启示[J]. 中国国土资源经济, 2020, 33(1): 35-42. ZHANG S X, MA P L. The Enlightenment of U. S. rare earth research and policy to China[J]. Natural Resource Economics of China, 2020, 33(1): 35-42. |
| [8] |
李芳琴, 代涛, 王高尚. 稀土金属二次回收再利用研究综述[J]. 矿产保护与利用, 2019, 39(5): 84-89. LI F Q, DAI T, WANG G S. A review on recycling and reuse of rare earth metals[J]. Conservation and Utilization of Mineral Resources, 2019, 39(5): 84-89. |
| [9] |
冯瑞华, 姜山, 马廷灿, 等. 我国稀土永磁材料发展战略和建议[J]. 科技管理研究, 2012, 32(15): 164-167. FENG R H, JIANG S, MA T C, et al. Development strategies and recommendations of rare earth permanent magnet in China[J]. Science and Technology Management Research, 2012, 32(15): 164-167. |
| [10] |
姜力强, 陈巧玲, 郑精武, 等. NdFeB磁粉表面电沉积包覆纳米金属层研究[J]. 高校化学工程学报, 2006, 20(3): 433-436. JIANG L Q, CHEN Q L, ZHENG J W, et al. Nanometals electrodeposition on NdFeB magnetic powders[J]. Journal of Chemical Engineering of Chinese Universities, 2006, 20(3): 433-436. |
| [11] |
HONO K, SEPEHRI-AMIN H. Reprint of prospect for HRE-free high coercivity Nd-Fe-B permanentmagnets[J]. Scripta Materialia, 2018, 154: 277-283. DOI:10.1016/j.scriptamat.2018.05.003 |
| [12] |
ZENG H, LIU Z, LIU W, et al. Significantly enhancing thecoercivity of NdFeB magnets by ternary Pr-Al-Cu alloys diffusion and understanding the elementsdiffusion behavior[J]. Journal of Magnetism and Magnetic Materials, 2019, 471: 97-104. DOI:10.1016/j.jmmm.2018.09.080 |
| [13] |
付利雯, 汪金良, 雷翔, 等. 钕铁硼废料资源化回收利用研究进展[J]. 有色金属科学与工程, 2020, 11(1): 92-97. FU L W, WANG J L, LEI X, et al. Research progress on the recycling and utilization of Nd-Fe-B wastes[J]. Nonferrous Metals Science and Engineering, 2020, 11(1): 92-97. |
| [14] |
马莹, 赵永志. 钕铁硼废料回收方法研究进展[J]. 稀土信息, 2019, 428(11): 11-15. MA Y, ZHAO Y Z. Research progress on recovery method of NdFeb waste[J]. Rare Earth Information, 2019, 428(11): 11-15. |
| [15] |
田忆兰, 周璇, 余红雅, 等. 尿素共沉淀法回收钕铁硼废料中的稀土及铁元素[J]. 稀有金属, 2020, 44(4): 427-432. TIAN Y L, ZHOU X, YU H Y, et al. Recycling rare earth and Fe elements from NdFeB waste by urea co-precipitation method[J]. Chinese Journal of Rare Metals, 2020, 44(4): 427-432. |
| [16] |
刘庆生, 吕英威, 段旭. 钕铁硼废料(NH4)2SO4焙烧法回收稀土[J]. 中国稀土学报, 2019, 37(1): 91-98. LIU Q S, LV Y W, DUAN X. Recovery of rare earth from NdFeB by ammonium aulphate roasting[J]. Journal of the Chinese Society of Rare Earths, 2019, 37(1): 91-98. |
| [17] |
郭超. 回收钕铁硼废料的氧化焙烧-高压选择性浸出稀土研究[D]. 包头: 内蒙古科技大学, 2019. GUO C. Rare earth recovery from NdFeB magnet scrap by the oxidation roasting-high pressure selective leaching method [D]. Baotou: Inner Mongolia University of Science & Technology, 2019. |
| [18] |
邓华军, 段月红, 邓庚凤. 钕铁硼废料中稀土的回收[J]. 矿冶工程, 2019, 39(1): 76-78. DENG H J, DUAN Y H, DENG G F. Recovery of rare earth from NdFeB waste[J]. Mining and Metallurgical Engineering, 2019, 39(1): 76-78. |
| [19] |
邓永春. 火法-湿法联合回收钕铁硼/镍氢电池废料中有价元素的研究[D]. 北京: 北京科技大学, 2018. DENG Y C. Valuable metal recycling from NdFeB and Ni-metal hydride battery wastes using combined pyro-and hydrometallurgical techniques [D]. Beijing: University of Science and Technology Beijing, 2018. |
| [20] |
VENKATESAN P, HOOGERSTRAETE T V, HENNEBEL T, et al. Selective electrochemical extraction of REEs from NdFeB magnet waste at room temperature[J]. Green Chemistry, 2018, 20(5): 1065-1073. |
| [21] |
兰超群. 利用湿法与电沉积技术回收超细钕铁硼废料中稀土与铁的研究[D]. 包头: 内蒙古科技大学, 2019. LAN C Q. Recovery of rare earth and iron from ultrafine NdFeB waste by hydrometallurgy and electrodeposition [D]. Baotou: Inner Mongolia University of Science & Technology, 2019. |
| [22] |
MAKAROVA I, RYL J, SUN Z, et al. One-step recovery of REE oxalates in electro-leaching of spent NdFeB magnets[J]. Separation and Purification Technology, 2020, 251: 117362. |
| [23] |
MAKAROVA I, SOBOLEVA E, OSIPENKO M, et al. Electrochemical leaching of rare-earth elements from spent NdFeB magnets[J]. Hydrometallurgy, 2020, 192(3): 105264. |
| [24] |
ARDIZZONE S, FORMARO L. Temperature induced phase transformation of metastable Fe(OH)3 in the presence of ferrous ions[J]. Materials Chemistry and Physics, 1983, 8(2): 125-133. |
| [25] |
SCHIKORR G. Hydroxide and a ferromagnetic iron (III)-hydroxide[J]. Journal of Inorganic and General Chemistry, 1933, 212(1): 33-39. |
| [26] |
程宗敏. 钕铁硼废料中稀土金属回收工艺的研究与探索[J]. 世界有色金属, 2020, 17: 127-128. CHENG Z M. Research and exploration on recovery process of rare earth metals from NdFeB waste[J]. World Nonferrous Metals, 2020, 17: 127-128. |




