2. 河南省生态环境技术中心, 河南 郑州 450001;
3. 华北水利水电大学 水资源学院, 河南 郑州 450046
2. Henan Provincial Technical Center for Ecology and Environment, Zhengzhou 450001, China;
3. North China University of Water Resources and Electric Power, College of Water Resources, Zhengzhou 450046, China
药品和个人护理用品(PPCPs)是近些年新兴的微量有机污染物,在环境中广泛存在,甚至饮用水中均有被检测到[1]。其中卡马西平(CBZ)通常被作为环境中PPCPs污染状况的指示化合物。卡马西平是一种治疗癫痫、抑郁症和神经痛的常见药物,患者服用后部分母体或其代谢产物会随粪便排出进入环境[2]。卡马西平化学名是5H-二苯并[b, f]氮杂卓-5-甲酰胺,是含氮的芳香族化合物,分子量为236.269,化学结构复杂,质量浓度在几到几十μg⋅L−1。卡马西平具有药物活性成分,低浓度下难于生物降解,一般城市污水处理厂传统的物化及生物处理方法都很难将其高效地去除[3]。目前,欧洲认为卡马西平对环境具有长期的负面影响,已经立法将其列为危害水生生物的有毒物质之一。但是,卡马西平这一类物质对人类健康及环境的危害研究刚刚开展,相关的排放标准及法律法规还未建立起来。因此,对于卡马西平这类痕量有机污染物去除方法的研究将成为水污染控制领域的热点之一。
高级氧化法(AOPs)反应速度快,对难降解有机废水有极强的处理效果。其中,基于过一硫酸盐(PMS)的AOPs的原理是通过活化PMS产生·OH和SO4-∙来高效降解有机污染物,它能将水体中难降解有机污染物氧化为H2O、CO2和其他小分子有机物[4-5]。由于成本低廉、催化性能良好,目前已有部分研究人员将黄铜矿充当AOPs的活化剂。Zheng等[6]选择罗丹明B(RhB)和六价铬(CrVI)作为代表性目标污染物,模拟有机和无机污染物的二元系统,采用黄铜矿活化过二硫酸钠(PDS)同时完成对RhB和CrVI的去除。Peng等[7]采用天然黄铜矿活化PMS以降解双酚S(BPS),研究各种自由基(SO4-∙、∙OH和O2-∙)随初始pH变化的转变,该研究对黄铜矿活化PMS降解有机污染物提供了重要的理论支撑。本研究以天然黄铜矿(NCP)为催化剂,同时实现天然矿石的综合应用和水体污染物的氧化降解,分别考察NCP投加量、PMS投加量、初始pH值、反应温度对NCP/PMS工艺降解效果的影响,以期为CBZ废水的降解提供理论支撑。
2 实验部分 2.1 主要试验材料与试剂卡马西平(CBZ)(质量分数w > 99.5%),乙醇(EtOH)、叔丁醇(TBA)购自天津科密欧化学试剂有限公司,黄铜矿(w > 99%)购于大冶锦鹏摩擦材料有限公司。实验过程中所用黄铜矿在使用前需预处理,首先用水和稀盐酸洗涤矿石清除表面灰尘与杂质,再将黄铜矿凿成小块,放入多功能粉碎机粉碎,之后用蒸馏水和乙醇反复冲洗,105 ℃烘干过孔径为0.074 mm的筛子,密封备用。过硫酸氢钾(2KHSO5∙KHSO4∙K2SO4,PMS)、5, 5–二甲基–1–吡咯烷N–氧化物(DMPO)和2, 2, 6, 6–四甲基–4–哌啶醇(TEMP)购自上海阿拉丁试剂有限公司。氢氧化钠(NaOH)、硫酸(H2SO4)和盐酸(HCl)等购于洛阳化学试剂厂,所用药品均为分析纯。
2.2 催化剂的表征通过X射线衍射仪(XRD)来观测黄铜矿的元素的特征,利用扫描电子显微镜(SEM)观察样品的形貌,采用能量-色散光谱仪(EDS)分析NCP的元素组成。采用ASAP 2460型比表面积和孔隙分析仪对材料进行分析,对NCP进行比表面积分析。
2.3 实验方法NCP/PMS体系降解CBZ的实验在250 mL烧杯中进行。首先,配制一定浓度的CBZ溶液倒入烧杯中,然后分别加入一定量的NCP、PMS,打开搅拌装置,在一定的间隔时间段内取样,并在溶液中加入过量硫代硫酸钠溶液,摇匀淬灭,用膜孔径为0.45 μm聚四氟乙烯膜过滤溶液。采用紫外-可见分光光度计对其进行测量,通过全波段光谱扫描测得CBZ在285 nm下有最大吸收波长,与其他研究人员的扫描结果一致,因此CBZ的检测波长定为285 nm[8-10],将测得吸光度代入标准曲线中并计算其去除率。根据NCP活化过硫酸盐氧化CBZ的过程中所产生的自由基特性,选择乙醇、叔丁醇分别作为SO4−∙、∙OH淬灭剂,使用DMPO作为自由基捕获剂,电子顺磁共振波谱仪BRUKER A300(EPR)用于反应中自由基的测定,推测NCP/PMS体系产生自由基类型和贡献。采用液相色谱质谱(LC-MS)联用技术对CBZ氧化降解过程中的中间产物进行了鉴定。流动相:乙腈、超纯水体积比为55:45,柱温和流速分别为40 ℃和0.50 mL⋅min−1。
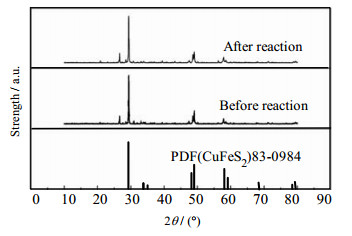
3 结果与讨论 3.1 NCP的表征 3.1.1 X射线衍射图 1为反应前后的NCP催化剂的X射线衍射(XRD)图谱,从图中可以看出样品衍射峰的位置,在衍射角2θ为29.4°、30.8°、33.9°、48.7°、49.1°、57.9°、58.6°、71.3°、78.9°和79.6°处的特征峰能够与标准卡片PDF#83-0984的峰位有很好的对应关系,它们分别对应CuFeS2的{112}、{103}、{200}、{220}、{204}、{312}、{116}、{400}、{332}、{316}晶面,表明NCP主要由CuFeS2构成[11-13]。除了CuFeS2的特征峰之外,NCP的XRD图谱中还存在其他一些杂峰,这是由于天然黄铜矿中含有少量杂质所致。
|
图 1 黄铜矿反应前后的XRD图谱 Fig.1 XRD patterns of chalcopyrite before and after reaction |
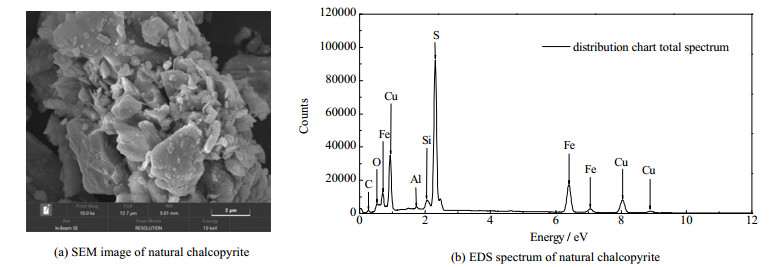
从表 1可以看出NCP中所含的主要元素有Fe、Cu、S、Si、Al、O等,其中Fe元素质量分数为33.01%,Cu元素质量分数为33.02%,S元素质量分数为29.63%。由图 2(a)可知,NCP是一种形状不规则的块状颗粒,表面较为粗糙,比表面积较小。NCP的EDS谱图分别如图 2(b)所示,可以看出NCP中含有多种元素。
|
|
表 1 NCP的主要元素组成 Table 1 Main element composition of NCP |
|
图 2 样品的SEM谱图以及EDS谱图 Fig.2 SEM image and EDS spectra of samples |
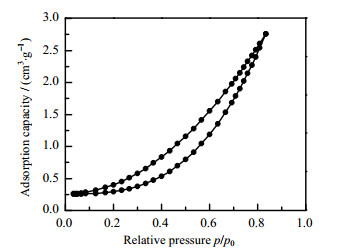
为了进一步探究天然黄铜矿的性质,对天然黄铜矿进行BET比表面积分析。图 3为天然黄铜的N2吸附脱附曲线。
|
图 3 氮气吸附脱附等温线 Fig.3 Nitrogen adsorption-desorption isotherm |
从图 3可以看出,NCP的等温线保持下凹状态,低压端与x轴相近,说明材料与N2之间的作用力较弱。同时,随着组分分压增大,材料的氮气吸附量也随之上升,结合图 3与相关文献[14]确定NCP的等温线属于Ⅲ型等温线。除此之外,图 3中NCP材料因毛细凝聚作用,使其吸附脱附等温线未完全重合形成回滞环,该回滞环的饱和吸附平台不明显,为H3型[15]。此类型的回滞环能够反映出裂缝、平板狭缝和楔形等结构,因此上述结果可以表明NCP材料具有介孔结构,经过计算得出NCP的比表面积为2.357 m2⋅g−1。
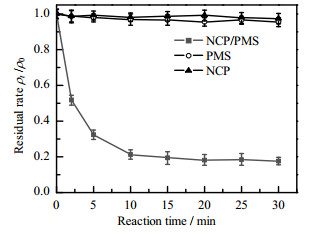
3.2 NCP催化PMS降解CBZ的效能分析 3.2.1 不同反应体系中CBZ降解效能分析通过前期的预实验表明该反应在初期反应速率较快,因此在反应进行2 min时增加取样点,选定CBZ初始质量浓度ρ0为5.0 mg⋅L−1,PMS质量浓度为0.5 g⋅L−1。为研究不同反应体系对CBZ降解效率的影响,分别对NCP体系、PMS体系,以及NCP/PMS体系降解CBZ的反应过程进行分析。从图 4(图中ρt为CBZ在t时刻质量浓度)可以看出,单独投加1.0 g⋅L−1 NCP时,CBZ的去除率仅有2.67%,说明NCP对CBZ有一定的吸附效果,但吸附效果较差,这与Peng等[7]的研究基本一致。同时,单独投加0.5 g⋅L−1的PMS对CBZ的降解效果只有4.53%,表明单独PMS对CBZ分子有一定的氧化能力,但因未被活化,其氧化能力不高,可能是因为未被活化的PMS的氧化能力太低,不足以破坏CBZ的化学键[16]。由此看出,在单独的NCP体系与PMS反应体系中,CBZ的去除效率并不高。相比之下,在1.0 g⋅L−1 NCP、0.5 g⋅L−1 PMS的条件下,NCP/PMS体系对CBZ的降解效率提高至82.34%,这表明NCP能高效地活化PMS,对CBZ进行氧化降解,因此,本研究采用NCP/PMS体系来降解CBZ。
|
图 4 不同反应体系下CBZ的降解效果 Fig.4 CBZ degradation under different reaction systems (Experimental condition: 5.0 mg⋅L−1 CBZ, 0.5 g⋅L−1 PMS, 1.0 g⋅L−1 NCP, pH=6.76) |
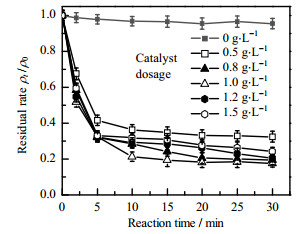
催化剂的投加量会直接影响CBZ降解的效率,投加量过小时,活化PMS效率低,污染物的去除难以达到期望值;NCP投加量过大时,不仅会增加成本,还会因金属离子溶出引发二次污染。不同NCP投加量对CBZ降解的影响如图 5所示。该反应在pH为6.76、PMS投加量为0.5 g⋅L−1、CBZ的质量浓度为5.0 mg⋅L−1的条件下进行。当反应体系中NCP投加量为0 g⋅L−1时,CBZ的去除率仅为4.53%。而在NCP投加量增大到0.5 g⋅L−1时,反应速度快速得到提升,去除率可高达66.96%,表明NCP能高效活化PMS产生活性物质将CBZ分子降解。随着NCP投加量继续加大至1.0 g⋅L−1时,CBZ的去除率达到峰值,可高达82.34%,表明NCP投加量从0.5 g⋅L−1提升至1.0 g⋅L−1,随着NCP的增加可以使PMS的活化位点增多,产生更多的自由基[17]。但NCP的投加量继续提升至1.2 g⋅L−1时,CBZ的去除率却有所下降,这是因为当溶液中NCP质量浓度过高时,催化剂可能会发生团聚[17],导致活性位点变少,从而导致催化效率降低。综上分析,出于CBZ去除率和经济性考虑,选择NCP最佳投加量为1.0 g⋅L−1。
|
图 5 催化剂投加量对CBZ的降解效果的影响 Fig.5 Effect of catalyst dosage on CBZ degradation (Experimental condition: 5.0 mg⋅L−1 CBZ, 0.5 g⋅L−1 PMS, pH=6.76) |
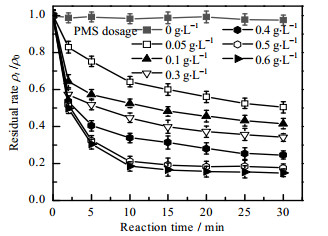
在最佳NCP投加量(1.0 g⋅L−1)的基础上探究PMS投加量对反应体系的影响。不同PMS投加量对CBZ去除率的影响如图 6所示。当反应体系中没有PMS投加时,对CBZ的降解率仅有5.8%,表明单独的NCP的吸附效果并不显著。随着PMS投加量的增加,水体中SO4−∙和∙OH的浓度不断提高,大大提高了CBZ的降解效果。当PMS投加量进一步提高,大于0.5 g⋅L−1时,CBZ的去除效果没有显著上升。造成这样的原因是当PMS质量浓度大于0.5 g⋅L−1时,NCP催化剂的活性位点有限,只是增加了PMS与NCP的接触率,提高了活化效率,因此CBZ去除率略有提高,基于经济性考虑,PMS最佳投加量为0.5 g⋅L−1。
|
图 6 PMS投加量对CBZ去除效果的影响 Fig.6 Influence of PMS dosage on CBZ degradation (Experimental condition: 5.0 mg⋅L−1 CBZ, 1.0 g⋅L−1 NCP, pH=6.76) |
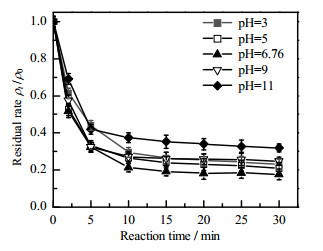
由于分子中电子分布的差异,酸度和碱度一般会影响CBZ的降解效率。为了考察初始pH值对反应体系的影响,分别对pH值为3、5、7、9、11时的CBZ去除效果进行了研究。为了避免使用缓冲液,溶液的pH值由0.1 mol⋅L−1的HCl和0.1 mol⋅L−1的NaOH进行调节。从图 7中可以看出,初始pH为3.00、5.00、6.76、9.00、11.00时,CBZ在30 min的去除率分别为76.99%、79.13%、82.34%、75.22%、68.04%。由此可见,初始pH对CBZ的去除效果有一定的影响,在初始pH为6.76时,CBZ的去除率最高(82.34%),初始pH为11时CBZ的去除率最低(68.04%)。在酸性条件下、偏酸性条件下、弱碱性条件下,CBZ去除率较高,但均低于中性条件下的去除率,而在强碱性条件下CBZ去除率较低,分析其原因有:1)强酸环境中,PMS会以H2SO5的形式存在,而不是以HSO5−的形式存在,从而造成去除率略低于中性条件[18];2)在酸性、偏酸性条件下NCP/PMS体系降解CBZ效率比碱性条件高,可能是由于酸性条件下浸出了较多的金属离子同时,对PMS进行了均相活化,产生了更多的自由基,从而CBZ去除率高于碱性[19];3)在强碱性条件下,体系中SO4-∙含量下降,∙OH含量上升,∙OH和SO4-∙会发生淬灭,导致自由基含量下降,CBZ去除率降低;碱性条件下NCP溶出的Fe2+会与反应中的OH-反应生成Fe(OH)2,降低了Fe2+对反应体系的活化能力[20]。
|
图 7 初始pH值对CBZ去除效果的影响 Fig.7 Influence of initial pH on CBZ degradation (Experimental condition: 5.0 mg⋅L−1 CBZ; 0.5 g⋅L−1 PMS, 1.0 g⋅L−1 NCP) |
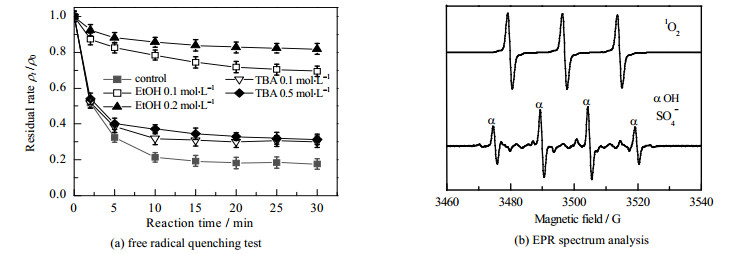
乙醇、叔丁醇分别是SO4-∙、∙OH淬灭剂,为了研究NCP/PMS体系中活性氧化物质对CBZ降解的贡献,分别考察乙醇、叔丁醇对此体系降解CBZ的影响。该方法是基于体系中产生的自由基与特定醇之间的反应性和反应速率的差异,其中乙醇可以同时淬灭SO4-∙和∙OH,而TBA只作为∙OH的捕获剂[15]。为了避免加入捕获剂而导致溶液浓度发生变化,所有曲线均为扣除捕获剂本身做空白。结果如图 8(a)所示,当体系中引入叔丁醇和乙醇时,CBZ的去除率分别为60.73%、17.01%,由此可以看出SO4-∙和∙OH是主要的活性物质。为了直接检测NCP/PMS体系中所产生的自由基,DMPO用于捕获自由基以证明反应是否产生了SO4−∙、∙OH和1O2,当NCP/PMS反应30 s时,向反应溶液中加入DMPO,检测EPR谱图,用于测定反应中自由基。由图 8(b),可以看出在NCP/PMS在DMPO体系中,典型的∙OH和SO4-∙波谱被检测到,而且信号较强,表明在活化PMS降解反应过程中,溶液中产生了大量的∙OH和SO4-∙。Qin等[21]研究表明活化PMS体系中通常存在单线态氧(1O2),2, 2, 6, 6–四甲基–4–哌啶醇是一种典型的自旋捕获探针,能够捕获1O2以形成2, 2, 6, 6-四甲基哌啶氧自由基(TEMPO)加合物。为了验证体系中1O2的存在,向反应溶液中添加TEMP,得到EPR图谱如图 8(b)所示,可以看出强度比为1:1:1的TEMPO的特征信号,所以1O2也是NCP/PMS体系中的活性物质。
|
图 8 自由基淬灭试验及EPR分析 Fig.8 Free radical quenching test and EPR analysis (Experimental condition: 5.0 mg⋅L−1 CBZ, 0.5 g⋅L−1 PMS, 1.0 g⋅L−1 NCP, pH=6.76) |
为了进一步探究NCP/PMS体系降解CBZ的机理,采用LC-MS检测CBZ的降解产物,将其与初始的CBZ溶液进行比较,鉴定出8种主要的降解产物,检测结果如表 2所示,产物的结构式等详细信息均列于表 2中。
|
|
表 2 NCP/PMS体系降解CBZ中间产物 Table 2 Intermediates of CBZ degradation in NCP/PMS process |
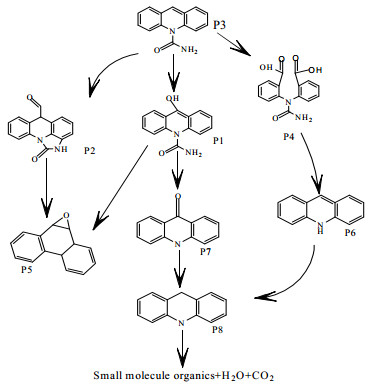
经过降解产物初步鉴定,分析上述8种中间产物的种类和组成,可以推测出卡马西平可能的降解路径,具体如图 9所示。反应开始后,由于SO4-∙和∙OH具有很强的亲电性,导致自由基倾向于攻击CBZ分子中的富电子部分,而CBZ分子的烯烃双键的电子密度较高,因此成为NCP/PMS氧化CBZ过程中的主要攻击位点。体系中的SO4-∙、∙OH将双键氧化后并插入氧原子形成环氧卡马西平,并且环氧卡马西平是降解过程中的主要中间产物。随着反应的进行,环氧卡马西平脱去一个酰胺基形成P5,进而逐步降解成P6、P7、P8,最终苯环逐渐被打开,降解成CO2、H2O和其他小分子有机物。
|
图 9 NCP/PMS降解CBZ可能的降解路径图 Fig.9 Proposed pathways for CBZ degradation in NCP/PMS process |
黄铜矿是一种天然的PMS的活化剂,将天然黄铜矿应用于水处理领域,拓展了天然黄铜矿材料的应用范围。通过试验条件的优化,得出了非均相活化PMS体系的最佳反应条件。此外,自由基淬灭试验和EPR分析表明NCP/PMS体系中存在3种主要的活性物质。最后推测了卡马西平的降解路径,随着反应的进行,苯环逐渐被打开,最终降解物质为H2O、CO2和其他小分子有机物。
| [1] |
吴秀, 方迪, 危亚云, 等. 热活化过一硫酸盐调理强化厌氧消化污泥脱水的研究[J]. 环境科学学报, 2021, 41(11): 4547-4553. WU X, FANG D, WEI Y Y, et al. Improved dewaterability of anaerobically digested sewage sludge by thermally activated peroxymonosulfate[J]. Acta Scientiae Circumstantiae, 2021, 41(11): 4547-4553. |
| [2] |
ULUCAN-ALTUNTAS K, YAZICI GUVENC S, CAN-GÜVEN E, et al. Degradation of oxytetracycline in aqueous solution by heat-activated peroxydisulfate and peroxymonosulfate oxidation[J]. Environmental Science and Pollution Research, 2022, 29(6): 9110-9123. DOI:10.1007/s11356-021-16157-7 |
| [3] |
THELUSMOND J R, KAWKA E, STRATHMANN T J, et al. Diclofenac, carbamazepine and triclocarban biodegradation in agricultural soils and the microorganisms and metabolic pathways affected[J]. Science of the Total Environment, 2018, 640/641: 1393-1410. DOI:10.1016/j.scitotenv.2018.05.403 |
| [4] |
ZHANG T H, LIU Y J, RAO Y D, et al. Enhanced photocatalytic activity of TiO2 with acetylene black and persulfate for degradation of tetracycline hydrochloride under visible light[J]. Chemical Engineering Journal, 2020, 384: 123350. DOI:10.1016/j.cej.2019.123350 |
| [5] |
WANG J L, WANG S Z. Activation of persulfate (PS) and peroxymonosulfate (PMS) and application for the degradation of emerging contaminants[J]. Chemical Engineering Journal, 2018, 334: 1502-1517. DOI:10.1016/j.cej.2017.11.059 |
| [6] |
ZHENG R J, LI J, ZHU R L, et al. Enhanced Cr(Ⅵ) reduction on natural chalcopyrite mineral modulated by degradation intermediates of RhB[J]. Journal of Hazardous Materials, 2022, 423: 127206. DOI:10.1016/j.jhazmat.2021.127206 |
| [7] |
PENG J L, ZHOU H Y, LIU W, et al. Insights into heterogeneous catalytic activation of peroxymonosulfate by natural chalcopyrite: pH-dependent radical generation, degradation pathway and mechanism[J]. Chemical Engineering Journal, 2020, 397: 125387. DOI:10.1016/j.cej.2020.125387 |
| [8] |
中华人民共和国卫生部. 中国卫生统计年鉴[M]. 北京: 中国协和医科大学出版社, 2005. Ministry of Health of the People's Republic of China. China health statistics yearbook[M]. Beijing: China Union Medical University Press, 2005. |
| [9] |
DAUGHTON C G, TERNES T A. Pharmaceuticals and personal care products in the environment: Agents of subtle change?[J]. Environmental Health Perspectives, 1999, 107(Suppl.6): 907-938. |
| [10] |
RAO Y F, QU L, YANG H S, et al. Degradation of carbamazepine by Fe (Ⅱ)-activated persulfate process[J]. Journal of Hazardous Materials, 2014, 268: 23-32. |
| [11] |
HUANG X T, ZHU T H, DUAN W T, et al. Comparative studies on catalytic mechanisms for natural chalcopyrite-induced Fenton oxidation: Effect of chalcopyrite type[J]. Journal of Hazardous Materials, 2020, 381: 120998. DOI:10.1016/j.jhazmat.2019.120998 |
| [12] |
NIE W S, MAO Q H, DING Y B, et al. Highly efficient catalysis of chalcopyrite with surface bonded ferrous species for activation of peroxymonosulfate toward degradation of bisphenol A: A mechanism study[J]. Journal of Hazardous Materials, 2019, 364: 59-68. DOI:10.1016/j.jhazmat.2018.09.078 |
| [13] |
XU X J, TANG D D, CAI J H, et al. Heterogeneous activation of peroxymonocarbonate by chalcopyrite (CuFeS2) for efficient degradation of 2, 4-dichlorophenol in simulated groundwater[J]. Applied Catalysis B: Environmental, 2019, 251: 273-282. |
| [14] |
WANG S J. Copper leaching from chalcopyrite concentrates[J]. Jom, 2005, 57(7): 48-51. DOI:10.1007/s11837-005-0252-5 |
| [15] |
王羽中. 电催化协同CoFe2O4@HAP活化过一硫酸盐处理老龄垃圾渗滤液[D]. 郑州: 郑州大学, 2021. WANG Y Z. Treatment of aged landfill leachate by electrocatalysis combined with Cofe2O2@HAP activation permonosulfate [D]. Zhengzhou: Zhengzhou University, 2021. |
| [16] |
KUO C S, LIN C F, HONG P K A. Photocatalytic degradation of methamphetamine by UV/TiO2–kinetics, intermediates, and products[J]. Water Research, 2015, 74: 1-9. |
| [17] |
高乃云, 张晏晏, 马艳. UV/TiO2去除水中磺胺甲唑的动力学及影响因素分析[J]. 中国环境科学, 2013, 3(11): 1958-1964. GAO N Y, ZHANG Y Y, MA Y. Kinetics and impact factors of sulfamethoxazole (SMX) degradation in drinking water by UV/TiO2[J]. China Environmental Science, 2013, 3(11): 1958-1964. |
| [18] |
REN Y M, LIN L Q, MA J, et al. Sulfate radicals induced from peroxymonosulfate by magnetic ferrospinel MFe2O4 (M=Co, Cu, Mn, and Zn)as heterogeneous catalysts in the water[J]. Applied Catalysis B: Environmental, 2015, 165: 572-578. |
| [19] |
范燕. 负载型钙钛矿催化剂活化过硫酸盐降解磺胺甲恶唑的研究[D]. 北京: 北京化工大学, 2021. FAN Y. Research on degradation of sulfamethoxazole by activating persulfate with supported perovskite catalyst [D]. Beijing: Beijing University of Chemical Technology, 2021. |
| [20] |
DHAKA S, KUMAR R, KHAN M A, et al. Aqueous phase degradation of methyl paraben using UV-activated persulfate method[J]. Chemical Engineering Journal, 2017, 321: 11-19. |
| [21] |
QIN Q D, LIU T, ZHANG J X, et al. Facile synthesis of oxygen vacancies enriched α-Fe2O3 for peroxymonosulfate activation: A non-radical process for sulfamethoxazole degradation[J]. Journal of Hazardous Materials, 2021, 419: 126447. |




