2. 广西民族大学 广西林产化学与工程重点实验室,广西 南宁 530006
2. Guangxi Key Laboratory of Chemistry and Engineering of Forest Products, Guangxi University for Nationalities, Nanning 530006, China
β-石竹烯是一种天然双环倍半萜烯,是重质松节油的主要化学成分[1]。同时重质松节油还含有多种沸点相近的倍半萜烯同分异构体如长叶烯,以及少量单萜烯组分如对伞花烃和3-蒈烯等。据报道β-石竹烯可以有效治疗由鱼藤酮引起的帕金森病[2]。Basha等也确定β-石竹烯能有效地缓解由链脲佐菌素引起的高血糖症状[3]。另外,β-石竹烯自20世纪30年代以来一直被广泛用作芳香化学品[4]。在Sk ld的研究中,1998年欧洲市场上45%的除臭剂含有β-石竹烯[5]。目前,β-石竹烯不仅在香料中广泛使用,而且它的乙酰化物也是一种高品味的香料,可用于香水中[6]。对伞花烃可作为用途广泛的有机合成中间体[7],包括作为麝香香料和香料中的添加剂[8],抗炎和抗菌剂以及清漆和染料溶剂[9]。对伞花烃还具有祛痰止咳的功效,临床上可用于治疗气管炎[10]。此外,3-蒈烯分子结构中同时具有三元环、六元环以及环内双键,是少数几种具有特殊三元环结构和生物活性的天然手性化合物之一[11],可用于各种食用香料[12, 13],杀虫剂以及药物[14],在许多贵重化学品如增塑剂和无毒溶剂中也有很重要的应用[15]。
虽然重质松节油组分在精细化学品合成、药物合成以及香料行业有广泛的应用,但重质松节油的沸点高、黏度大,提纯分离操作困难。因此测定重质松节油体系的超额焓数据可为重质松节油体系的提纯分离操作和设计提供基础数据及理论依据。超额焓即混合热是衡量溶液非理想性的重要标志之一,通过测定超额焓数据可以分析不同分子的相互作用[16],对化工过程的设计、优化和开发具有重要意义[17]。目前关于轻质松节油体系的超额焓测定已有文献报道。Berlin和Comelli测定了(s)-(-)-柠檬烯分别与α-蒎烯、β-蒎烯和对伞花烃三个二元体系的超额焓数据[18]。廖丹葵等测定了α-蒎烯+对伞花烃和β-蒎烯+对伞花烃二元体系的超额焓数据[19]。孙丽霞测定了α-蒎烯分别与β-蒎烯、对伞花烃和柠檬烯等多个二元体系的超额焓数据[20]。而松节油体系中含重质松节油组分的超额焓数据尚无报道,本文采用C80型Calvet微量量热仪测定对伞花烃+β-石竹烯,3-蒈烯+β-石竹烯和3-蒈烯+对伞花烃三个二元体系在常压及298.15 K下的超额焓,为松节油体系的分离提纯提供重要的基础数据。
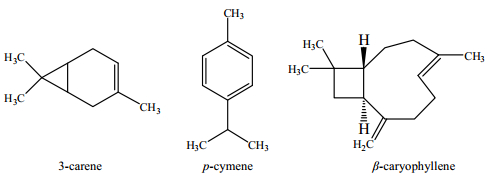
2 实验部分 2.1 试剂实验所用β-石竹烯、对伞花烃和3-蒈烯均由Tokyo Chemical Industry (TCI试剂公司)提供,其化学结构如图 1所示。Agilent 7890B气相色谱分析该三种试剂的纯度分别为97.98%(w)、98.31%(w)和96.88%(w)。上述试剂在高纯氮气保护下减压蒸馏提纯,经气相色谱检测纯度均大于99%(w)。利用Anton Paar DMA 4500M密度计与RXA170阿贝折光仪测定试剂密度和折光率,结果如表 1所示,试剂符合实验要求。
|
图 1 试剂的化学结构 Fig.1 Chemical structures of reagents |
|
|
表 1 298.15 K下实验试剂的密度ρ及折光率nD Table 1 Densities and refractive indices of the experiment chemical reagents at 298.15 K |
超额焓数据采用C80型Calvet微量量热仪(法国Setaram公司)测定。C80型Calvet微量量热仪拥有多种样品池可供选择,其中包括密封间歇池或可导入反应物带搅拌器的混合池等。本实验采用带搅拌器的不锈钢薄膜混合池,即通过混合两种物质(固体或液体)研究其反应热。C80型Calvet微量量热仪有两个相对独立的量热器,量热器中的混合池分为参比池和样品池。参比池和样品池均位于圆柱形量热器的中心,每个量热器列阵有共有9个同心圆环,每个圆环包含38对热电偶以形成圆柱体[25]。因此,样品池和参比池完全被热电偶检测器所包围,这些检测器可以测量所有放出或吸附的热量。当混合池体中的样品发生放热或吸热变化时,必定会发生热交换,从而两界面间的热流量会发生相应的变化。若测试样品混合是放热过程,则样品池中的热流量高于参比池的热流量;若测试样品混合是吸热过程,则样品池中的热流量低于参比池的热流量[20]。基于测试体系的温度与导热速率成正比关系,在环境温度相同的条件下(即温差为零),两个量热器以热量补偿的方式来保持整个系统温度恒定不变,从而得出测量样品的热量吸收或放出对于温度或时间的关系式。
C80型Calvet微量量热仪是基于Tian-Calvet热流原理的热导式量热仪,Tian-Calvet热流原理[26]的热效应Q符合下列方程:
| $Q = KA$ | (1) |
其中,A为量热过程中热谱曲线的积分面积,m2;K为量热常数,J·m-2。
二元溶液的超额焓
| ${H^{\rm E}} = Q/n$ | (2) |
其中,n为混合物的总摩尔数。
2.3 实验过程电子分析天平(Sartorius BSA124S-CW,精度为±0.1 mg)用于称量纯组分质量。待混合的两种试剂经称量后分别放入样品池的上下两侧,并置于量热器通道内。同时,参比池的上下两侧放入与样品池下侧相同且质量配比相同的试剂,并置于另一个量热器通道内。打开Calisto软件设置恒温程序,在298.15 K下恒定5 h且热流信号稳定后,在软件中运行预先设置的实验程序。待热流基线平坦后,同时压下搅拌杆刺破参比池与样品池的薄膜并以相同速度旋转搅拌杆,使薄膜上下两种物质混和充分[20]。程序运行结束后,热谱曲线和基线之间的面积积分为反应混合热,即超额焓
为检验C80型Calvet微量量热仪及操作方法的可靠性,选用国际纯粹与应用化学联合会(IUPAC)推荐的环己烷(1)+正己烷(2)为标准体系,在298.15 K下测定超额焓。使用IUPAC推荐的式(3)计算标准体系在298.15 K的超额焓[27]。
| ${H^{\rm E}} = x(1 - x)[866.10 - 249.4(1 - 2x) + 97.0{(1 - 2x)^2} - 31.8{(1 - 2x)^3}$ | (3) |
|
|
表 2 298.15 K下环己烷正己烷体系的超额焓 Table 2 Excess enthalpies of cyclohexane +n-hexane at 298.15 K |
其中,x为环己烷的摩尔分数。
采用Redlich-Kister方程关联超额焓数据,如式(4)所示:
| ${H^{\rm E}} = x(1 - x)\sum\limits_{k = 0}^N {{h_k}{{(1 - 2x)}^k}} $ | (4) |
其中,hk, k = 0, 1, 2, 3—Redlich-Kister方程系数,可由实验数据关联得到。
标准偏差由式(5)计算:
| $\sigma ({H^{\rm{E}}}) = {\left( {\frac{1}{{N - n}}{{\sum\limits_{i = 1}^N {\left( {H_{{\rm{cal}}}^{\rm{E}} - H_{{\rm{exp}}}^{\rm E} \right)} }^2}} \right)^{1/2}}$ | (5) |
其中,N为试验点数;n为系数的个数;
实验结果、IUPC推荐方程计算结果以及Redlich-Kister方程关联结果列于表 2,标准体系的拟合系数对比结果列于表 3。
|
|
表 3 标准体系的拟合系数对比 Table 3 Comparison of the correlative coefficients of standard systems |
由表 2及表 3可见,采用C80型Calvet微量量热仪测定环己烷+正己烷体系超额焓数据与方程(4)关联结果较好吻合,标准误差为0.4830 J·mol-1,表明使用该仪器测定的实验数据是可靠的。
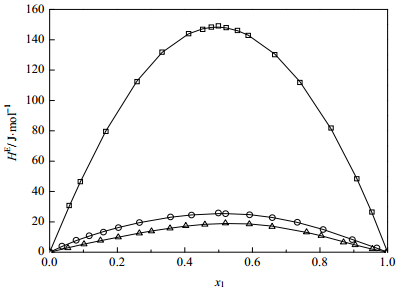
3.2 二元体系超额焓测定采用C80型Calvet微量量热仪测定3-蒈烯+对伞花烃,3-蒈烯+β-石竹烯和对伞花烃+β-石竹烯三个二元体系在常压及298.15 K下的超额焓数据。实验结果及Redlich-Kister方程的关联结果如表 4至表 6所示,Redlich-Kister方程的拟合系数与标准误差如表 7所示。三个二元体系的超额焓数据测定结果与关联结果如图 2所示。
|
|
表 4 298.15 K下对伞花烃+β-石竹烯体系的超额焓 Table 4 Excess enthalpies of p-cymene+β-caryophyllene at 298.15 K |
|
|
表 5 298.15 K下3-蒈烯+β-石竹烯体系的超额焓 Table 5 Excess enthalpies of 3-carene +β-caryophyllene at 298.15 K |
|
|
表 6 298.15 K下3-蒈烯+对伞花烃体系的超额焓 Table 6 Excess enthalpies of 3-carene +p-cymeneat 298.15 K |
|
|
表 7 Redlich-Kister方程系数及标准误差 Table 7 Coefficients and standard errors of Redlich-Kister equation |
|
图 2 298.15 K下对伞花烃(1)+β-石竹烯和3-蒈烯(1)+β-石竹烯以及3-蒈烯+对伞花烃二元体系的超额焓
Fig.2 Excess enthalpies HE of p-cymene +β-caryophyllene, 3-carene +β-caryophyllene and 3-carene +p-cymene at 298.15 K
○ p-cymene + β-caryophyllene △ 3-carene + β-caryophyllene □ 3-carene + p-cymene — Redlich-Kister correlation |
由表 4~6可知,三个二元体系超额焓的实验值与Redlich-Kister方程的关联值的相对偏差及相对误差均较小,表明测量数据准确可靠。由表 7及图 2可知,三个二元体系对伞花烃+β-石竹烯,3-蒈烯+β-石竹烯以及3-蒈烯+对伞花烃的超额焓均为正值,且最大值均在摩尔分数x1 = 0.5附近。利用Redlich-Kister方程关联三个二元体系的超额焓的标准偏差较小,分别为0.2151、0.1733和0.4483 J·mol-1,关联结果较为满意。
通常情况下,两种不同液体混合,当异种分子之间相互作用小于同种分子间相互作用之和时,超额混合焓为正值[28],因此从实验结果可得出,各个二元体系的异种分子间的相互作用均大于同种分子间的相互作用之和。此外,在298.15 K下3-蒈烯+对伞花烃体系的超额焓均大于含重质松节油组分的对伞花烃+β-石竹烯和3-蒈烯+β-石竹烯体系。这是由于3-蒈烯与对伞花烃均为环内双键,空间效应使得3-蒈烯与对伞花烃混合需要更多的热量。而β-石竹烯分子中的双键均裸露在环外,因此与3-蒈烯或对伞花烃混合吸收的热量较少。对伞花烃与3-蒈烯虽同属单萜化合物,但由于对伞花烃的大π键比3-蒈烯的双键稳定,因此对伞花烃+β-石竹烯体系的超额焓稍大于3-蒈烯+β-石竹烯体系。
4 结论(1) 使用C80型Calvet微量量热仪测定了标准体系环己烷+正己烷在298.15 K下的超额焓,同时采用Redlich-Kister方程进行关联实验数据。实验结果与IUPAC推荐方程及Redlich-Kister方程关联结果均吻合较好,标准偏差为0.4830 J·mol-1,表明使用该量热仪所测定的实验数据是可靠的。
(2) 使用C80型Calvet微量量热仪测定了对伞花烃+β-石竹烯和3-蒈烯+β-石竹烯以及3-蒈烯+对伞花烃三个二元体系的超额焓,各个体系的超额焓在全浓度范围内均大于零,其最大值均出现在摩尔分数x1 = 0.5附近。采用Redlich-Kister方程对实验数据关联进行关联,标准偏差分别为0.2151、0.1733和0.4483 J·mol-1。从关联结果可知,本实验测定的超额焓与关联结果吻合较好。
(3) 在298.15 K下,三个二元体系超额焓的大小顺序为:3-蒈烯+对伞花烃体系 > 对伞花烃+β-石竹烯体系 > 3-蒈烯+β-石竹烯体系。
符号说明:
| A | — 热谱曲线的积分面积,m2 | Q | — 热效应,J |
| AD | — 相对偏差,J·mol-1 | RD | — 相对误差,% |
| HE | — 二元溶液超额焓,J·mol-1 | x | — 组分的摩尔分数,无量纲 |
| hk | — Redlich-Kister方程系数,无量纲 | ρ | — 密度,g·cm-3 |
| i | — 试验点数,无量纲 | σ | — 标准偏差,J |
| K | — 量热常数,J·m-2 | 下标 | |
| N | — 试验点数,无量纲 | cal | — 计算值 |
| n | — 混合物的总摩尔数,无量纲 | exp | — 实验值 |
| nD | — 折射率,无量纲 | k | — 0, 1, 2, 3 |
| [1] | Huang M, Sanchez-Moreiras A M, Abel C, et al. The major volatile organic compound emitted from arabidopsis thaliana flowers, the sesquiterpene (E)-β-caryophyllene, is a defense against a bacterial pathogen[J]. New Phytologist, 2012, 193(4): 997-1008. |
| [2] | Ojha S, Javed H, Azimullah S, et al. β-Caryophyllene, a phytocannabinoid attenuates oxidative stress, neuroinflammation, glial activation, and salvages dopaminergic neurons in a rat model of Parkinson disease[J]. Molecular and Cellular Biochemistry, 2016, 418(1): 59-70. |
| [3] | Basha R H, Sankaranarayanan C. β-Caryophyllene, a natural sesquiterpene lactone attenuates hyperglycemia mediated oxidative and inflammatory stress in experimental diabetic rats[J]. Chem-Biological Interactions, 2016, 245(5): 50-58. |
| [4] | Jung J I, Kim E J, Kwon G T, et al. β-Caryophyllene potently inhibits solid tumor growth and lymph node metastasis of B16F10 melanoma cells in high-fat diet-induced obese C57BL/6N mice[J]. Carcinogenesis, 2015, 36(9): 1028-1039. |
| [5] | Sköld M, Karlberg A T, Matura M, et al. The fragrance chemical β-caryophyllene-air oxidation and skin sensitization[J]. Food and Chemical Toxicology, 2006, 44(4): 538-545. |
| [6] | LIU Xiao-yu(刘晓宇), CHEN Xu-bing(陈旭冰), CHEN Guang-yong(陈光勇). Research progress in bioactivity and synthesis of β-caryophyllene and its derivatives(β-石竹烯及其衍生物的生物活性与合成研究进展)[J]. Chemistry and Industry of Forest Products(林产化学与工业), 2012, 1(32): 104-110. |
| [7] | WANG Lin-lin (王琳琳). The catalytic process of intermolecular hydrogen transfer reaction of rosin (松香、松节油及松脂中分子间氢转移催化反应的研究)[D]. Nanning (南宁): Guangxi University (广西大学), 2007. http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=Y1319491 |
| [8] | Retajczyk M, Wróblewska A. The isomerization of limonene over the Ti-SBA-15 catalyst-the influence of reaction time, temperature, and catalyst content[J]. Catalysts, 2017, 7(9): 273. |
| [9] | Sun L X, Liao D K, Yang Z Y, et al. Measurement and correlation of (vapor + liquid) equilibrium data for {α-pinene +p-cymene +(S)-(-)-limonene} ternary system at atmospheric pressure[J]. Journal of Chemical Thermodynamics, 2013, 58: 416-421. |
| [10] | XU Xiao-qin(徐晓琴), LIAO Dan-kui(廖丹葵), LI Li-shuo(李立硕), et al. Determination and correlation of atmospheric VLE data of α-pinene +β-pinene +p-cymene(α-蒎烯+β-蒎烯+对伞花烃常压汽液平衡测定与关联)[J]. Journal of Chemical Industry and Engineering(化工学报), 2007, 58(12): 2970-2974. DOI:10.3321/j.issn:0438-1157.2007.12.003. |
| [11] | Banina O A, Sudarikov D V, Frolova L L, et al. Carane amino alcohols as organocatalysts in asymmetric aldol reaction of isatin with acetone[J]. Russian Chemical Bulletin, 2017, 66(2): 293-296. |
| [12] | Yan Z L, Wang C L, Hou L H, et al. Extraction of oleoresin from Dao-Kou roasted chicken flavor spice blends using supercritical carbon dioxide[J]. Food Analytical Methods, 2017, 10(4): 900-909. DOI:10.1007/s12161-016-0614-3. |
| [13] | Torregiani E, Lorier S, Sagratini G, et al. Comparative analysis of the volatile profile of 20 commercial samples of truffles, truffle sauces, and truffle-flavored oils by using HS-SPME-GC-MS[J]. Food Analytical Methods, 2017, 10(6): 1857-1869. DOI:10.1007/s12161-016-0749-2. |
| [14] | Lee H R, Lee S C, Lee D H, et al. Identification of the aggregation-sex pheromone produced by male monochamus saltuarius, a major insect vector of the pine wood nematode[J]. Journal of Chemical Ecology, 2017, 43(7): 670-678. |
| [15] | Alparslan Y, Baygar T. Effect of chitosan film coating combined with orange peel essential oil on the shelf life of deep water pink shrimp[J]. Food and Bioprocess Technology, 2017, 10(5): 842-853. |
| [16] | MA Pei-sheng(马沛生), XIA Shu-qian(夏淑倩), WU Xiao-xiang(吴小香). The experimental determination and correlation of excess enthalpies of binary systems of cyclohexanone with different alcohols(环己酮-醇二元系统超额焓测定与关联的研究)[J]. Acta Physico-Chimica Sinica(物理化学学报), 2002, 18(7): 644-648. DOI:10.3866/PKU.WHXB20020716. |
| [17] | RUAN Fu-xian(阮付贤), CHE Jin-jie(车锦楷), HU Jing(胡静), et al. Vapor-liquid equilibrium of α-pinene-pinnae-longifolene systems and their excess Gibbs free energy and excess enthalpy(α-蒎烯-蒎烷-长叶烯体系汽液平衡及其过量Gibbs自由能与超额焓)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报), 2015, 29(6): 1306-1322. DOI:10.3969/j.issn.1003-9015.2015.06.004. |
| [18] | Berlin A, Comlli F. Excess molar enthalpies of binary mixtures containing pine resins in the range 288.15~313.15 K, and at atmospheric pressure:use of the extended cell model of prigogine[J]. Thermochimica Acta, 2001, 373(1): 45-51. |
| [19] | LIAO Dan-kui(廖丹葵), MENG Xue-lin(孟学林), WU Xiang-hong(武向红), et al. Determination of excess enthalpies for binary systems of α-pinene +p-cymene and β-pinene +p-cymene(α-蒎烯+对伞花烃和β-蒎烯+对伞花烃二元体系超额焓的测定)[J]. Acta Physico-Chimica Sinica(物理化学学报), 2006, 22(11): 1419-1422. DOI:10.3866/PKU.WHXB20061122. |
| [20] | SUN Li-xia (孙丽霞). Measurement and calculation of vapor-liquid equilibrium and excess enthalpy data for main constituents in turpentine oil system (松节油体系主要成分的汽液平衡与超额焓的测定与计算)[D]. Nanning (南宁): Guangxi University (广西大学), 2013. http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=Y2407543 |
| [21] | Speight J G. Lange's handbook of chemistry[M]. 16th ed. New York: Mc Graw-Hill, 2005. |
| [22] | Haynes W M, Lide D R, Bruno T J. CRC handbook of chemistry and physics[M].95th ed, Boca Raton: CRC Press, 2014. |
| [23] | MA Pei-sheng(马沛生). Experimental handbook of physical properties of organic compounds-carbon, hydrogen, oxygen, halogen section(有机化合物实验物性数据手册-含碳、氢、氧、卤部分)[M].Beijing(北京): Chemical Industry Press(化学工业出版社), 2006. |
| [24] | Ribeiro A, Bernado-Gil M G. Densities and refractive indices of components of pine resin[J]. Journal of Chemical Engineering Data, 1990, 35(2): 204-206. |
| [25] | Letyanina I, Tsvetov N, Zvereva I, et al. Excess molar enthalpies for binary mixtures of n-propanol, acetic acid, and n-propyl acetate at 313.15 K and atmospheric pressure[J]. Fluid Phase Equilibria, 2014, 381(15): 77-82. |
| [26] | Calvet E, Prat H. Microcalorimétrie: applications physico-chimiques et biologiques[M]. Paris: Masson et Cie, 1956. |
| [27] | McGlashan M L, Hugill J A. The vapor pressure from 451 K to the critical temperature, and the critical temperature and critical pressure, of cyclohexane[J]. Journal of Chemical Thermodynamics, 1978, 10(1): 95-100. |
| [28] | Gruszkiewicz M S, Sipowska J T, Qtt J B, et al. Excess enthalpies for (ethane + ethene) at the temperatures (273.15, 298.15, 323.15, 348.15, and 363.15) K and the pressures (5, 7.5, 10, 12.5, and 15) MPa[J]. Journal of Chemical Thermodynamics, 1995, 27(5): 507-524. |




