2. 新能源系统工程与装备陕西省高校工程研究中心, 陕西 西安 710049
2. Engineering Research Center of New Energy System Engineering and Equipment, University of Shaanxi Province, Xi'an 710049, China
氨(NH3)作为重要的工业化学品之一,在氮肥生产、医药研发、炸药研制等方面均有广泛应用[1]。然而,如何在温和条件下实现NH3的合成是当今的主要化学难题之一[2]。传统的Haber-Bosch工艺,因其严苛的反应条件以及资本、能源高度集中的生产规模,其每年的化石燃料消耗量占据全球总量的1%[3]。对此,人们亟须开发一种绿色环保的合成NH3途径,以替代目前主导工业NH3生产的Haber-Bosch工艺。近年来,NH3的电催化合成被视为可能的替代路线已被大量学者研究报道[1-2, 4-5]。然而,受限于氮N2分子三键的活化障碍以及水溶液中强烈的析氢反应(HER)竞争,致使氮还原反应(NRR)的电催化选择性被严重抑制,相关催化剂的开发设计也尚未达到实际的应用需求[6-7]。1993年,Tsuneto等[8]创新性地提出了锂介导的电化学合成NH3方法(LM-NRR),其采用有机溶剂(如四氢呋喃)(THF)替代电催化的水相体系,通过提供易于N2反应的活性Li表面以及浓度可控的外加质子源,如乙醇(EtOH),克服了惰性N2活化以及HER竞争的两大难题[9]。此外,该方法的机理可行性以及NH3来源的真实性也被大量研究报道所证实[6, 10-11],并显示出较高的法拉第效率(FE)[10, 12],具有良好的工业化发展潜力[8]。
目前,学者们普遍认可LM-NRR过程遵循均相的循环机理[8-9],包括Li+的沉积、Li的氮化以及Li3N的质子化3个步骤。首先,溶液中的Li+获得电子还原沉积在电极上;随后,单质Li在室温条件下自发分解N2并生成高能中间产物Li3N;最后,在弱酸性质子源的作用下,Li3N发生质子化,产生NH3和Li+并结束循环过程。因此,如何在反应界面处稳定提供充足的Li源,并使其有效参与NRR过程是决定LM-NRR体系持续高效产NH3的关键。然而,在实际的生产NH3过程中,由于Li的高反应活性,反应界面上的表面Li会同时诱导诸如HER、电解质分解等一系列副反应发生,降低体系的NH3合成性能。此外,NH3生产过程中的水污染问题也会对LM-NRR体系的电化学性能造成严重的影响[7, 13]。Lazouski等[7]研究发现,使用未经干燥处理的THF用于合成实验,其自身固有的微量水(约0.03 mol⋅L−1)会使体系的NRR性能下降近40%。Sažinas[14]及Cai等[15]的研究表明,随着反应的进行,电极表面的高能活性Li会不断地与有机电解质发生一系列的副反应。其中不乏微量水的生成,随着这些微量水不断积聚累加,会进一步参与并引发新的界面副反应,降低体系的电化学性能及稳定性。近年来,学者们针对LM-NRR界面上复杂反应问题,通过电解质的筛选[14, 16-18]、电极材料制备[15, 19-20]、电解液添加剂的设计[11, 21-22]以及电解策略的开发[10]等方面进行综合优化,实现了表面Li的均匀沉积以及竞争性析氢的有效抑制,取得了一定的实质性进展。但在水污染问题上,已有的文献报道仅局限于性能影响的对比测试和纯化干燥策略的提出[7, 19, 23],尚未对其参与或诱导的界面副反应进行综合分析,相关的影响规律及界面作用机理仍较为匮乏。
基于以上考虑,本研究采用自制的双室反应器在室温常压下实现了NH3的连续合成,测试了体系在不同含水量下的电化学性能,归纳了水含量对体系的影响规律,并进一步通过SEM,XRD,XPS等表征手段探讨了水在反应界面上的作用机理,旨在为LM-NRR体系的界面调节策略开发以及新型电解质设计优化提供参考。
2 实验材料与方法 2.1 化学试剂与材料实验所用的四氢呋喃(纯度为99.5%),水杨酸(纯度为99.5%),氢氧化钠(纯度为98%)及氢氧化钾(1 mol⋅L−1)购自江苏艾康生物医药研发有限公司;四氟硼酸锂(纯度为98%),购自上海蔚霆商贸有限公司;次氯酸钠(有效氯质量分数为13%~16%),购自北京迈瑞达科技有限公司;氯化铵(纯度为99%),购自成都科隆化学品有限公司;硝普钠(纯度为99.0%),购自上海迈瑞尔化学技术有限公司;乙醇(纯度为99.7%),盐酸(质量分数为36%~37%),购自国药集团化学试剂陕西有限公司;3501隔离膜(膜厚25 μm),购自东莞科路得实验器材科技有限公司;氮气,氩气,购自陕西快特气体有限公司。上述试剂使用前无需进一步纯化,所有实验用水均为自制超纯水。
2.2 电解质的配制首先,将LiBF4置于真空烘箱120 ℃干燥12 h后转入手套箱中保存备用。称取适量LiBF4溶于THF溶液中,搅拌2 h得到1 mol⋅L-1 LiBF4的溶液。随后,额外加入体积分数ϕ=1% 的无水乙醇至上述溶液中,搅拌2 h以形成透明澄清的电解质溶液。电解质的配制均在手套箱中进行,并在配制后12 h内使用。
2.3 电极制备以1 cm×1 cm的铜片和铂片分别作为电解池的工作电极和对电极,电极使用前需用砂纸抛光,并用超纯水冲洗后在80 ℃下干燥30 min备用。
2.4 电化学测试实验借助电化学工作站(CHI 660e,上海辰华有限公司),采取三电极系统进行电化学测试。如图 1所示,电化学实验在定制的双室电解池中进行,电解池腔室间通过3501膜分隔,所有电池部件均用超纯水洗涤以去除任何污染,并在电解池组装前在80 ℃下干燥30 min以去除残留的水分。其中,电极的反应面积为1 cm2,各腔分别加入1.6 mL电解质溶液(含水量的对比实验需额外加入定量的超纯水,加入量分别为0、20、50 μL),铂丝插入阴极室,作为电化学测量的准参考电极。实验前,通过线性扫描伏安法(LSV)测得Li/Li+的还原电位为−3.5 V,并以此值作为后续电极电位测量的参考标准。除对照实验外,所有的电化学性能测试均在恒定电流为3 mA⋅cm−2、N2流量为4 mL⋅min−1的条件下进行。N2先后经KOH及THF溶液清洗后通入反应器,并连续吹扫30 min以使电解质中的N2达到饱和。随后,依据实验条件对体系施加恒定电流,进行NH3合成实验,并随时记录体系的反应电位变化。合成实验结束后,迅速将电解液从阴极室取出,并用水稀释定容至50 mL用于后续NH3的定量。

|
图 1 双室电解池 Fig.1 Schematic diagram and images of the two compartments cell |
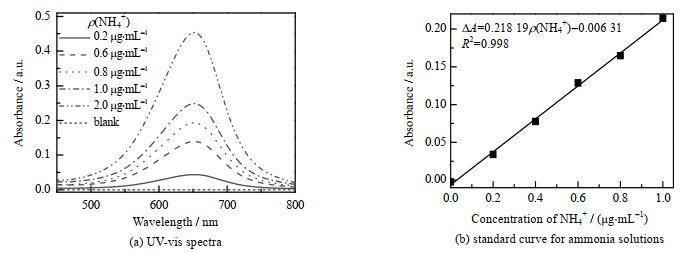
本研究采用靛酚蓝法测定电解液中NH3的浓度。每次移取待测样品4 mL,依次加入硝普钠、次氯酸钠以及水杨酸溶液后充分混合,并在黑暗中静置反应2 h,最后将显色后的样品依次放入紫外/可见分光光度计(UV-1800S,上海美析仪器有限公司)中进行检测。如图 2所示,为降低有机溶剂对吸光度的影响,采用扣除空白样后的650 nm吸光度值进行NH3标准浓度梯度曲线的建立。图中,ρ(NH4+)为标准显色样品中NH4+质量浓度,μg⋅mL−1;ΔA为扣除空白样后的650 nm吸光度值;R2为相关系数。
|
图 2 标准溶液的紫外-可见光谱及有机标准曲线图 Fig.2 UV-vis spectra and standard curve of ammonia standard solutions |
NH3的生产速率v(μg⋅s−1⋅cm−2)计算式如下:
| $v=\frac{n_{\mathrm{NH}_3}}{A t}$ | (1) |
NH3的法拉第效率FE(%)计算式如下:
| $\mathrm{FE}=\frac{z F n_{\mathrm{NH}_3}}{Q} \times 100 \%$ | (2) |
式中:nNH3为生成物的实际物质的量,mol;A为电极反应面积,cm2;t为电解时间,s;z为每摩尔生成物反应转移的电子数,z=3;F为法拉第常数,F=96 485 C⋅mol−1;Q为反应总电荷量,C。
2.6 NH3来源检测对照实验对照实验借助控制锂盐含量、供给气体、电流大小3个方面进行NH3来源的检测鉴定。每组对照实验均只涉及单一变量的控制变化。对照实验除特定的控制条件与常规测试不同,其余实验条件和操作细节均与常规测试保持一致。具体的对照实验条件如下:
对照实验1:配制不添加LiBF4的ϕ=1%无水乙醇的THF溶液代替原有电解质溶液,其余实验条件和操作细节与常规测试保持一致;
对照实验2:使用Ar气代替原有的N2,其余实验条件和操作细节与常规测试保持一致;
对照实验3:恒电流条件由常规的3 mA⋅cm−2替换成0 mA⋅cm−2,即在不施加任何电流的条件下进行锂介导合成氨实验,其余实验条件和操作细节与常规测试保持一致。
2.7 电极结构和表面形貌表征本研究采用X射线衍射仪(XRD,XRD-6100,日本Shimadzu)分析电极材料的晶体结构和组成,以Cu作为靶面,扫描角度为20°~80°;电极表面元素及其价态则采用X射线光电子能谱仪(XPS,Thermo Fisher ESCALAB Xi+,赛默飞世尔科技)分析;电极的表面形貌演变则通过扫描电子显微镜(SEM,GEMINI 500,Zeiss)观测。
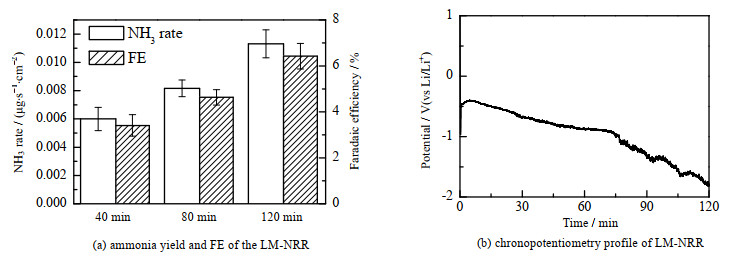
3 实验结果与讨论 3.1 LM-NRR电化学性能为探究LM-NRR的电化学性能,在3 mA⋅cm−2恒定电流条件下测试了体系在不同反应时间下的产NH3速率和FE。如图 3(a)所示,在测试时间范围内,随着反应时间的延长,LM-NRR体系的NH3合成速率不断提高,反应120 min后的NH3合成速率为0.012 4 μg⋅s−1⋅cm−2,FE可达7.05%。进一步分析图 3(b)可知,反应体系经约−1 V(电极电位的测量参考标准为Li/Li+的还原电位(vs Li/Li+))的反应过电位后趋于稳定,电位随反应的进行而缓慢下降。这一现象与Lazouski等[7]的报道一致,表明Li+在反应过程中不断地在Cu表面发生还原沉积,尽管这在一定程度上增大了界面阻抗并使反应电位下降,但随着Cu电极表面的活性Li不断增多,单位时间内可活化的N2量增大,进而有效地促进NRR进行,提高了N2的转化速率。但同时,当反应进行至近75 min时,体系的反应电位急剧下降并伴随着明显的波动。结合已有文献报道[10],推测是由于实验进行至后期,Cu电极表面由于大量副反应产生的固态电解质组分积聚以及Li的多层堆叠沉积所致。伴随着表面Li层的不断增厚,过多的Li源会进一步促进各类反应发生,使得界面反应电位剧烈波动的同时,相关反应副产物的界面累积也使得界面阻抗激增,反应电位急剧下降。
|
图 3 LM-NRR电化学测试结果 Fig.3 Electrochemical performance of LM-NRR |
综合上述分析可知,随着反应的连续进行,Li+不断地在Cu表面还原沉积,增大了界面电阻的同时也提供了更多的活性Li表面,宏观上促进了NRR的进行,提高了体系的合成NH3性能和FE;但在反应后期,随着Li重复堆叠沉积形成更厚的界面(SEI),界面阻抗急剧增大,体系的稳定性逐渐受到影响。尽管进一步延长反应时间可能会得到更高的NH3产率,但这种牺牲体系反应稳定性换取高NH3生产速率的研究不具有现实意义。为此,本研究的测试时间均限制在2 h内。表 1列举了本工作与近期报道的电化学NRR体系的NH3合成性能,表中1% 为乙醇的体积分数。由表可知,本工作通过使用有机溶剂THF替代水相体系,克服了水相体系中的强烈析氢难题,避免了高选择性电极催化材料的复杂制备过程,利用廉价易得的Cu电极即可实现常温常压下NH3的连续合成,并具有较高的NH3合成速率和FE。
|
|
表 1 与文献报道的电化学NRR体系的合成氨性能对比 Table 1 Comparison of ammonia synthesis performance with reported electrochemical NRR systems |
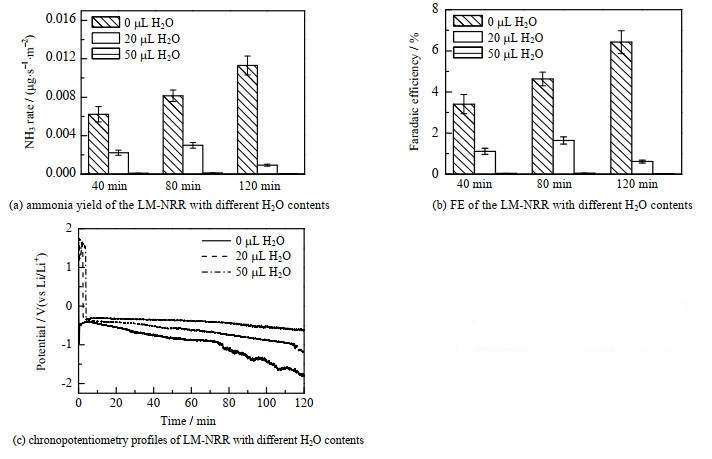
正如前文所述,尽管LM-NRR体系能有效抑制HER竞争,但由于有机试剂自身固有的含水量以及溶剂副反应产生的痕量水累积等问题[7, 14],体系在实验过程中不可避免地受到微量水污染的影响,在反应界面处诱导一系列副反应发生,致使NRR电化学活性下降。因此,为探究水污染对体系的性能影响,测试了不同含水量下LM-NRR体系的电化学性能,结果如图 4所示。由图 4(a)、(b)可知,随着体系含水量的增加,LM-NRR体系的产NH3速率和FE急剧下降,当外加水量为50 μL时,反应体系几乎丧失NRR活性。此外,在外加水量为20 μL的条件下,随着反应时间的延长,体系合成NH3的能力呈现先增后减的趋势,这可能与质子源过多供给所导致的高电位下HER竞争加剧有关[23]。进一步分析图 4(c)的反应电位测试结果可知,在外加水源的影响下,含水体系在反应过程初期均出现了一个新的反应阶段,且其反应电位明显高于Li的沉积电位。结合已有文献报道[15, 23],推测该阶段的主要反应为HER,表明水的引入造成了质子源的过多供给,进而极大地促进了HER发生,致使反应初期阶段优先发生HER,严重降低了体系的FE及NH3的合成能力。
|
图 4 水污染对LM-NRR电化学性能影响 Fig.4 Effects of water contents on electrochemical performance of LM-NRR |
综合上述性能分析结果可知,即便是微量水的引入也会对体系的合成NH3性能造成严重的影响。为进一步研究水含量对反应界面的影响,探讨可能的作用影响机理,本研究采用SEM对比观察了不同含水量(0 μL、50 μL)下反应2 h的Cu电极表面,结果如图 5所示。由图 5(a)可见,无H2O条件下Li的表面沉积较为均匀,无明显的枝晶形成。图 5(b)中进一步的放大观察可知,无水条件下的Li以细小的点粒状沉积,表明体系中新沉积的活性Li能及时参与界面反应,避免了枝晶形成,有利于体系的NH3合成性能及FE的提高[25]。对比图 5(c)、(d)中的表面形貌不难发现,高含水量下Li层的表面粗糙不均,并且Li的沉积呈现丛状的聚集结构。这种连片的丛状聚集沉积不同于常见的Li枝晶结构,推测是由于锂表面在水的作用下生成了大量的反应惰性SEI组分,这些SEI组分在有效传导Li+定向沉积的同时,也隔绝了Li与界面物质的接触,使得Cu电极表面沉积大量无法参与界面反应的“惰性Li”,进而降低了体系的NRR活性。

|
图 5 Cu电极表面SEM测试结果 Fig.5 SEM images of Cu electrode |
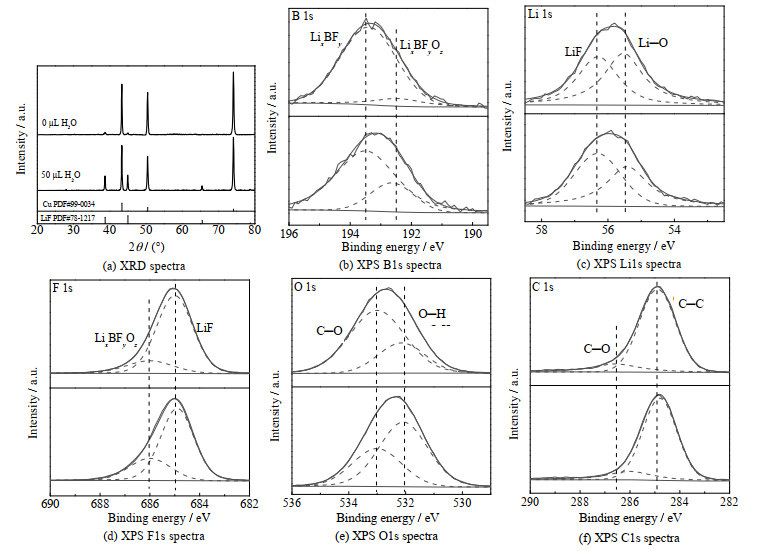
为验证上述猜想,本研究进一步对Cu电极进行了XRD测试以及表面XPS表征,结果如图 6所示。图 6(a)为XRD的测试结果,其中2θ为43.3°、50.4°、74.1°的衍射峰对应于金属电极Cu(PDF#99-0034),而2θ为40.1°、44.9°、65.5°、78.8°的衍射峰对应于LiF(PDF#78-1217)。对比不同含水量下XRD衍射峰信号的强弱可知,体系在引入50 μL水进行NRR反应后Cu电极上的LiF衍射峰信号明显增强,表明水的引入会促进Li表面副产物LiF的生成,推测是由于LiBF4发生水解并产生LiF、BOF以及HF等副产物所致[26]。
|
图 6 Cu电极表面XRD及XPS表征结果对比 Fig.6 XRD patterns and XPS spectra of Cu electrode surface |
进一步分析图 6(b)~(d)表面XPS表征结果,其中,Li 1s 56.4 eV及F 1s 684.9 eV处的峰表明LiF的存在[27],这与XRD的测试结果一致;B 1s 193.5 eV的B─F键表明体系可能存在LixBFy[28];Li 1s 55.4 eV处的Li─O键、O 1s 532 eV处的O─H键以及C 1s处的C─O键特征峰则可归因于Li的副反应产物LiOH[29]及有机Li化合物RLi[30],推测是LiBF4水解[26]及THF副反应[14]所产生;此外,B 1s 192.6 eV的B─O键特征峰以及F 1s 686 eV处O─F键特征峰表明Cu电极表面可能存在着LixBFyOz等物质[31]。通过对比不同含水量下的物质组成变化可知,随着含水量提高,体系中B─F键的特征峰强度下降,而─OH、B─O、O─F以及LiF的峰强度均有所增大,表明微量水的引入会促进Li盐的水解,并在电极表面副反应产生更多的LiF、LiOH以及LixBFyOz等物质。
结合上述结果可知,水的引入会诱导界面副反应产生大量的LiF、LiOH等物质,随着这些组分的不断生成,Li层表面逐渐被覆盖而失去反应活性,进而在Cu的表面沉积大量丛状聚集结构的“惰性Li”,增大界面阻抗的同时,也极大地降低了体系的NH3合成性能。综上,结合相关文献报道[26, 32-33],作者推测水在反应界面上的影响作用机理可归纳为以下3个方面:(1)加剧HER竞争;(2)促进LiBF4水解;(3)降低活性Li表面位点。其过程可能涉及的典型副反应如下:
| $2 \mathrm{H}_2 \mathrm{O} \xrightarrow{\mathrm{e}^{-}} 2 \mathrm{OH}^{-}+\mathrm{H}_2 \uparrow \xrightarrow{\mathrm{Li}} 2 \mathrm{LiOH}+\mathrm{H}_2 \uparrow$ | (3) |
| $\mathrm{LiBF}_4+\mathrm{H}_2 \mathrm{O} \longrightarrow 2 \mathrm{HF}+\mathrm{LiF} \downarrow+\mathrm{BOF} \uparrow$ | (4) |
| $2 \mathrm{Li}+2 \mathrm{HF} \longrightarrow 2 \mathrm{LiF} \downarrow+\mathrm{H}_2 \uparrow$ | (5) |
| $\mathrm{Li}+\left(\mathrm{CH}_2\right)_4 \mathrm{O} \xrightarrow{\mathrm{H}^{+}} \mathrm{CH}_3\left(\mathrm{CH}_2\right)_3 \mathrm{OLi}$ | (6) |
如式(1)所示,水的引入一方面提高了反应界面的H+浓度,加剧了HER竞争[32];另一方面,水还会促进LiBF4的分解产生HF、LiF以及BOF[26](式2),这些物质在一定条件下还会进一步生成无机化合物LixBFyOz[31]。此外,水解产物中的HF作为强酸质子给体,会诱导反应界面上HER(式3)及电解质副反应(式4)的发生[14, 33],使得更多的表面活性Li被上述副反应占据,降低了体系NRR活性及FE[26]。其次,伴随着大量副反应的发生,LiF会逐渐富集并覆盖于Li层表面形成无机的SEI膜。LiF作为锂离子电池SEI膜中常见的无机组分,其良好的Li+传输特性能使Li+穿过SEI膜并均匀沉积在电极表面[34],加之LiF自身高度的反应惰性,能有效隔绝电极/电解液的反应界面,降低Li的反应损耗[35],致使图 5(c)中SEM观察下Li沉积的形貌结构才会呈现块状的丛状聚集,且无明显的枝晶形成。这正是由于H2O的引入促进了LiF等SEI组分的生成,使得大量Li在其下沉积而无法参与界面反应,并最终形成局部的“惰性Li”。这种“惰性Li”的产生无疑降低了NRR所需的活性Li位点,进而使LM-NRR体系的NH3合成性能急剧下降。
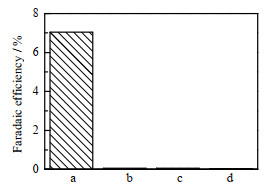
3.4 NH3来源检验尽管LM-NRR体系NRR真实性已被大量文献所证实[6-7, 15],为进一步排除外界NH3源对数据真实性的影响,研究分别在Li盐缺失、Ar取代N2气氛、不外加电源的控制条件下进行NRR测试,并与正常实验条件下的FE进行对比,见图 7。由图 7可知,正常条件下的FE明显高于其他对照实验数据,表明NH3来源于LM-NRR体系的合成过程,证明了NH3合成数据的真实性。
|
图 7 LM-NRR控制实验 Fig.7 Control experiments of LM-NRR a. normal conditions b. no LiBF4 c. Ar atmosphere d. no current applied |
(1) 选用双室电解池的LM-NRR体系,在常温常压下实现了NH3的电化学连续合成,随着反应时间的延长,LM-NRR体系的电化学性能不断提高,在反应时间为120 min、N2的流速为4 mL⋅min−1、电流密度为3 mA⋅cm−2的条件下的NH3合成速率为0.012 4 μg⋅s−1⋅cm−2,FE达7.05%。
(2) 探究了含水量对LM-NRR体系的电化学性能影响。结果表明,含水量对体系的合成NH3性能影响较大,即便是微量水的引入也会导致强烈的HER竞争,50 μL水量条件下的竞争性析氢反应剧烈,致使LM-NRR体系几乎丧失NRR活性。
(3) 利用SEM、XRD、XPS进一步表征了反应后Cu电极表面物质的结构及组成,探讨了水在反应界面中的作用机理。在水的作用下,受反应界面的HER竞争加剧、LiBF4水解增加以及活性Li位点降低的影响,Cu电极表面副反应产生了更多的LiF、LiOH等SEI组分,致使大量丛状聚集结构的“惰性Li”在其上沉积而无法参与界面反应,增大了界面电阻,降低LM-NRR体系的NH3合成性能。
| [1] |
WANG J, YU L, HU L, et al. Ambient ammonia synthesis via palladium-catalyzed electrohydrogenation of dinitrogen at low overpotential[J]. Nature Communications, 2018, 9(1): 1795. DOI:10.1038/s41467-018-04213-9 |
| [2] |
WANG Y, CUI X Q, ZHAO J X, et al. Rational design of Fe-N/C hybrid for enhanced nitrogen reduction electrocatalysis under ambient conditions in aqueous solution[J]. ACS Catalysis, 2019, 9(1): 336-344. DOI:10.1021/acscatal.8b03802 |
| [3] |
MONTOYA J H, TSAI C, VOJVODIC A, et al. The challenge of electrochemical ammonia synthesis: A new perspective on the role of nitrogen scaling relations[J]. ChemSusChem, 2015, 8(13): 2180-2186. DOI:10.1002/cssc.201500322 |
| [4] |
JIN H Y, LI L Q, LIU X, et al. Nitrogen vacancies on 2D layered W2N3: A stable and efficient active site for nitrogen reduction reaction[J]. Advanced Materials, 2019, 31(32): e1902709. DOI:10.1002/adma.201902709 |
| [5] |
LIN Y X, ZHANG S N, XUE Z H, et al. Boosting selective nitrogen reduction to ammonia on electron-deficient copper nanoparticles[J]. Nature Communications, 2019, 10(1): 4380. DOI:10.1038/s41467-019-12312-4 |
| [6] |
ANDERSEN S Z, ČOLIĆ V, YANG S, et al. A rigorous electrochemical ammonia synthesis protocol with quantitative isotope measurements[J]. Nature, 2019, 570(7762): 504-508. DOI:10.1038/s41586-019-1260-x |
| [7] |
LAZOUSKI N, SCHIFFER Z J, WILLIAMS K, et al. Understanding continuous lithium-mediated electrochemical nitrogen reduction[J]. Joule, 2019, 3(4): 1127-1139. DOI:10.1016/j.joule.2019.02.003 |
| [8] |
TSUNETO A, KUDO A, SAKATA T. Efficient electrochemical reduction of N2 to NH3 catalyzed by lithium[J]. Chemistry Letters, 1993, 22(5): 851-854. DOI:10.1246/cl.1993.851 |
| [9] |
TSUNETO A, KUDO A, SAKATA T. Lithium-mediated electrochemical reduction of high pressure N2 to NH3[J]. Journal of Electroanalytical Chemistry, 1994, 367(1/2): 183-188. |
| [10] |
ANDERSEN S Z, STATT M J, BUKAS V J, et al. Increasing stability, efficiency, and fundamental understanding of lithium-mediated electrochemical nitrogen reduction[J]. Energy & Environmental Science, 2020, 13(11): 4291-4300. |
| [11] |
SURYANTO B H R, MATUSZEK K, CHOI J, et al. Nitrogen reduction to ammonia at high efficiency and rates based on a phosphonium proton shuttle[J]. Science, 2021, 372(6547): 1187-1191. DOI:10.1126/science.abg2371 |
| [12] |
GOMEZ J R, GARZON F. Preliminary economics for green ammonia synthesis via lithium mediated pathway[J]. International Journal of Energy Research, 2021, 45(9): 13461-13470. DOI:10.1002/er.6674 |
| [13] |
CHEREPANOV P V, KREBSZ M, HODGETTS R Y, et al. Understanding the factors determining the Faradaic efficiency and rate of the lithium redox-mediated N2 reduction to ammonia[J]. The Journal of Physical Chemistry C, 2021, 125(21): 11402-11410. DOI:10.1021/acs.jpcc.1c02494 |
| [14] |
SAŽINAS R, ANDERSEN S Z, LI K, et al. Towards understanding of electrolyte degradation in lithium-mediated non-aqueous electrochemical ammonia synthesis with gas chromatography-mass spectrometry[J]. RSC Advances, 2021, 11(50): 31487-31498. DOI:10.1039/D1RA05963G |
| [15] |
CAI X Y, FU C H, IRIAWAN H, et al. Lithium-mediated electrochemical nitrogen reduction: Mechanistic insights to enhance performance[J]. iScience, 2021, 24(10): 103105. DOI:10.1016/j.isci.2021.103105 |
| [16] |
PAPPENFUS T M, LEE K M, THOMA L M, et al. Wind to ammonia: Electrochemical processes in room temperature ionic liquids[J]. ECS Transactions, 2009, 16(49): 89-93. DOI:10.1149/1.3159311 |
| [17] |
KIM K, YOO C Y, KIM J N, et al. Electrochemical synthesis of ammonia from water and nitrogen in ethylenediamine under ambient temperature and pressure[J]. Journal of the Electrochemical Society, 2016, 163(14): F1523-F1526. DOI:10.1149/2.0741614jes |
| [18] |
KRISHNAMURTHY D, LAZOUSKI N, GALA M L, et al. Closed-loop electrolyte design for lithium-mediated ammonia synthesis[J]. ACS Central Science, 2021, 7(12): 2073-2082. DOI:10.1021/acscentsci.1c01151 |
| [19] |
LAZOUSKI N, CHUNG M, WILLIAMS K, et al. Non-aqueous gas diffusion electrodes for rapid ammonia synthesis from nitrogen and water-splitting-derived hydrogen[J]. Nature Catalysis, 2020, 3(5): 463-469. DOI:10.1038/s41929-020-0455-8 |
| [20] |
GAO L F, CAO Y, WANG C, et al. Domino effect: Gold electrocatalyzing lithium reduction to accelerate nitrogen fixation[J]. Angewandte Chemie International Edition, 2021, 60(10): 5257-5261. DOI:10.1002/anie.202015496 |
| [21] |
KIM K, CHO H, JEON S H, et al. Lithium-mediated ammonia electro-synthesis: Effect of CsClO4 on lithium plating efficiency and ammonia synthesis[J]. Journal of the Electrochemical Society, 2018, 165(13): F1027-F1031. DOI:10.1149/2.1091811jes |
| [22] |
KIM K, CHEN Y F, HAN J I, et al. Lithium-mediated ammonia synthesis from water and nitrogen: A membrane-free approach enabled by an immiscible aqueous/organic hybrid electrolyte system[J]. Green Chemistry, 2019, 21(14): 3839-3845. DOI:10.1039/C9GC01338E |
| [23] |
SCHWALBE J A, STATT M J, CHOSY C, et al. A combined theory-experiment analysis of the surface species in lithium-mediated NH3 electrosynthesis[J]. ChemElectroChem, 2020, 7(7): 1542-1549. DOI:10.1002/celc.201902124 |
| [24] |
TAO H C, CHOI C, DING L X, et al. Nitrogen fixation by Ru single-atom electrocatalytic reduction[J]. Chem, 2019, 5(1): 204-214. DOI:10.1016/j.chempr.2018.10.007 |
| [25] |
KIM K, LEE S J, KIM D Y, et al. Electrochemical synthesis of ammonia from water and nitrogen: A lithium-mediated approach using lithium-ion conducting glass ceramics[J]. ChemSusChem, 2018, 11(1): 120-124. DOI:10.1002/cssc.201701975 |
| [26] |
ARAVINDAN V, GNANARAJ J, MADHAVI S, et al. Lithium-ion conducting electrolyte salts for lithium batteries[J]. Chemistry-A European Journal, 2011, 17(51): 14326-14346. DOI:10.1002/chem.201101486 |
| [27] |
ZHANG L J, SUN Y X, ZHOU Y, et al. Investigation of the synergetic effects of LiBF4 and LiODFB as wide-temperature electrolyte salts in lithium-ion batteries[J]. Ionics, 2018, 24(10): 2995-3004. DOI:10.1007/s11581-018-2470-1 |
| [28] |
RASKAR D, RINKE M T, ECKERT H. The mixed-network former effect in phosphate glasses: NMR and XPS studies of the connectivity distribution in the glass system (NaPO3)1-x(B2O3)x[J]. The Journal of Physical Chemistry C, 2008, 112(32): 12530-12539. DOI:10.1021/jp8035549 |
| [29] |
LIU X B, LIU J P. Effect of air humidity on microstructure and phase composition of lithium deuteride corrosion products[J]. Corrosion Science, 2017, 115: 129-134. DOI:10.1016/j.corsci.2016.11.017 |
| [30] |
CHAI R K, LIU Y T, LIU Q J, et al. Interaction mechanism of calcite and four representative organic molecules: Experiments and DFT study[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2021, 612: 125822. DOI:10.1016/j.colsurfa.2020.125822 |
| [31] |
DUNCAN H, DUGUAY D, ABU-LEBDEH Y, et al. Study of the LiMn1.5Ni0.5O4/electrolyte interface at room temperature and 60 ℃[J]. Journal of the Electrochemical Society, 2011, 158(5): A537-A545. DOI:10.1149/1.3567954 |
| [32] |
HU L, XING Z, FENG X F. Understanding the electrocatalytic interface for ambient ammonia synthesis[J]. ACS Energy Letters, 2020, 5(2): 430-436. DOI:10.1021/acsenergylett.9b02679 |
| [33] |
LI F, LIU J D, HE J, et al. Additive-assisted hydrophobic Li+-solvated structure for stabilizing dual electrode electrolyte interphases through suppressing LiPF6 hydrolysis[J]. Angewandte Chemie International Edition, 2022, 61(27): e202205091. DOI:10.1002/anie.202205091 |
| [34] |
YUAN Y X, WU F, BAI Y, et al. Corrigendum for "Regulating Li deposition by constructing LiF-rich host for dendrite-free lithium metal anode" [Energy Storage Mater. 16 (2019) 411-418][J]. Energy Storage Materials, 2020, 29: 386. DOI:10.1016/j.ensm.2020.03.028 |
| [35] |
XU K. Nonaqueous liquid electrolytes for lithium-based rechargeable batteries[J]. Chemical Reviews, 2004, 104(10): 4303-4418. DOI:10.1021/cr030203g |




