随着日益增长的能源消耗和日渐加剧的环境问题,近年来大力提倡可持续发展[1]。植物油具有类似于石化原料的长烃链结构,含有许多可修饰官能位点,是有望部分替代石化原料的重要可再生能源[2-3]。从植物油衍生的不饱和脂肪酸甲酯可被氧化裂解为醛类和羧酸类产物,可用于制备生物基产品,例如润滑油、增塑剂、胶黏剂、表面活性剂、高分子聚合物等[4-9]。目前有多种途径可实现不饱和脂肪酸甲酯的氧化裂解,其中,以过渡金属钨为催化剂,采用双氧水氧化裂解的方法是研究的热点,常用的钨催化剂有氧化钨、钨酸、磷钨酸盐、钨金属杂多酸及其盐等[10-18]。KERENKAN等[10]制备无机-有机多钨酸盐[(CH3CH2CH2)4N]3.31[H4.69W12O40]·1.08H2O,用于氧化裂解油酸制壬酸和壬二酸,在120 ℃反应5 h,油酸基本完全转化,壬酸和壬二酸收率为78%~79%。GARZA等[15]报道了以两亲性二吡啶鎓-磷钨酸盐为催化剂,在90 ℃氧化裂解油酸甲酯24 h,得到壬酸和壬二酸收率为89%。LI等[17]采用WO3为催化剂,Na2SnO3为助催化剂,在130 ℃下氧化裂解油酸3.5 h,油酸转化率达到100%,主要产物为壬酸和壬二酸,其收率分别为51%和42%。然而,这些方法大都需要添加有机溶剂,且反应产物多以羧酸为主。这主要是因为碳碳双键稳定性好,对其氧化裂解需要较苛刻的反应条件。通常,用钨和双氧水催化氧化裂解不饱和脂肪酸甲酯会经历如下3个过程:环氧化→水解→氧化裂解[19-21]。因此,从环氧脂肪酸甲酯出发制备生物基醛类产物或羧酸类产物在理论上是可行的。另外,由于环氧键的稳定性较碳碳双键差,使得该反应可能在较温和的条件下进行。据文献报道,上述的第2步水解过程是一个酸催化反应[22]。SPANNRING等[23]在油酸甲酯的氧化裂解过程中,加入H2SO4促进反应的进行。HOANG等[24]采用介孔ZSM-5固体酸载体负载钨和铬,用于氧化裂解不饱和脂肪酸。比起液体酸,固体酸结合了液体酸和非均相催化剂的优点,并避免了使用液体酸引起的设备腐蚀、环境污染、产物分离复杂等问题[25-26]。
综上所述,本研究以环氧脂肪酸甲酯为原料,将氧化钨负载于固体酸载体上,用作双功能催化剂,生产生物基脂肪醛。鉴于反应底物为长烷烃链油脂类分子,采用孔径2~10 nm、具有高比表面积、酸度可调的介孔分子筛Al-MCM-41为固体酸载体[27-28]。催化剂采用X射线衍射(X-ray diffraction,XRD)、N2吸附/脱附实验、透射电镜(transmission electron microscope,TEM)和吡啶吸附红外光谱实验(Pyridine-adsorption fourier transform infrared,Py-FTIR)进行表征分析,测试了催化剂在环氧油酸甲酯氧化裂解反应中的催化活性,并考察了反应温度、催化剂用量、双氧水用量和反应时间对氧化裂解反应的影响。
2 实验(材料与方法) 2.1 材料与仪器实验所用环氧油酸甲酯为实验室自制[29],主要组成为约88%的环氧油酸甲酯和约12%的硬脂酸甲酯。其余试剂均为分析纯,购自阿拉丁试剂公司。
X’Pert Pro型XRD射线衍射仪;Micromeritics ASAP-2020-PLUS-HD88型比表面积及孔径分析仪;Tecnai G2 F30 S-Twin高分辨透射电子显微镜;Thermo fisher Nicolet iS50型红外光谱仪(Py-FTIR);Shimadzu GC-2014气相色谱仪;Agilent 7890A/5975C气质联用仪GC-MS;反应装置如图 1。
|
图 1 反应装置 Fig.1 Schematic diagram of the reaction setup |
介孔分子筛MCM-41和Al-MCM-41的制备参考Lu等人的报告[28]。在35 ℃下将9.111 3 g十六烷基三甲基溴化铵(cetyltrimethylammonium bromide,CTAB)、1.823 0 g四甲基氢氧化铵(tetramethylammonium hydroxide,TMAOH)和72.000 0 g去离子水混合,搅拌至澄清透明,再往其中缓慢滴加0.408 5 g异丙醇铝和20.833 0 g正硅酸乙酯(ethyl orthosilicate,TEOS),滴加完毕后继续在35 ℃下搅拌反应2 h,然后在室温下静置72 h,过滤分离出固体,固体经去离子水洗涤、干燥后,置于马弗炉中550 ℃热处理8 h,即得到硅铝摩尔比50的含铝MCM-41,样品命名为Al-MCM-41。纯硅MCM-41制备方法与之类似,唯一区别为不添加异丙醇铝,样品命名为MCM-41。
采用等体积浸渍法制备WO3负载的MCM-41和Al-MCM-41催化剂。室温下将0.038 5 g偏钨酸铵溶解于适量去离子水中,缓慢滴加到1 g MCM-41或Al-MCM-41上,于室温下静置24 h后,70 ℃下干燥,然后置于马弗炉中550 ℃热处理8 h,即得到WO3负载量3.5%(质量分数)的MCM-41和Al-MCM-41催化剂,样品分别命名为WO3/MCM-41和WO3/Al-MCM-41。
2.3 催化剂的表征采用X’Pert Pro型XRD射线衍射仪对催化剂进行XRD表征,测定参数为Cu靶、Kα辐射源(λ=0.154 056 nm)、管电压40 kV、管电流40 mA、扫描范围2θ=0.5° ~80°。低温N2吸附-脱附实验采用Micromeritics ASAP-2020-PLUS-HD88型比表面积及孔径分析仪,由BET(Brunauer-Emmet-Teller)方程计算比表面积,由BJH(Barrett-Joyner-Halenda)法计算平均孔径分布。TEM图片在Tecnai G2 F30 S-Twin高分辨透射电子显微镜上测得。采用Thermo fisher Nicolet iS50型红外光谱仪测定样品的B酸和L酸含量,样品在300 ℃真空处理2 h,降温至50 ℃记录谱图作为背景,保持在50 ℃通入吡啶使样品吸附至饱和,再真空处理1 h,除去样品表面物理吸附的吡啶,然后缓慢升温,分别在50 ℃和200 ℃记录谱图。
2.4 催化剂的活性评价采用环氧油酸甲酯的氧化裂解反应对催化剂的活性进行评价(化学方程式如下)。典型反应为:将10 mmol环氧油酸甲酯和156.3 mg(含0.023 6 mmol WO3)WO3/MCM-41或WO3/Al-MCM-41在80 ℃下搅拌混合均匀,再缓慢滴入20 mmol H2O2(质量分数30%),保持在80 ℃下搅拌反应2 h,再离心得到油状液体产物。
采用Agilent 7890A/5975C气质联用仪(GC-MS)对产物进行定性分析,采用Shimadzu GC-2014气相色谱仪对产物进行定量分析。色谱升温程序为:50 ℃保持3 min→10 ℃·min-1升至150 ℃,保持1 min→10 ℃·min-1升至220 ℃,保持3 min→10 ℃·min-1升至280 ℃,保持10 min。采用内标法对产物进行定量分析,以十一醛为内标物,计算公式如下:
| $ 原料转化率\left( {\rm{\% }} \right){\rm{ = }}\left( {原料转化量/原料加入量} \right) \times 100\% ; $ |
| $ 产物收率\left( {\rm{\% }} \right){\rm{ = }}\left( {实际生成的产物量/按原料加入量理论得到的产物量} \right) \times 100\% 。$ |
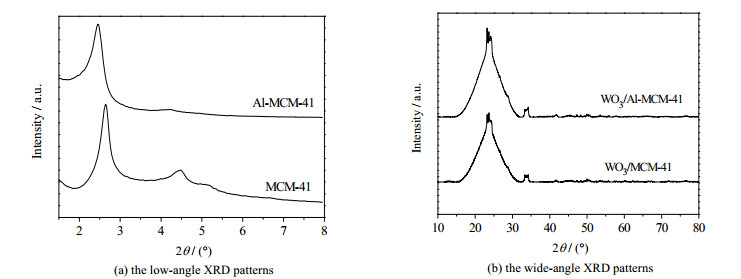
MCM-41和Al-MCM-41的小角XRD衍射图如图 2(a)。由图可见,实验合成的MCM-41和Al-MCM-41均大约在2θ = 2.5°、4.3°和5.1°表现出明显的特征衍射峰,分别对应于(100)、(110)和(200)晶面,表明合成的MCM-41和Al-MCM-41均具有典型MCM-41介孔分子筛特有的六方介孔结构。比起MCM-41,Al-MCM-41在(110)和(200)晶面衍射峰强度明显减弱,这表明Al-MCM-41孔道具有较差的长程有序性[30]。另外,Al-MCM-41的(100)晶面衍射角小于MCM-41的(100)晶面衍射角,表明Al-MCM-41具有较大的d100晶面间距,即具有较大的孔径。图 2(b)为WO3/MCM-41和WO3/Al-MCM-41的广角XRD衍射图。由图可见,WO3/MCM-41和WO3/Al-MCM-41均在2θ = 23.07°、23.54°、24.35°、33.18°和34.19°表现出微弱的WO3特征衍射峰,与XRD标准PDF卡片对比可知,负载的WO3为单斜晶相(JCPDS no. 43-1035)。
|
图 2 催化剂的XRD图 Fig.2 XRD patterns of the catalysts |
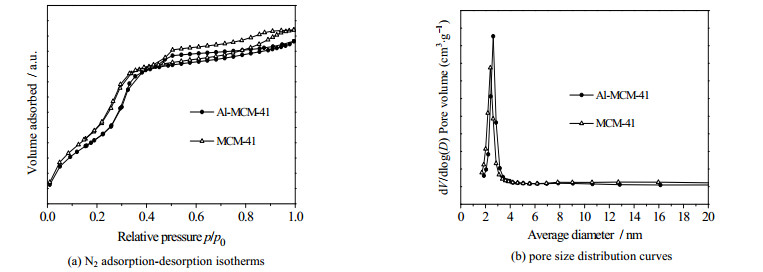
图 3为MCM-41和Al-MCM-41的N2吸附-脱附等温线和孔径分布曲线。由图可见,MCM-41和Al-MCM-41均为Ⅳ型吸附等温线,具有H1型滞后环,为典型的介孔结构特征。另外,MCM-41和Al-MCM-41均具有狭窄、均一的孔径分布。表 1列出了MCM-41和Al-MCM-41的孔结构参数。MCM-41的BET表面积、孔容和平均孔径分别为1 517.77 m2·g-1、1.04 cm3·g-1和2.68 nm,而Al-MCM-41具有较小的BET表面积、孔容和较大的平均孔径,分别为1 279.44 m2·g-1、0.97 cm3·g-1和2.88 nm,这主要是因为Al-MCM-41中含有Al-O键,其键长(0.175 nm)大于Si-O键(0.160 nm)[31]。
|
图 3 MCM-41和Al-MCM-41的N2吸附-脱附实验结果 Fig.3 N2 adsorption-desorption results of MCM-41 and Al-MCM-41 |
|
|
表 1 MCM-41和Al-MCM-41的孔结构性质和酸性 Table 1 Structural properties and acidities of MCM-41 and Al-MCM-41 |
图 4为催化剂的TEM图片。由图 4(a)和(b)可以看出,MCM-41和Al-MCM-41的孔道结构呈蠕虫状,孔道较短,这有利于反应物和产物的扩散。其中,MCM-41的孔道长程有序性明显优于Al-MCM-41,这与小角XRD表征结果一致。从图 4(c)和(d)可以观察到,WO3在MCM-41和Al-MCM-41上分布均匀,粒径2 nm左右。结合广角XRD衍射图可知,WO3被成功负载于MCM-41和Al-MCM-41上。

|
图 4 催化剂的透射电镜图片 Fig.4 TEM micrographs of the catalysts |
MCM-41和Al-MCM-41的酸性采用吡啶-红外测定,结果列于表 1中。从表中可以看出,MCM-41不含有B酸位点,只含有L酸位点,而Al-MCM-41同时含有B酸和L酸位点。比较在不同温度下脱附吡啶后的酸性可知,MCM-41和Al-MCM-41的酸性强度适中。
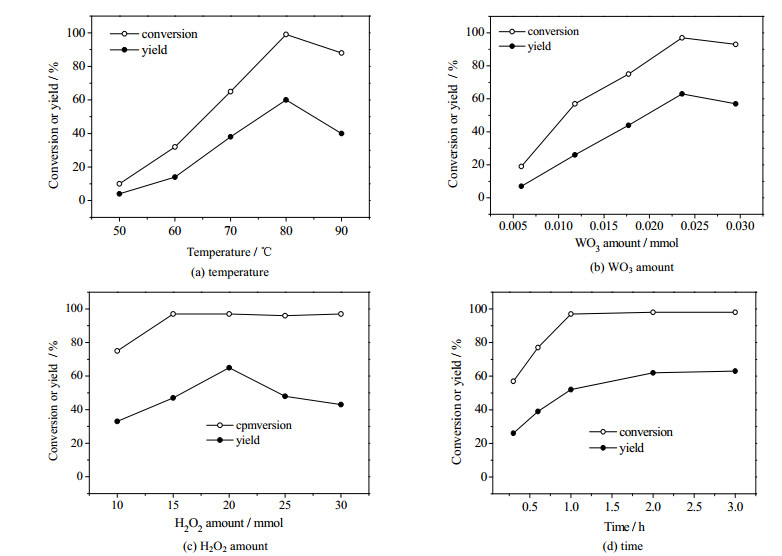
3.2 催化剂的活性评价采用单因素实验考察了反应温度、催化剂用量、双氧水用量以及反应时间等因素对环氧油酸甲酯氧化裂解反应的影响,结果见图 5。
|
图 5 各因素对环氧油酸甲酯氧化裂解反应的影响 Fig.5 Effects of various factors on the oxidative cleavage reaction of epoxy methyl oleate |
图 5(a)为反应温度对环氧油酸甲酯氧化裂解反应的影响,以WO3/Al-MCM-41为催化剂,反应温度为50~90 ℃,反应时间为2 h,底物摩尔量为:10 mmol环氧油酸甲酯、0.023 6 mmol WO3、20 mmol H2O2。由图可知,随着反应温度的升高,环氧油酸甲酯转化率和产物收率先增加。当反应温度高于80 ℃时,转化率和收率减少,这主要是因为高温增加了双氧水的分解。因此,最佳的反应温度为80 ℃,此时转化率和收率分别达到99%和60%。
图 5(b)考察了催化剂用量对环氧油酸甲酯转化率和产物收率的影响,以WO3/Al-MCM-41为催化剂,反应温度为80 ℃,反应时间为2 h,底物摩尔量为:10 mmol环氧油酸甲酯、0.005 9~0.029 5 mmol WO3、20 mmol H2O2。从图中可以看出,环氧油酸甲酯转化率和产物收率均随着催化剂用量的增加呈现出先增加后减少的趋势,在催化剂用量为0.023 6 mmol(即环氧油酸甲酯与WO3摩尔比为1/0.002 4)时取得最佳的转化率和收率,分别为97%和63%。
图 5(c)为双氧水用量对环氧油酸甲酯氧化裂解反应的影响,以WO3/Al-MCM-41为催化剂,反应温度为80 ℃,反应时间为2 h,底物摩尔量为:10 mmol环氧油酸甲酯、0.023 6 mmol WO3、10~30 mmol H2O2。由图可见,随着双氧水用量的增加,环氧油酸甲酯转化率先增加后基本保持不变,而产物收率先增加后减少,这主要是因为产物被增加的双氧水进一步氧化。最佳的双氧水用量为20 mmol(即为环氧油酸甲酯摩尔量的2倍),此时转化率和收率分别为97%和65%。
图 5(d)考察了反应时间对环氧油酸甲酯氧化裂解反应的影响,以WO3/Al-MCM-41为催化剂,反应温度为80 ℃,反应时间为0.3~2 h,底物摩尔量为:10 mmol环氧油酸甲酯、0.023 6 mmol WO3、20 mmol H2O2。从图中可以观察到,随着反应时间的延长,环氧油酸甲酯转化率和产物收率先增加,在反应时间超过2 h后基本保持不变,表明反应已经结束,因此最佳的反应时间为2 h。
基于上述单因素实验结果,通过正交试验L9(34)法,按4因素3水平实验(表 2),以产物的收率作为评价指标,从而选择最佳的反应工艺条件,结果见表 3。表中R值和P值分别为正交试验的极差分析结果和方差分析结果。从R值可以看出,反应温度对应的极差最大,即反应温度是影响产物收率的最主要因素。另外,反应温度对应的K2 > K3 > K1,说明选择第二水平较好,即80 ℃为最佳的反应温度。同理,可得出最佳的WO3用量、H2O2用量和反应时间分别为0.024 mmol(即为环氧油酸甲酯摩尔量的0.002 4倍)、20 mmol(即为环氧油酸甲酯摩尔量的2倍)和1.5 h。根据P值可得出,实验考察的4个反应因素对产物收率的影响主次顺序为:反应温度 > H2O2用量 > WO3用量 > 反应时间,这与极差分析结果基本符合。
|
|
表 2 正交试验的因子和水平 Table 2 Factors and levels of the orthogonal experiments |
|
|
表 3 正交试验设计及结果 Table 3 Design and results of the orthogonal experiments |
进一步比较了不同催化剂对环氧油酸甲酯氧化裂解反应的影响,结果列于表 4中。当使用MCM-41和Al-MCM-41为催化剂时,环氧油酸甲酯的氧化裂解反应不进行。比较催化剂WO3、WO3/MCM-41和WO3/Al-MCM-41,WO3/Al-MCM-41具有较好的催化活性,这主要归功于Al-MCM-41更多的B酸和L酸位点,而WO3/MCM-41的催化活性比WO3略有提升,这说明L酸性对环氧油酸甲酯的氧化裂解反应没有明显的促进效果(见表 1)。
|
|
表 4 不同催化剂氧化裂解环氧油酸甲酯 Table 4 Oxidative cleavage of epoxy methyl oleate with different catalysts |
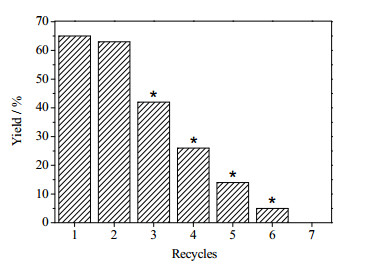
图 6考察了催化剂的可重复使用性能。由图可知,催化剂的可重复使用性能并不理想,仅可重复使用2次。在第3次重复使用时,催化剂的活性明显下降,于重复使用6次后,催化剂完全失活。进一步采用ICP-MS检测产物中的钨含量,得出催化剂失活主要是由活性组分浸出造成。
|
图 6 催化剂的可重复使用性能 Fig.6 Reusability results of the catalyst. (Reaction condition: 80℃, 1.5 h, 10 mmol epoxy methyl oleate, 0.024 mmol WO3 (WO3/Al-MCM-41), 20 mmol H2O2 (w=30%); * the liquid product contained tungsten) |
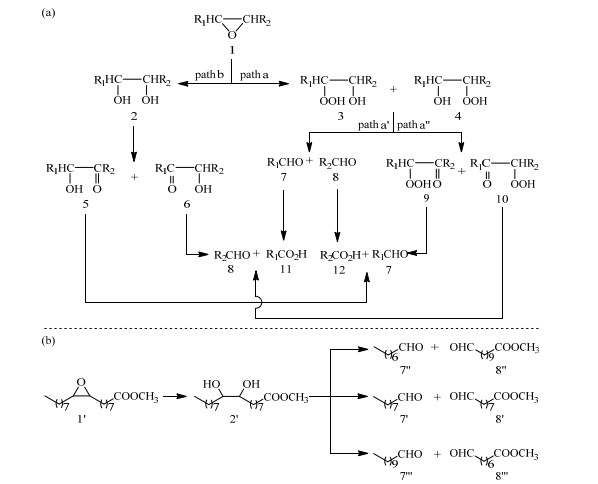
据文献报道,环氧脂肪酸甲酯氧化裂解会经历如下两条路径(见图 7(a))[32]。路径a(path a):环氧化物1经途径a(path a,过羟基化),转变为过羟基化合物3和4,再裂解为醛类产物7和8(path a'),之后氧化为羧酸类产物11和12,或者是过羟基化合物3和4进一步氧化为羰基化合物9和10(path a''),再裂解为醛类产物7和8以及羧酸类产物11和12。路径b(path b):环氧化物1经途径b(path b,羟基化),转变为羟基化合物2,再进一步氧化为邻位羟基酮类化合物5和6,最后氧化裂解为醛类产物7和8以及羧酸类产物11和12。然而,在本文所述的环氧油酸甲酯氧化裂解反应产物中,只检测到羟基化产物2以及醛类产物7和8,因此,得出如图 7(b)所示的反应机理过程,即环氧油酸甲酯1'先被羟基化为9, 10-二羟基硬脂酸甲酯2',之后再氧化裂解为醛类产物7'和8',另外还得到醛类副产物7''和8''以及7'''和8'''。
|
图 7 环氧脂肪酸甲酯氧化裂解反应的路径 Fig.7 Reaction paths of oxidative cleavage of epoxy fatty acid methyl ester (a) literature[32] (b) this work |
(1) 通过XRD、BET、TEM以及Py-FTIR对催化剂进行表征分析,结果表明MCM-41和Al-MCM-41具有良好的介孔结构,是典型的MCM-41型分子筛。其中MCM-41的孔道长程有序性优于Al-MCM-41,MCM-41具有更小的孔径和更大的比表面积。WO3在MCM-41和Al-MCM-41上分布均匀,粒径2 nm左右。另外,MCM-41只具有L酸性,而Al-MCM-41同时具有B酸性和L酸性。
(2) 采用环氧油酸甲酯氧化裂解反应测试催化剂的催化活性,不使用任何有机溶剂,考察了反应温度、催化剂用量、双氧水用量和反应时间对反应的影响,结果表明WO3/Al-MCM-41具有优异的催化活性,最佳反应温度、环氧油酸甲酯/WO3/双氧水的摩尔比和反应时间分别为80 ℃、1/0.0024/2和1.5 h,在此条件下,环氧油酸甲酯转化率和醛类产物收率分别高于95%和60%。
(3) 比较WO3、WO3/MCM-41和WO3/Al-MCM-41的催化活性,WO3/Al-MCM-41具有较好的催化活性,而WO3/MCM-41与WO3的催化活性相当,这说明B酸性对环氧油酸甲酯的氧化裂解有较好的促进作用,而L酸性没有明显的促进效果。
| [1] |
王海周, 王东军, 李山山, 等. 植物油加氢脱氧路径调控催化剂的制备[J]. 高校化学工程学报, 2018, 32(4): 840-847. WANG H Z, WANG D J, LI S S, et al. Preparation of catalysts for reaction pathway-control in vegetable oil hydrodeoxygenation[J]. Journal of Chemical Engineering of Chinese Universities, 2018, 32(4): 840-847. DOI:10.3969/j.issn.1003-9015.2018.04.013 |
| [2] |
FRAILE J M, GARCIA J I, HERRERIAS C I, et al. Synthetic transformations for the valorization of fatty acidderivatives[J]. Synthesis, 2017, 49(7): 1444-1460. DOI:10.1055/s-0036-1588699 |
| [3] |
刘迎新, 曾茂, 楼炯涛, 等. 5-羟甲基糠醛选择性加氢制备2, 5-二甲基呋喃研究进展[J]. 高校化学工程学报, 2018, 32(2): 255-265. LIU Y X, ZENG M, LOU J T, et al. Review on 2, 5-dimethylfuran synthesis via selective hydrogenation of 5-hydroxymethylfufural[J]. Journal of Chemical Engineering of Chinese Universities, 2018, 32(2): 255-265. DOI:10.3969/j.issn.1003-9015.2018.02.002 |
| [4] |
SPANNRING P, YAZERSKI V, BRUIJNINCX P C A, et al. Fe-catalyzed one-pot oxidative cleavage of unsaturated fatty acids into aldehydes with hydrogen peroxide and sodium periodate[J]. Chemistry-A European Journal, 2013, 19(44): 15012-15018. DOI:10.1002/chem.201301371 |
| [5] |
OMONOV T S, KHARRAZ E, FOLEY P, et al. The production of biobased nonanal by ozonolysis of fatty acids[J]. RSC Advances, 2014, 4(96): 53617-53627. DOI:10.1039/C4RA07917E |
| [6] |
DERUER E, DUGUET N, LEMAIRE M. Thiazolylidene-catalyzed cleavage of methyl oleate-derived α-hydroxy ketone to the corresponding free aldehydes[J]. ChemSusChem, 2015, 8(15): 2481-2486. DOI:10.1002/cssc.201500462 |
| [7] |
LOUIS K, VIVIER L, CLACENS J M, et al. Sustainable route to methyl-9-hydroxononanoate (polymer precursor) by oxidative cleavage of fatty acid methyl ester from rapeseed oil[J]. Green Chemistry, 2014, 16(1): 96-101. DOI:10.1039/C3GC41491D |
| [8] |
SPANNRING P, BRUIJNINCX P C A, WECKHUYSEN B M, et al. Transition metal-catalyzed oxidative double bond cleavage of simple and bio-derived alkenes and unsaturated fatty acids[J]. Catalysis Science & Technology, 2014, 4(8): 2182-2209. |
| [9] |
KOCKRITZ A, MARTIN A. Oxidation of unsaturated fatty acid derivatives and vegetable oils[J]. European Journal of Lipid Science and Technology, 2008, 110(9): 812-824. DOI:10.1002/ejlt.200800042 |
| [10] |
KERENKAN A E, GANDON A, DO T O. Novel tetra-propyl/butylammonium encapsulated Keggin-type polyoxotungstates: synthesis, structural characterization, and catalytic capability in oxidative cleavage of unsaturated fatty acids[J]. Dalton Transactions, 2018, 47(4): 1214-1222. DOI:10.1039/C7DT04469K |
| [11] |
KERENKAN A E, BELAND F, DO T O. Chemically catalyzed oxidative cleavage of unsaturated fatty acids and their derivatives into valuable products for industrial applications: A review and perspective[J]. Catalysis Science & Technology, 2016, 6(4): 971-987. |
| [12] |
LU M, PENG L, XIE Q, et al. Solvent-free oxidative cleavage of epoxy fatty acid methyl esters by a "release and capture" catalytic system[J]. Green Chemistry, 2019, 21(3): 560-566. DOI:10.1039/C8GC03201G |
| [13] |
HAIMOV A, COHEN H, NEUMANN R. Alkylated polyethyleneimine/polyoxometalate synzymes as catalysts for the oxidation of hydrophobic substrates in water with hydrogen peroxide[J]. Journal of the American Chemical Society, 2004, 126(38): 11762-11763. DOI:10.1021/ja046349u |
| [14] |
GODARD A, CARO P D, ROUX S T, et al. New environmentally friendly oxidative scission of oleic acid into azelaic acid and pelargonic acid[J]. Journal of the American Oil Chemists Society, 2013, 90(1): 133-140. DOI:10.1007/s11746-012-2134-7 |
| [15] |
GARZA L C, VIGIER K D O, CHATEL G, et al. Amphiphilic dipyridinium-phosphotungstate as an efficient and recyclable catalyst for triphasic fatty ester epoxidation and oxidative cleavage with hydrogen peroxide[J]. Green Chemistry, 2017, 19(12): 2855-2862. DOI:10.1039/C7GC00298J |
| [16] |
KERENKAN A E, ELLO A S, DO T O. Synthesis, organo-functionalization, and catalytic properties of tungsten oxide nanoparticles as heterogeneous catalyst for oxidative cleavage of oleic acid as a model fatty acid into diacids[J]. Industrial & Engineering Chemistry Research, 2017, 56(38): 10639-10647. |
| [17] |
LI X, SYONG J C P, ZHANG Y. Sodium stannate promoted double bond cleavage of oleic acid by hydrogen peroxide over a heterogeneous WO3 catalyst[J]. Green Chemistry, 2018, 20(15): 3619-3624. DOI:10.1039/C8GC00949J |
| [18] |
OAKLEY M A, WOODWARD S, COUPLAND K, et al. Practical dihydroxylation and C-C cleavage of unsaturated fatty acids[J]. Journal of Molecular Catalysis A: Chemical, 1999, 150(1/2): 105-111. |
| [19] |
WANG M, MA J, LIU H, et al. Sustainable productions of organic acids and their derivatives from biomass via selective oxidative cleavage of C-C bond[J]. ACS Catalysis, 2018, 8(3): 2129-2165. DOI:10.1021/acscatal.7b03790 |
| [20] |
ANTONELLI E, D'ALOISIO R, GAMBARO M, et al. Efficient oxidative cleavage of olefins to carboxylic acids with hydrogen peroxide catalyzed by methyltrioctylammoniumtetrakis(oxodiperoxotungsto)phosphate(3-) under two-phase conditions. Synthetic aspects and investigation of the reaction course[J]. The Journal of Organic Chemistry, 1998, 63(21): 7190-7206. DOI:10.1021/jo980481t |
| [21] |
LU M, PENG L, XIE Q, et al. Oxidative cleavage of methyl 9, 10-epoxystearate over WO3/MCM-41 for methyl 9-oxononanoate production[J]. European Journal of Lipid Science and Technology, 2018, 120(7): 1700415. DOI:10.1002/ejlt.201700415 |
| [22] |
PILETIC I R, EDNEY E O, BARTOLOTTI L J. A computational study of acid catalyzed aerosol reactions of atmospherically relevant epoxides[J]. Physical Chemistry Chemical Physics, 2013, 15(41): 18065-18076. DOI:10.1039/c3cp52851k |
| [23] |
SPANNRING P, PRAT I, COSTAS M, et al. Fe(6-Me-PyTACN)-catalyzed, one-pot oxidative cleavage of methyl oleate and oleic acid into carboxylic acids with H2O2 and NaIO4[J]. Catalysis Science & Technology, 2014, 4(3): 708-716. |
| [24] |
HOANG P H, DON B V, CHUNG N H. Cleavage of double bond using metal-loaded ZSM-5 zeolite catalysts for renewable biochemical application[J]. The Canadian Journal of Chemical Engineering, 2018, 97(5): 1-7. |
| [25] |
GUPTA P, PAUL S. Solid acids: Green alternatives for acid catalysis[J]. Catalysis Today, 2014, 236(1): 153-170. |
| [26] |
SANI Y M, DAUD W M A W, AZIZ A R A. Activity of solid acid catalysts for biodiesel production: A critical review[J]. Applied Catalysis A: General, 2014, 470(30): 140-161. |
| [27] |
CHEN F, HUANG L, YANG X, et al. Synthesis of Al-substituted MCM-41 and MCM-48 solid acids with mixed cationic-anionic surfactants as templates[J]. Materials Letters, 2013, 109(15): 299-301. |
| [28] |
LU M, LIU X, LI Y, et al. Hydrocracking of bio-alkanes over Pt/Al-MCM-41 mesoporous molecular sieves for bio-jet fuel production[J]. Journal of Renewable and Sustainable Energy, 2016, 8(5): 053103. DOI:10.1063/1.4962561 |
| [29] |
WU Z, NIE Y, CHEN W, et al. Mass transfer and reaction kinetics of soybean oil epoxidation in a formic acid-autocatalyzed reaction system[J]. The Canadian Journal of Chemical Engineering, 2016, 94(8): 1576-1582. DOI:10.1002/cjce.22526 |
| [30] |
CHEN X, HUANG L, DING G, et al. Characterization and catalytic performance of mesoporous molecular sieves Al-MCM-41 materials[J]. Catalysis Letters, 1997, 44(1/2): 123-128. DOI:10.1023/A:1018968823654 |
| [31] |
BORADE R B, CLEARFIELD A. Synthesis of aluminum rich MCM-41[J]. Catalysis Letters, 1995, 31(2/3): 267-272. |
| [32] |
ANTONELLI E, D'ALOISIO R, GAMBARO M, et al. Efficient oxidative cleavage of olefins to carboxylic acids with hydrogen peroxide catalyzed by methyltrioctylammonium tetrakis(oxodiperoxotungsto)phosphate(3-) under two-phase conditions. synthetic aspects and investigation of the reaction course[J]. The Journal of Organic Chemistry, 1998, 63(21): 7190-7206. DOI:10.1021/jo980481t |




