2. 中国地质大学(北京)工程技术学院, 北京 100083;
3. 宁波材料科学与工程研究所, 浙江 宁波 315201
2. School of Engineering and Technology, China University of Geoscience, Beijing 100083, China;
3. Ningbo Institute of Material Technology and Engineering(NIMTE), Ningbo 315201, China
制氢储能具有可持续、环保、长寿命和低成本的特性,被认为是极具潜力的未来新型大规模储能技术。在化石能源枯竭和环境恶化的背景下,通过可再生能源电力的电解制氢储能技术受到了欧美日发达国家的广泛关注[1~3]。作为一种重要的是制氢方式—电解水制氢,目前已经发展了三种基于不同电解质种类的电解装置,分别是碱性电解池(Alkaline Electrolysis Cell,AEC)、固体聚合物电解池(Solid Polymer Electrolyzer,SPE)以及固体氧化物电解池(Solid Oxide Electrolysis Cell,SOEC)。与低温电解装置(AEC、SPE)相比,高温的SOEC系统制氢效率是碱性电解池的2倍多,是质子交换膜电解池的1.5倍左右[4]。因此,固体氧化物电解池高温电解水蒸汽是目前最有前景的高效电解制氢方法。
国际上已有美国、日本、丹麦、德国、加拿大等国家开展了SOEC 高温电解制氢技术的研究工作,SOEC 作为能源领域的一项新技术,发展中国家则刚刚起步。SOEC 是固体氧化物燃料电池(SOFC)的逆过程,主要以钇稳定的氧化锆(YSZ)为电解质、Ni-YSZ为氢电极、(La, Sr)MnO3 (LSM)-YSZ为氧电极。电解过程中,YSZ/LSM-YSZ界面的空隙会由于过量氧气的产生,而导致氧电极的剥离和极化电阻的增加,而且YSZ/LSM界面La2Zr2O7新相的形成,也会加速氧电极剥离[5~7]。Pattaraporn[8]对比以LSM-YSZ、(La, Sr)(Co, Fe)O3 (LSCF)为氧电极的电解池,在550~800℃电解水蒸气的性能,结果表明LSCF具有更高的电化学活性。相对于LSM,氧电极材料LSCF具有离子和电子混合电导特性,更低的极化阻抗[9]。但是由于LSCF与YSZ在SOEC的工作温度下发生反应[10],因此需在它们之间加一阻隔层(Gd, Ce)O2(GDC),以提高工作稳定性。
目前,SOEC高温电解水蒸汽主要集中在单电池的性能研究,而固体氧化物电解池堆的电解性能不仅与单电池片的性能有关,而且与电解池堆的连接件、密封材料以及其他因素都有关。 仅有的一些有关电解池堆性能研究也是基于以LSM-YSZ为氧电极材料[11~14],而以LSCF-GDC为氧极材料的电解池堆电解性能研究鲜有报道。
本实验通过对不同实验条件下Ni-YSZ|YSZ|GDC/ LSCF-GDC电解池堆高温电解的电流—电压曲线进行分析,研究不同工况对各极化的影响,并计算比较各条件下的系统制氢效率,以确定最佳制氢条件。
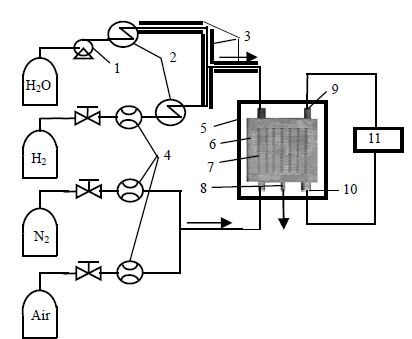
2 实验 2.1 高温蒸汽电解制氢实验采用商业的30单元平板式氢电极支撑的Ni-YSZ|YSZ|GDC/LSCF-GDC(其中GDC:Ce0.9Gd0.1O1.95; LSCF:La0.6Sr0.4Co0.2Fe0.8O3-δ)电池堆。其制备过程为:通过流延法制得厚为400 μm 的Ni/3YSZ氢电极基层,随后在基层上喷涂上10 μm厚的Ni/8YSZ和10 μm厚的8YSZ电解质层,共烧制得半电池后,在基层上依次丝网印刷上3 μm的GDC阻隔层和30 μm厚的LSCF- GDC氧电极。单电池片和电池堆的具体制备过程可参考文献[15]。电池堆的总面积为10 cm×10 cm,有效活性面积为62 cm2。高温电解水(HTE)的流程如图 1所示。测试时,水通过平流泵注入加热装置中,经气化后与预热好的氢气混合,通入SOEC氢电极。水的流速通过平流泵精确控制,因此能准确地控制混合气中水蒸气与氢气的比例。氧电极则通入空气、氮气或不通入任何气体。系统组装好后,电池以2℃⋅min-1升温至750℃,保温2 h后,氢电极通入2 L·min-1 纯N2,将管道中的空气完全排出。在电解池堆正常工作之前,分别向氢电极和氧电极通入氢气和空气至少2 h,使氢电极中的NiO充分还原。
|
图 1 高温电解水示意图 Fig.1 Schematic diagram of the HTE system 1.pump 2. pre-heater 3. line-heater 4. mass flowmeter 5. furnace 6. stack 7. air outlet 8. fuel outlet 9. cathode 10. anode 11. DC power source |
实验在不同的工作温度、混合气体流量、水蒸气含量下,测试电池堆电解水蒸汽的电流—电压曲线。同时测试了氧电极通入纯N2和空气条件下,电解水的电流—电压曲线。后文的电解电压为一个单元的电解电压。
2.2 制氢的系统效率计算由于SOEC电解制氢在高温下运行,因此除了电能外,还需要高温热能加热反应气体,所以SOEC电解水制氢系统的效率(ηsys)可以定义为:生成氢气的高热值(HHV=285.8 kJ⋅mol-1)与电解所需电能和热能之比。其中假设电流的效率为100%,ηsys表达式如式(1) :
| ${{\eta }_{sys}}=\frac{{\text{HHV}\cdot iAS}/{\left( 2F \right)}\;}{{{Q}_{h}}+{}^{{{Q}_{e}}}\!\!\diagup\!\!{}_{{{\eta }_{{AC}/{DC}\;}}}\;+{{Q}_{extra}}+{{Q}_{cell}}}$ | (1) |
其中A是单电池片数(30片),S是有效活性面积,Qh是预热气体所需能量,Qe是电解所需能量,ηAC/DC是设备直流/交流的转换效率,F是法拉第常数,Qcell是电解池预热所需的热量。
当然,除了对气体加热外,电池堆也需要热量维持在操作的温度,根据电池堆内部温度的分布[16],可以将这部分热量损失忽略[17]。当电解电压v大于热中性电压vtn(所测试温度内,vtn≈ 1.28 V),提供的电能大于电池电解所需要的电能,而多余的电能以热能形式释放;而当v小于vtn时,由于提供的电能小于电解所需电能,因此需要额外的能量,即Qextra。另外公式(1) 也忽略了系统工作时的热量散失。
| $\begin{align} & {{Q}_{h}}={{f}_{{{H}_{2}}O}}\times \left( \int_{298}^{373}{{{C}_{p,{{H}_{2}}O\left( L \right)}}dT+{{\Delta }_{vap}}{{H}_{m}}+\int_{373}^{T}{{{C}_{p,{{H}_{2}}O\left( L \right)}}dT}} \right) \\ & {{_{_{{}}}}_{_{{}}}}{{_{{}}^{{}}}_{{}}}+{{f}_{{{H}_{2}}}}\times \int_{298}^{T}{{{C}_{p,{{H}_{2}}}}dT}+{{f}_{{{N}_{2}}}}\times \int_{298}^{T}{{{C}_{p,{{N}_{2}}}}dT}+{{f}_{{{O}_{2}}}}\times \int_{298}^{T}{{{C}_{p,{{O}_{2}}}}dT} \\ \end{align}$ | (2) |
| ${{Q}_{e}}=ivAS$ | (3) |
| ${{Q}_{extra}}=i\left( {{v}_{tn}}-v \right)AS$ | (4) |
其中f是对应物质的摩尔流量,Cp是相应的热容,Cp, H2O(L)为液态水的热容75.44 J⋅mol-1×K-1,ΔvapHm是水的潜热(40.7 kJ⋅mol-1)。根据热力学数据[18],Cp, H2O(G) = 30.00 + 10.7×10-3T - 2.022×10-6T2,Cp, H2= 29.09 + 0.836×10-3T - 0.3265×10-6T2,Cp, N2= 27.32 + 6.226×10-3T - 0.9502×10-6 T2,Cp, O2= 36.16 + 0.845×10-3T - 0.7494×10-6T2。
3 结果与讨论 3.1 操作条件对i-v曲线的影响 3.1.1 温度对i-v曲线的影响向氢电极通入12 L⋅min-1加湿90%的氢气,阳极不通入任何气体,不同温度下的电流密度—电解电压曲线,如图 2所示。电池堆的开路电压随着温度变化不大,大约0.67 V;随着电流密度的增加,电解电压随温度升高而降低,在电流密度为0.51 A⋅cm-2时,三个温度对应的电解电压为1.75、1.49、1.39 V。

|
图 2 不同温度i-v曲线 Fig.2 i-v curves at different temperatures |
在低电流密度区,随着操作温度的降低,曲线上凸越来越明显,这是主要因为温度的增加,增加了活化分子所占的比例,使反应速度加快,从而使交换电流密度增大,而降低电化学过电位。随着电流密度增加,极化曲线呈线性,这部分的斜率的大小直接反映了欧姆电阻的大小。随着温度的增加,线性部分的面积电阻分别为1.59、1.11、1.05 Ω⋅cm2。在高电流密度区,没有出现明显的下凹,说明在实验的操作条件下,温度对浓差极化影响不明显。虽然温度的增加有利于气体的扩散,降低浓差极化的影响;但是在浓差过电位的表达式[9]中系数(RT/2F),随温度增加而增大,这样抵消了扩散造成的影响,最终使得温度对浓差极化的影响不大。
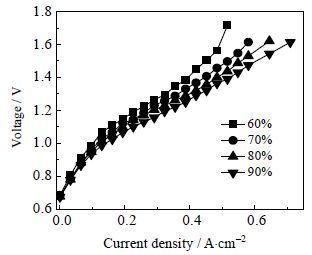
3.1.2 水蒸气含量对i-v曲线的影响电池堆在800℃的工作温度下,向氢电极通入12 L⋅min-1不同湿度的H2,阳极不通任何气体情况下,电解的i-v曲线如图 3所示。电解的开路电压随着水蒸气含量的增加而降低,但是变化非常有限,随着水蒸气含量的增加,氢电极氢气的分压偏低,开路电压降低;另外,由于氧电极氧气分压过低,使电解的开路电压变化不大。
|
图 3 不同湿度氢气下的 i-v 曲线 Fig.3 i-v curves studied using hydrogen gases with different steam concentrations |
在低电流密度区,水蒸气含量的增加导致交换电流密度更大,而使电化学过电位相对更小。电堆的欧姆电阻与材料、结构和温度有关,考虑到实验过程使用同一电解池堆,材料与结构的变化可以忽略,这样电堆的欧姆电阻只与操作温度有关,因此欧姆电阻是一致的。随着电流密度增加,水蒸气含量低的曲线出现明显上翘,说明此条件下的浓差过电位更大。因为在较高的电流密度下,电解所需水蒸气量更多,以及生成的氢气量也增多,水蒸气的供给和氢气扩散更为困难,导致浓差超电势激增,而低水蒸气含量的反应气本身具有更高的氢气分压和更小的水蒸气分压,这使得浓差过电位相对也更大。
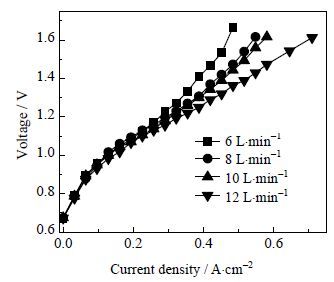
3.1.3 阴极通入气体流量对i-v曲线的影响图 4是在800℃下,向氢电极通入不同流量90%加湿H2,阳极不通入气体时,电解的i-v曲线。四种情况下的开路电压约为0.67 V。在低电流密度下,四条曲线比较接近,这说明氢电极通入气体的流量对电化学极化的影响较小。随着i的增加,曲线逐渐分开,较小流量的气体不能及时供应电解所需的水蒸气,也不能很好将生成的氢气从三相界面带出,使得在高电流密度时,浓差极化的影响越来越明显,在高电流密度区,极化曲线表现出明显的上翘。
|
图 4 氢电极通入不同流量气体的i-v曲线 Fig.4 i-v curves at different gas flow rates |
之前考察都是温度及氢电极气体对极化曲线的影响,而未考虑氧电极通入气体对极化的影响。虽然说,SOEC电解水蒸汽制备氢气,可以将氧电极的浓差极化忽略[19],同时也合并了氢电极、氧电极的电化学极化损失[20],并不是说改变通入氧电极气体的条件对SOEC电解水蒸气的性能没有影响。因此本部分主要考察氧电极通入气体对SOEC电解的i-v曲线的影响。
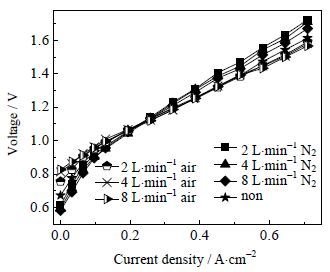
在800℃,阴极通入12 L⋅min-1含水量为90%的H2,向氧电极通入不同流量的N2或空气,得到的i-v曲线如图 5所示。从图中可以看出,随着通入空气流量的增加,电解的开路电压逐步增大,而增加N2的通入则使开路电压下降,这主要与氧电极氧气的分压有关。由于开路电压的影响,使得在低电流密度下,通入空气的电解电压更大;而随着电流密度的增加,另外两种情况的电解电压逐渐超过通入氧气的,由于在相同的温度和阴极供给条件下,所以欧姆降和浓差过电位基本相等,因此这主要是由电化学极化造成。因为向氧电极通入N2或空气使氧电极表面的氧分压的减小,造成LSCF中的晶格氧损失、氧离子空穴增多、电子空穴减少[21],这样可能导致氧电极三相界面的长度相对减小,电化学极化损失增大。同时,载流子浓度的下降[22, 23],使氧电极的导电性能减弱,极化损失增大。
|
图 5 氧电极通入不同气体的i-v曲线 Fig.5 i-v curves with different gases in the air electrode |
在高电流密度区域,各曲线都没有明显的上翘现象,这说明向氧电极通入不同流量的空气或氮气,对浓差过电位的影响不大。Ni[19]也指出氧离子是在氧气极—电解质界面被氧化,而并未扩散到多孔的氧气极中,可以忽略氧电极的浓差过电位。因此氧电极通入气体对浓差极化影响不大。
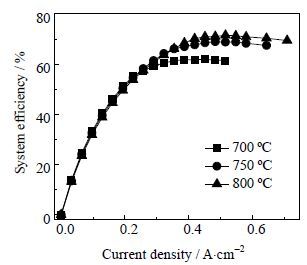
3.2 操作条件对SOEC制氢系统效率的影响 3.2.1 操作温度对系统效率的影响图 6是分别在700、750、800℃时,向阴极通入12 L⋅min-1湿度为90%的氢气,阳极不通入气体条件下,电解系统的效率曲线。由于在高温下电解时,电解池的极化损失也相对更少,能弥补将反应气体加热到更高的温度,所需的能量,因此在低电流密度,三条曲线基本一致。但是在高电流密度区,由于较低温度下的极化损失快速增加,电解电压也快速增大,电解所消耗的电能也迅速增多,系统效率开始缓慢增涨,甚至减小。而高温条件下电解,电解电压相对增涨更为缓慢,在高电流密度区有更高的电解效率。
|
图 6 不同温度下的i-ηsys曲线 Fig.6 i-ηsys curves at different temperatures |
图 7是氧电极不通入空气,氢电极通入不同流量90%加湿氢气的i-ηsys图。从图中可以看出,在低电流密度时,氢电极气体流量的降低,加热气体所需能量减小,有利于提高系统的效率高系统的效率。在流量为6 L⋅min-1,i为0.323 A⋅cm-2(v=1.27 V),系统效率达到最大值80.8%,此时的氢气产生速率为4.57 L·min-1。但是在更大的电流密度情况下,低流量会导致高的浓差过电位,增加电能的损失,导致ηsys快速下降。需要指出的是,如果将尾气热余热用于预热反应气体,SOEC电解制氢的系统效率将会更加高。

|
图 7 氢气极通入不同流量气体的i-ηsys曲线 Fig.7 i-ηsys curves at different gas flow rates |
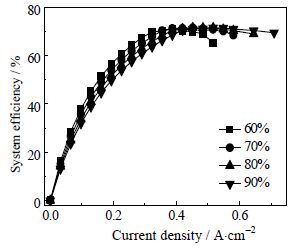
800℃,阳极不通入气体,阴极通入12 L⋅min-1不同水蒸气含量氢气,不同电流密度下的系统效率如图 8所示。与前面两种情况类似,由于水蒸气含量的增加,一方面增加了加热气体所耗能量;同时也有利于降低电解的过电位,节约电能。在低电流密度区,由于电解电压较小,加热气体消耗的能量占得比例较大,低水蒸气含量的系统效率更高。但是随着电流密度增加,极化造成的能量损失比例增大,此时高水蒸气含量气体的电解电压增加速度明显更低,而表现更高的系统效率。
|
图 8 不同水蒸气含量下的i-ηsys曲线 Fig.8 i-ηsys curves at different steam concentrations in the hydrogen electrode gas |
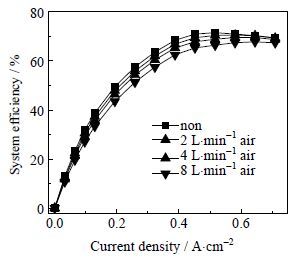
图 9是800℃,氢电极通入12 L⋅min-1 90%加湿氢气,氧电极通入不同流量空气的i-ηsys曲线。虽然向氧电极通入空气可以降低电化学过电位,提高电能的利用率,但是,通入的空气需要预热,消耗了能量。在低电流密度下,电解电压相近,极化损失相差不多,Qe也相差不多,因此不通空气的系统效率更高,在电流密度0.516 A⋅cm-2(v=1.39 V)时达到最大值71.48%,电池堆的氢气产生速率为7.29 L⋅min-1。但随着电流密度的增加,不通空气的电能损失越来越大,Qe比重逐渐增大,系统效率降低。而向氧电极通入不同流量N2的i-ηsys曲线(本文未给出)与通入空气的类似,但是由于N2的通入增大了电化学极化造成的能量损失,所以氧电极通入同流量的N2的ηsys值更小。
|
图 9 空气极通入不同流量空气的i-ηsys曲线 Fig.9 i-ηsys curves with different gas flow rates in the air electrode |
通过对燃料电极支撑的Ni-YSZ/YSZ/GDC/ LSCF-GDC电池堆电解水蒸汽性能研究,发现在实验的操作条件下,高温有利于欧姆降和电化学过电位的降低;氢气中水蒸气的含量增加可以降低电解的电化学过电位和浓差过电位;增加氢电极的反应气体流量对电化学极化影响不大,但有利于浓差过电位的减小;向氧电极通入空气可以降低电解的电化学过电位,但是氮气的通入却使电化学过电位增大。
虽然提高氧电极和氢电极气体流量可以降低过电位,降低Qe值,但是也增加了加热气体所耗能量。根据计算,在氧电极不通入气体,氢电极通入6 L⋅min-1 湿度为90%氢气,电流密度为0.323 A⋅cm-2时,系统效率最大80.8%,单位面积的产氢速率为2.45 mL⋅min-1,整堆的产氢速率为4.57 L⋅min-1。
| [1] | Laguna-Bercero M A . Recent advances in high temperature electrolysis using solid oxide fuel cells:A review[J]. Journal of Power Sources , 2012, 203 : 4-16 DOI:10.1016/j.jpowsour.2011.12.019 |
| [2] | ZHANG Zhi-yong(张志勇), CUI Qun(崔群), WANG Hai-yan(王海燕) . Cu1Zn1Al3.2 catalyst for hydrogen production by steam reforming of methanol(甲醇水蒸汽转化制氢Cu1Zn1Al3.2催化剂研究)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报) , 2007, 21 (2) : 251-256 |
| [3] | ZHANG Xuan(张旋), FU Guo-jia(付国家), TIAN Hong-jing(田红景) . Hydrogen generation from catalytic hydrolysis of alkaline sodium borohydride solution using sludge-S supported Co-B catalyst(污泥基载体负载Co基催化剂催化NaBH4水解制氢反应性能研究)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报) , 2013, 27 (6) : 1020-1026 |
| [4] | LIU Ming-yi(刘明义), YU Bo(于波), XU Jing-ming(徐景明) . Efficiency of solid oxide water electrolysis system for hydrogen production(固体氧化物电解水制氢系统效率)[J]. Journal of Tsinghua University(清华大学学报) , 2009, 49 (6) : 868-871 |
| [5] | Laguna-Bercero M A, Campama R, Larrea A . Electrolyte degradation in anode supported microtubular yttria stabilized zirconia-based solid oxide steam electrolysis cells at high voltages of operation[J]. Journal of Power Sources , 2011, 196 (21) : 8942-8947 DOI:10.1016/j.jpowsour.2011.01.015 |
| [6] | Chen K, Jiang S P . Failure mechanism of (La, Sr)MnO3 oxygen electrodes of solid oxide electrolysis cells[J]. International Journal of Hydrogen Energy , 2011, 36 (17) : 10541-10549 DOI:10.1016/j.ijhydene.2011.05.103 |
| [7] | Keane M, Mahapatra M K, Verma A . LSM-YSZ interactions and anode delamination in solid oxide electrolysis cells[J]. International Journal of Hydrogen Energy , 2012, 37 (22) : 16776-16785 DOI:10.1016/j.ijhydene.2012.08.104 |
| [8] | Kim-Lohsoontorn P, Bar J . Electrochemical performance of solid oxide electrolysis cell electrodes under high-temperature coelectrolysis of steam and carbon dioxide[J]. Journal of Power Sources , 2011, 196 (17) : 7161-7168 DOI:10.1016/j.jpowsour.2010.09.018 |
| [9] | Hjalmarsson P, Sun X F, Liu Y L . Influence of the oxygen electrode and inter-diffusion barrier on the degradation of solid oxide electrolysis cells[J]. Journal of Power Sources , 2013, 223 : 349-357 DOI:10.1016/j.jpowsour.2012.08.063 |
| [10] | kim S, Choi G M . Stability of LSCF electrode with GDC interlayer in YSZ-based solid oxide electrolysis cell[J]. Solid State Ionics , 2014, 262 : 303-306 DOI:10.1016/j.ssi.2014.01.001 |
| [11] | Schefold J, Brisse A, Zahid M. Long term testing of solid oxide fuel cell stacks with yttria stabilized zirconia electrolyte in the H2O electrolysis mode[C]//7th Symposium on Ionic and Mixed Conducting Ceramics held during the 217th Meeting of the Electrochemical-Society. Vancouver:ELECTROCHEMICAL SOCIETY, 2010, 28(11):357-367. |
| [12] | Stoots C M, O'Brien J E, Condie K G . High-temperature electrolysis for large-scale hydrogen production from nuclear energy-experimental investigations[J]. International Journal of Hydrogen Energy , 2009, 35 (10) : 4861-4870 |
| [13] | Ebbesen S D, Høgh J, Nielsen K A . Durable SOC Stacks for production of hydrogen and synthesis gas by high temperature electrolysis[J]. International Journal of Hydrogen Energy , 2011, 36 (13) : 7363-7376 DOI:10.1016/j.ijhydene.2011.03.130 |
| [14] | Zheng Y F, Li Q S, Guan W B . Comparison of performance and degradation of large-scale solid oxide electrolysis cells in stack with different composite air electrodes[J]. International Journal of Hydrogen Energy , 2014, 40 (6) : 2460-2472 |
| [15] | Guan W B, Jin L, Wu W . Effect and mechanism of Cr deposition in cathode current collecting layer on cell performance inside stack for planar solid oxide fuel cells[J]. Journal of Power Sources , 2014, 245 : 119-128 DOI:10.1016/j.jpowsour.2013.06.112 |
| [16] | Guan W B, Zhai H J, Jin L . Temperature measurement and distribution inside planar SOFC stacks[J]. Fuel Cells , 2012, 12 (1) : 24-31 DOI:10.1002/fuce.201100127 |
| [17] | Li Q S, Zheng Y F, Guan W B . Achieving high-efficiency hydrogen production using planar solid-oxide electrolysis stacks[J]. International Journal of Hydrogen Energy , 2014, 39 (21) : 10833-10842 DOI:10.1016/j.ijhydene.2014.05.070 |
| [18] | FU Xian-cai(傅献彩), SHEN Wen-xia(沈文霞), YAO Tian-yang(姚天扬) . Physical chemistry(物理化学)[M]. Beijing (北京): High Education Press(高等教育版社), 2006 : 481 . |
| [19] | Meng N, Michael K H L, Dennis Y C L . An electrochemical model of a solid oxide steam electrolyzer for hydrogen production[J]. Chemical Engineering & Technology , 2006, 29 (5) : 636-642 |
| [20] | Noten D A, Hoffman M A . Clarifying the butler-volmer equation and related approximations for calculating activation losses in solid oxide fuel cell models[J]. Journal of Power Sources , 2005, 152 : 175-181 DOI:10.1016/j.jpowsour.2005.03.174 |
| [21] | Jun A, Yoo S, Gwon O . Thermodynamic and electrical properties of Ba0.5Sr0.5Co0.8Fe0.2O3-δ and La0.6Sr0.4Co0.2Fe0.8O3-δ for intermediate-temperature solid oxide fuel cells. Electrochemical Acta[M]. 2013 : 372 -376. |
| [22] | Ge L, Zhou w, Ran R . Properties and performance of A-site deficient (Ba0.5Sr0.5)1-xCo0.8Fe0.2O3-δfor oxygen permeating membrane. Journal of Membrane Science[M]. 2007 : 318 -328. |
| [23] | Kostogloudis G C, Ftikos C . Properties of a-site-deficient La0.6Sr0.4Co0.2Fe0.8O3-δ perovskite oxides[J]. Solid State Ionics , 1999, 126 : 143-151 DOI:10.1016/S0167-2738(99)00230-1 |




