2. 四川之江高新材料股份有限公司,四川 遂宁 629100
2. Sichuan Zhijiang High-tech Material Co., Ltd, Suining 629100, China
N, N-二甲基二甘醇胺[2-(2-Dimethylaminoethoxy) ethanol,DMAEE]是重要的聚氨酯发泡催化剂,其催化生产的聚氨酯泡沫塑料具有低气味的特点,可生产硬质包装泡沫塑料,高回弹泡沫,广泛应用于汽车、家用器具等领域[1~5]。
工业上常用以下几种方法来合成DMAEE:

|

|
(3) 二甘醇胺甲基化法[12]:
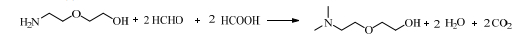
|
(4) N, N-二甲基乙醇胺(2-Dimethylaminoethanol, DAME)环氧化法[13~17]:

|
上述生产方法的工艺特点对比如表 1:
| 表 1 DMAEE合成工艺对比 Table 1 Comparison of DMAEE synthetic process |
综合比较上述生产工艺优缺点,本文认为从反应过程、工艺条件和排放处理等方面来看,DMAE环氧化工艺都是较优的选择。此工艺的缺点为:当环氧乙烷量大于或等于1当量时,容易产生高沸副产物使DMAEE选择性降低;环氧乙烷小于1当量时,原料DMAE转化率降低。为了克服此缺点,本文开发了DMAEE合成的新工艺。
2 DMAEE合成新工艺 2.1 工艺简述新工艺采用二甲胺(Dimethyl amine,DMA)和环氧乙烷(Ethylene oxide,EO)为原料,反应生成DMAE和DMAEE[18~19]。当EO通入过量时,也会发生副反应生成N, N-二甲基三甘醇胺(DMAEEE)和副产物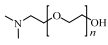
反应式如下:
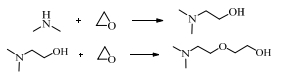
|
主要副反应:
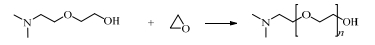
|
此反应以DMAEE作为主产物,DMAE为副主产物。原料EO和DMA的摩尔比是影响产物中DMAEE和DMAE组成的主要因素。调节原料EO/DMA摩尔比和反应工艺条件,可调整产物组成,因而此工艺可以根据市场需求调整产物组成,即达实现产品集成功能。原料配比对产物分配的影响如图 1所示。
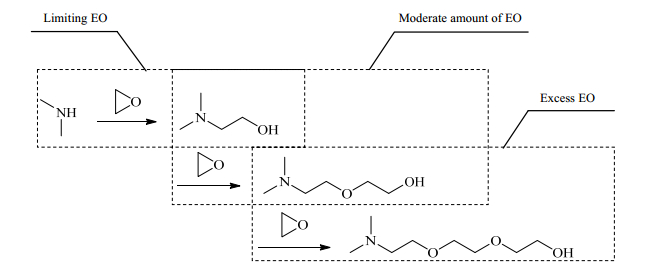
|
图 1 原料配比对产物分布的影响 Fig.1 Effeets of reactant ratio on product distribution |
如图 1,按原料摩尔比EO/DMA,可以将反应进程控制在三个区域:
EO欠量区:EO/DMA<1。主要产物DMAE,DMAEE生成极少,DMA有剩余,原料转化率低。
EO适量区:1<EO/DMA<2。主要产物是DMAE和DMAEE,原料EO和DMA均有较高的转化率。DMAE与DMAEE产出比例主要由EO/DMA决定,EO/DMA越大,DMAEE选择性越高。
EO过量区:EO/DMA>2,产物主要成分是DMAEE和高阶混合物(如DMAEEE)。DMA无剩余,EO可能有剩余,造成原料浪费,且高阶缩合物增多,分离能耗变大。
相比于常规以DMAE和EO为原料制取DMAEE的工艺,新工艺既能实现DMA和EO的高转化率,又能以较高选择性同时生产DMAE和DMAEE,并且保留了常规工艺条件温和、排放较少的优点。除此之外,在适量区内调整原料EO/DMA配比,可生成DMAE和DMAEE组成不同的产物,充分适应市场需求。
2.2 实验部分 2.2.1 仪器和试剂反应器为250 mL磁力搅拌高压釜。精馏柱高20 cm,直径2 cm,填料为不锈钢精密丝网。
主要试剂:33%二甲胺水溶液(CP),环氧乙烷(LR),N, N-二甲基乙醇胺(CP)。
2.2.2 检测方法检测仪器为安捷伦1790A气相色谱仪。氢气和载气氮气的柱前压为0.1 MPa,空气柱前压为0.03 MPa,进样器和检测器的温度为260℃,柱箱起始温度为100℃,初始时间为2 min,升温速率为20℃·min-1。
2.2.3 实验过程(1) 合成:
常压反应:三口瓶中加入一定量DMA水溶液,开启加热、搅拌和冷却水,缓慢通入一定量EO,恒温反应5 h左右,此时反应已基本完成;冷却,取样检测。
高压反应:高压釜中加入一定量DMA水溶液,密封高压釜;氮气置换4~5次;缓慢连续通入一定量EO;升温至所需温度,充入氮气至一定压力。恒温反应5 h左右;冷却、泄压;取样检测。
(2) 精馏:第(1)步反应产物在压力0.04 bar进行精馏,分别获得30℃、30~85℃、85~95℃馏分。
3 结果与讨论在EO与DMA的反应中,EO/DMA摩尔比、压力、温度和溶剂等都会影响产物组成。
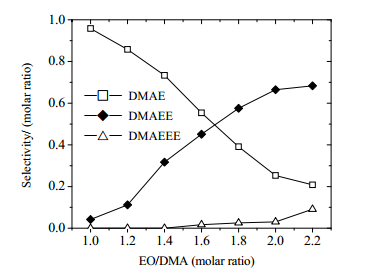
3.1 EO/DMA的影响反应温度80℃,常压,反应5 h。EO/DMA比值为1~2.25,产物的分布规律如图 2所示。本文以选择性确定产物的分布,选择性=目的产物中氮元素物质的量/总产物中氮元素物质的量。
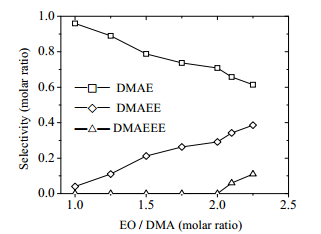
|
图 2 产物选择性随EO/DMA摩尔比变化的曲线 Fig.2 Product selectivity as a function of molar ratio of EP/DMA |
如图,在1<EO/DMA<2.25范围内,随着EO/DMA的增加,产物DMAE选择性逐渐降低,DMAEE选择性逐渐升高,而副产物DMAEEE则在EO/DMA>2时才开始出现并逐渐升高。因此反应须控制EO/DMA在适量区,产物中只有DMAE和DMAEE。因为此组实验为常压反应,DMAEE选择性较低,但分离产物中DMAE并循环回用,可提高DMAEE的产率[20, 21]。
原料配比EO/DMA是影响产物中DMAEE含量的最重要因素,调节原料配比可调节产物中DMAEE和DMAE的比例,适应市场需求,是实现产品集成工艺的重要手段。
3.2 温度的影响原料配比EO/DMA为2,压力1.2 MPa,温度是45~93℃,反应时间均为5 h。产物中无DMA和EO残余,DMAE和DMAEE的总收率达到90%以上。产物中各组分选择性随温度变化情况如图 3。
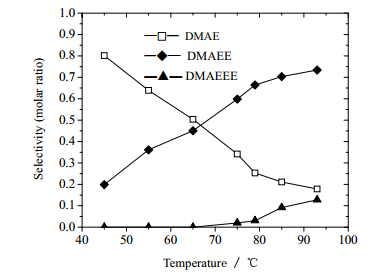
|
图 3 产物选择性随温度变化的曲线 Fig.3 Product selectivity as a function of temperature |
由图 3,随着温度上升,DMAE选择性逐渐下降;DMAEE的选择性逐渐上升且上升速度逐渐减慢;DMAEEE选择性逐渐上升;反应温度为80℃时,副产物生成较少且反应速度较快。
随着温度升高,气相中反应物DMA和EO浓度升高,系统压力随之变大,产物分布与反应温度之间的对应关系也受压力影响,比较复杂;而且温度过高时EO容易与水或DMAEE反应生成副产物。反应动力学和热力学分析[22, 23]认为随着温度升高,反应速度和副反应速度均会加快,因此副产物DMAEEE产量也会变大,不能通过升高温度来大幅调节产物比例。
3.3 压力的影响原料摩尔比EO/DMA为2,反应温度为80℃,压力1.0~1.75 MPa,反应时间为5 h。产物中均无DMA和EO存在,当压力为1.2 MPa时,DMAE和DMAEE总收率达到了95%以上。产物中各组分选择性分布如图 4。
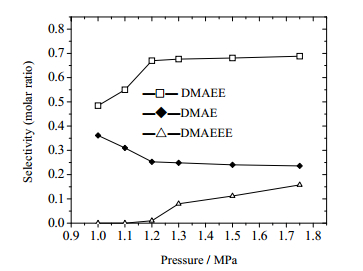
|
图 4 产物选择性随压力变化的曲线 Fig.4 Product selectivity as a function of pressure |
由图 4,随着反应釜内压力升高,产物中DMAE的选择性逐渐下降;DMAEE选择性逐渐升高;DMAEEE选择性逐渐升高。当压力大于1.2 MPa时,随着EO溶解度随压力的变化幅度变小,产物选择性变化幅度变小。
实验结果表明,通入氮气可降低反应釜气相中EO分压,提高EO在液相中的溶解度,并提高EO的转化率;但压力过高时,容易生成高沸副产物。除此之外,压力过高,对反应釜的强度要求也升高。
3.4 溶剂的影响选用33%二甲胺水溶液可认为是水作为反应溶剂。然而此时,产物易溶于水,分离能耗较高,因此可以尝试更换不同溶剂。
根据文献[24~27],EO和胺类在无水条件下是很难发生反应的,而在水存在下两者可以发生反应;而在高温高压条件下,胺类和EO可以在无水存在下反应。而Lowe等[28]发现,羟基化合物参与了环氧乙烷胺化的过程。冯汝明等[29]证明,EO与胺类反应需要的活化能较高,提供活性氢原子是提高胺化活性的重要途径,而羟基中含有活性氢原子。因此,也可选用醇类作为溶剂。
3.4.1 溶剂种类的影响原料摩尔比EO/DMA为2,反应温度80℃,压力1.2 MPa,反映5 h,分别在无溶剂、溶剂为乙醇和水的条件下实验,此时溶剂乙醇和水的用量均为原料的55%(wt)。实验结果如表 2。
| 表 2 不同溶剂对产物各组分含量的影响 Table 2 Effects of different solvents on product selectivity |
上表结果说明,水作溶剂时DMAE和DMAEE的选择性最好,醇溶剂次之,无溶剂最差;水作溶剂时的原料转化率最高,醇作溶剂次之,无溶剂最差;水作溶剂时的高沸副产物的产生最少,醇溶剂次之,无溶剂最多。针对这种现象,Holubka等[30]认为,EO与胺类反应时,活性质子的存在能显著降低EO与胺类反应的活化能,大大提高反应速度。在水溶液中,水具有很强的供质子能力;一些简单的醇类化合物也能提供质子,但因其分子结构较大,其效果不如水,如下所示:
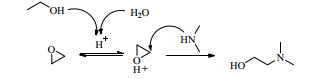
|
选用水作溶剂,常精馏得到DMAE-水混合馏分。为了分离得到较纯的DMAE,往往需要消耗大量能量。若能将混合馏分可进行循环回用[31],不仅降低能耗,还能提高产物DMAEE的收率。因此,为了确定循环混合液中DMAE-水的组成,就需要测定在反应时溶剂水用量对产物的影响。
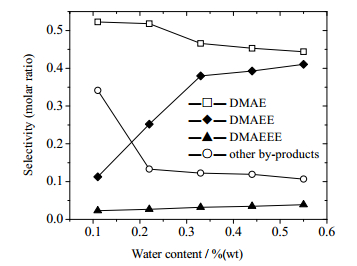
原料摩尔比EO/DMAE为1,温度80℃,压力1.2 MPa,水用量11%(wt)~55%(wt),其结果如图 5。
|
图 5 溶剂水用量对结果的影响 Fig.5 Product selectivity as a function of water consumption |
如图 5,随着用水量的增加,产物中DMAE含量逐渐下降,DMAEE的选择性先上升后逐渐稳定,DMAEEE的选择性逐渐上升;其他副产物的选择性先迅速下降后稳定。当水含量大于33%(wt)时,各产物选择性都趋于稳定。冯汝明等[29]认为,溶剂水用量在很大程度上影响产物分布;而有文献[32, 33]认为,水含量过少,胺类浓度过大时,容易产生高沸副产物。因此,水在反应中的用量需控制在合适的范围内。在实验条件下,水含量应控制在33%为宜。
3.5 产物分布调控根据上述研究,合适的反应条件为:温度80℃,压力1.2 MPa,溶剂水用量33%,在原料摩尔比DMA/EO为1~2.2进行产物分布调控,其结果如图 6。
|
图 6 适宜条件下的产物调控 Fig.6 Product profiles prepared under controlled conditions |
由图 6,在1<EO/DMA<2时,产物中无DMA残留,产物中DMAE选择性从95.8%~25.2%逐渐降低,DMAEE选择性从4.2%逐渐升高至66.4%,两者总收率(DMAE+DMAEE)均大于90%。原料DMA转化率为95%,EO转化率83.5%。因此,在环氧乙烷适量区内,EO/DMA对产品组成具有良好的调控效果。
4 结论(1) 原料投料EO/DMA是控制产物中DMAE与DMAEE比例的关键。在1<EO/DMA<2时,EO/DMA越大,产物中DMAEE含量越高。
(2) 合适的工艺条件:EO/DMA为1~2,含水量33%,温度80℃,压力1.2 MPa,反应时间5 h。此时,原料DMA转化率大于90%,EO转化率大于80%。产物主要成分DMAE和DMAEE的总收率大于95%。
本实验研究结果对于DMAEE的工业生产工艺研发具有一定程度的指导意义。
| [1] | SUN Gang(孙刚), LIU Yu(刘预), FENG Fang(冯芳). Development of research on polyurethane foams(聚氨酯泡沫材料的研究进展)[J]. Materials Review(材料导报) , 2006, 20(3): 29-32. |
| [2] | TAN Mei-jun(谭美军). Polyurethane foam organic amine catalysts(聚氨酯泡沫有机胺类催化剂)[J]. Hunan Chemical Industry(湖南化工) , 1991, 21(1): 21-23. |
| [3] | LIU Yi-jun(刘益军). Polyurethane additives(聚氨酯的助剂)[J]. Polyurethane(聚氨酯) , 2008(6): 90-94. |
| [4] | LI Ren-cui(李人粹). Amine catalyst composition for polyurethane(聚氨酯用胺催化剂组成物)[J]. Polyurethane(聚氨酯) , 2006(6): 72-74. |
| [5] | LI Wei(李伟). Environmentally friendly catalyst for polyurethane elastomer(环保聚氨酯弹性体催化剂)[J]. Rubber Reference Material(橡胶参考资料) , 2014, 44(6): 56-56. |
| [6] | Rattay B, Rettig W. 1, 2-Di-O-hexadecylglycero-3-phosphocholines with ethylene glycol units adjacent to the head group[J]. Pharmazie , 1997, 52(9): 676-679. |
| [7] | De Amici M, De Micheli C, Pratesi P, et al. Santagostino-Barbone M G. Synthesis, biological activity and conformational analysis of some acyclic cholinergic ligands[J]. Farmaco; Edizione Scientifica , 1987, 42(12): 921-930. |
| [8] | Haese F, Boettcher A, Stein B, et al. Method for the continuous production of an amine:EU Patent, 1, 747, 187, A1[P]. 2007-01-31. |
| [9] | Labadie J W, Dixon D D. Selective catalytic synthese of mixed alkyl amines[J]. Journal of Molecular Catalysis , 1987, 42(3): 367-378. DOI:10.1016/0304-5102(87)85013-7. |
| [10] | Wolfgang F. Process for preparing dimethylamines:German Offen, 3, 422, 610[P]. 1985-12-19. |
| [11] | Fischer R, Mercker H J, Mueller H. Process for the preparation of aliphatic dialkyl amino alcohols:EU Patent, 0, 227, 904(B1)[P]. 1990-10-17. |
| [12] | Kordas I, Speulta K, Gaspar A, Nyari M, Aranyi P. Process for the preparation of N-methylated amines by metal-catalyzed reductive methylation:Hungary Patent, 9, 701, 207[P]. 1999-06-28. |
| [13] | YANG Yu-feng(杨玉峰). Synthesis of N, N-dimethylethanolamine(N, N-二甲基乙醇胺合成的研究)[J]. Henan Science(河南科学) , 2004, 22(4): 458-460. |
| [14] | SHI Ying-hua(石英华). Synthesis and purification of N, N-dimethylethanolamine(二甲基乙醇胺合成与精制)[J]. Shijiazhuang Chemical Industry(石家庄化工) , 1994(1): 23-26. |
| [15] | XUAN Mei-fu(宣美福). Application of N, N-dimethylethanolamine(二甲基乙醇胺的应用开发)[J]. Chemical Propellants & Polymeric Materials(化学推进剂与高分子材料) , 1991(3): 18-21. |
| [16] | ZHAO Bin(赵彬), CHEN Dian-jun(陈殿军). Synthesis of polyether modified quaternary ammonium ionic liquids and their catalysis on the cycloaddition of CO2 to epichlorohydrin(聚醚季铵离子液体合成及其催化CO2与环氧烷加成反应)[J]. Journal of Molecular Catalysis(分子催化) , 2008, 22(6): 487-490. |
| [17] | Yilmaz G, Guler E, Barlas F B, et al. Polymeric thioxanthones as potential anticancer and radiotherapy agents[J]. Macromolecular Rapid Communications , 2016, 37(13): 1046-1051. DOI:10.1002/marc.v37.13. |
| [18] | Melder J P. A method for the preparation of N, N-dimethylaminoethoxy ethanol:CN 101405256 B[P]. 2009-04-08. |
| [19] | Frank H. Preparation of N, N-dimethylamino ethoxyethanol by reacting reacting dimethylamine with ethylene oxide:WO, 2, 007, 107, 557[P]. 2007-09-27. |
| [20] | Nygarrd D M, Diguilio R M. Production of diethanolamine:US 6, 063, 965[P]. 2000-05-16 |
| [21] | Diguilio R M, Mckinney M W. Selective production of diethanolamine:EU Patent 6, 075, 168[P]. 2000-06-13 |
| [22] | LUO Ming-fang (罗铭芳). Process simulation and development of ethanol ammonia plant (乙醇胺装置流程模拟与开发研究) [D].Tianjin (天津): Tianjin University (天津大学), 2003 http://d.wanfangdata.com.cn/Thesis/Y591671 |
| [23] | WEI Hai-guo (魏海国). Pipeline reaction process of ethanolamine (乙醇胺的管道化反应工艺)[D]. Hangzhou (杭州): Zhejiang University (浙江大学), 1993 |
| [24] | Carleton E. The chemistry of petroleum derivatives[J]. Chemistry of Petroleum Derivatives , 1934(1) 541-544, 563-567. |
| [25] | Miller S A. Ethylene and its industrial derivatives[M]. London:Ernest Benn, 1969, 22:632-635. |
| [26] | ZHAO Yu-ying(赵玉英). Synthesis of N, N-diethylethanolamine, a pharmaceutical intermediates(医药中间体N, N-二乙基乙醇胺的合成)[J]. Anhui Chemical Industry(安徽化工) , 2003(04): 11-12. DOI:10.3969/j.issn.1008-553X.2003.04.005. |
| [27] | WU Zhao-li (吴兆立), XIE Rong-jin (谢荣锦), CAI Zhen-yun (蔡振云). The water-free tubular reaction method of ethanolamine production (乙醇胺生产的无水管式反应方法): CN 96100557.2 [P]. 1997-01-01. |
| [28] | Lowe A J. Butler D, Meade E M. Manufacture of alkanolamines:GB 760215(A)[P]. 1956-10-31. |
| [29] | FENG Ru-ming(冯汝明), LIU Zhong-neng(刘仲能), GU Rong(顾荣), et al. Amination of ethylene oxide to product ethanolamine(环氧乙烷胺化制乙醇胺)[J]. Progress in Chemistry(化学进展) , 2009, 21(7/8): 1636-1643. |
| [30] | Holubka J W, Bach R D, Andres J L. Theoretical study of the reactions of ethylene oxide and ammonia:a model study of the epoxy adhesive curing mechanism[J]. Macromolecules , 1992, 25(3): 1189-1192. DOI:10.1021/ma00029a028. |
| [31] | WANG Yu-ping (王宇平), WANG Sheng-li (王胜利), QIAN Chun-yang (钱春阳), et al. Synthesis of N, N - dimethylethanolamine (N,N-二甲基乙醇胺制备方法): CN101648880 [P]. 2010-02-17 |
| [32] | Hammer H, Reutemann W. Production of ethanolamines:US 5, 545, 757 A[P]. 1996-08-13. |
| [33] | Johnson F L. Selective production of monoalkanolamines from alkylene oxides and ammonia over acidic inorganic catalysts:US 4, 438, 281[P]. 1984-03-20 |




