2. 绍兴文理学院 化学化工学院, 浙江 绍兴 312000
2. College of Chemistry and Chemical Engineering, Shaoxing University, Shaoxing 312000, China
铅是一种常见的重金属污染物,不仅会损伤肠胃及肝肾、导致儿童智力缺陷,并能够在人体和动植物体富集,严重威胁人类健康和生态环境[1]。常规处理铅污染废水的方法主要为化学沉淀,化学还原,离子交换,膜分离,矿物吸附,生物吸附等。然而这些方法同时也存在处理周期长,成本高,仅适用于低浓度铅污染废水修复等缺点[2]。
零价铁(zero valent iron,ZVI)具有原料廉价易得,操作简单、二次污染少、运行成本低等优点,用于污染物的处理是一种很有发展潜力的修复技术[3~6]。由于零价铁与污染物之间的反应主要在表面上进行的,因此增大零价铁的比表面积或改善零价铁表面性能提高对污染物的吸附能力有助于增强其还原去除污染物的能力[7, 8]。与微米级零价铁相比,纳米零价铁粒径小,比表面积大,表面活性强,将其用于有机氯化物[9, 10]、重金属离子[11]、染料废水的处理[12]以及地下水的原位修复[13]中,均取得了显著的效果。但由于胶体效应及自身的铁磁性,纳米零价铁在使用过程中极易团聚,为了克服这个缺陷,一些学者选用合适的载体制得负载型纳米零价铁,如Zhang等[14]以片状剥落的石墨为载体制备负载型纳米零价铁,去除废水中的硝酸盐显示了良好的实验效果;Hoch等[15]制备了具有较好分散性的碳负载纳米零价铁在三天内将废水中10 ppm Cr(VI)去除到低于1 ppm的水平;Ponder等[16]以树脂为载体制得的负载型纳米零价铁,能够快速高效去除Cr(VI)和Pb(Ⅱ);He等[17]将羧甲基纤维素负载纳米Fe-Pd用于降解三氯乙烯,具有反应速度快、降解彻底的优点。这些负载型纳米零价铁虽能在一定程度上解决了纳米零价铁的团聚问题,但其制备过程比较复杂、成本较高。
膨润土是一类具有良好离子交换能力和吸附性能的天然矿物质,它具有比表面积大、微孔量高、表面酸性强以及层间和表面存在疏水或亲水基团等特点,用作吸附剂、催化剂及催化剂载体在石油化工、废气、废水处理等领域具有良好的应用前景[18~20]。与其他载体相比,它可以根据目标污染物的性质进行合适的改性,得到表面Zeta电位各异、疏水性不同的改性膨润土。本文利用对无机污染物具有良好吸附性能的羟基铝柱撑膨润土为载体,通过FeSO4与NaBH4反应制备羟基铝柱撑膨润土负载纳米零价铁,以Pb(Ⅱ)作为目标污染物,考察羟基铝柱撑膨润土负载纳米零价铁对废水中Pb(Ⅱ)的去除能力,并与相同铁量的纳米零价铁反应体系进行比较。
2 实验 2.1 材料与试剂钠基膨润土系内蒙古钙基膨润土经NaCl溶液处理得到,其阳离子交换容量用乙酸铵法测定为115 mmol·(100g)-1[21],AlCl3·6H2O、FeSO4·7H2O、NaBH4、Pb(NO3)2、铁粉等试剂均为分析纯,实验用水为去离子水。
2.2 材料的制备 2.2.1 羟基铝柱撑膨润土的制备将所需量的AlCl3·6H2O溶解在烧杯中,置70℃水浴中不断搅拌下按[OH-]/[Al3+]=2.0的比例用蠕动泵慢慢注入NaOH溶液,加完后将制得的柱撑液在室温下放置2d,再以[Al3+]/土=10 mmol·g-1的比例将该柱撑液通过蠕动泵注入到膨润土浆液中进行离子交换,加完后在70℃烘箱中老化2d,离心洗涤至无Cl-检出,70℃下干燥,研磨过100目筛,最后在115℃下活化2h,得到的柱撑膨润土用Al-PILC表示。
2.2.2 纳米零价铁的制备在搅拌下,将0.108 mol NaBH4的250 mL水溶液逐滴滴入到等体积的0.054 mol FeSO4·7H2O水溶液中,待NaBH4溶液滴加完,继续搅拌0.5h,溶液中铁离子被还原成零价铁:Fe(H2O)62++ 2BH4-→ Fe↓ + 2B(OH)3+ 7H2↑。将产物倾析,然后抽滤、洗涤,最后置于真空干燥器中干燥。产物标记为:NZVI。
2.2.3 羟基铝柱撑膨润土负载纳米零价铁的制备将一定量的羟基铝柱撑膨润土加入到0.054 mol FeSO4·7H2O的250 mL水溶液中,搅拌数小时,然后按上述方法与NaBH4反应,制得羟基铝柱撑膨润土负载纳米零价铁。产物标记为:NZVI/Al-PILC。
2.3 实验方法在一系列250mL碘量瓶中,将含铁量相同的ZVI、NZVI、NZVI/Al-PILC以及与NZVI/Al-PILC含土量相同的Al-PILC分别加入到150 mL一定浓度的Pb(Ⅱ)溶液中(通氮气10 min,pH=7,pH试验除外),25℃下以150 r·min-1的速度振荡,定时取样,经微孔滤膜(0.22 μm)过滤后用原子吸收法测定Pb(Ⅱ)的含量[2]。
2.4 测试方法样品的XRD测定是在日本理学D/MAX2500型X射线衍射仪上进行(Cu靶、Kα线);TEM表征是在日子电子JEM-1010型透射电子显微镜上进行(加速电压80kV)。样品比表面积是在美国Coulter公司Omnisorp 100CX型比表面积和孔隙分析仪上测定的。溶液中Pb(Ⅱ)浓度,以及样品中铁含量、反应过程中铁溶出量均用原子吸收法测定(AA-6300原子吸收光谱仪,岛津(香港)有限公司)。溶液的pH是用精密pH计进行测量(PHS-3C精密pH计,上海安亭科学仪器厂)。
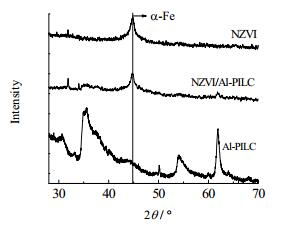
3 结果与讨论 3.1 材料表征XRD测定表明(图 1),NZVI和NZVI/Al-PILC都在2θ=44.8°处都出现了α-Fe特征峰且没有出现明显的铁氧化物特征峰。图 2是NZVI/Al-PILC和NZVI的TEM图,从图中可以看出,NZVI/Al-PILC(b)中Fe0粒子呈现出良好的分散状态,而NZVI(a)中的Fe0粒子团聚现象比较明显。这表明Al-PILC作为NZVI的载体,能有效地克服NZVI的团聚。经测定,NZVI/Al-PILC、NZVI的铁含量分别为19.8%和82.0%,比表面积分别为29.8和33.5 m2·g-1。
|
图 1 NZVI, NZVI/Al-PILC和Al-PILC的XRD图像 Fig.1 XRD patterns of NZVI, NZVI/Al-PILC and Al-PILC |

|
图 2 NZVI (a)和NZVI / Al-PILC (b)的TEM图像 Fig.2 TEM micrographs of NZVI (a) and NZVI/Al-PILC (b) |
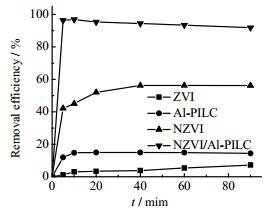
图 3为含铁量相同的铁粉(ZVI,0.0200 g)、NZVI(0.0244 g)、NZVI/Al-PILC(0.1012 g)以及与NZVI/Al-PILC含土量相同的Al-PILC(0.0812 g)对150 mL 100 mg·L-1的Pb(Ⅱ)溶液中Pb(Ⅱ)的去除率。由图 3可见,在相同的实验条件下,反应90 min后,各种材料对Pb(Ⅱ)的去除率分别为ZVI: 7.23%,Al-PILC: 14.4%,NZVI: 56.2%,NZVI/Al-PILC: 91.8%。Al-PILC主要是通过吸附去除Pb(Ⅱ),与ZVI相比,NZVI对Pb(Ⅱ)的去除率大大提高,这主要是因为NZVI比表面积更大、表面活性位点更多。而NZVI/Al-PILC对Pb(Ⅱ)的去除率远高于含铁量相同的NZVI,也明显大于NZVI和Al-PILC的加和(70.6%),这表明NZVI/Al-PILC对Pb(Ⅱ)的去除存在明显吸附与还原的协同作用,这是由于在铁还原污染物的过程中,金属表面直接的电子转移是反应的决速步骤,因此,以具有良好吸附性能的Al-PILC为载体可以有效增加铁与Pb(Ⅱ)之间的电子转移速度,从而明显提高了对Pb(Ⅱ)的还原能力。
|
图 3 不同材料对Pb(Ⅱ)的去除率 Fig.3 Pb(Ⅱ) removal efficiency of different materials |
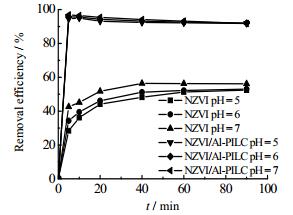
图 4为含铁量相同的NZVI(0.0244 g)和NZVI/Al-PILC(0.1012 g)对初始pH值分别为5.0、6.0、7.0的150 mL 100 mg·L-1 Pb(Ⅱ)溶液的处理效果。由图可见,在初始pH为5.0、6.0、7.0时,反应进行90 min后,NZVI对Pb(Ⅱ)的去除率分别为52.4%、53.0%、56.2%,而NZVI/Al-PILC对Pb(Ⅱ)的去除率则分别为91. 8%、92.0%、91.8%,从图 4可得出:
|
图 4 pH对Pb(Ⅱ)的去除率的影响 Fig.4 Effects of pH on Pb(Ⅱ) removal |
(1) 在三种不同pH介质中,NZVI/Al-PILC对Pb(Ⅱ)的去除率都远大于NZVI。
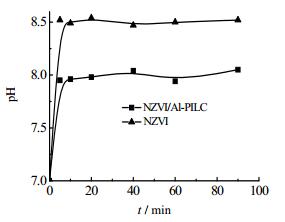
(2) NZVI对Pb(Ⅱ)的去除率随pH增大有一定的增加,而NZVI/Al-PILC对Pb(Ⅱ)的去除率受pH影响不大。图 5是NZVI/Al-PILC和NZVI在初始pH7.0时与Pb(Ⅱ)反应过程中介质pH的变化。由图可知,载体Al-PILC的引入使NZVI/Al-PILC体系的介质pH维持在一个相对较低的水平(~8.0)。这是因为Al-PILC表面含有众多的Al-OH、Si-OH基团,这些两性基团具有一定的缓冲介质pH的能力[23]。随着反应过程中H+的消耗,Al-OH、Si-OH基团可以释放出质子来中和产生的OH-,从而使NZVI/Al-PILC对Pb(Ⅱ)的去除率受pH影响较小。至于介质pH增大对Pb(Ⅱ)的去除率稍有提高这是由于反应体系中存在NO3-,而NO3-与Fe0的反应为酸促反应[14],当pH较低时,NO3-与Fe0反应的倾向增大,从而会减少Fe0表面活性位点与Pb(Ⅱ)的反应。但Li等[22]的实验表明:NZVI对Pb(Ⅱ)的去除是还原与吸附共存的过程,pH降低不利于对Pb(Ⅱ)的吸附,上述两方面的综合结果,将导致pH增大,NZVI对Pb(Ⅱ)的去除率稍增。
|
图 5 反应过程中介质pH变化 Fig.5 pH variation during reaction processes |
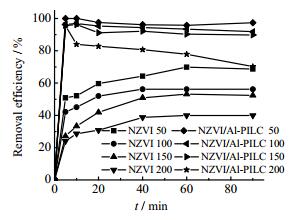
图 6为含铁量相同的NZVI(0.0244 g)和NZVI/Al-PILC (0.1012 g)对初始浓度分别为50、100、150和200 mg·L-1的150 mL Pb(Ⅱ)溶液中Pb(Ⅱ)的去除率。可以看出,经过90 min的反应,NZVI/Al-PILC对这四种初始浓度的Pb(Ⅱ)的去除率分别为97.4%、91.8%、89.8%、70.2%,而NZVI对这四种初始浓度的Pb(Ⅱ)的去除率分别为68.7%、56.2%、52.4%、40.0%。可见,在相同实验条件下,对于各种不同初始浓度的Pb(Ⅱ),NZVI/Al-PILC都比NZVI具有更显著的去除能力。
|
图 6 NZVI/Al-PILC和NZVI对不同浓度Pb(Ⅱ)的去除 Fig.6 Pb(Ⅱ) removal efficiency of NZVI/Al-PILC and NZVI for Pb(Ⅱ) solutions with different concentrations |
污染物与零价铁之间的反应是一个表面反应,用Langmuir-Hinshelwood方程
| 表 1 L-H动力学方程拟合 Table 1 L-H kinetic equation fitting |
从表中可以看出,NZVI/Al-PILC和NZVI与Pb(Ⅱ)的反应较好地符合L-H动力学模型。其中,NZVI/Al-PILC的表观反应速率常数和吸附常数都比NZVI大,表明反应速率与NZVI/Al-PILC、NZVI对Pb(Ⅱ)的吸附性能呈正相关关系。由此说明,NZVI/Al-PILC对Pb(Ⅱ)的去除率高与其对Pb(Ⅱ)的吸附能力提高直接相关。
3.5 NZVI/Al-PILC和NZVI重复使用性的比较催化剂的反应活性与重复使用性是两个很重要的参数,为此本实验考察了NZVI/Al-PILC和NZVI对Pb(Ⅱ)去除反应的重复使用性。具体操作如下:分别向含有150 mL浓度为100 mg·L-1,pH为7的Pb(Ⅱ)溶液的锥形瓶中加入相同铁量的NZVI/Al-PILC和NZVI,反应90 min以后,分别移取2 mL溶液,测定溶液中Pb(Ⅱ)的浓度,然后再分别加入合适浓度的硝酸铅溶液2 mL,重新调整pH,使体系中的Pb(Ⅱ)浓度,pH与第一次反应时一致。此过程重复四次。其结果如图 7所示。
|
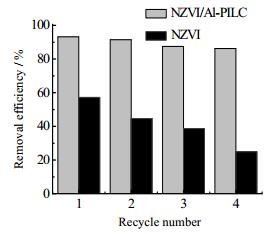
图 7 NZVI/Al-PILC和NZVI对Pb(Ⅱ)的重复去除效率 Fig.7 Pb(Ⅱ) removal efficiency of NZVI/Al-PILC and NZVI after different recycle times |
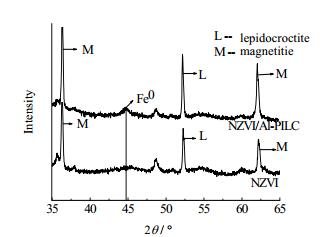
由图 7可知,在四次重复性实验中,NZVI对Pb(Ⅱ)的去除效率由第一次的57.2%下降到第四次的24.9%,而NZVI/Al-PILC体系的去除效率从93.2%降低到86.3%,呈现出较好的重复使用性。为了说明两者间重复去除性能的差异,我们对4次重复性实验后在氮气中干燥得到的样品进行了XRD测定(图 8)。由图 8可知4次处理后的NZVI/Al-PILC依然能够检测出有明显的零价铁特征峰(2θ=44.8°),而NZVI的零价铁特征峰则基本上消失。图 5中反应pH值的变化表明,NZVI/Al-PILC体系中较低的pH有利于减少铁表面生成的腐蚀产物(铁氧化物或氢氧化物),从而增强了材料的稳定性[24]。此外,我们前期用XAFS实验手段研究膨润土/纳米零价铁复合材料去除Cr(VI)中证实[25]:膨润土作为载体,可使反应腐蚀产物从铁表面转移到土上,因而延缓了铁的钝化进程。
|
图 8 NZVI/Al-PILC和NZVI经过4次重复性试验后的XRD图像 Fig.8 XRD patterns of NZVI/Al-PILC and NZVI after 4 reaction cycles |
1) 在相同实验条件下,NZVI/Al-PILC对废水中Pb(Ⅱ)的去除率远高于含铁量相同的NZVI,也明显优于含铁量相同的NZVI和含土量相同的Al-PILC对Pb(Ⅱ)的去除率的加和,体现了吸附作用与还原反应之间良好的协同效应。
2) NZVI/Al-PILC和NZVI与废水中Pb(Ⅱ)的反应符合Langmuir-Hinshelwood动力学方程,并且NZVI/Al-PILC去除Pb(Ⅱ)的反应速率常数是NZVI的7倍。
3) 与NZVI相比,NZVI/Al-PILC在处理Pb(Ⅱ)的实验中表现出良好的重复使用性,体现了柱撑膨润土优异的载体效应。
符号说明:| [1] | Alluri H K, Ronda S R, Settalluri V S . Biosorption:an eco-friendly alternative for heavy metal removal[J]. Afr J Biotechnol , 2007, 6 (25) : 2924-2931 DOI:10.5897/AJB |
| [2] | Zhang X, Shen L, Chen Z L . Removal of Pb(Ⅱ) from water using synthesized kaolin supported nanoscale zero-valent iron[J]. Chem Eng J , 2010, 163 (3) : 243-248 DOI:10.1016/j.cej.2010.07.056 |
| [3] | Hussein H, Ibrahim S F, Kandeel K . Biosorption of heavy metals from waste water using pseudomonas[J]. Electron J Biotechnol , 2004, 7 (1) : 38-46 |
| [4] | Jyotsna G, Kadirvelu K, Chitra R . Investigation of adsorption of lead, mercury and nickel from aqueous solutions onto carbon aerogel[J]. J Chem Technol Biotechnol , 2005, 80 (4) : 469-476 DOI:10.1002/(ISSN)1097-4660 |
| [5] | Rehman A, Shakoori F R, ShakooriA R . Uptake of heavy metals by stylonychia mytilus and its possible use in decontamination of industrial wastewater[J]. World J Microbiol Biotechnol , 2008, 24 (1) : 47-53 DOI:10.1007/s11274-007-9436-1 |
| [6] | YE Guo-xiang(叶国祥), ZHOU Shuo-ling(周烁灵), TANG Jia-yu(唐佳玙) . High concentration dyeing waste water pretreatment by Fe-C micro-electrolysis(Fe-C微电解法预处理高浓度印染废水的研究)[J]. J Chem Eng of Chinese Univ(高校化学工程学报) , 2011, 25 (3) : 489-494 |
| [7] | Li Z H, Williams C, Alley J . A shift in pathway of iron-mediated perchloroethylene reduction in the presence of sorbed surfactant-a column study[J]. Water Res , 2006, 40 (20) : 3811-3819 DOI:10.1016/j.watres.2006.08.025 |
| [8] | Varanasi P, Fullana A, Sidhu S . Remediation of PCB contaminated soils using iron nano-particles[J]. Chemosphere , 2007, 66 (6) : 1031-1038 DOI:10.1016/j.chemosphere.2006.07.036 |
| [9] | Song H, Carraway E R . Reduction of chlorinated ethanes by nanosized zero-valent iron:kinetics, pathways, and effects of reaction conditions[J]. Environ Sci Technol , 2005, 39 (16) : 6237-6245 DOI:10.1021/es048262e |
| [10] | Zhang X, Lin Y M, Chen Z L . 2, 4, 6-Trinitrotoluene reduction kinetics in aqueous solution using nanoscale zero-valent iron[J]. J Hazard Mater , 2009, 165 (1-3) : 923-927 DOI:10.1016/j.jhazmat.2008.10.075 |
| [11] | Yang G C C, Lee H L . Chemical reduction of nitrate by nanosized iron:kinetics and pathways[J]. Water Res , 2005, 39 (5) : 884-894 DOI:10.1016/j.watres.2004.11.030 |
| [12] | Fan J, Guo Y H, Wang J J . Rapid decolorization of azo dye methyl orange in aqueous solution by nanoscale zero-valent iron particles[J]. J Hazard Mater , 2009, 166 (2-3) : 904-910 DOI:10.1016/j.jhazmat.2008.11.091 |
| [13] | Puls R W, Paulc J, Powell R M . Application of in situ permeable reactive(zero-valent iron) barrier technology for the remediation of chromate-contaminated groundwater:a field test[J]. Appl Geochem , 1999, 14 (8) : 989-1000 DOI:10.1016/S0883-2927(99)00010-4 |
| [14] | Zhang H, Jin Z H, Han L . Synthesis of nanoscale zero-valent iron supported on exfoliated graphite for removal of nitrate[J]. Trans Nonferrous Met Soc China , 2006, 16 (S1) : 345-349 |
| [15] | Hoch L B, Mack E J, Hydutsky B W . Carbothermal synthesis of carbon-supported nanoscale zero-valent iron particles for the remediation of hexavalent chromium[J]. Environ Sci Technol , 2008, 42 (7) : 2600-2605 DOI:10.1021/es702589u |
| [16] | Ponder S M, Darab J G, Mallouk T E . Remediation of Cr(VI) and Pb(Ⅱ) aqueous solutions using supported nanoscalezero-valent iron[J]. Environ Sci Technol , 2000, 34 (12) : 2564-2569 DOI:10.1021/es9911420 |
| [17] | He F, Zhao D Y . Hydrodechlorination of trichloroethene using stabilized Fe-Pd nanoparticles:reaction mechanism and effects of stabilizers, catalysts and reaction conditions[J]. Appl Catal B:Environ , 2008, 84 (3-4) : 533-540 DOI:10.1016/j.apcatb.2008.05.008 |
| [18] | Tian S L, Zhu L Z, Yao S . Characterization of sorption mechanisms of VOCs with organobentonites using a LSER approach[J]. Environ Sci Technol , 2004, 38 (2) : 489-495 DOI:10.1021/es034541a |
| [19] | Belkhadem F, Clacens J M, Bengueddach A . Acidity and catalytic properties for the alkylation of aromatics of PILCs with mixed oxide pillars prepared from two different bentonites[J]. Appl Catal A:Gen , 2006, 298 (10) : 188-193 |
| [20] | Bouras O, Bollinger J C, Baudu M . Adsorption of diuron and its degradation products from aqueous solution by surfactant-modified pillared clays[J]. Appl Clay Sci , 2007, 37 (3-4) : 240-250 DOI:10.1016/j.clay.2007.01.009 |
| [21] | Vazquez A, López M, Kortaberria G . Modification of montmorillonite with cationic surfactants.Thermal and chemical analysis including CEC determination[J]. Appl Clay Sci , 2008, 41 (1-2) : 24-36 DOI:10.1016/j.clay.2007.10.001 |
| [22] | Li X Q, Zhang W X . Sequestration of metal cations with zerovalent iron nanoparticles-a study with high resolution X-ray photoelectron spectroscopy(HR-XPS)[J]. J Phys Chem C , 2007, 111 (19) : 6939-6946 DOI:10.1021/jp0702189 |
| [23] | Li Z H, Jones H K, Zhang P F . Chromate transport through columns packed with surfactant-modied zeolite/zero valent iron pellets[J]. Chemosphere , 2007, 68 (10) : 1861-1866 DOI:10.1016/j.chemosphere.2007.03.011 |
| [24] | Sheng G D, Shao X Y, Li Y M . Enhanced removal of uranium(VI) by nanoscale zerovalent iron supported on Na-bentonite and an investigation of mechanism[J]. J Phys Chem A , 2014, 118 (16) : 2952-2958 DOI:10.1021/jp412404w |
| [25] | Li Y M, Li J F, Zhang Y L . Mechanism insights into enhanced Cr(VI) removal using nanoscale zerovalent iron supported on the pillared bentonite by macroscopic and spectroscopic studies[J]. J Hazard Mater , 2012, 227-228 (15) : 211-218 |




