2. 齐鲁师范学院 化学与化工学院, 山东 济南 250200
2. College of Chemistry and Chemical Engineering, Qilu Normal University, Jinan 250200, China
芳烃抽提过程常用的有机溶剂有环丁砜(SUL)、乙二醇、碳酸丙烯酯、二甲基亚砜、N-甲基吡咯烷酮(NMP)等[1-2],但有机溶剂具有回收能耗高、用量大、不能同时兼顾高选择性和高溶解度,有必要研究更高性能萃取剂[3]。离子液体因具有高选择性、高化学稳定性和高热稳定性而受到广泛的关注[4-5]。但离子液体的低纯度和相对较高的成本限制了它们的应用[3]。深度共晶溶剂弥补了离子液体的不足[6-8],与传统有机溶剂相比,其研究还不够深入,不能广泛应用于芳烃抽提过程。因此,寻找一种兼顾高溶解度和高选择性的混合有机溶剂对于芳烃抽提具有重要意义。
由于萃取剂的种类较多,仅通过实验进行萃取剂的筛选十分困难,选择一种高效快速的筛选方法是必要的。目前,包括使用机器学习阐述的经验相关性,活度系数/过剩吉布斯能(gE)模型,状态方程和计算机模拟多种预测热力学性质的方法已被广泛应用,但大多数方法需要特定化合物信息(例如需要基于实验数据确定方程参数),应用受到限制[9-10]。真实溶剂的类导体筛选模型(COSMO-RS)因不需要任何实验数据,基于量子化学和统计热力学便可获得相关性质而广泛应用于气液平衡(VLE)、液液平衡(LLE)、溶解度、无限稀释活度系数等各种热力学性质的计算中[11-13]。近年来,COSMO-RS方法也成功应用于离子液体、深度共晶溶剂的筛选中[14]。例如,Dong等[15]利用COSMO-RS方法筛选出[EMIM][BF4]分离苯和乙腈共沸混合物;Sun等[16]从45个阳离子和32个阴离子组成的离子液体中筛选出[BMIM]I3为分离苯和环己烷的潜在萃取剂;Wang等[17]采用COSMO-RS模型从210种离子液体中筛选出[EMIM][BF4]用作氯甲烷干燥实验;Wang等[18]在133种深度共熔溶剂中筛选出13种溶解度高的水溶性农药活性成分。因此,基于COSMO-RS方法进行萃取剂筛选是一个不错的选择。
本研究使用苯代替芳烃,正己烷代替非芳烃进行了混合萃取剂筛选以及液液相平衡数据研究。主要包括以下几个部分:第一,利用COSMO-RS模型对工业常用萃取剂进行筛选,筛选出合适的混合萃取剂用于分离苯和正己烷混合物;第二,通过实验对不同比例的混合萃取剂进行探究,并通过Othmer-Tobias及Hand方程检验实验数据的可靠性;第三,通过分配系数、分离因子及分配指数的计算,确定效果最佳的混合萃取剂比例;最后,采用NRTL模型及UNIQUAC模型对LLE实验数据进行关联得到二元交互作用参数,并对模拟数据进行理论验证与分析。
2 实验 2.1 化学试剂实验所用化学试剂如表 1所示,表中w为质量分数。
|
|
表 1 实验化学试剂说明 Table 1 Experimental chemical reagents used in the study |
在101.3 kPa、313.2 K下,采用夹套式液液平衡釜进行实验,用超恒温水浴(Julabo F12-EH)进行温度控制。实验过程中,在平衡釜中加入预制的NMP与环丁砜混合溶液和正己烷溶液,然后逐渐加入芳烃试剂,其中,萃取剂与正己烷的质量比为2:1。将循环冷却水置于平衡釜上,开启磁力搅拌器恒温搅拌30 min。静置至溶液完全分层,分别提取上下层平衡液,用气相色谱分析。取3次进行平行分析后取平均值,以确定两相的组成。
2.3 分析方法样品采用Agilent GC7820A气相色谱分析,色谱柱为DB-5毛细管(30 m×0.2 mm)。柱初始温度为343.15 K,在20 K⋅min−1下加热至503.15 K,保持2 min。检测器温度为523.15 K,汽化室温度为493.15 K。本实验以苯为外标物,采用外标法对样品进行分析,同时计算校正因子。
3 方法与模型 3.1 Othmer-Tobias及Hand方程Othmer-Tobias及Hand方程可检验实验数据的一致性[19],其表达式如式(1)和(2)所示
| $ {\text{l}}{{\text{n}}_{}}\left( {\frac{{{\text{1}} - x_{\text{3}}^L}}{{x_{\text{3}}^L}}} \right){\text{ = }}a{\text{ + }}b{\text{l}}{{\text{n}}_{}}\left( {\frac{{{\text{1}} - x_{\text{1}}^U}}{{x_{\text{1}}^U}}} \right) $ | (1) |
| $ {\text{l}}{{\text{n}}_{}}\frac{{x_{\text{2}}^U}}{{x_{\text{1}}^U}}{\text{ = }}c{\text{ + }}d{\text{l}}{{\text{n}}_{}}\frac{{x_{\text{2}}^L}}{{x_{\text{3}}^L}} $ | (2) |
式中:
利用分配系数D、分离因子S及性能指数PI对萃取剂的溶解度、选择性及整体性能进行评估,相关计算公式如下[20-21]:
| $ D{\text{ = }}\frac{{x_2^L}}{{x_2^U}} $ | (3) |
| $ S{\text{ = }}\frac{{x_2^Lx_1^U}}{{x_2^Ux_1^L}} $ | (4) |
| $ PI{\text{ = }}D \times S $ | (5) |
式中:
COSMO-RS计算是基于COSMO这一理论基础上,通过统计力学和量子化学相结合的方法预测物质的热力学性质及相互作用,已被应用于溶液中各组分的活度系数的计算。利用COSMOtherm软件对体系的无限稀释活度系数计算分为两个部分:首先,选择化合物,BP_TZVP_C30_1601参数化条件下在COSMOtherm数据库中获得化合物的COSMO文件。然后通过软件在101.3 kPa、313.15 K下对体系中苯和正己烷的无限稀释活度系数进行计算。COSMOtherm操作流程如图 1所示。

|
图 1 COSMOtherm计算步骤 Fig.1 Flowchart of COSMOtherm calculation |
LLE实验数据采用NRTL模型及UNIQUAC模型进行关联[22-24]。其中,NRTL模型相关方程如下[25]:
| $ {\text{l}}{{\text{n}}_{}}{\gamma _i}{\text{ = }}\frac{{\sum\limits_j {{\tau _{ji}}} {G_{ji}}{x_j}}}{{\sum\limits_k {{G_{ki}}{x_k}} }} + \sum\limits_j {\frac{{{G_{ij}}{x_j}}}{{\sum\limits_k {{G_{ki}}{x_k}} }}} \left( {{\tau _{ij}} - \frac{{\sum\limits_l {{\tau _{lj}}} {G_{lj}}{x_l}}}{{\sum\limits_k {{G_{kj}}{x_k}} }}} \right) $ | (6) |
| $ {\tau _{ij}}{\text{ = }}{a_{ij}} + \frac{{{b_{ij}}}}{T}{;_{}}{G_{ij}} = exp\left( { - {a_{ij}}{\tau _{ij}}} \right) $ | (7) |
式中:xj、
UNIQUAC模型相关方程如下[26]:
| $ {\text{l}}{{\text{n}}_{}}\gamma {\text{ = l}}{{\text{n}}_{}}\gamma _i^C + {\text{l}}{{\text{n}}_{}}\gamma _i^R $ | (8) |
| $ {\text{l}}{{\text{n}}_{}}\gamma _i^C{\text{ = l}}{{\text{n}}_{}}\frac{{{\varphi _i}}}{{{x_i}}} + \left( {\frac{Z}{{\text{2}}}} \right){q_i}{\text{l}}{{\text{n}}_{}}\frac{{{\theta _i}}}{{{\varphi _i}}} + {l_i} - \frac{{{\varphi _i}}}{{{x_i}}}\sum\limits_{j = 1}^n {{x_j}{l_j}} $ | (9) |
| $ {\text{l}}{{\text{n}}_{}}\gamma _i^{\text{R}}{\text{ = }}{q_i}\left( {{\text{1}} - {\text{l}}{{\text{n}}_{}}\sum\limits_{j{\text{ = 1}}}^n {{\theta _{_j}}} {\tau _{ji}} - \sum\limits_{j{\text{ = 1}}}^n {\frac{{{\theta _{_j}}{\tau _{ij}}}}{{\sum\limits_{k{\text{ = 1}}}^n {{\theta _{_k}}} {\tau _{_{kj}}}}}} } \right) $ | (10) |
| $ {\tau _{ij}}{\text{ = }}ex{p_{}}\left( {{A_{ij}} + \frac{{{B_{ij}}}}{T}} \right) $ | (11) |
式中:
为反映实验数据与预测数据的差异,采用均方根偏差(RMSD)值评价回归数据的质量,其方程如下[27]:
| $ {\text{RMSD = }}{\left\{ {\frac{{\sum\limits_i {\sum\limits_e {\sum\limits_f {{{\left( {x_{ief}^{\exp } - x_{ief}^\text{cal}} \right)}^2}} } } }}{{6n}}} \right\}^{{\text{1/2}}}} $ | (12) |
式中:
用COSMOtherm软件中的活度系数模块进行了萃取剂的筛选,模拟计算了在101.3 kPa、313.15 K下,苯和正己烷在萃取剂中的无限稀释活度系数。并利用无限稀释的活度系数对萃取剂的最大容量
| $ {C^\infty }{\text{ = }}\frac{1}{{\gamma _2^\infty }} $ | (13) |
| $ {S^\infty }{\text{ = }}\frac{{\gamma _1^\infty }}{{\gamma _2^\infty }} $ | (14) |
| $ P{I^\infty }{\text{ = }}{C^\infty } \times {S^\infty } $ | (15) |
式中:
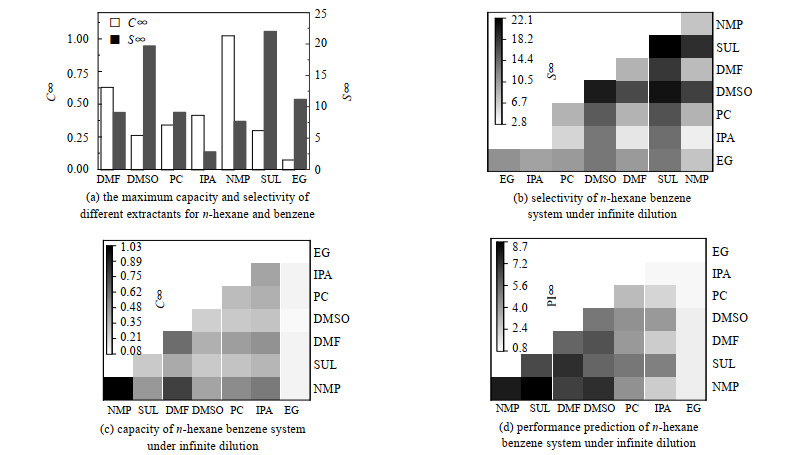
COSMOtherm软件模拟计算结果如图 2所示。由图 2(a)可知,几种萃取剂的最大容量大小顺序为:N-甲基吡咯烷酮(NMP) > N, N-二甲基甲酰胺(DMF) > 2-丙醇(IPA) > 碳酸丙烯酯(PC) > 环丁砜(SUL) > 二甲基亚砜(DMSO) > 乙二醇(EG);最大选择性大小的顺序为:SUL > DMSO > EG > PC > DMF > NMP > IPA;溶解度最好的为NMP,选择性最好的为SUL。将以上7种萃取剂分别以质量比1:1混合,计算得到混合萃取剂的最大容量及最大选择性及溶解度与选择性的乘积
|
图 2 313.15 K,101.3 kPa下单一萃取剂及混合萃取剂的模拟结果 Fig.2 Simulation results of single extractant and mixed extractant at 313.15 K and 101.3 kPa |
表 2、3分别为101.3 kPa、313.15 K下测得的正己烷+ 苯+ 环丁砜三元体系、正己烷+苯+NMP+环丁砜四元体系的液液平衡数据,表 3中mNMP: mSUL为NMP和SUL的质量比。图 3为相关体系相图。这里根据式(16)计算标准不确定度。
| $ u = \frac{1}{{n(n - 1)}}\sum\nolimits_{i = 0}^n {({x_i}} - {\bar x_i}{)^2} $ | (16) |
|
|
表 2 正己烷(1) +苯(2) +环丁砜(3) 在313.15 K, 101.3 kPa下的LLE实验数据(摩尔分数)、分配系数D、分离因子S和性能指数PI a Table 2 Experimental LLE data (mole fraction), distribution coefficient D, separation factor S and performance index PI of n-hexane (1) + benzene (2) + sulfolane (3) at 313.15 K under 101.3 kPaa |
|
|
表 3 正己烷 (1) + 苯(2) + NMP (3) + 环丁砜 (4) 在313.15 K,101.3 kPa下的LLE实验数据(摩尔分数)、分配系数D、分离因子S和性能指数PI b Table 3 Experimental LLE data (mole fraction), distribution coefficient D, separation factor S and performance index PI of n-hexane (1) + benzene (2) + NMP (3) + sulfolane (4) at 313.15 K under 101.3 kPa |

|
图 3 芳烃萃取体系实验值与NRTL和UNIQUAC模型计算值的对比 Fig.3 Comparison of experimental values with calculated values using NRTL and UNIQUAC models |
式中:
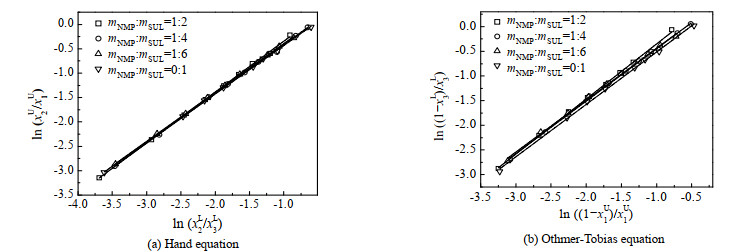
Othmer-Tobias方程和Hand方程的常数及关联系数如图 4及表 4所示,4组数据的R2分别为0.999 7,0.999 7,0.999 4,0.999 8。接近于1,说明实验数据具有较高的可靠性。
|
图 4 研究体系的Hand和Othmer-Tobias方程 Fig.4 Hand and Othmer-Tobias equations of the ternary system |
|
|
表 4 研究体系的Othmer-Tobias和Hand方程的常数及相关系数 Table 4 Constants and correlation coefficients of Othmer-Tobias and Hand equations of the system |
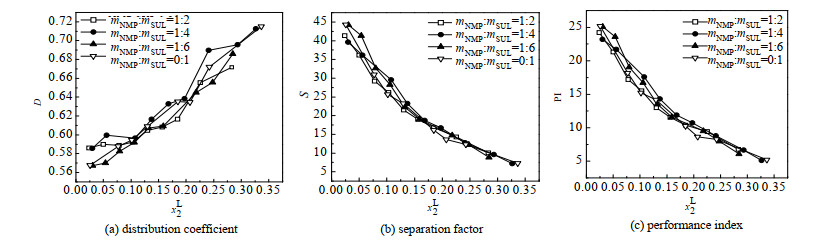
如图 5所示,随着萃取相中苯摩尔分数的增大,分配系数整体呈增大的趋势,说明高浓度的苯有利于苯在萃取剂中的溶解。分配系数小于1,说明单级萃取工艺只萃取出少量苯,在工业中一般要采取多级萃取。当萃取剂中mNMP: mSUL为1:4时,分配系数最大,溶解度最好。
|
图 5 313.15 K和101.3 kPa下不同配比萃取剂的分配系数、分离因子和性能指数 Fig.5 Distribution coefficient, separation factor and performance index of the extractants mixed in different proportions |
随着萃取相中苯摩尔分数的增大分离因子呈减小的趋势。分离因子远超于1说明萃取剂对芳烃和非芳烃有良好的分离能力。苯的分离因子随萃取相中苯摩尔分数的增加而降低,表明萃取相中苯摩尔分数越高,萃取剂的选择性越差。萃取相中苯摩尔分数小于0.07时,萃取剂中mNMP: mSUL为1:6时分配系数大于其他比例;萃取相中苯摩尔分数大于0.075时,萃取剂中mNMP: mSUL为1:4时性能指数整体大于其他比例。因此,mNMP: mSUL为1:6和1:4时选择性相对较好。
由性能指数可看出:萃取相中苯摩尔分数小于0.07时,萃取剂中NMP:环丁砜为1:6时性能指数整体大于其他比例;萃取相中苯摩尔分数大于0.075时,萃取剂中mNMP: mSUL为1:4时性能指数整体大于其他比例。由于mNMP: mSUL为1:4时溶解度较好,因此,此比例为最佳比例。
4.5 液液平衡数据的相关性表 5为101.3 kPa、313.15 K下的正己烷+ 苯+ 环丁砜三元体系、正己烷+ 苯+ NMP + 环丁砜四元体系的二元交互作用参数和RMSD值。实验结果与计算结果的RMSD值不超过0.010 8,表明NRTL及UNIQUAC模型可成功地将正己烷+ 苯+ 萃取剂的实验LLE数据关联起来,且二元交互作用参数可用于萃取过程模拟。图 2为相应的三元相图,将实验数据与NRTL及UNIQUAC模型模拟结果进行比较,结果表明NRTL及UNIQUAC模型计算结果与实验LLE数据吻合较好。
|
|
表 5 体系的NRTL和UNIQUAC的二元交互作用参数及均方偏差 Table 5 NRTL and UNIQUAC binary interaction parameters and root mean square deviation |
本研究通过COSMO-RS模型筛选出高溶解度的NMP及高选择性的环丁砜。以不同质量比的NMP和环丁砜为混合萃取剂,对正己烷+ 苯+ 萃取剂体系进行液液平衡研究,得到结论如下:
(1) 在313.15 K、101.3 kPa下,以不同比例的NMP和环丁砜作为混合萃取剂,用气相色谱仪测定了正己烷+苯+萃取剂的LLE数据。利用Othmer-Tobias及Hand方程对LLE实验数据进行了验证,R2接近于1,说明所得数据有较好的一致性和可靠性。
(2) 通过对分配系数、分离因子及分配指数计算表明,mNMP: mSUL为1:4的萃取剂对苯和正己烷体系具有良好的分离性能。
(3) 通过NRTL模型及UNIQUAC模型对实验LLE数据进行关联,回归了二元交互作用参数,RMSD小于0.010 8,模拟数据与实验数据的吻合程度较高,为工业上以NMP和环丁砜为混合溶剂分离芳烃和非芳烃提供了数据支持。
| [1] |
LI H, GUO J J, ZHANG Y H, et al. Influence of solvent structure on the extraction of aromatics from FCC diesel and computational thermodynamics study[J]. Fuel Processing Technology, 2021, 224: 107021. DOI:10.1016/j.fuproc.2021.107021 |
| [2] |
ZHANG Y Q, ZHANG Q Q, XIN H, et al. COSMO-RS prediction, liquid-liquid equilibrium experiment and quantum chemistry calculation for the separation of n-butanol and n-heptane system using ionic liquids[J]. The Journal of Chemical Thermodynamics, 2022, 167: 106719. DOI:10.1016/j.jct.2021.106719 |
| [3] |
MA S T, SHANG X Y, LI J F, et al. Liquid–liquid extraction of benzene using low transition temperature mixtures: COSMO-SAC predictions and experiments[J]. Journal of Chemical & Engineering Data, 2018, 63(12): 4749-4760. |
| [4] |
LIU Q, ZHANG X L. Highly efficient separation of phenolic compounds from low-temperature coal tar by composite extractants with low viscosity[J]. Journal of Molecular Liquids, 2022, 360: 119417. DOI:10.1016/j.molliq.2022.119417 |
| [5] |
YU K, DING W L, LU Y M, et al. Ionic liquids screening for lignin dissolution: COSMO-RS simulations and experimental characterization[J]. Journal of Molecular Liquids, 2022, 348: 118007. DOI:10.1016/j.molliq.2021.118007 |
| [6] |
NEMATI M, TUZEN M, ALTUNAY N, et al. Development of sodium hydroxide-induced homogenous liquid-liquid extraction-effervescent assisted dispersive liquid-liquid microextraction based on deep eutectic solvents; Application in the extraction of phytosterols from cow cream samples[J]. Journal of Food Composition and Analysis, 2022, 106: 104291. DOI:10.1016/j.jfca.2021.104291 |
| [7] |
REZAEE M, FEYZI F, DEHGHANI M R. Extractive desulfurization of dibenzothiophene from normal octane using deep eutectic solvents as extracting agent[J]. Journal of Molecular Liquids, 2021, 333: 115991. DOI:10.1016/j.molliq.2021.115991 |
| [8] |
FARIAS F O, PASSOS H, SANGLARD M G, et al. Designer solvent ability of alcohols in aqueous biphasic systems composed of deep eutectic solvents and potassium phosphate[J]. Separation and Purification Technology, 2018, 200: 84-93. DOI:10.1016/j.seppur.2018.02.029 |
| [9] |
PADUSZYŃSKI K, KRÓLIKOWSKA M. Extensive evaluation of performance of the COSMO-RS approach in capturing liquid–liquid equilibria of binary mixtures of ionic liquids with molecular compounds[J]. Industrial & Engineering Chemistry Research, 2020, 59(25): 11851-11863. |
| [10] |
HOSSEINI S M, MULERO A, ALAVIANMEHR M M. Predictive methods and semi-classical equations of state for pure ionic liquids: A review[J]. The Journal of Chemical Thermodynamics, 2019, 130: 47-94. DOI:10.1016/j.jct.2018.09.022 |
| [11] |
WEI X J, CHEN X P, WANG L L, et al. Measurement and correlation of isothermal vapor–liquid equilibrium data for (−)-α-pinene + (−)-β-pinene + water + phenoxyacetic acid[J]. Industrial & Engineering Chemistry Research, 2023, 62(9): 4122-4134. |
| [12] |
JIANG C H, CHENG H Y, QIN Z X, et al. COSMO-RS prediction and experimental verification of 1, 5-pentanediamine extraction from aqueous solution by ionic liquids[J]. Green Energy & Environment, 2021, 6(3): 422-431. |
| [13] |
ECKERT F, KLAMT A. Prediction of halocarbon thermodynamics with COSMO-RS[J]. Fluid Phase Equilibria, 2003, 210(1): 117-141. DOI:10.1016/S0378-3812(03)00166-3 |
| [14] |
SONG Z, ZHOU T, QI Z W, et al. Systematic method for screening ionic liquids as extraction solvents exemplified by an extractive desulfurization process[J]. ACS Sustainable Chemistry & Engineering, 2017, 5(4): 3382-3389. |
| [15] |
DONG Y C, YANG Q C, LI Z W, et al. Extractive distillation of the benzene and acetonitrile mixture using an ionic liquid as the entrainer[J]. Green Energy & Environment, 2021, 6(3): 444-451. |
| [16] |
SUN D Z, FENG H S, XIN F, et al. Evaluation of COSMO-RS model for the LLE prediction of benzene plus cyclohexane plus ionic liquid system[J]. The Journal of Chemical Thermodynamics, 2020, 145: 106032. |
| [17] |
WANG Z H, LIU S L, JIANG Y F, et al. Methyl chloride dehydration with ionic liquid based on COSMO-RS model[J]. Green Energy & Environment, 2021, 6(3): 413-421. |
| [18] |
WANG J, GUO Y Y, LIU F M, et al. COSMO-RS prediction and experimental verification of deep eutectic solvents for water insoluble pesticides with high solubility[J]. Journal of Molecular Liquids, 2022, 349: 118139. |
| [19] |
WANG Y C, ZHOU S M, TANG J H, et al. Measurement and correlation of phase equilibrium data of the mixtures consisting of water, resorcinol, mesityl oxide at different temperatures[J]. Chinese Journal of Chemical Engineering, 2018, 26(12): 2573-2580. |
| [20] |
EL BLIDI L, HADJ-KALI M K, AL-ANAZI A M, et al. Liquid-liquid separation of n-hexane/1-hexene and cyclohexane/ cyclohexene using deep eutectic solvents[J]. Journal of Molecular Liquids, 2021, 344: 117776. |
| [21] |
SANTHI V M, RAMALINGAM A, SREEKALA D J, et al. Ammonium based deep eutectic solvents (DESs) on extraction of benzothiophene from iso-octane: Experiment and COSMO-RS model[J]. Journal of Dispersion Science and Technology, 2022, 43(12): 1778-1788. |
| [22] |
HAGHTALAB A, PARAJ A. Computation of liquid–liquid equilibrium of organic-ionic liquid systems using NRTL, UNIQUAC and NRTL-NRF models[J]. Journal of Molecular Liquids, 2012, 171: 43-49. |
| [23] |
ZHANG Y, PAN Y Q, ZHANG T, et al. A comprehensive method of ionic liquid screening and experimental verification for simultaneous separation of multiple sulfides from oil[J]. Separation and Purification Technology, 2023, 315: 123714. |
| [24] |
ZHANG Y H, WANG H, SUN D X, et al. Separation of olefins from FCC naphtha by propylene carbonate: Influence of critical component structure and correlation of ternary LLE thermodynamic models[J]. Fuel Processing Technology, 2020, 197: 106198. |
| [25] |
SUN L Y, LUO F, LIU R, et al. Isobaric liquid–liquid equilibrium measurements and thermodynamics modeling for systems: Benzene + cyclohexane + DESs at 303.15 and 323.15 K[J]. Journal of Chemical & Engineering Data, 2019, 64(3): 1113-1121. |
| [26] |
WANNACHOD T, HRONEC M, SOTÁK T, et al. Effects of salt on the LLE and tie-line data for furfuryl alcohol – n-butanol–water at T = 298.15 K[J]. Journal of Molecular Liquids, 2016, 218: 50-58. |
| [27] |
HADJ-KALI M K, MULYONO S, HIZADDIN H F, et al. Removal of thiophene from mixtures with n-heptane by selective extraction using deep eutectic solvents[J]. Industrial & Engineering Chemistry Research, 2016, 55(30): 8415-8423. |
| [28] |
GUI C M, LI Z W, LEI Z G, et al. Combinatorial screening of ionic liquid extractant for removal of methanol from methylal[J]. Chemical Engineering Science, 2022, 249: 117317. |




