氢燃料电池是氢能源的重要应用方式。然而氢气中含有的杂质气体H2S、CO等会使质子交换膜燃料电池中的铂电极中毒,极大地影响了铂电极的活性及使用寿命。需要将燃料氢气中CO体积分数降低到2×10−6以下[1],因此研究富氢气体中CO的深度脱除具有重要意义。
现有的氢能源的获取方法仍以化石燃料为主,其中甲烷水蒸气重整制氢是成本最低的制氢技术,占世界制氢总量的70% 左右,其产气组成(体积分数)通常为75% H2、1% CO以及20% CO2及CH4等。将CO与氢气进行甲烷化反应脱除CO是一种常用的脱除CO的方法[2]。
钌基催化剂被认为是催化CO甲烷化反应的最佳催化剂,在多种载体上均能够将CO体积分数由1% 降低至10−5甚至更低[3-6],因为钌金属具有较强的CO和H2的吸附解离能力[7],从而对CO甲烷化反应具有较高的转化率。相较于贵金属钌的高昂价格,镍基催化剂则具有较好的性价比,但Ni/ TiO2[8],Ni/ SiO2[9],Ni/ CeO2等[10]催化剂深度脱除CO的能力仍有不足。最新研究发现,Ni基催化剂采用ZrO2载体具有较好的深度脱除CO能力。Gao等[11]通过浸渍法制备了Ni(Cl0.1)/ ZrO2催化剂,可以将CO体积分数由1% 降低至3×10−5。Xiao等[12]通过浸渍法制备了Ni/ZrO2催化剂,可以将CO体积分数由1% 降低至10−5左右。Wang等[9]研究了2种载体的Ni/SiO2催化剂与Ni/SiO2-ZrO2催化剂的差别,认为ZrO2载体上的酸性位点有利于CO的吸附。da Silva等[13]的研究也认为ZrO2载体上CO的吸附是Ni/ ZrO2催化剂具有较高CO甲烷化转化率的关键。尽管目前研究报道采用ZrO2为载体可以增强CO的吸附,但Ni/ZrO2催化剂仍无法将富氢气体中的CO体积分数脱除至2×10−6以下。
本研究采用尿素水解法制备纳米二氧化锆作为催化剂载体,制备不同Ni负载量的纳米Ni/ZrO2催化剂。以反应吸附强化甲烷水蒸气重整制氢(reactive sorption enhanced reforming,ReSER)工艺产气(组成气体积分数为:95% H2,3% CO,2% CO2)为富氢气体原料,在固定床反应器上评价确定纳米Ni/ ZrO2催化剂的最佳工作条件和深度脱除CO的效果和催化剂的寿命,并分析纳米ZrO2载体对CO吸附性能以及对甲烷化反应性能的影响。同时制备了Ni/ Al2O3催化剂,以探究ZrO2载体的作用;制备了微米ZrO2载体负载的Ni催化剂,以探究ZrO2载体尺寸对于催化剂活性的影响。
2 实验部分 2.1 实验试剂硝酸锆五水合物(Zr(NO3)4·5H2O,分析纯,上海麦克林生化科技有限公司);硝酸镍六水合物(Ni(NO3)2·6H2O,分析纯,阿拉丁化学试剂有限公司);尿素(CO(NH2)2,分析纯,国药集团化学试剂有限公司);聚乙二醇(HO(CH2CH2O)nH,相对分子质量Mn=20 000,阿拉丁化学试剂有限公司);无水乙醇(C2H5OH,分析纯,上海沃凯生物技术有限公司);氧化铝(Al2O3,分析纯,北京伊诺凯科技有限公司);氢氧化钠(NaOH,分析纯,阿拉丁化学试剂有限公司)。
2.2 催化剂制备 2.2.1 纳米ZrO2载体的制备方法本研究采用尿素水解法制备纳米ZrO2载体。将五水硝酸锆溶于适量去离子水中,75 ℃下加热搅拌溶解。将上述溶液置于200 mL带有聚四氟乙烯内衬的反应釜中,加入适量尿素和聚乙二醇,在120 ℃下反应2~6 h。产物经抽滤置于110 ℃烘箱中烘干。将烘干后的样品研磨呈粉末态,置于450 ℃的马弗炉中,空气气氛下煅烧2~4 h,即可得到纳米ZrO2粉末。
2.2.2 纳米Ni/ ZrO2催化剂制备方法纳米Ni/ ZrO2催化剂的制备采用尿素水解法。将适量六水硝酸镍配制成溶液,加入纳米ZrO2置于三口烧瓶中,加入适量尿素。加热至90 ℃,使尿素充分水解2~6 h,镍离子完全沉淀于二氧化锆表面。产物经洗涤过滤,置于110 ℃烘箱中烘干。固体在马弗炉中450 ℃下煅烧2 h。分别制备得到NiO负载质量分数为10%、20%、30% 和40% 的纳米NiO/ ZrO2 4种催化剂。
2.2.3 微米ZrO2的制备方法本研究采用直接沉淀法制备微米ZrO2载体。将适量Zr(NO3)4·5H2O和NaOH分别溶解于适量去离子水中。在40 ℃搅拌条件下,向硝酸锆溶液中逐滴加入氢氧化钠溶液,在40 ℃下反应0.5~1 h。产物置于110 ℃烘箱中烘干。将烘干后的样品研磨呈粉末态,置于450 ℃的马弗炉中,空气气氛下煅烧2~4 h,即可得到微米ZrO2粉末。
2.2.4 微米NiO/ZrO2催化剂制备方法本研究使用微米NiO-ZrO2催化剂作为对照实验。载体采用2.2.3节中的微米ZrO2催化剂,以2.2.2节中的方法制备了质量分数为30% 的微米NiO/ZrO2催化剂。
2.2.5 NiO/ Al2O3催化剂的制备本研究使用NiO/ Al2O3催化剂为对照实验。载体采用商业品Al2O3,NiO/Al2O3催化剂的制备方法以及NiO负载量与2.2.2节方法相同。
2.3 催化剂活性评价方法采用固定床反应器评价自制的纳米NiO / ZrO2催化剂的CO甲烷化反应性能。固定床反应器为Φ15 mm×500 mm不锈钢管,加热套温度由程序升温控制仪控制。原料气组成为3% CO、2% CO2和95% H2,由上海伟创标准气体有限公司提供。在开始反应前,NiO/ ZrO2催化剂先在氢气气氛中450 ℃还原1~2 h。纳米Ni/ ZrO2催化剂的催化性能评价条件:反应温度为200~450 ℃、体积空速WHSV为1 000~3 500 h−1,常压范围内。原料气流量由质量流量计控制,反应后气体进入气相色谱仪在线分析气体组成。气相色谱仪由杭州捷岛GC1690提供,CO转化率x计算如式(1):
| $ x{\text{ = }}\frac{{\varphi {{{\text{(CO)}}}_{{\text{in}}}}{\text{ }} - \varphi {{{\text{(CO)}}}_{{\text{out}}}}{\text{ }}}}{{\varphi {{{\text{(CO)}}}_{{\text{in}}}}{\text{ }}}} \times {{100\% }} $ | (1) |
采用以上固定床反应器系统进行纳米NiO/ZrO2催化剂的寿命评价实验。催化剂选用NiO质量分数为30% 的纳米NiO/ZrO2催化剂,在反应温度为350 ℃、体积空速为1 000 h−1,常压条件下对催化剂进行连续100 h的催化活性评价。反应过程中每隔1 h进行一次在线取样检测出口气体CO体积分数,并计算CO的转化率。
2.5 催化剂表征方法采用BELSORP-mini Ⅱ测试仪进行载体及催化剂的比表面积、孔容和平均孔径的表征;采用日本D/MAX-RA X射线衍射仪测定载体及催化剂的物相组成,并使用谢勒公式计算其晶粒尺寸数据;采用AutoChem1 Ⅱ 2920程序升温化学吸附仪器进行氢气程序升温还原(hydrogen temperature programmed reduction,H2-TPR)测试,得到催化剂的还原温度曲线;在Bel Cata Ⅱ程序升温化学吸附仪器上进行了CO程序升温脱附(CO temperature programmed desorption,CO-TPD)测试,得到载体和催化剂对CO的吸附能力数据。
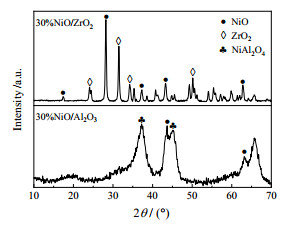
3 结果与讨论 3.1 催化剂表征结果为了分析纳米NiO/ZrO2催化剂和NiO/Al2O3催化剂的物相差别,对30% 纳米NiO/ZrO2和30% NiO/Al2O3催化剂进行了XRD图谱分析,如图 1所示。
|
图 1 纳米NiO/ ZrO2和NiO/ Al2O3的XRD图谱 Fig.1 XRD patterns of NiO/ Al2O3 and nano NiO/ ZrO2 |
由图 1可知,在30% NiO/Al2O3中,NiO元素除了以NiO的形式存在,还与Al元素形成较为稳定的NiAl2O4尖晶石结构。较为稳定的NiAl2O4在之后的CO甲烷化反应中不易被还原,无法为反应提供活性位点。而在纳米NiO/ZrO2中,NiO元素全部以NiO的形式存在,Zr元素则以纳米ZrO2的形式存在。NiO与纳米ZrO2之间没有形成新的晶相结构,以NiO的形式存在的Ni元素,可以被充分还原为低价态的Ni,可以为CO甲烷化反应提供更多的反应位点,更有利于反应进行。
根据谢勒公式对XRD图中的晶粒尺寸进行计算,30% NiO/Al2O3催化剂中NiO晶粒的大小约为14 nm,而在中30% 纳米NiO/ZrO2催化剂中NiO晶粒大小约为22 nm,ZrO2尺寸在25 nm左右。30% NiO/Al2O3催化剂中NiO晶粒更小,这是因为Al2O3具有更大的比表面积,以及NiO和Al2O3之间更强的金属载体相互作用有利于NiO的分散所致。
如图 2所示为纳米ZrO2载体,30% 纳米NiO/ZrO2,30% 微米NiO/ZrO2以及30% NiO/Al2O3催化剂的扫描电镜图片。

|
图 2 催化剂及载体的扫描电镜图像 Fig.2 SEM image of support and catalysts |
由图 2(a)可知,通过尿素水解法合成的ZrO2颗粒呈较为均匀的球形,ZrO2颗粒的粒径在30 nm左右,与谢勒公式计算数据相吻合。图 2(b)为通过尿素水解法制备的30% 纳米NiO/ZrO2催化剂。NiO负载在纳米ZrO2颗粒上,催化剂形貌转变为不规则状态,但整体仍呈球状,催化剂颗粒的粒径仍在30 nm左右。图 2(c)所示为30% 微米NiO/ZrO2催化剂,催化剂尺寸在1 μm左右。由于直接沉淀法制备过程中,溶液中氢氧根离子浓度不易控制,导致催化剂呈不规则的块状结构。图 2(d)为30% NiO/Al2O3催化剂,Al2O3呈丰富的孔道结构,氧化镍颗粒负载在Al2O3表面。Al2O3载体为微米级,NiO/Al2O3催化剂尺寸在5 μm左右。
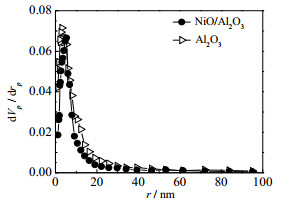
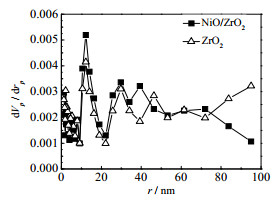
对催化剂及载体在真空液氮条件下进行吸脱附氮气测试,获得载体及催化剂的比表面积、孔容和孔径数据,如表 1所示。Al2O3载体及30% NiO/Al2O3催化剂比表面积分别为290.07和182.29 m2·g−1。ZrO2载体及30% NiO/ZrO2催化剂的比表面积较小。Al2O3载体及30NiO/Al2O3催化剂的孔径分布如图 3所示,图 4为纳米ZrO2载体及30% 纳米NiO/ZrO2催化剂的孔径分布图。30% NiO/Al2O3催化剂的孔容较大,孔径在5 nm左右,这是因为微米Al2O3具有发达的孔隙结构,其丰富的孔隙结构更有利于活性组分的分散,有利于CO甲烷化反应的进行。而纳米ZrO2载体及30% 纳米NiO/ZrO2催化剂的孔容较小,孔径分布均匀,可能是颗粒间的堆积间隙。微米ZrO2载体及30% 微米NiO/ZrO2催化剂的孔容孔径数据与纳米ZrO2载体及纳米NiO/ZrO2催化剂相似,而30%纳米NiO/ZrO2催化剂催化效果优于30% 微米NiO/ZrO2催化剂,表明纳米ZrO2载体对催化剂的催化效果具有关键作用。ZrO2载体负载催化剂的比表面积及孔容孔径数据均不如Al2O3负载催化剂,但NiO/ZrO2催化剂的催化效果远优于30% NiO/Al2O3催化剂,表明载体的种类为影响催化效果的重要因素,而比表面积并不是导致催化剂活性差异的关键。
|
|
表 1 载体及催化剂的比表面积、孔容、孔径数据表 Table 1 Specific surface area, pore volume and pore size of supports and catalysts |
|
图 3 Al2O3及NiO/Al2O3的BJH孔径分布图 Fig.3 Pore size distribution of Al2O3 and NiO/Al2O3 |
|
图 4 ZrO2及NiO/ZrO2的BJH孔径分布图 Fig.4 Pore size distribution of ZrO2 and NiO/ZrO2 |
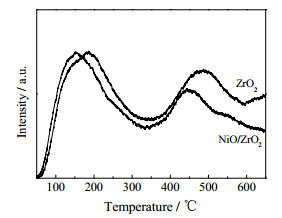
为了探究ZrO2对CO的吸附作用,本研究对纳米NiO/ZrO2催化剂、纳米ZrO2载体进行了CO-TPD实验。进行CO-TPD测试前,先在400 ℃、10% H2/He中将催化剂活化。吸附强度随温度变化如图 5所示。
|
图 5 纳米ZrO2及纳米NiO/ZrO2的CO程序升温吸附图 Fig.5 CO-TPD images of nano ZrO2 and nano NiO/ZrO2 |
其中纳米ZrO2载体在100~300 ℃和400~500 ℃各有一个吸收峰,吸附强度分别在186.2和487.1 ℃达到顶峰。这可能与CO在ZrO2上的吸附位点的不同有关。186.2 ℃的峰对应CO在ZrO2上的锆桥位的吸附,高温487.1 ℃对应CO在ZrO2上稳定的锆顶位的吸附。相对应的NiO/ZrO2催化剂上CO的吸附强度与ZrO2载体类似,也有2个吸收峰,分别在152.4和443.2 ℃达到顶峰。纳米NiO/ZrO2催化剂的CO吸附曲线相较于ZrO2载体整体向低温区域偏移,这是由于负载镍对CO吸附作用的影响。
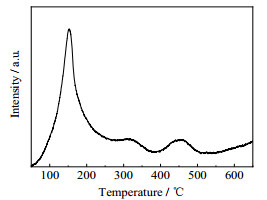
研究对单独的还原态金属Ni也进行了CO-TPD实验,其吸附强度曲线如图 6所示。金属Ni对CO的吸附曲线也显现出两个吸收峰,分别在152.4和460.3 ℃达到顶峰。其中金属Ni对CO的吸附主要集中于100~200 ℃的低温区,而在大于300 ℃的高温区间内对CO的吸附较弱。纳米Ni/ ZrO2催化剂与纳米ZrO2载体的CO吸附曲线相似,表明在纳米NiO/ZrO2催化剂上吸附的CO主要吸附于纳米ZrO2载体上。研究认为,纳米ZrO2载体上CO的吸附可能是纳米NiO/ZrO2催化剂脱CO性能优越的原因。
|
图 6 Ni的CO程序升温吸附图 Fig.6 CO-TPD image of Ni |
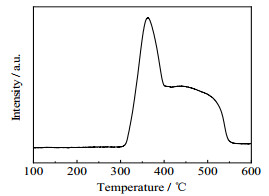
30% 纳米NiO/ZrO2的H2-TPR表征如图 7所示。30% 纳米NiO/ZrO2的氢气还原图像上只在363 ℃有一个还原峰,在300~550 ℃均有氢气损耗。其中300~400 ℃的还原峰可以归因于小颗粒的松散的NiO组分的还原,400~550 ℃的氢损耗峰是由附着在ZrO2表面的、与ZrO2载体间存在一定相互作用的NiO组分的还原造成的。此外纳米NiO/ZrO2催化剂在高温区域(> 550 ℃)没有氢损耗,表明尿素水解法制备的催化剂上,NiO与ZrO2载体之间的相互作用较弱。
|
图 7 30% nano NiO/ZrO2的H2-TPR图 Fig.7 H2-TPR of 30% nano NiO/ZrO2 |
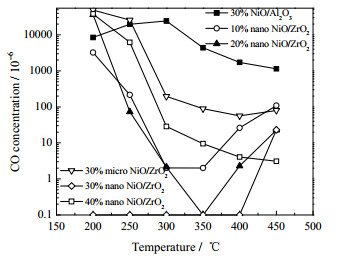
以NiO/Al2O3催化剂为参照,对不同氧化镍负载量的纳米NiO/ZrO2催化剂在固定床上进行CO甲烷化反应,其深度脱除CO的能力如图 8所示。
|
图 8 不同催化剂脱除CO结果图 Fig.8 CO removal results with different catalysts (reaction temperature: 200-450 ℃; space velocity: 1 000 h−1; gas composition: 3% CO, 2% CO2, 95% H2) |
由图 8可以看出,纳米NiO/ZrO2催化剂大多具有优秀的脱CO性能,随着负载量的不同,其深度脱除CO的效果有所不同。但纳米NiO/ZrO2催化剂脱除CO能力并未随着氧化镍负载量的增大而增大,其脱除CO的次序为30% 纳米NiO/ZrO2 > 20% 纳米NiO/ZrO2 > 10% 纳米NiO/ZrO2 > 40% 纳米NiO/ZrO2。结果表明,10% 纳米NiO/ZrO2与20% 纳米NiO/ZrO2催化剂的催化活性随温度的变化具有相似的曲线,因为NiO负载量低,催化活性不足;随温度的升高其催化活性先升高后下降,在350 ℃时达到最佳。而40% 纳米NiO/ZrO2催化剂随温度的升高其催化活性升高,可能是NiO负载量过大,导致ZrO2暴露不充分、催化活性不足。因而优选的是30% 纳米NiO/ZrO2催化剂,可以在200~400 ℃内将CO体积分数由3% 降低至10−7。30% 微米NiO/ZrO2催化剂则可以在400~450 ℃将CO体积分数脱除至10−10,与30% 纳米NiO/ZrO2催化剂存在较大差距。而NiO/Al2O3催化剂深度脱除CO的能力较差,仅可将CO的体积分数降低至0.1% 左右,而且最佳反应温度区间在大于400 ℃的高温区。
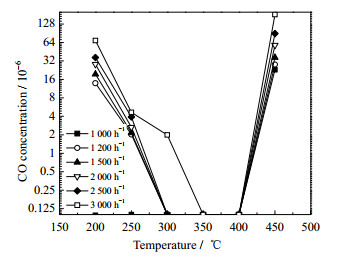
图 9为优选的30% 纳米NiO/ZrO2催化剂在不同空速下,脱除CO能力随温度的变化图。在空速为1 000 h−1时,30% 纳米NiO/ZrO2催化剂可以在200~400 ℃的宽温度范围内深度脱除CO至2×10−6以下。当空速升至3 000 h−1时,30% 纳米NiO/ZrO2催化剂仍然可以在350~400 ℃内将CO体积分数由3% 降至10−7。
|
图 9 30% nano-NiO/ZrO2不同空速、温度下脱CO结果图 Fig.9 CO removal results of 30% nano NiO/ZrO2 at different temperatures and different space velocities (reaction temperature: 200-450 ℃; space velocity: 1 000-3 000 h−1; gas composition: 3% CO, 2% CO2, 95% H2) |
30% 纳米NiO/ ZrO2催化剂脱除CO的稳定性随时间变化如图 10所示。
|
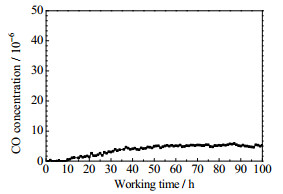
图 10 30% nano NiO/ZrO2脱除CO的稳定性变化图 Fig.10 Stability of 30% nano NiO/ZrO2 in CO removal (reaction temperature: 350 ℃; space velocity: 1 000 h−1; gas composition: 3% CO, 2% CO2, 95% H2) |
在温度为350 ℃,体积空速为1 000 h−1常压条件下,100 h内30% 纳米NiO/ZrO2催化剂脱除CO能力稍有下降。在20 h的工作时间内,纳米NiO/ZrO2催化剂仍可以将CO的体积分数脱除至2×10−6以下,符合质子膜燃料电池对氢气CO含量的需求。随着时间的推移,其催化CO甲烷化反应能力逐渐下降,最终稳定在5×10−6,仍具有较优良的脱除CO能力。
图 11为工作100 h后的30% 纳米NiO/ZrO2扫描电镜图。由图 11可知,在连续工作100 h后,催化剂的形貌并未发生明显变化,未观察到明显的烧结现象,进一步表明纳米NiO/ZrO2催化剂具有良好的稳定性。

|
图 11 反应100 h后催化剂的SEM图 Fig.11 SEM image of 30% nano NiO/ZrO2 after reaction for 100 h (reaction temperature: 350 ℃; space velocity: 1 000 h−1; gas composition: 3% CO, 2% CO2, 95% H2) |
(1) 采用尿素水解法制备的纳米NiO/ZrO2催化剂为纳米颗粒,且NiO与ZrO2之间的相互作用力较弱,有利于NiO还原为低价的活性镍,有利于CO的深度脱除。
(2) NiO负载量在质量分数为30% 的纳米NiO/ZrO2催化剂催化CO甲烷化性能最佳,在体积空速为1 000 h−1,反应温度为200~400 ℃时,将CO体积分数由3% 脱除至10−7,CO转化率接近100%。
(3) 催化剂寿命研究表明,30% 纳米NiO/ZrO2催化剂能够在100 h内将CO体积分数稳定在5×10−6。
(4) 30% 纳米NiO/ZrO2催化剂优异的甲烷化性能与载体ZrO2有关,ZrO2对CO的吸附作用,有利于反应的进行。ZrO2载体在反应中的作用需要进一步研究。
符号说明:
A —比表面积,m2·g−1 x —转化率
r —孔径,nm φ —体积分数,%
rp —对应压力下的孔径,nm 下标
V —孔容,m3·g−1 in —进口
Vp —对应压力下的孔容,m3·g−1 out —出口
| [1] |
国家市场监督管理总局、中国国家标准化管理委员会. 质子交换膜燃料电池汽车用燃料氢气: GB/T 37244-2018 [S]. 北京: 中国标准出版社, 2018. State Administration for Market Regulation, China National Standardization Administration. Fuel specification for proton exchange membrane fuel cell vehicles——Hydrogen. GB/T 37244-2018 [S]. Beijing: Standards Press of China, 2018. |
| [2] |
PARK E D, LEE D, LEE H C. Recent progress in selective CO removal in a H2-rich stream[J]. Catalysis Today, 2009, 139(4): 280-290. DOI:10.1016/j.cattod.2008.06.027 |
| [3] |
DJINOVIC P, GALLETTI C, SPECCHIA S, et al. Ru-based catalysts for CO selective methanation reaction in H2-rich gases[J]. Catalysis Today, 2011, 164(1): 282-287. DOI:10.1016/j.cattod.2010.11.007 |
| [4] |
GALLETTI C, SPECCHIA S, SARACCO G, et al. CO-selective methanation over Ru-gamma Al2O3 catalysts in H2-rich gas for PEM FC applications[J]. Chemical Engineering Science, 2010, 65(1): 590-596. DOI:10.1016/j.ces.2009.06.052 |
| [5] |
PING D, DONG X, ZANG Y. Highly efficient Ru/TiO2-NiAl mixed oxide catalysts for CO selective methanation in hydrogen-rich gas[J]. International Journal of Energy Research, 2017, 41(14): 2308-2317. DOI:10.1002/er.3797 |
| [6] |
PING D, DONG C, ZHAO H, et al. A novel hierarchical RuNi/Al2O3-carbon nanotubes/Ni foam catalyst for selective removal of CO in H2-rich fuels[J]. Industrial & Engineering Chemistry Research, 2018, 57(16): 5558-5567. |
| [7] |
LANG S M, BERNHARDT T M, KRSTIC M, et al. The origin of the selectivity and activity of Ruthenium-cluster catalysts for fuel-cell feed-gas purification: A gas-phase approach[J]. Angewandte Chemie-International Edition, 2014, 53(21): 5467-5471. DOI:10.1002/anie.201310134 |
| [8] |
TADA S, SHIMIZU T, KAMEYAMA H, et al. Ni/CeO2 catalysts with high CO2 methanation activity and high CH4 selectivity at low temperatures[J]. International Journal of Hydrogen Energy, 2012, 37(7): 5527-5531. DOI:10.1016/j.ijhydene.2011.12.122 |
| [9] |
WANG Y, WU R, ZHAO Y. Effect of ZrO2 promoter on structure and catalytic activity of the Ni/SiO2 catalyst for CO methanation in hydrogen-rich gases[J]. Catalysis Today, 2010, 158(3/4): 470-474. |
| [10] |
ZHANG X, RUI N, JIA X, et al. Effect of decomposition of catalyst precursor on Ni/CeO2 activity for CO methanation[J]. Chinese Journal of Catalysis, 2019, 40(4): 495-503. DOI:10.1016/S1872-2067(19)63289-4 |
| [11] |
GAO Z, WANG L, MA H, et al. Durability of catalytic performance of the chlorine-doped catalyst Ni(Clx)/ZrO2 for selective methanation of CO in H2-rich gas[J]. Applied Catalysis a-General, 2017, 534: 78-84. DOI:10.1016/j.apcata.2017.02.001 |
| [12] |
XIAO M, ZHANG L, SANG Y, et al. Effects of supports and combined process on hydrogen purification over nickel supported catalysts[J]. Journal of Rare Earths, 2020, 38(1): 52-58. DOI:10.1016/j.jre.2019.07.003 |
| [13] |
DA SILVA D C D, LETICHEVSKY S, BORGES L E P, et al. The Ni/ZrO2 catalyst and the methanation of CO and CO2[J]. International Journal of Hydrogen Energy, 2012, 37(11): 8923-8928. DOI:10.1016/j.ijhydene.2012.03.020 |




