甲醇不仅是重要的化工原料,也是洁净的绿色燃料和能源载体,因此,甲醇的制备成为众多研究者关注的焦点[1~3]。目前,甲醇的工业化生产主要采用甲烷间接转化法,即先通过高温高压将甲烷转化为合成气,进而由合成气生成甲醇,这种工艺能耗较大,成本偏高。资料显示[4],仅合成气的制备成本就占总生产成本的40%。因而,研究者一直寻求不经合成气,直接将甲烷转化为甲醇的方法。
应用低温等离子体技术可实现甲烷的“非平衡”直接转化[5],因为低温等离子体系统中富含大量活性粒子,具有极高的化学反应活性,利于甲烷的活化转化[6]。虽然应用低温等离子体技术能使甲烷在温和条件下得以活化,但产物选择性普遍较低,为了提高产物的选择性,人们将等离子体对甲烷的活化与催化剂的定向转化有机的结合起来[7],等离子体与催化剂结合,能够充分发挥等离子体和化学催化的协同作用[8]。Mahammadunnisa[9]和Antonius [10]以NOx为氧化剂进行了CH4等离子体-催化制甲醇的研究,发现CuO/CeO2、NiO/CeO2和Cu-Ni(5-5)/CeO2三种催化剂中Cu-Ni(5-5)/CeO2的催化效果最佳,甲醇选择性接近于36%。上述研究所用氧化剂为NOx,从环保和成本角度而言,最好的氧化剂应该是O2。Chen等[11]构建了甲烷和空气混合物的离子体-催化反应体系,对比了Pt/CP、Fe2O3/CP和CeO2/CP三种催化剂的催化性能,结果表明,Fe2O3/CP的催化效果最好,甲醇的选择性较未添加催化剂的单纯等离子体提高了36%。在Fe2O3/CP催化剂中添加CuO助剂构成Fe2O3-CuO/CP复合催化剂,更利于甲醇的生成,甲醇的选择性较Fe2O3/CP又提高了6.3%,较单纯等离子体提高了45.07%[12]。对于负载型催化剂,除了活性组分,载体也会影响催化剂性能。文献[13]以Fe2O3-CuO/Al2O3为催化剂,进行甲烷离子体-催化转化,得到甲醇收率1.6%的实验结果。Huang等[14]选用CuO/Al2O3和Mo-CuO/Al2O3两种催化剂进行了甲烷等离子体转化合成甲醇的研究,结果显示,在等离子体-催化体系中激发态物种的形成降低了甲烷转化所需的表观活化能,提高了反应速率,且Mo-CuO/Al2O3比CuO/Al2O3具有更高的催化活性。Antonius Indarto等[15]报道,对于甲醇的合成,Cu-Zn-Al比其他金属材料具有更好的催化活性。Cu-Zn-Al催化剂之所以表现出很好的催化性能,原因在于Cu和Zn之间存在协同作用[16]。将Cu-Zn-Al催化剂填装于介质阻挡反应器中进行甲烷部分氧化合成甲醇,可大大提高甲醇的选择性[15, 17]。
本文将Cu-Zn-Al基催化剂引入介质阻挡放电系统,以甲烷体积分数40%的甲烷和空气的混合物为反应气,进行催化剂与等离子体协同转化甲烷制甲醇的实验研究,考察催化剂填装方式、催化剂载体、催化剂助剂对甲醇生成的影响。
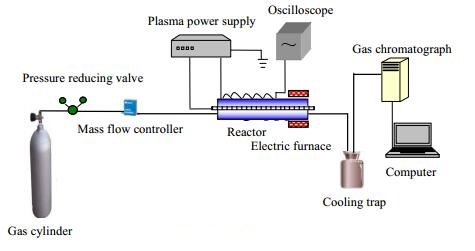
2 实验装置与方法 2.1 实验装置实验装置主要由气源、反应器、等离子体电源、示波器、温控电炉、冷阱、气相色谱等组成。实验装置示意图如图 1所示。反应器为同轴式介质阻挡反应器,以刚玉管作为介质层(外径26 mm,内径20.4 mm,长790 mm),管内的高压电极为不锈钢螺纹棒,管外低压电极为不锈钢网。等离子体电源为南京苏曼等离子体科技有限公司生产的CTP-2000K实验电源,输出频率调节范围为5~20 kHz。示波器为北京普源精电科技有限公司生产的DS1102E数字示波器。气相色谱仪为浙江福立分析仪器有限公司生产的9790和9790Ⅱ型色谱仪。
|
图 1 实验装置示意图 Fig.1 Schematic diagram of the experimental setup |
反应气经流量计控制后,以195 mL·min-1的流量进入介质阻挡反应器,在峰值电压12 kV、频率10.5 kHz、放电间隙1.2 mm的条件下进行等离子体活化反应,经温控电炉控制催化段床层温度,进行催化反应。生成的甲醇经蒸馏水冷凝吸收后,用GC9790型气相色谱仪检测,GDX-102型填充柱,FID检测器,外标法计算;不凝气用GC9790Ⅱ型气相色谱仪检测,TDX-01型填充柱,FID检测器,外标法计算。
以单位能耗甲烷转化量、单位能耗甲醇产量、甲醇收率及选择性作为反应活性的评价指标。
| $ {\text{Conversion ability of C}}{{\text{H}}_{\text{4}}} = \frac{{{\text{Moles of C}}{{\text{H}}_{\text{4}}}{\text{ converted}}}}{{{\text{Discharge energy}}}}\left( \rm{{ \mathsf{ μ} mol \cdot {J^{ - 1}}}} \right) $ | (1) |
| $ {\text{Production ability of C}}{{\text{H}}_{\text{3}}}{\text{OH}} = \frac{{{\text{Moles of C}}{{\text{H}}_{\text{3}}}{\text{OH produced}}}}{{{\text{Discharge energy}}}}\left( \rm{{ \mathsf{ μ} mol \cdot {J^{ - 1}}}} \right) $ | (2) |
| $ {\text{Yield of C}}{{\text{H}}_{\text{3}}}{\text{OH}} = \frac{{{\text{Moles of C}}{{\text{H}}_{\text{3}}}{\text{OH produced}}}}{{{\text{Moles of C}}{{\text{H}}_{\text{4}}}{\text{ in feed }}}} \times 100\% $ | (3) |
| $ {\text{Selectivity of C}}{{\text{H}}_{\text{3}}}{\text{OH}} = \frac{{{\text{Moles of C}}{{\text{H}}_{\text{3}}}{\text{OH produced}}}}{{{\text{Moles of C}}{{\text{H}}_{\text{4}}}{\text{ converted }}}} \times 100\% $ | (4) |
(1) Cu-Zn-Al催化剂
采用共沉淀法制备Cu-Zn-Al催化剂。将0.02813 mol Cu(OAc)2·H2O、0.02813 mol Zn(OAc)2·2H2O和0.00625 mol Al(NO3)3·9H2O同时溶解于100 mL的去离子水中,制成Cu-Zn-Al溶液。将0.1313 mol Na2CO3溶解于另外100 mL去离子水中,制成Na2CO3溶液。之后,将Cu-Zn-Al溶液与Na2CO3溶液用分液漏斗同时缓慢加入到烧杯中,不断搅拌,调整溶液PH值为7~9,在70℃下搅拌老化2 h,制得Cu-Zn-Al-Na溶液。经抽滤、烘干、研磨后,在350℃条件下灼烧3 h,自然冷却至室温,得Cu-Zn-Al粉末催化剂,记为Cu-Zn-Al。
(2) Cu-Zn-Al/HC及Cu-Zn-Al/HC-AE催化剂
采用过量浸渍法制备Cu-Zn-Al/HC及Cu-Zn-Al/HC-AE催化剂。在上述制备的Cu-Zn-Al-Na溶液中加入蜂窝陶瓷或经酸蚀处理过的蜂窝陶瓷,搅拌浸泡10 min,取出,用吹风机吹干蜂窝陶瓷孔道中的液体,在110℃干燥30 min后,于350℃灼烧30 min,如此循环多次后,在110℃烘2 h、350℃灼烧3 h,自然冷却至室温,制得Cu-Zn-Al/HC或Cu-Zn-Al/HC-AE催化剂。
(3) Cu-Zn-Al-Ce/HC-AE催化剂
分别称取0.02813 mol Cu(OAc)2·H2O、0.02813 mol Zn(OAc)2·2H2O、0.00625 mol Al(NO3)3·9H2O和0.00625 mol Ce(NO3)3·6H2O同时溶解于100 mL的去离子水中,制成Cu-Zn-Al-Ce溶液。后续制备方法与Cu-Zn-Al/HC-AE相同,将最终制备的催化剂记为Cu-Zn-Al-Ce/HC-AE。
2.3.2 催化剂表征催化剂及载体SEM观测在MX2600FE扫描电子显微镜上进行,激发电压15.00 kV,分辨率1.5 nm。催化剂及载体的XRD谱采用Bruker D8 Advance型X射线粉末衍射仪测定,测定条件为:Cukα1(λ = 0.15406 nm),管电压40 kV,管电流40 mA,扫描范围10~80°。催化剂及载体的XRF分析采用Bruker S4 Explorer型X射线荧光分析仪进行。催化剂的比表面积通过PoreMaster 33压汞仪测定。
3 结果与讨论 3.1 催化剂中各金属组分的作用及含量分析对于合成甲醇铜基催化剂表面上的活性位的研究,一直是研究者关注的焦点。一般认为,Cu是Cu-Zn-Al催化剂的活性中心,但Zn又不可缺少[18],因为甲醇合成的中间物种甲氧基键合在Zn上[16],而Al通过对Cu-Zn起分散作用而提高催化剂的热稳定性[19]。
在甲醇合成反应中,Cu-Zn-Al基催化剂的组成对其催化性能也有较大的影响。对Cu-Zn-Al/HC、Cu-Zn-Al/HC-AE、Cu-Zn-Al-Ce/HC-AE 3种催化剂及载体HC中各元素组分的含量进行了XRF分析,结果列于表 1。从表 1可看出,3种催化剂中Cu、Zn、Al的质量分数基本保持一致,且Al > Zn > Cu。堇青石蜂窝陶瓷的理论化学式为2MgO·2Al2O3·5SiO2,但实际的堇青石中会残留一些制备过程中用作烧结助剂或助溶剂的TiO2、CaO、ZnO等物质[20]。堇青石载体XRF分析结果也证实了这一点。虽然表 1所列的3种催化剂的Cu、Zn和Al质量分数去除了堇青石载体本体Al和Zn,但Al和Zn的质量分数仍明显高于Cu,这可能是催化剂制备过程中的碱性环境致使两性氧化物Al2O3和ZnO不同程度溶出导致的。
|
|
表 1 催化剂及载体组分含量(质量分数) Table 1 Elemental contents of catalysts and cordierite support (mass fraction) |
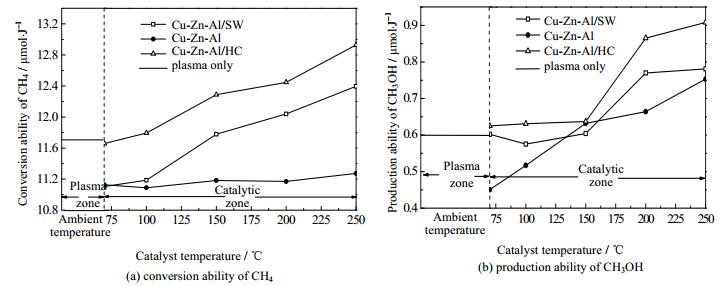
称取1.0000 g Cu-Zn-Al催化剂,用石英棉包裹(记为Cu-Zn-Al/SW)后填装于反应器的催化区域,另称取1.0000 g Cu-Zn-Al催化剂平铺于催化区域反应器的内壁上。在两种催化剂填装方式下分别进行等离子体-催化甲烷制备甲醇的实验研究,考察催化剂填装方式对实验结果的影响,实验结果如图 2所示。
|
图 2 催化剂填装方式对单位能耗甲烷转化量和单位能耗甲醇产量的影响 Fig.2 Effects of catalyst filling mode on CH4 conversion and CH3OH productivity per unit energy consumption |
从图 2(a)可以看出,催化剂平铺于反应器内壁的填装方式,对甲烷转化没有明显的促进作用;而石英棉包裹的催化剂填装方式利于甲烷转化。这可从以下两方面解释:一是石棉包裹的催化剂填装方式,导致反应气体流速变慢,在反应区域停留的时间较长,与高能电子碰撞的几率增大,甲烷被解离的概率也相应增大;二是平铺时催化剂无法在整个反应器截面上充分填充,导致反应气体只和部分催化剂接触,而石棉包裹的催化剂填装方式增大了反应气体和催化剂的接触面积,利于甲烷转化。分析图 2(b)可知,石英棉包裹的催化剂填装方式单位能耗甲醇的最大产量为0.78 μmol·J-1,比平铺的催化剂填装方式高4%,比单纯等离子体体系(不添加催化剂)高30%。因此,石英棉包裹的催化剂填装方式利于甲醇的生成。
虽然采用石英棉包裹的催化剂填装方式利于甲烷的转化和甲醇的生成,但无法保证催化剂在整个反应器断面内均匀分布。因堇青石蜂窝陶瓷具有优良的吸附性能、较好的耐火性和机械强度,是催化剂的良好载体[21],于是,使用浸渍法将Cu-Zn-Al催化剂负载在堇青石蜂窝陶瓷上,制成了整体催化剂(记为Cu-Zn-Al/HC),以解决催化剂在反应器断面内分布不均匀的问题。根据图 2计算得知,催化剂负载在堇青石蜂窝陶瓷上填装方式与用石英棉包裹填装方式比较,单位能耗甲烷最大转化量提高了4.3%,单位能耗甲醇的最大产量提高了16.2%,即采用将催化剂负载在堇青石蜂窝陶瓷上的填装方式效果较好。
3.3 催化剂载体的影响蜂窝陶瓷是在高温下挤压成型的,其比表面积并不大(< 1 m2·g-1)。为了提高堇青石蜂窝陶瓷的比表面积,便于催化剂的负载,对其进行了酸蚀处理(用饱和草酸溶液恒温煮沸2 h),并以此为载体制备了催化剂(记为Cu-Zn-Al/HC-AE)。使用压汞仪对酸蚀前后的载体比表面积进行了测试,测试结果表明,载体比表面积从酸蚀前的0.76 m2·g-1变为酸蚀后的16.40 m2·g-1,比表面积足足增加了20倍左右。比较酸蚀前后的SEM图像(图 3),也同样验证草酸酸蚀的良好效果。从图 3中可看出,经酸蚀处理过后的堇青石,表面凹凸感增强,孔洞系统更加复杂。

|
图 3 酸蚀前后的堇青石SEM图 Fig.3 SEM micrographs of honeycomb ceramics (a) and (b): before acid etching (c) and (d): after acid etching |
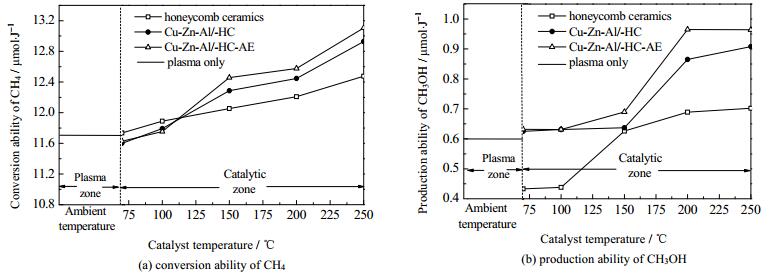
图 4是Cu-Zn-Al/HC、Cu-Zn-Al/HC-AE和堇青石用于等离子体-催化甲烷制甲醇的实验结果。从图 4可看出,Cu-Zn-Al/HC-AE催化剂对甲烷转化和甲醇生成的促进作用均强于Cu-Zn-Al/HC。这说明载体堇青石表面结构对甲烷转化和甲醇生成具有显著的影响,将催化剂负载在经酸蚀处理的堇青石蜂窝陶瓷上,可使单位能耗甲醇产量较单纯等离子体体系提高28%。图 4显示,堇青石载体对甲烷转化和甲醇生成也表现出一定的促进作用。为了探究这种促进作用的原因,将堇青石载体直接填装于催化体系中(即不加等离子体作用)进行甲烷转化,主要产物为CO2,没有检测到甲醇的生成。这说明,在等离子体-催化体系中堇青石载体的促进作用表现为引入放电区域以外的载体形成了吸附位,从而促进甲醇的生成。
|
图 4 不同催化剂对单位能耗甲烷转化量和单位能耗甲醇产量的影响 Fig.4 Effects of different catalysts on CH4 conversion and CH3OH productivity per unit energy consumption |
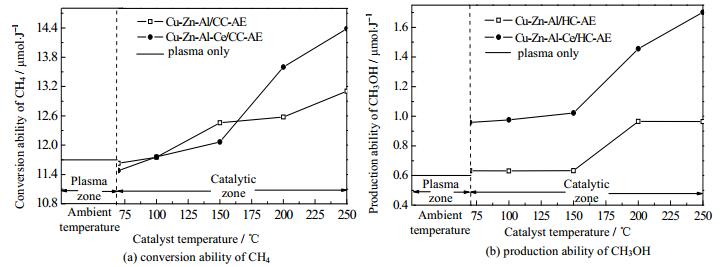
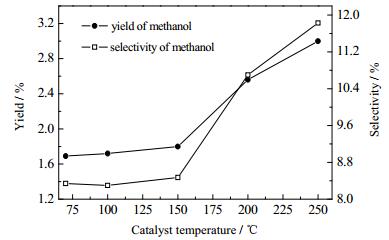
虽然应用Cu-Zn-Al/HC-AE催化剂可使单位能耗甲醇产量比单纯应用等离子体大幅提高,但甲醇的单位能耗产量仍然维持在较低的水平,最大仅为0.965 μmol·J-1。于是,考虑通过添加催化剂助剂的方法,提高单位能耗甲醇产量。Mazzoeehia等[22]的研究结果表明,在Rh/SiO2催化剂中加入Ce,可使甲烷及总烃类含量大大减少,而低碳醇的含量大量增加。士丽敏等[23]发现,在Cu-Co催化剂中加入Ce,可以增加催化剂的比表面积,使催化剂的活性组分分布更加均匀,可以促进醇类的活性中心生成。毛东森等[24]发现,在Cu-Fe/SiO2催化剂中添加Ce,也有助于提高催化剂的活性和醇的选择性。基于上述文献的启示,本文在催化剂制备过程中添加了Ce助剂,制备了Cu-Zn-Al-Ce/HC-AE催化剂。图 5是Cu-Zn-Al/HC-AE和Cu-Zn-Al-Ce/HC-AE两种催化剂应用于等离子体-催化转化甲烷制甲醇的实验结果。从图 5(a)可以看出,添加Ce的催化剂更利于甲烷的活化。在250℃时,Cu-Zn-Al-Ce/HC-AE与Cu-Zn-Al/HC-AE比较,单位能耗甲烷转化量提高了9.75%。这可能是添加Ce以后,活性组分在催化剂上的分散度更好,催化剂活性中心更多,更利于甲烷的转化。图 5(b)显示,应用Cu-Zn-Al-Ce/HC-AE催化剂的体系单位能耗甲醇产量明显高于添加Cu-Zn-Al/HC-AE催化剂的体系。填装Cu-Zn-Al-Ce/HC-AE催化剂时,单位能耗甲醇最大量为1.7 μmol·J-1,高于填装Cu-Zn-Al/HC-AE催化剂体系76.6%,高于单纯等离子体体系183.7%。Okumoto[25]利用低温等离子体转化甲烷,得到单位能耗最大甲醇产量为0.7 μmol·J-1。Yao等[26]以CH4/O2为反应气,应用DBD制备甲醇,单位能耗甲醇产量为0.1 μmol·J-1。可见,本研究的实验结果好于上述文献报道的结果。应用Cu-Zn-Al-Ce/HC-AE催化剂时,甲醇最大收率为3.00% (见图 6),高于单纯等离子体体系175.2%。催化段温度250℃时,甲醇选择性达11.83%,略高于文献[11]报道的11.33%。
|
图 5 Ce对单位能耗甲烷转化量和单位能耗甲醇产量的影响 Fig.5 Effects of Ce addition on CH4 conversion and CH3OH productivity per unit energy consumption |
|
图 6 温度对甲醇收率和选择性的影响 Fig.6 Effects of temperature on methanol yield and selectivity |
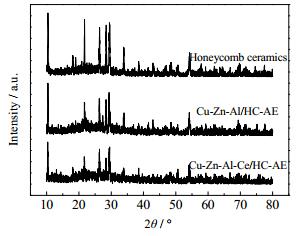
图 7中(a)和(b)是Cu-Zn-Al/HC-AE催化剂放大500和2000倍的SEM照片,(c)和(d)是Cu-Zn-Al-Ce/HC-AE催化剂放大500和2000倍的SEM照片。对比两催化剂的SEM照片可以看出,添加了Ce以后催化剂活性组分分布更加均匀,覆盖载体更加全面。图 8是堇青石及Cu-Zn-Al/HC-AE、Cu-Zn-Al-Ce/HC-AE催化剂的XRD谱图。图 8显示,两种催化剂及载体的XRD谱图差别不大,均没有检测到Cu、Zn、Al、Ce元素的衍射峰,这可能是这些金属元素和相应的氧化物以无定性态分散在载体表面的缘故。

|
图 7 Cu-Zn-Al/HC-AE和Cu-Zn-Al-Ce /HC-AE催化剂的SEM图 Fig.7 SEM micrographs of Cu-Zn-Al/HC-AE and Cu-Zn-Al-Ce /HC-AE (a) and (b): Cu-Zn-Al/HC-AE (c) and (d): Cu-Zn-Al-Ce /HC-AE |
|
图 8 催化剂及载体的XRD图 Fig.8 XRD patterns of catalysts and carriers |
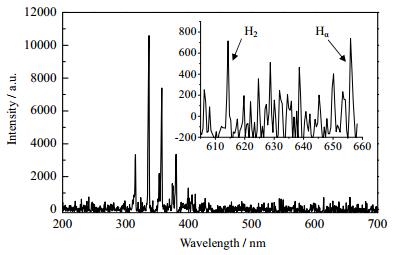
甲烷合成甲醇的反应由等离子体转化阶段和催化剂催化反应阶段组成。在等离子体反应阶段,反应气的CH4、O2、N2在等离子体的作用下会产生CH3O·、CH3·、CH2·、CH·、OH·、O·、H·等自由基,然后通过自由基反应生成甲醇。而对于催化反应阶段,因自由基的存活时间大概只有100 ns到秒量级[27],无法到达催化反应区域,因而只有稳定的物质才能到达催化区域。以石英管代替刚玉管,在常温条件下进行了等离子体转化甲烷的实验,并用HR2000+光纤光谱仪(美国海洋光学公司生产)对激发态物种进行原位诊断。图 9是甲烷浓度40%的反应气等离子体发射光谱图。在波长为614.34和655.96 nm处各存在一个较微弱的峰,根据文献[28, 29],其分别为H2分子和Hα原子的特征谱线峰。实验过程中,对反应尾气进行色谱分析证明其中含有大量的CO。Chen等[16]报道,当Cu-Zn-Al催化剂暴露于H2和CO中时,CO吸附于CuO的活性位,H2吸附于ZnO的活性位,且在甲醇合成过程中CuO和ZnO能彼此增强吸附气体的能力,从而对CO加氢生成甲醇起到协同增效的作用。基于此,推断在催化反应阶段,一部分甲醇是通过费托合成生成的。
|
图 9 反应气的等离子体发射光谱 Fig.9 Plasma emission spectra of reaction gas |
利用介质阻挡放电系统,进行了催化剂与等离子体协同转化甲烷制甲醇的实验研究,探讨了Cu-Zn-Al基催化剂对等离子体转化甲烷制甲醇的影响,得到如下主要结论:
(1) 催化剂的填装方式对单位能耗甲烷转化量和单位能耗甲醇的产量具有较为显著的影响,石英棉包裹的催化剂填装方式甲醇的单位能耗最大产量为0.78 μmol·J-1,比平铺的催化剂填装方式高4%,比单纯等离子体体系高30%。
(2) 为保证催化剂在整个反应器断面内均匀分布,以堇青石蜂窝陶瓷作为载体,制备了Cu-Zn-Al/HC催化剂,以酸蚀处理的堇青石为载体制备了Cu-Zn-Al/HC-AE催化剂。其中,Cu-Zn-Al/HC-AE催化剂更利于甲醇的生成,应用该催化剂时单位能耗甲醇产量较单纯等离子体体系提高28%。
(3) 在催化剂中添加助剂Ce,可以改善活性组分在载体上的分散度,使催化剂活性中心增多,更利于甲烷的转化和甲醇的生成。Cu-Zn-Al/HC-AE催化剂中添加Ce以后,单位能耗甲烷转化量提高了9.75%,单位能耗甲醇产量提高了76.6%,高于单纯等离子体体系183.7%。
(4) 推断了甲醇的两条合成路径,即单纯等离子体自由基生成和催化剂作用下合成气反应生成(费托合成反应)。
| [1] | DONG Xiao-su(董晓素), LI Feng(李枫), ZHAO Ning(赵宁), et al. CO2 hydrogenation to methanol over Cu/Zn/Al/Zr catalysts prepared by liquid reduction(液相还原法制备Cu/Zn/Al/Zr催化剂用于CO2加氢合成甲醇)[J]. Chinese Journal of Catalysis(催化学报), 2017, 38(4): 717-725. |
| [2] | Olah G A, Goeppert A, Prakash G K S. Chemical recycling of carbon dioxide to methanol and dimethyl ether:from greenhouse gas to renewable, environmentally carbon neutral fuels and synthetic hydrocarbons[J]. Journal of Organic Chemistry, 2009, 74(2): 487-498. |
| [3] | Olah G A, Prakash G K S, Goeppert A. Anthropogenic chemical carbon cycle for a sustainable future[J]. Journal of the American Chemical Society, 2011, 133(33): 12881-12898. DOI:10.1021/ja202642y. |
| [4] | Aasberg-Petersen K, Bak Hansen J H, Christensen T S, et al. Technologies for large-scale gas conversion[J]. Applied Catalysis A:General, 2001, 221(1-2): 379-387. DOI:10.1016/S0926-860X(01)00811-0. |
| [5] | XU Feng(徐锋), LI Chuang(李创), ZHU Li-hua(朱丽华). Study on activation and conversion of methane using non-thermal plasma(低温等离子体促进煤层甲烷活化转化)[J]. Journal of Heilongjiang University of Science & Technology(黑龙江科技大学学报), 2015, 25(6): 597-601. DOI:10.3969/j.issn.2095-7262.2015.06.005. |
| [6] | SHAO Tao(邵涛), ZHANG Cheng(章程), WANG Rui-xue(王瑞雪), et al. Atmospheric-pressure pulsed gas discharge and pulsed plasma application(大气压脉冲气体放电与等离子体应用)[J]. High Voltage Engineering(高电压技术), 2016, 42(3): 685-705. |
| [7] | LI Ming-shu(李铭书), LI Sheng-li(李胜利), LI Dong(李东), et al. Experimental study of the synergistic effect of catalyst and pulsed discharge plasma on removal of dimethyl sulfide(催化剂协同脉冲放电等离子体处理甲硫醚气体的实验研究)[J]. High Voltage Engineering(高电压技术), 2016, 42(2): 462-467. |
| [8] | WU Zu-liang(吴祖良), ZHU Zhou-bin(朱周彬), ZHANG Xu-ming(章旭明), et al. Study on n-decane removal by plasma assisted noble metal catalysis(等离子体强化贵金属催化净化正葵烷的研究)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报), 2017, 31(6): 1452-1458. DOI:10.3969/j.issn.1003-9015.2017.06.026. |
| [9] | Mahammadunnisa S K, Krushnamurty K, Subrahmanyam C H. Catalytic nonthermal plasma assisted co-processing of methane and nitrous oxide for methanol production[J]. Catalysis Today, 2015, 256(part1): 102-107. |
| [10] | Indarto A. Partial oxidation of methane to methanol with nitrogen dioxide in dielectric barrier discharge plasma:experimental and molecular modeling[J]. Plasma Sources Science and Technology, 2016, 25(2): 25002. DOI:10.1088/0963-0252/25/2/025002. |
| [11] | Chen L, Zhang X W, Huang L, et al. Partial oxidation of methane with air for methanol production in a post-plasma catalytic system[J]. Chemical Engineering and Processing, 2009, 48(8): 1333-1340. DOI:10.1016/j.cep.2009.06.007. |
| [12] | Chen L, Zhang X W, Huang L, et al. Post-plasma catalysis for methane partial oxidation to methanol:role of copper promoted iron oxide catalyst[J]. Chemical Engineering & Technology, 2010, 33(12): 2073-2081. |
| [13] | Chen L, Zhang X W, Huang L, et al. Application of in-plasma catalysis and post-plasma catalysis for methane partial oxidation to methanol over a Fe2O3-CuO/γ-Al2O3 catalyst[J]. Journal of Natural Gas Chemistry, 2010, 19(6): 628-637. DOI:10.1016/S1003-9953(09)60129-8. |
| [14] | Huang L, Zhang X W, Chen L, et al. Direct oxidation of methane to methanol over Cu-based catalyst in an AC dielectric barrier discharge[J]. Plasma Chem Plasma Process, 2011, 31(1): 67-77. DOI:10.1007/s11090-010-9272-1. |
| [15] | Indarto A, Song H K. Partial oxidation of methane with Cu-Zn-Al catalyst in a dielectric barrier discharge[J]. Chemical Engineering and Processing, 2008, 47(5): 780-786. DOI:10.1016/j.cep.2006.12.015. |
| [16] | Lau S P, Chen L, Lin J, et al. Synergism between Cu and Zn sites in Cu/Zn catalysts for methanol synthesis[J]. Applied Surface Science, 1999, 152(3-4): 193-199. DOI:10.1016/S0169-4332(99)00317-7. |
| [17] | Indarto A. Methanol synthesis from methane and oxygen with[Ga Cr]/Cu-Zn-Al catalyst in a dielectric barrier discharge[J]. Ionics, 2014, 20(3): 445-449. DOI:10.1007/s11581-014-1077-4. |
| [18] | LI Zhi-xiong(李志雄), NA Wei(纳薇), WANG Hua(王华), et al. Direct syntheses of Cu-Zn-Zr/SBA-15 mesoporous catalysts for CO2 hydrogenation to methanol(Cu-Zn-Zr/SBA-15介孔催化剂的制备及CO2加氢合成甲醇的催化性能)[J]. Chemical Journal of Chinese Universities(高等学校化学学报), 2014, 35(12): 2616-2623. DOI:10.7503/cjcu20140684. |
| [19] | ZHAO Jiu-sheng(赵九生), CHEN Bao-shu(陈宝树), MA Fu-shan(马福善), et al. The effects of the composition of a Cu-based catalyst for methanol systhesis on its structure and property(合成甲醇Cu-Zn-Al催化剂中组成对其结构及催化性能的影响)[J]. Journal of Chemical Industry and Engineering (China)(化工学报), 1988, 39(5): 562-569. |
| [20] | NI Wen(倪文), CHEN Na-na(陈娜娜). Advance in the study of cordierite mineralogy-Ⅰ. Structure and composition of cordierite(堇青石矿物学研究进展-Ⅰ堇青石的结构与化学成分)[J]. Journal of Mineralogy and Petrolog(矿物岩石), 1996, 16(4): 12. |
| [21] | LU Gui-zeng(路贵增), LEI Ze(雷泽), ZHAO Hao-ying(赵昊鹰), et al. Preparation and catalytic activities of lanthanum strontium manganite based catalysts supported on honeycomb ceramics(蜂窝陶瓷负载锰酸锶镧基催化剂制备及性能)[J]. Clean Coal Technology(洁净煤技术), 2014, 20(6): 104-108. |
| [22] | Mazzocchia C, Gronchi P, Kaddouri A, et al. Hydrogenation of CO over Rh/SiO2-CeO2 catalysts:kinetic evidences[J]. Journal of Molecular Catalysis A:Chemical, 2001, 165(1-2): 219-230. DOI:10.1016/S1381-1169(00)00425-8. |
| [23] | SHI Li-min(士丽敏), CHU Wei(储伟), XU Hui-yuan(徐慧远), et al. Effect of Ce addition on the structure and properties of CuCo oxide catalyst(稀土Ce对CuCo氧化物催化剂结构与性能的影响)[J]. Rare Metal Materials and Engineering(稀有金属材料与工程), 2009, 38(8): 1382-1385. DOI:10.3321/j.issn:1002-185X.2009.08.015. |
| [24] | MAO Dong-sen(毛东森), GUO Sheng-qiang(郭胜强), YU Jun(俞俊), et al. Effect of cerium addition on the catalytic performance of Cu-Fe/SiO2 for the synthesis of lower alcohols from syngas(Ce添加对Cu-Fe/SiO2催化合成气制低碳醇性能的影响)[J]. Acta Physico-Chimica Sinica(物理化学学报), 2011, 27(11): 2639-2645. DOI:10.3866/PKU.WHXB20111125. |
| [25] | Okumoto M, Kim H H, Takashima K, et al. Reactivity of methane in nonthermal plasma in the presence of oxygen and inert gases at atmospheric pressure[J]. IEEE Trangactions on Industry Applications, 2001, 37(6): 1618-1624. DOI:10.1109/28.968169. |
| [26] | Yao S L, Takemoto T, Ouyang F, et al. Selective oxidation of methane using a non-thermal pulsed plasma[J]. Energy Fuels, 2000, 14(2): 459-463. DOI:10.1021/ef9901692. |
| [27] | QIN Kun-yuan(丘坤元). Progress of free radical polymerization in recent years(自由基聚合近20年的发展)[J]. Polymer Bulletin(高分子通报), 2008, 21(7): 15-28. |
| [28] | LI Jin-ping(李金平), DAI Bin(代斌), FAN Ting(范婷). Study on optical emission spectroscopy of pulse corona methane plasma(甲烷电离特性的等离子体发射光谱法研究)[J]. Spectroscopy and Spectral Analysis(光谱学与光谱分析), 2009, 29(7): 1979-1982. DOI:10.3964/j.issn.1000-0593(2009)07-1979-04. |
| [29] | WU Li-feng (吴利峰). Emission spectroscopy diagnosis of hydrogen microwave plasma (微波氢等离子体发射光谱诊断)[D]. Wuhan (武汉): Wuhan Institute of Technology (武汉工程大学), 2010. |




