2. 六盘水师范学院 计划财务处, 贵州 六盘水 553004;
3. 六盘水市钟山区环保局, 贵州 六盘水 553001
2. Planning and Finance Division, Liupanshui Normal University, Liupanshui 553004, China;
3. Environmental Protection Bureau of Zhongshan District, Liupanshui 553001, China
活性炭广泛用于化工、石油、冶金、环境等领域[1-2]。我国生产活性炭的原料以煤炭为主,煤基活性炭产量约占活性炭总产量的70% 以上[3-4],生产方法分为2类:以酸、碱、盐为活化剂的化学活化和以水蒸汽或CO2为活化剂的物理活化[5]。由于化学活化带来的污染问题,逐渐限制工业化应用[6-7]。对于物理活化,CO2活化目前还多应用于实验室中,工业化生产多采用水蒸汽活化法[8-9]。原因是H2O的分子尺寸比CO2小,H2O在颗粒中的扩散速度大于CO2的扩散速度,活化反应时间短[10]。目前活性炭制备的研究还集中在选择合适原料及产品应用方面[11-12],对活化条件的系统研究及反应动力学均缺乏研究。
贵州煤炭储量丰富,多用作燃料煤,以煤制活性炭可以提升煤的附加值及资源综合利用效益[13-15]。贵州无烟煤、烟煤有机质及固定碳质量分数高,挥发分低,黏结性好,低灰低硫,且本身具有较好的孔结构及吸附性能[16]。本文设计煤制活性炭的工艺流程,以贵州无烟煤、烟煤及二者混合物为原料,以水蒸汽为活化剂制活性炭。考察了活化温度、活化时间、水蒸汽流量、水蒸汽压力等对活性炭吸附性能的影响,建立了活化过程的反应动力学,对活性炭产品进行了扫描电子显微镜(SEM)、布鲁诺尔-埃米特-泰勒(BET)比表面积等表征,揭示了贵州无烟煤、烟煤、混合煤制活性炭的协同效应。
2 实验仪器、煤样及工艺流程 2.1 主要仪器及煤样试验所用仪器:SRJK-2-13型定炭炉,天津市大港区红杉实验设备厂;S100-1B+TH10A型微流量蠕动泵,保定迪创电子科技有限公司;722S型可见分光光度计,上海精密科学仪器有限公司;特制石英玻璃反应器,东海县驼峰乡美东石英制品厂;Versa3D型场发射扫描电子显微镜,美国FEI公司;JW-BK132F型高精度全自动比表面及孔径分析仪,北京精微高博科学技术有限公司;1904型奥氏气体分析仪,上海隆拓仪器设备有限公司。
试验所用煤样及煤焦油:无烟煤,贵州省纳雍矿区;烟煤,贵州省水城矿区;煤焦油,首钢水钢煤焦化有限责任公司。煤样的工业分析和元素分析见表 1。
|
|
表 1 煤样的工业分析和元素分析 Table 1 Proximate and ultimate analyses of coal sample |
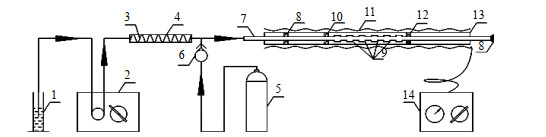
本文设计了煤制活性炭的工艺流程,其中炭化-活化部分工艺流程如图 1所示。
|
图 1 煤制活性炭炭化-活化部分工艺流程图 Fig.1 Flow chart of the carbonization-activation for preparing activated carbon from coal 1. cylinder 2. peristaltic pump 3. heater band 4. quartz tube 5. nitrogen cylinder 6. flowrator 7. copper pipe 8. silica gel stopple 9. opening of copper tube 10. single hole quartz glass 11. carbon fixing furnace 12. porous quartz glass 13. quartz glass reactor 14. temperature controller |
图中,石英玻璃反应器内置开孔铜管,将开孔石英片固定在铜管开孔区两边,石英玻璃反应器中石英片之间的区域为反应区。将质量均为20.0 g的无烟煤、烟煤及二者混合物(质量比为1:1,以下相同)分别破碎并过200目筛得到煤粉。将浓盐酸、氟硅酸与蒸馏水按质量比1:1:7混匀并加入煤粉,搅拌、抽滤、烘干后得到除灰煤粉。将水、煤焦油、除灰煤粉按质量比10:25:65混匀后装入图 1中的反应区,在温度550 ℃下炭化0.5 h并以体积流量为10 mL·min-1的氮气保护,冷却后得到炭化料。将定炭炉以速率为10 ℃·min-1升温到活化温度并通入水蒸汽。水蒸汽经铜管开孔扩散并与炭化料充分接触活化,反应气、煤焦油与水蒸汽穿过多孔石英玻璃片,煤焦油和水蒸汽经冷凝后回收,收集反应气并用奥氏气体分析仪分析其组分。
3 试验部分 3.1 各因素对活性炭亚甲蓝吸附值的影响由于亚甲蓝吸附值是衡量活性炭吸附性能的基本参数,所以选择活性炭的亚甲蓝吸附值作为指标,按GB/T 7702.6-2008测定[17-18]。选取活化温度、活化时间、水蒸汽体积流量、水蒸汽压力为因素,单因素实验和正交实验确定的煤基活性炭的最佳制备工艺条件如表 2所示。
|
|
表 2 以活性炭亚甲蓝吸附值为指标的最佳工艺条件 Table 2 The optimum conditions of water vapor activation |
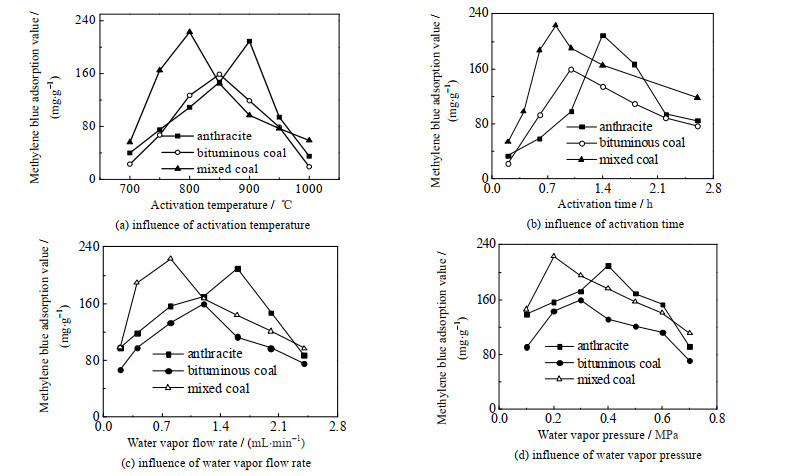
保持以上最佳工艺条件中的3个因素不变,改变另外一个因素,活性炭的亚甲蓝吸附值的变化曲线如图 2所示。
|
图 2 各因素对活性炭亚甲蓝吸附值的影响 Fig.2 Influences of activation conditions on the methylene blue adsorption values of the activated carbon |
由图 2可知,最佳工艺条件下制备的无烟煤基活性炭、烟煤基活性炭及混合煤基活性炭的亚甲蓝吸附值分别为209、159、223 mg·g-1,得率分别为44.9%、41.1%、45.3%。从图 2中可知,活化温度和活化时间的影响规律是一致的,温度过低或活化时间过短,活化不充分,其吸附能力有限;温度过高或活化时间过长,导致活性炭内部孔结构熔融坍塌,微孔扩大为大孔或中孔[19-21]。且温度过高,水蒸汽与炭反应剧烈,炭损耗过大,甚至烧损严重,活性炭的吸附能力大幅降低甚至失活。当活化温度超过1 100 ℃时,活性炭的得率迅速降至20% 以下。水蒸汽流量过小,反应速率过慢,活化程度低,当体积流量增大到一定程度,不能忽略炭化料向水蒸汽的热传导,使活化体系温度大幅降低,偏离了最佳活化温度。水蒸汽压力对活性炭亚甲蓝吸附值的影响将在3.2节讨论。
烟煤基活性炭的最佳制备条件的4因素水平均低于无烟煤基活性炭。而比起单一煤基活性炭,混合煤基活性炭的最佳制备条件的4因素水平均较低,即制备条件更加温和,且亚甲蓝吸附值的峰值也高于单一煤基活性炭。实验发现,无论是炭化过程还是活化过程,无烟煤的尾气中CH4体积分数均较低,O2与H2O体积分数均较高;而烟煤的尾气中CH4体积分数均较高,O2与H2O体积分数均较低。而相对于单一煤,混合煤的炭化过程及活化过程尾气中的CH4、O2与H2O的体积分数均大幅降低,CO、H2与CO2的体积分数则大幅提高。认为混合煤在炭化过程与活化过程发生了“协同效应”,即发生了以下3个气体膨胀反应:2CH4+O2=2CO+4H2;CH4+H2O=CO+3H2;CH4+2H2O=4H2+CO2。
由于协同效应引起的3个气体膨胀反应,混合的2种煤基炭化料在炭化过程及活化过程中发生了“体积膨胀”效应,即混合煤基炭化料在炭化过程及活化过程中的表观体积均大于无烟煤或烟煤单一煤基炭化料。无烟煤基炭化料及烟煤基炭化料在活化过程中的平均表观密度及平均热导率均存在差异(平均表观密度分别是0.94和0.69 g·cm-3,平均热导率分别为0.47和0.20 W·m-1·K-1),2种炭化料的混合形成了骨架与填料的组合结构。一方面无烟煤的加入进一步降低了烟煤基炭化料的密度(混合煤基炭化料在活化过程中的平均表观密度仅为0.54 g·cm-3),另一方面无烟煤的加入极大增强了烟煤的热传导能力。即无烟煤与烟煤的混合减小了热量传递和水蒸汽传递的阻力,所以混合煤基活性炭的亚甲蓝吸附值高于单一煤基活性炭的亚甲蓝吸附值。同时,2种单一煤基炭化料的混合规避了单一煤基炭化料分布不均引起的沟流问题,增大了水蒸汽与炭化料的接触几率[22]。
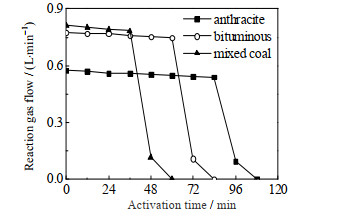
3.2 煤制活性炭的活化动力学煤制活性炭活化过程的反应器出口气包括反应气、煤焦油及水蒸汽。其中,煤焦油和水蒸汽经冷凝后循环使用,反应气(主要组分为CO、H2及CO2)收集后用奥氏气体分析仪分析瞬时组分。在表 1所示的最佳工艺条件下,反应气体积流量(标准状况)及炭化料质量随活化时间变化曲线如图 3、4所示。
|
图 3 反应气体积流量随活化时间的变化 Fig.3 Change of reaction gas flow rate with activation time |
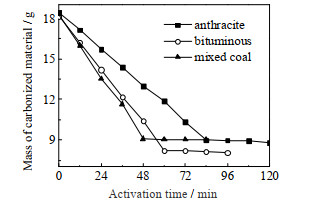
|
图 4 炭化料质量随活化时间的变化 Fig.4 Change of carbonized material mass with activation time |
从图 3、4中可以看出,在炭化料达到恒重之前,反应气的体积流量及组成基本不随活化时间变化。在其他工艺条件下也均是类似情形,即在炭化料达到恒重之前其质量线性减小,而反应气的流量与组成不变,且与活化温度、水蒸汽流量等基本无关,而水蒸汽压力对反应气体积流量及组成有重要影响。
活化过程的反应有
| ${\rm{C}} + {{\rm{H}}_{\rm{2}}}{\rm{O}} \rightleftharpoons {\rm{CO}} + {{\rm{H}}_{\rm{2}}}$ | (1) |
| ${\rm{C}} + {\rm{2}}{{\rm{H}}_{\rm{2}}}{\rm{O}} \rightleftharpoons {\rm{C}}{{\rm{O}}_{\rm{2}}} + {\rm{2}}{{\rm{H}}_{\rm{2}}}$ | (2) |
| ${\rm{2C}} + {\rm{2}}{{\rm{H}}_{\rm{2}}}{\rm{O}} \rightleftharpoons {\rm{C}}{{\rm{H}}_{\rm{4}}} + {\rm{C}}{{\rm{O}}_{\rm{2}}}$ | (3) |
| ${\rm{3C}} + {\rm{2}}{{\rm{H}}_{\rm{2}}}{\rm{O}} \rightleftharpoons {\rm{C}}{{\rm{H}}_{\rm{4}}} + {\rm{2CO}}$ | (4) |
由于历次实验反应气中CH4的体积分数均低于1%,因此忽略式(3)、(4)。将活化过程认为是温度、速率恒定且存在固定相(活性炭)的C的缓慢气化过程,引入化学反应工程学方法,炭化料表面能与气相分子起反应的原子称为活性中心,用σ表示。假设CO、CO2及H2不吸附,将活化过程的气固相反应的机理步骤写作:
| $ \mathrm{H}_{2} \mathrm{O} \text { 在 } \sigma \text { 上的吸附过程 }~~~~{{\rm{H}}_{\rm{2}}}{\rm{O}} + {\rm{ \mathsf{ σ} }} \rightleftharpoons {{\rm{H}}_{\rm{2}}}{\rm{O \mathsf{ σ} }} $ | (5) |
| $ 生成 \mathrm{CO} 的表面反应过程~~~~{\rm{C}} + {{\rm{H}}_{\rm{2}}}{\rm{O \mathsf{ σ} }} \rightleftharpoons {\rm{CO}} + {{\rm{H}}_{\rm{2}}} + {\rm{ \mathsf{ σ} }} $ | (6) |
| $ 生成 \mathrm{CO}_{2} 的表面反应过程~~~~~{\rm{C}} + {\rm{2}}{{\rm{H}}_{\rm{2}}}{\rm{O \mathsf{ σ} }} \rightleftharpoons {\rm{C}}{{\rm{O}}_{\rm{2}}} + {\rm{2}}{{\rm{H}}_{\rm{2}}} + {\rm{2 \mathsf{ σ} }} $ | (7) |
假设表面反应过程为控制步骤,则本征反应速率式为
| ${r_2} = {k_2}{\theta _{{{\rm{H}}_{\rm{2}}}{\rm{O}}}} - {k'_2}{p^2}{\varphi _{{\rm{CO}}}}{\varphi _{{{\rm{H}}_{\rm{2}}}}}{\theta _{\rm{v}}}$ | (8) |
| ${r_3} = {k_3}{\theta _{{{\rm{H}}_{\rm{2}}}{\rm{O}}}}^2 - {k'_3}{p^3}{\varphi _{{\rm{C}}{{\rm{O}}_{\rm{2}}}}}{\varphi _{{{\rm{H}}_{\rm{2}}}}}^2{\theta _{\rm{v}}}^2$ | (9) |
式中:
由于水蒸汽是过量的,在整个活化过程,均有出口气中H2O的体积分数
| ${r_{\rm{2}}} = {k_{\rm{2}}}{\theta _{{{\rm{H}}_{\rm{2}}}{\rm{O}}}}$ | (10) |
| ${r_{\rm{3}}} = {k_3}{\theta _{{{\rm{H}}_{\rm{2}}}{\rm{O}}}}^{\rm{2}}$ | (11) |
此时吸附已达到平衡,即
| ${r_1} = {k_{\rm{1}}}{p_{{{\rm{H}}_{\rm{2}}}{\rm{O}}}}{\theta _{\rm{v}}} - {k'_{\rm{1}}}{\theta _{{{\rm{H}}_{\rm{2}}}{\rm{O}}}} = 0$ | (12) |
式中:
同时根据覆盖率定义:
| ${\theta _{{{\rm{H}}_{\rm{2}}}{\rm{O}}}} + {\theta _{\rm{v}}} = 1$ | (13) |
由式(12)有
| $ {\theta _{{{\rm{H}}_{\rm{2}}}{\rm{O}}}} = \frac{{{k_1}}}{{{{k'}_1}}}{p_{{{\rm{H}}_{\rm{2}}}{\rm{O}}}}{\theta _{\rm{v}}} = {K_{\rm{1}}}{p_{{{\rm{H}}_{\rm{2}}}{\rm{O}}}}{\theta _{\rm{v}}},其中{K_{\rm{1}}} = \frac{{{k_1}}}{{{{k'}_{\rm{1}}}}} $ | (14) |
式中:
| $ 将式(14)代入(13),有 ~~~~ {\theta _{\rm{v}}} = \frac{1}{{1 + {K_{\rm{1}}}{p_{{{\rm{H}}_{\rm{2}}}{\rm{O}}}}}} $ | (15) |
| ${\theta _{{{\rm{H}}_{\rm{2}}}{\rm{O}}}} = \frac{{{K_{\rm{1}}}{p_{{{\rm{H}}_{\rm{2}}}{\rm{O}}}}}}{{1 + {K_{\rm{1}}}{p_{{{\rm{H}}_{\rm{2}}}{\rm{O}}}}}}$ | (16) |
出口气经冷凝除去水蒸汽和煤焦油后得到反应气。将反应气中CO与CO2体积分数之比记为
| $H = \frac{{{{\varphi '}_{{\rm{CO}}}}}}{{{{\varphi '}_{{\rm{C}}{{\rm{O}}_{\rm{2}}}}}}} = \frac{{{r_2}}}{{{r_3}}}$ | (17) |
式中:
将式(10)、(11)、(16)代入(17),得到
| $ H = \frac{{{{\varphi '}_{{\rm{CO}}}}}}{{{{\varphi '}_{{\rm{C}}{{\rm{O}}_{\rm{2}}}}}}} = \frac{{{k_{\rm{2}}}}}{{{k_{\rm{3}}}{\theta _{{{\rm{H}}_{\rm{2}}}{\rm{O}}}}}} = \frac{{K'}}{{{p_{{{\rm{H}}_{\rm{2}}}{\rm{O}}}}}} + K'',其中K' = \frac{{{k_{\rm{2}}}}}{{{k_{\rm{3}}}{K_{\rm{1}}}}}, K'' = \frac{{{k_2}}}{{{k_3}}} $ | (18) |
式中:
从式(18)可知,CO与CO2在反应气中的体积分数之比与水蒸汽绝对压力
质量均为20.0 g的无烟煤、烟煤及混合煤在图 1所示的流程中经炭化后分别在900、850、800 ℃下活化1.4、1.0、0.8 h,水蒸汽体积流量分别为1.60、1.20、0.80 mL·min-1,收集全部反应气并用奥氏气体分析仪测定其组分含量。改变水蒸汽压力
|
|
表 3 pH2O和H的实验值 Table 3 The experimental values of the pH2O and H |
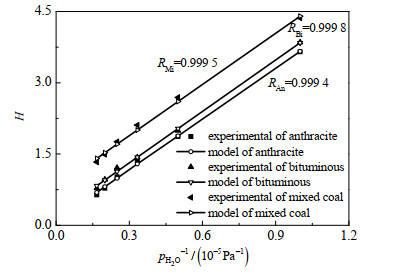
用式(18)拟合表 3数据,最小二乘法确定的拟合曲线及实验值如图 5所示。
|
图 5 H的模型计算值 Fig.5 H calculated values on models |
无烟煤制活性炭活化过程反应气组成拟合曲线为
保持活化时间及水蒸汽体积流量不变,改变水蒸汽压力
|
|
表 4 不同活化温度下K'和K"的回归值 Table 4 Regression values of K' and K"at different activation temperatures |
不同活化温度下,无烟煤、烟煤及二者混合煤的拟合直线的斜率
将
| $ \ln K'' = - \frac{{\Delta E}}{{RT}} + \ln A,其中\Delta E = {E_{\rm{2}}} - {E_{\rm{3}}}, A = \frac{{{k_{{\rm{20}}}}}}{{{k_{{\rm{30}}}}}} $ | (19) |
式中:
由3.2节结论,
| $ B = \frac{A}{{K'}},其中B = \frac{{{k_{{\rm{10}}}}}}{{{{k'}_{{\rm{10}}}}}} $ | (20) |
式中:
将表 4的数据代入式(19)、(20)进行线性拟合得到
|
|
表 5 ΔE、A和B的回归值 Table 5 Regression values of ΔE, A and B |
即在活化过程各反应速率式均符合Arrhenius方程的情形下,斜率
由式(6)、(7)可知,活化过程反应气中3种主要组分CO2、CO和H2的体积分数满足
由式(15)、(16)可知,在水蒸汽压力
现在讨论水蒸汽压力
采用美国FEEI公司Versa3D型场发射扫描电子显微镜进行扫描,原煤及表 2所确定的最佳工艺条件下制得的活性炭的SEM照片如图 6所示。

|
图 6 煤与煤基活性炭产品的SEM照片 Fig.6 SEM photos of the coal and the coal based activated carbon products |
将煤基活性炭与原煤进行对比,可以明显看出原煤表面光滑且有光泽,而煤基活性炭的表面粗糙且疏松多孔。无烟煤基活性炭与烟煤基活性炭呈现蜂窝状多孔结构,而混合煤基活性炭则呈现出“酥饼”的结构,其孔隙更为发达,结构更为疏松。测得无烟煤基活性炭、烟煤基活性炭、混合煤基活性炭的表观密度分别为0.74、0.81、0.70 g·cm-3,其规律为混合煤﹤无烟煤﹤烟煤,与SEM结果一致。由于协同效应,混合煤基炭化料及混合煤基活性炭的密度均为最低。而烟煤炭化料经活化后,得率较低,即碳损耗较高。而烟煤的灰分较高,由于灰分的密度远大于活性炭,导致烟煤基活性炭的密度大于无烟煤基活性炭。
采用北京精微高博科学技术有限公司生产的JW-BK132F型高精度全自动比表面及孔径分析仪对最佳工艺条件下制备的煤基活性炭进行BET比表面测试及微孔分析(HK法;<2 nm孔),所制无烟煤基活性炭、烟煤基活性炭及混合煤基活性炭的BET比表面积分别为1 121.37、908.58、1 342.88 m2·g-1,吸附累积微孔总孔体积分别是0.28、0.18、0.32 m3·g-1。3种贵州煤基活性炭的BET比表面积均超过800 m2·g-1。其中混合煤基活性炭不仅其SEM结果表明其结构更为疏松,且其BET比表面积也最高。即在最佳工艺条件下,无论是亚甲蓝吸附值、BET比表面积还是吸附累积微孔总孔体积,均是混合煤基活性炭高于单一煤基活性炭。混合煤基活性炭的最可几孔径仅为0.58 nm,说明其微孔比例高于单一煤基活性炭。协同效应生成的CO、H2等小分子的气体膨胀效应在活性炭内部形成部分微孔,一方面增大了活性炭比表面积,另一方面增大了微孔比例。
目前,国内应用于活性炭生产最多的是宁夏太西无烟煤和山西大同烟煤。以上2种煤在图 1所示的流程中所制活性炭的亚甲蓝吸附值分别为154、149 mg·g-1,得率分别为40.7%、40.1%,比表面积分别为848.34、814.17 m2·g-1,最可几孔径分别为0.71、0.73 nm。即其亚甲蓝吸附值、得率、比表面积及微孔比例均低于贵州煤基活性炭,说明贵州煤是制备活性炭的优良原料。而相对于太西无烟煤及大同烟煤,贵州煤具有显著的高碳、低灰及低硫特征。
5 结论(1) 混合煤基活性炭的亚甲蓝吸附值及BET比表面积均高于单一煤基活性炭,且其工艺制备条件更加缓和,说明发生了协同效应。
(2) 建立了气固相反应动力学,3条拟合H函数基本平行,说明水蒸汽压力对活化反应气组分的影响程度相同。
(3) 发现在炭化料达到恒重之前,活化反应的速率趋于恒定,并从反应动力学角度进行了证明。
(4) 动力学方程证明了水蒸汽压力对活化过程反应速率的影响规律。
(5) 比起太西无烟煤及大同烟煤,贵州煤是制备活性炭的更加优良的原料。
| [1] |
李栋, 汪印, 杨娟, 等. 生物质和煤基活性炭制备过程的活化特性比较[J]. 化工学报, 2013, 64(9): 3338-3347. LI D, WANG Y, YANG J, et al. Activation characteristics comparison of activated carbons prepared from biomass and lignite[J]. CIESC Journal, 2013, 64(9): 3338-3347. |
| [2] |
吴小华, 徐龙君, 刘科, 等. 煤基活性炭制备工艺对吸附铜离子性能的影响[J]. 煤炭转化, 2013, 36(3): 76-79. WU X H, XU L J, LIU K, et al. Effect of coal-based activated carbon preparation process on Cu(Ⅱ) adsorption capacity[J]. Coal Conversion, 2013, 36(3): 76-79. |
| [3] |
LI W, ZHU Y M. Structural characteristics of coal vitrinite during pyrolysis[J]. Energy Fuels, 2014, 28(6): 3645-3654. DOI:10.1021/ef500300r |
| [4] |
董丹丹, 杨省师, 程晓峰, 等. 煤基活性炭不同制备方法对其性质影响的研究[J]. 洁净煤技术, 2009, 16(2): 87-89. DONG D D, YANG S S, CHEN X F, et al. Preliminary study on influence of different preparation method to coal-based activated carbon[J]. Clean Coal Technology, 2009, 16(2): 87-89. |
| [5] |
岳晓明, 吴雅俊, 张双全, 等. 物理化学两步活化法制备煤基活性炭电极材料[J]. 中国矿业大学学报, 2017, 46(4): 888-894. YUE X M, WU Y J, ZHANG S Q, et al. Preparation of coal-based activated carbon electrodes by two steps of physical-chemical activation[J]. Journal of China University of Mining & Technology, 2017, 46(4): 888-894. |
| [6] |
LI T T, ZHANG L, DONG L, et al. Effects of gasification atmosphere and temperature on char structural evolution during the gasification of collie subbituminous coal[J]. Fuel, 2014, 117: 1190-1195. DOI:10.1016/j.fuel.2013.08.040 |
| [7] |
LIU D D, GAO J H, CAO Q X, et al. Improvement of activated carbon from Jixi Bituminous coal by air peroxidation[J]. Energy Fuels, 2017, 31(2): 1406-1415. DOI:10.1021/acs.energyfuels.6b02875 |
| [8] |
BUTUZOVA L, MARINOV S P, MAKOVSKYI R, et al. Extracts of the plastic layer of coals of different reductivity type and their blends[J]. Bulgarian Chemical Communications, 2015, 47(4): 1028-1033. |
| [9] |
解强. 煤基活性炭定向制备的概念与原理[J]. 西北煤炭, 2003, 1(2): 19-24. XIE Q. Concept and principles of directional preparation of coal-based activated carbon[J]. Northwest Coal, 2003, 1(2): 19-24. |
| [10] |
JIMÉNEZ-CORDERO D, HERAS F, GILARRANZ M A, et al. Grape seed carbons for studying the influence of texture on supercapacitor behaviour in aqueous electrolytes[J]. Carbon, 2014, 71: 127-138. DOI:10.1016/j.carbon.2014.01.021 |
| [11] |
MENG F, YU J, TAHMASEBI A, et al. Characteristics of chars from low-temperature pyrolysis of lignite[J]. Energy & Fuels, 2014, 28(1): 275-284. |
| [12] |
CHOI P R, LEE E, KWON S H, et al. Characterization and organic electric-double-layer-capacitor application of KOH activated coal-tar-pitch-based carbons: Effect of carbonization temperature[J]. Journal of Physics Chemistry of Solids, 2015, 87(1): 72-79. |
| [13] |
WANG X G, ZHANG Y, DONG L, et al. Experimental study on the pyrolysis of Shenhua coal to produce hydrogen[J]. Journal of Thermal Science, 2013, 22(1): 282-286. |
| [14] |
邢宝林, 谌伦建, 张传祥, 等. NaOH活化法制备煤基活性炭的研究[J]. 煤炭转化, 2010, 33(1): 69-73. XING B L, CHEN L J, ZHANG C X, et al. Study on preparation of coal-based activated carbons by NaOH activation[J]. Coal Conversion, 2010, 33(1): 69-73. |
| [15] |
倪小明, 苏现波, 张小东. 煤层气开发地质学[M]. 北京: 化学工业出版社, 2010. NI X M, SU X B, ZHANG X D. Coal bed methane development geology[M]. Beijing: Chemical Industry Press, 2010. |
| [16] |
房俊卓, 何康丽, 马琴, 等. 太西煤及其煤基活性炭制备纳米碳化硅的比较[J]. 煤炭转化, 2016, 39(3): 82-85. FANG J Z, HE K L, MA Q. Comparison between nano silicon carbide made from Taixi coal and its coal-based activated carbon[J]. Coal Conversion, 2016, 39(3): 82-85. |
| [17] |
WU D. An experimental investigation on heating rate effect in the thermal behavior of perhydrous bituminous coal during pyrolysis[J]. Journal of Thermal Analysis & Calorimetry, 2015, 119(3): 2195-2203. |
| [18] |
TANNER J, KABIR K B, MULLER M, et al. Low temperature entrained flow pyrolysis and gasification of a victorian brown coal[J]. Fuel, 2015, 154: 6364-6367. |
| [19] |
STENEHJEM E D, ZIATDINOV V R, STACK T D P, et al. Gas-phase azide functionalization of carbon[J]. Journal of the American Chemical Society, 2013, 135(3): 1110-1116. |
| [20] |
ZHOU X X, QU X, ZHANG R, et al. Study of the microtextural transformation of coal char during supercritical water activation[J]. Fuel Processing Technology, 2015, 135(SI): 195-202. |
| [21] |
LIU H Y, XU L, JIN Y, et al. Effect of coal rank on structure and dielectric properties of chars[J]. Fuel, 2015, 153: 249-256. |
| [22] |
YANG X, ZHANG C, TAN P, et al. Properties of upgraded Shengli lignite and its behavior for gasification[J]. Energy Fuels, 2014, 28(1): 264-274. |




