2. 西昌学院 轻化工程学院,四川 西昌 610000
2. School of Applied and Chemical Engineering of Xichang College, Xichang 610000, China
糠醛渣是玉米芯、玉米秆、稻壳、棉籽壳以及花生壳和甘蔗渣等农副产品的下脚料的聚戊糖成分水解生产糠醛(呋喃甲醛)产生的生物质废弃物[1]。生产每吨糠醛会产生12~15吨的糠醛渣,我国糠醛渣年总量可达几百万吨[2],其盐分含量高、呈酸性,大量堆积会对大气、土壤、河流造成污染[3]。但糠醛渣含有大量的纤维素,具有良好的再利用价值。因此,合理地资源化利用糠醛渣,消除其对环境的污染,同时增加糠醛渣的经济附加值,对实现绿色环保经济具有重大意义。
目前对糠醛渣的利用主要体现在以下几个方面:1)糠醛渣作为有机肥原料;2)用于改善土壤盐碱沙漠化[4];3)制备木质素基炭黑[5]。以上利用方式均存在利用量少、利用率低的问题。要解决工业糠醛渣的大规模有效利用,需对其纤维成分进行水解综合利用。目前主要是采用纤维素酶对糠醛渣进行水解[6],尽管纤维素转化率达到78%,但是纤维素酶具有成本高、难回收及反应时间长等缺点,从成本和效率上考虑都不是最理想选择。考虑到经济性及绿色环保的要求,探索更佳的糠醛渣纤维素水解方法是实现工业糠醛渣合理利用和解决其污染问题的关键。
纤维素水解的方法主要有浓酸水解法、稀酸水解法和酶水解法[7]。浓硫酸水解的研究比较早,技术较为成熟。但由于浓酸的使用及酸的回收较为困难,限制了该方法的发展;酶水解选择性高,糖产率高,但是时间长、成本高,且原料须经预处理;稀酸水解温度高,条件剧烈且影响因素较多,但稀酸水解是目前最广泛的纤维素水解方法,因为使用酸的浓度较低,可以不用回收。
本文首先进行了稀酸体系水解糠醛渣纤维素的条件研究,在此基础上,重点探究了醇酸体系乙醇用量及水解时间对糠醛渣纤维素水解的影响,并与稀酸体系水解糠醛渣纤维素的效果进行了对比分析。
2 实 验 2.1 原料、试剂及仪器原料来源于山东某糠醛厂的玉米芯糠醛渣。
地衣酚、氯化铁、浓硫酸、糠醛、乙二胺四乙酸、十水四硼酸钠、十二烷基硫酸钠、十六烷基三甲基溴化铵、3,5-二硝基水杨酸、氢氧化钠、D-木糖、无水葡萄糖、乙二醇乙醚、无水乙醇、磷酸氢二钠、苯酚等均为分析纯。
电子天平:上海力能电子仪器公司;恒温水浴锅:余姚市东方电工仪器厂;DGG-9140AD型电热恒温鼓风干燥箱:上海森信实验仪器有限公司;TU-1810型紫外可见分光光度计:北京普析通用仪器有限责任公司;98-1-B型电子调温加热套:天津市泰斯特仪器有限公司;SHB-Ⅲ型循环水式多用真空泵:郑州长城科工贸有限公司;AUY220型精密电子天平。
2.2 分析方法 2.2.1 还原糖含量测定采用DNS法[8](1) 葡萄糖标准曲线的绘制:在6支试管内分别加入1 mg⋅mL-1标准葡萄糖溶液0.0、0.2、0.4、0.6、0.8、1.0 mL,加入DNS试剂2 mL,补加蒸馏水至5 mL,摇匀后置于沸腾的水浴中加热5 min取出,迅速用自来水冷却至室温,定容至20 mL,摇匀,静置30 min待其吸光度稳定,用紫外分光光度计在520 nm处测吸光度,绘制标准曲线。
(2) 水解液中葡萄糖含量的测定:先把水解液稀释一定倍数,取1 mL稀释后的水解液加入试管中,按上述步骤做相同处理,以空白试剂作为对照,用紫外分光光度计在520 nm处测吸光度。
2.2.2 采用Van Soest法测定半纤维素、纤维素、木质素含量[9~11](1) 计算中洗纤维量(NDF)的含量:取1 g干燥糠醛渣样本,置于500 mL烧杯中,加入100 mL中性洗溶液,在电加热套上加热沸腾5~10 min后,降低火强度,保持微沸状态60 min,接着用预先称重的定性滤纸抽滤,用90℃水洗涤2次,后用丙酮清洗、过滤2次。最后于干燥箱内低温干燥24 h,称重并计算中洗纤维量。
(2) 计算酸洗纤维量(ADF)的含量:取1 g干燥糠醛渣样本,置于500 mL烧杯中,加入100 mL酸性洗溶液,在电加热套上加热沸腾5~10 min后,降低火强度,保持微沸状态60 min,接着用预先称重的定性滤纸抽滤,用90℃水洗涤2次,后用丙酮清洗、过滤2次。最后于干燥箱内低温干燥24 h,称重并计算酸洗纤维量。
(3) 计算酸洗木质素(ADL)的含量:延续酸洗纤维的实验,将酸洗纤维置于50 mL烧杯中,加入25 mL72% 的硫酸并搅拌成糊状,之后每小时加入2 mL 72% 的硫酸,连续反应3 h,接着使用预先称重的滤纸抽滤,然后以90℃ 热水清洗并过滤5次,再在干燥箱内低温干燥24 h,称重并计算酸洗木质素含量。
(4) 计算半纤维素含量:样品中中洗纤维(NDF)与酸洗纤维(ADF)的差值,即为半纤维素含量。
(5) 计算纤维素含量:样品中酸洗纤维(ADF)与酸洗木质素(ADL)之差,即为纤维素含量。
(6) 计算木质素含量:将所得酸洗木质素(ADL)的质量减去灰分的质量,即为木质素含量。
2.3 计算公式| $葡萄糖标准曲线~y=0.001x-0.109{{R}^{2}}=0.9993$ |
| $纤维素水解率\left( Hydrolysis\text{ }rate\text{ }of\text{ }cellulose,\text{ }HRC \right)=\frac{水解的纤维素质量}{原料中纤维素质量}\times 100%$ |
| $葡萄糖实际产率\left( \text{Actual yield of glucose, AYG} \right)=\frac{水解液中葡萄糖的实际产量}{糠醛渣原料纤维素折合的葡萄糖量}\times 100%$ |
| $葡萄糖理论产率\left( \text{Theoretical yield of glucose, TYG} \right)=\frac{水解液中葡萄糖的理论产量}{糠醛渣原料纤维素折合的葡萄糖量}\times 100%$ |
| $葡萄糖收率\left( \text{Yield of glucose, YG} \right)=\frac{水解液中葡萄糖实际产量}{水解液中葡萄糖理论产量}\times 100%$ |
| $木质素去除率\left( \text{Removal rate of lignin RRL} \right)=\frac{原料中木质素质量残渣中木质素质量}{原料中木质素质量}\times 100%$ |
取一定量的糠醛渣,置于500 mL的三口烧瓶中,液固比为5:1 mL⋅g-1,稀酸水解体系中加入稀硫酸水解液,醇酸水解体系中加入稀硫酸和乙醇混合水解液,助剂氯化铁含量为7%。充分振荡使水解液和糠醛渣混合均匀后加热至沸腾,加热回流反应1.5 h后,每隔半小时取样分析,直到样品中还原糖浓度(纤维素水解产生的还原性糖主要为葡萄糖)不再改变,停止反应。冷却后用滤布进行压滤,将滤液装入锥形瓶中密封保存。水解后的残余糠醛渣置于50℃ 的烘箱中干燥24 h后,用于残渣分析。以纤维素水解率、葡萄糖产率、收率作为指标考察水解效果。
3 结果与讨论 3.1 稀酸水解工业糠醛渣纤维素 3.1.1 硫酸浓度对纤维素水解率的影响液固比(mL⋅g-1)为5,助剂氯化铁含量为7%,硫酸体积分数分别取2%、4%、6%、8%、10%,加热回流4 h,水解过程中体系温度分别为100、100、100、101、102℃,考察纤维素水解效果(如图 1)。
|
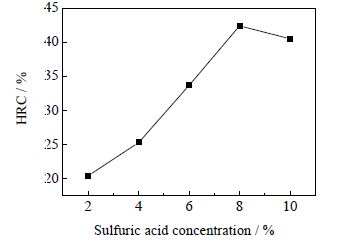
图 1 硫酸浓度对纤维素水解率的影响 Fig.1 Effects of sulfuric acid concentration on cellulose hydrolysis |
由图 1可知,在硫酸浓度低于8% 时,纤维素水解率随硫酸浓度升高而不断增加;硫酸浓度达到8%,纤维素水解率达最大值42.4%,而后,随着硫酸浓度升高,纤维素水解率出现下降趋势。主要原因在于,硫酸可以隔断纤维组分间的连接键,使得水解液中的氢离子和纤维素上的氧原子结合,并与水发生反应,纤维素长链断开,发生水解反应。在较低酸浓度条件下,随着水解进行,溶液中氢离子浓度不断升高,木质素去除率增加,纤维素水解率不断升高;硫酸浓度达到10% 时,纤维素水解率出现下降,是因为随着酸浓度的升高,水解液中溶入的木质素影响了水解液中氢离子与纤维素结合导致水解率下降。考虑到经济成本和操作安全,在稀酸水解纤维素过程中,确定硫酸最佳浓度为8%。
3.1.2 不同硫酸浓度条件下水解时间对纤维素水解率的影响液固比(mL⋅g-1)为 5,助剂氯化铁含量为 7%,硫酸体积分数分别取 2%、4%、6%、8%、10%,分别加热回流 1、2、3、4 h,考察纤维素水解效果(如图 2)。
|
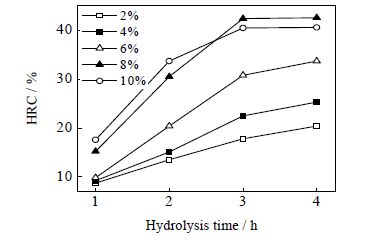
图 2 不同硫酸浓度下水解时间对纤维素水解率的影响 Fig.2 Effects of hydrolysis time on cellulose hydrolysis rate under different sulfuric acid concentrations |
由图 2可知,硫酸浓度低于8% 时,相同的水解时间内,随着酸浓度升高,纤维素水解率逐渐增加,说明在一定范围内,酸浓度越高,越能促进纤维素水解;达到相同纤维素水解率,硫酸浓度越高,所需时间越短。当硫酸浓度8%、水解时间3 h,水解率达到最大值42.4%,延长水解时间,水解率变化不大;硫酸浓度10%、水解时间小于2.5 h,纤维素水解率高于其它酸浓度,水解时间大于2.5 h反而低于8% 酸浓度下的水解率,说明低浓度的硫酸可以促进纤维素的水解,酸浓度高于8%,会对纤维素水解产生一定的抑制作用,使纤维素水解率下降。
3.1.3 硫酸浓度对葡萄糖产率、收率的影响液固比(mL⋅g-1) 为5,助剂氯化铁含量为7%,硫酸体积分数分别取2%、4%、6%、8%、10%,加热回流4 h,考察葡萄糖产率及收率如图 3和图 4。
|
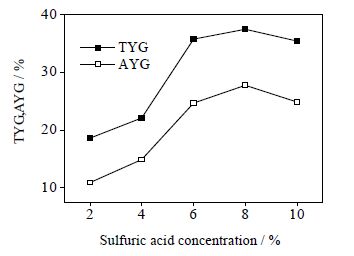
图 3 硫酸浓度对葡萄糖理论及实际产率的影响 Fig.3 Effects of sulfuric acid concentration on actual and theoretical glucose yield |
|
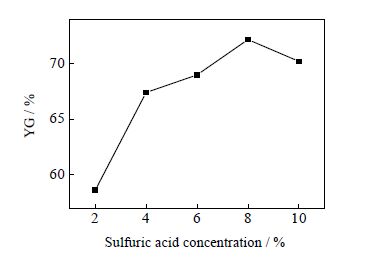
图 4 硫酸浓度对葡萄糖收率的影响 Fig.4 Effects of sulfuric acid concentration on glucose yield |
由图 3和图 4可知,葡萄糖产率及收率均随硫酸浓度的升高先增加后减少,与纤维素水解率的变化趋势是一致的。在硫酸浓度小于8%,葡萄糖产率及收率随硫酸浓度升高而不断增加,其原因在于随着酸浓度升高,纤维素水解率不断增大,生成葡萄糖量增多,葡萄糖产率及收率也随之升高;硫酸浓度升至大于8%,纤维素水解率下降,葡萄糖生成量减少,葡萄糖产率和收率都开始下降。由图 3中,葡萄糖理论产率和实际产率的对比可知:当硫酸浓度小于6%,葡萄糖理论产率和实际产率相差较小,说明葡萄糖损失较小;而硫酸浓度升高至大于6%,理论产率和实际产率差距变得明显,说明硫酸浓度升高使水解液中葡萄糖发生降解,葡萄糖损失增加,导致实际产率偏低。
3.2 醇酸水解工业糠醛渣纤维素 3.2.1 醇浓度对纤维素水解率的影响液固比(mL⋅g-1)为5,助剂氯化铁含量为7%,硫酸体积分数为8%,乙醇体积分数分别为20%、30%、40%、50%、60%、70%,水解过程中体系温度分别为87、84、83、82、81、80℃,考察纤维素水解效果(如图 5)。
|
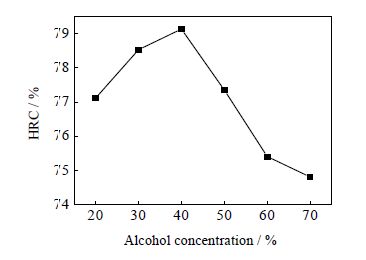
图 5 醇浓度对纤维素水解率的影响 Fig.5 Effects of alcohol concentration on cellulose hydrolysis rate |
由图 5可知,纤维素水解率随乙醇浓度的增加呈现先升高后下降的趋势。当乙醇浓度40%,纤维素水解率达到最大值60.1%;之后,随着乙醇浓度升高,纤维素水解率急剧下降,乙醇浓度为70% 时,纤维素水解率不足40%。主要原因在于,低浓度乙醇条件下,乙醇能够较好地溶解木质素,使得木质素对纤维素水解的干扰减弱,有利于纤维素水解;而醇浓度大于50% 会减弱酸与纤维的接触性,不能剥离纤维组分之间的相互联系,进而影响纤维素水解,导致纤维素水解率下降。
3.2.2 不同醇浓度条件下水解时间对纤维素水解率的影响液固比(mL⋅g-1)为5,助剂氯化铁含量为7%,硫酸体积分数8%,乙醇体积分数分别取0%、20%、30%、40%、50%,分别加热回流1、2、3、4 h,考察纤维素水解效果(如图 6)。
|
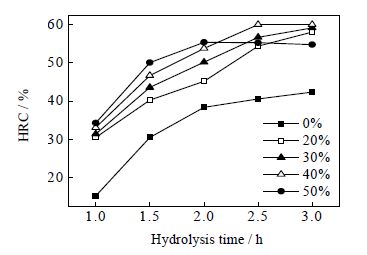
图 6 不同浓度乙醇的水解时间对纤维素水解率的影响 Fig.6 Effects of hydrolysis time on cellulose hydrolysis rate under different ethanol concentrations |
由图 6可知,相同水解时间内,添加了乙醇的醇酸体系中纤维素水解率均高于不加乙醇的稀酸体系,即乙醇的加入明显提高了纤维素水解率。稀酸体系中水解3 h后,纤维素水解率达到最大值42.4%;醇酸体系中乙醇浓度40%、水解2.5 h,纤维素水解率60.04%,延长水解时间,水解率变化不大。在乙醇浓度小于40% 时,相同的水解时间内,随着乙醇浓度升高,纤维素水解率逐渐增加,说明在一定范围内,乙醇浓度越高,纤维素水解效果越好;当乙醇浓度升高至50%,水解2 h,纤维素水解率达到最大值55.4%,与乙醇浓度40% 时水解率比,纤维素水解率降低,说明低浓度的乙醇可以有效促进纤维素的水解,但是当醇浓度高于40%,会对纤维素水解产生抑制作用,导致纤维素水解率下降。
3.2.3 醇浓度对葡萄糖产率、收率的影响液固比(mL⋅g-1)为5,助剂氯化铁含量为7%,硫酸体积分数8%,加热回流4 h,考察葡萄糖产率及收率(如图 7、8)。
|
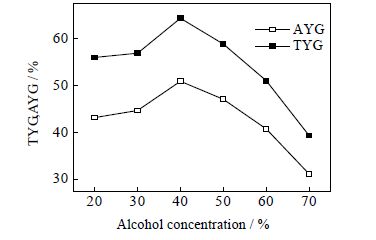
图 7 乙醇浓度对葡萄糖理论及实际产率的影响 Fig.7 Effects of alcohol concentration on actual and theoretical glucose yield |
|
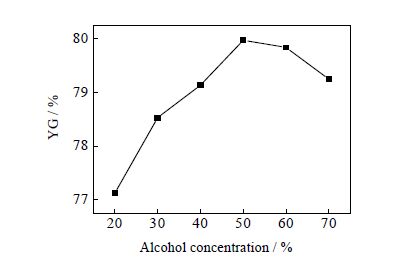
图 8 乙醇浓度对葡萄糖收率的影响 Fig.8 Effects of alcohol concentration on glucose yield |
由图 7和图 8知,葡萄糖产率及收率随乙醇浓度增加均呈现先升高后下降的趋势。在乙醇浓度低于40%,葡萄糖产率和收率均随乙醇浓度的增加而升高;当乙醇浓度40%,葡萄糖产率和收率均达到最大值,分别为50.9%、79.1%;之后随着乙醇浓度增加葡萄糖产率及收率均随乙醇浓度升高而不断下降。原因是低浓度乙醇不仅可以促进纤维素水解而且可以很好的保护葡萄糖,水解液中葡萄糖量不断增加,葡萄糖产率及收率随之升高;乙醇浓度大于40%,纤维素水解率下降,产生的葡萄糖量减少,导致葡萄糖产率及收率降低。图 7中,葡萄糖实际产率和理论产率的差距随着乙醇浓度的升高逐渐减小,说明乙醇浓度升高对水解液中的葡萄糖的保护作用越好,但是乙醇浓度升高对纤维素水解的抑制作用更明显,导致纤维素水解率下降,葡萄糖产率、收率也随之降低。
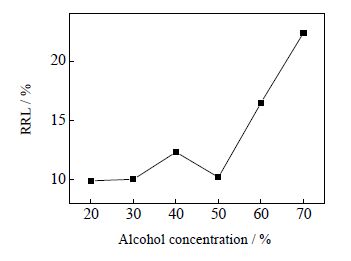
3.2.4 醇浓度对木质素去除率的影响液固比(mL⋅g-1)为5,助剂氯化铁含量为7%,硫酸体积分数为8%,乙醇体积分数分别为20%、30%、40%、50%、60%、70%,考察木质素去除效果(如图 9)。
|
图 9 乙醇浓度对木质素去除率的影响 Fig.9 Effects of alcohol concentration on lignin removal rate |
由图 9可知,木质素去除率基本随着乙醇浓度的增加而增加,只在50% 时出现了下降趋势,并且处于低谷,在超过50% 的浓度后木质素的去除率又上升。可见乙醇确实对脱除木质素有作用,并且在一定范围内随着木质素的脱出率增加而上升。虽然乙醇浓度较高时,对木质素的脱除效果较好,但是大量的木质素在酸性环境中会产生缩合作用形成不溶的体型结构,从而使得剩余纤维素更加难以渗透,难以水解,所以在水解过程中控制乙醇浓度在40% 既可以得到较高的纤维素水解率又可以较好的去除木质素。
4 结 论(1) 分别用稀酸和醇酸体系对糠醛渣纤维素水解制葡萄糖进行探究。硫酸浓度8%、水解温度101℃、水解时间3 h,纤维素水解率42.4%、葡萄糖产率27.8%、收率72.2%;在酸浓度8%、乙醇浓度40%、水解温度83℃、水解时间2.5 h下,纤维素水解率达到60.1%、葡萄糖产率50.9%、收率79.1%。与稀酸水解体系比较,纤维素水解率提高29.4%、葡萄糖产率提高45.4%、收率提高9.6%、水解时间减少0.5 h、水解温度降低18℃。
(2) 糠醛渣纤维素在醇酸体系中的水解效果明显优于稀酸体系,因为有机溶剂可以脱除木质素,具有溶剂可回收、对环境污染少等优点,在有机溶剂处理的同时加入催化剂氯化铁能够明显地降低反应温度、有效促进纤维素水解,而且反应体系稳定、操作简单、有效降低能耗。实验中所用乙醇可回收利用,回收率在90% 以上。醇酸体系水解糠醛渣纤维素为糠醛渣的合理利用提供了新的方法,对提高糠醛渣的利用价值、减少糠醛渣资源浪费和保护环境均具有积极意义。
| [1] | WANG Su-fen(王素芬), SU Dong-hai(苏东海) . Research progress of agricultural utilization of furfural residue(废物糠醛渣的农业利用研究进展)[J]. Journal of Hebei Agricultural Sciences(河北农业科学) , 2009, 13 (11) : 97-99 |
| [2] | YIN Yu-lei(尹玉磊), LI Ai-min(李爱民), MAO Liao-yuan(毛燎原) . Progress in utilization of furfural residue utilization technology(糠醛渣综合利用技术研究进展)[J]. Modern Chemical Industry(现代化工) , 2011, 31 (11) : 22-24 |
| [3] | YANG Rui (阳瑞). A new exploration of the comprehensive utilization of furfural residues (糠醛渣综合利用新探索) [D]. Guangzhou (广州) : South China University of Technology (华南理工大学), 2011. |
| [4] | LUO Cheng-ke(罗成科), LÜ Wen(吕雯), XU Xing(许兴) . The effect of furfural residue improved Solonetzic soil in northern Yinchuan(利用糠醛渣改良银川北部碱化土壤的效果)[J]. Jiangsu Agricultural Sciences(江苏农业科学) , 2008 (3) : 232-234 |
| [5] | WU Mei-dan (吴美丹). The preparation of carbon black with furfural residues and its modification of the rubber (糠醛渣制备炭黑及炭黑改性橡胶) [D]. Guangzhou (广州) : South China University of Technology (华南理工大学), 2012. |
| [6] | ZHANG Lei(仉磊), LI Tao(李涛), WANG Lei(王磊) . Enzymatic hydrolysis of corncob residues of furfural manufacture and optimum conditions for cellulose conversion(糠醛渣的纤维素酶水解及其最优纤维素转化条件)[J]. Transactions of the CSAE(农业工程学报) , 2009, 25 (10) : 226-230 |
| [7] | WANG Yu-gao(王玉高), ZHAO Wei(赵炜), GONG Shi-rui(贡士瑞) . Research progress of cellulose hydrolysis(纤维素水解的研究进展)[J]. Chemical Industry Times(化工时刊) , 2009, 23 (5) : 70-73 |
| [8] | ZHAO Kai(赵凯), XU Peng-ju(许鹏举), GU Guang-ye(谷广烨) . Study on determination of reducing sugar content using 3,5-dinitrosalicylic acid method(3,5-二硝基水杨酸比色法测定还原糖含量的研究)[J]. Food Science(食品科学) , 2008, 29 (8) : 534-536 |
| [9] | Determination of neutral detergent fiber in feedstuffs (饲料中中性洗涤纤维(NDF)的测定): GB/T 20806-2006 [S]. Beijing (北京) : China Standards Press (中国标准出版社), 2006. |
| [10] | Determination of acid detergent fiber in feedstuffs (饲料中酸性洗涤纤维(ADF)的测定): NY/T 1459-2007 [S]. Beijing (北京) : China Standards Press (中国标准出版社), 2007. |
| [11] | Determination of acid detergent lignin in feedstuffs (饲料中酸性洗涤木质素(ADL)的测定): GB/T 20805-2006 [S]. Beijing (北京): China Standards Press (中国标准出版社), 2006. |




