2. 江西水利职业学院, 江西 南昌 330013;
3. 江西饮用水安全重点实验室, 江西 南昌 330013
2. Jiangxi Water Resources Institute, Nanchang 330013, China;
3. Jiangxi Province Key Laboratory of Drinking Water Safety, Nanchang 330013, China
近年来,抗生素由于毒性较大,威胁着生态系统和人类健康[1]。其中,四环素(tetracyclines, TC)类抗生素在我国医药行业和养殖业中广泛使用,因易溶解性及难降解性,对整个生态系统造成了严重的危害[2-3]。此外,TC在地下水、地表水及土壤中的富集迁移过程会引起病原菌的耐药性,通过饮用水和生物链对人体健康造成危害[4-5]。
高级氧化技术(advanced oxidation process,AOPs)利用体系中产生的具有强氧化还原能力的自由基,氧化降解难以去除的有机物[6]。其中,基于过硫酸盐(persulfate,PS)活化产生的SO4−·自由基,因氧化还原电位较高、氧化性能强和半衰期长等优点而引人瞩目[7-8]。Cu[9]、Co[10]、Ag[11]、Fe[12-13]等过渡金属活化PS无需能量且活化效率高,虽然Co、Ag、Cu等可以有效激活PS,但存在着毒性较高、地质储量低的不足,而Fe是自然界中最常见的过渡金属元素,Fe基催化剂克服了上述缺点,但是直接采用过渡金属活化过硫酸盐降解污染有机物,存在有副反应发生、催化剂和氧化剂使用效率低、金属离子残留等缺陷[14-15]。金属有机骨架材料(metal-organic frameworks,MOFs)具有优越的骨架结构和比表面特性,能够较好地克服直接投加金属盐所带来的缺陷,具有理想的活化效果[16];其中,沸石咪唑酯骨架材料(zeolitic imidazolate frameworks,ZIFs)中含有的金属离子,具有大量配位不饱和金属中心,可作为活化氧化剂的活性位点,用来活化氧化剂生成氧化自由基,对ZIFs进行高温煅烧,有机会形成金属/氧化物/多孔碳复合材料[17-18]。有研究发现碳材料因官能团和结构而对PS展现出高效的非均相催化性能,具有非金属特性、绿色环保、耗能低、超高的机械和化学稳定性等优点[19];采用杂原子[6](N、S、P)掺杂改性,能够通过干扰sp2杂化碳的电子和改变碳材料表面结构、改善电子传输速率、增大比表面积等性质,增强碳材料的催化性能[20-21],其中N的掺杂因不会改变碳材料结构,能够保留碳材料的优异性能,并且氮原子电负性(3.04)大。
利用过渡金属与杂原子共掺杂制备的材料,在超级电容器、锂电池[22]及电化学催化[23]等新能源领域已有较为详细的研究,但在水处理领域鲜有报道。本研究以水热法制备了一种以过渡金属Fe为金属节点且富含N元素的MOFs材料(Fe-ZIFs),通过碳化技术在N2保护的高压作用下煅烧,实现碳材料的Fe、N共掺杂,最终生成催化材料Fe-N-C。在此基础上利用Fe-N-C活化PS降解TC,研究不同的环境条件(如催化剂质量浓度、TC质量浓度、PS质量浓度、pH值、离子强度等)对降解效果的影响,分析相应的反应机理。Fe-N-C材料集过渡金属与碳材料的催化性能于一体,Fe-N-C/PS体系发挥了碳吸附技术与SO4−·自由基氧化技术各自的优势,考虑协同增效原理和成本优化原则,为进一步的应用提供参考。
2 材料与方法 2.1 药品及仪器药品主要有Zn(NO3)2·6H2O(西陇科学股份有限公司)、FeSO4·7H2O(西陇科学股份有限公司)、2-甲基咪唑(上海麦克林生化科技有限公司)、TC(上海麦克林生化科技有限公司)、过硫酸钾(上海青析化工科技有限公司)、甲醇(西陇科学股份有限公司)、稀盐酸(国药集团化学试剂有限公司)、氢氧化钠(天津恒兴化学试剂有限公司)等,所有化学药品均为分析纯。仪器主要有85-2型恒温磁力搅拌器(常州丹瑞实验仪器设备有限公司)、UV-1801型紫外可见分光光度计(北京瑞利分析仪器有限公司)、LD-3B型电动离心机(常州国宇仪器制造有限公司)、JP-040S型超声波清洗机(深圳市洁盟清洗设备有限公司)、DHG-9203A型鼓风干燥箱(上海一恒科学仪器有限公司)等。
2.2 催化剂制备及表征将2-甲基咪唑(1 314 mg)、Zn(NO3)2·6H2O(594 mg)和FeSO4·7H2O(556 mg)分别在30 mL甲醇中超声溶解10 min,形成匀相溶液A、B、C。然后将溶液A和溶液B在搅拌下加入溶液C中,在35 ℃下持续搅拌4 h,形成Fe-ZIF。所得产物离心收集,甲醇洗涤3次,60 ℃烘干下过夜,制备的材料研磨成粉末。将制备的Fe-ZIF材料放在管式炉中,在N2保护下900 ℃的管式炉中煅烧2 h,以进行碳化处理,制备得到N元素掺杂的Fe-N-C材料。
采用蔡司Gemini300扫描电镜(SEM)对材料的表面形貌进行表征;利用EscaLab Xi+电子能谱仪获得了X射线光电子能谱(XPS);使用德国Bruke D8 Advance型射线衍射仪进行X射线衍射(XRD)分析;通过麦克ASAP2020型全自动比表面及孔隙度分析仪对材料的比表面积(BET)和孔隙(BJH)进行分析。
2.3 降解实验在100 mL锥形瓶中,投入一定量的TC和催化剂,预吸附30 min,实验发现吸附30 min后,继续延长吸附时间,TC吸附量没有大幅度增加,本研究取30 min为吸附平衡时间。再加入一定量的PS,利用浓度为0.1 mol·L−1的NaOH和H2SO4对初始pH进行调节,持续反应120 min。考察Fe-N-C质量浓度(0.2~0.6 g·L−1)、TC初始质量浓度(10~150 mg·L−1)、PS的质量浓度(1~15 mg·L−1)、pH=4~10和不同离子强度对TC降解效果的影响。反应每隔一定时间取样4 mL,水样使用直径为0.22 μm滤膜过滤。
2.4 分析方法一般情况下TC的质量浓度采用UV-Vis分光光度计(UV-1801)在最大吸收波长357 nm处测定。为了消除淬灭剂的干扰,自由基淬灭实验的TC质量浓度采用美国安捷伦1260高效液相色谱仪及C-18的色谱柱进行定量分析。
3 结果与讨论 3.1 催化剂表征分析(1) SEM表征分析
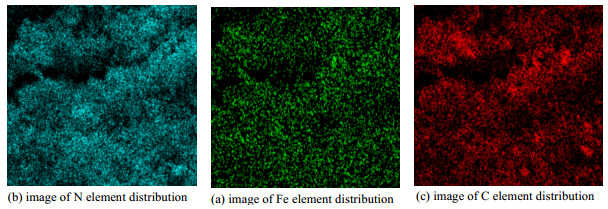
如图 1所示为Fe-N-C样品反应前后的SEM图,由图 1可知,反应前的Fe-N-C样品呈现规则形状的十二面体形状,根据标尺估算样品的尺寸约为90 nm;反应后的Fe-N-C样品表面附着了许多絮状团聚物,可能是残留的TC或者是Fe参与活化PS后生成含Fe的中间产物吸附在样品表面而造成的。如图 2所示为Fe-N-C样品反应前的EDS图,由图 2反应前Fe-N-C的EDS图可确定样品中的Fe、N、C元素均匀分布在样品的表面,分散度较高,没有出现明显的团聚现象。

|
图 1 Fe-N-C的反应前后SEM图 Fig.1 SEM micrographs of Fe-N-C before and after reaction |
|
图 2 反应前Fe-N-C的EDS Fig.2 EDS maps of Fe-N-C before reaction |
(2) XPS表征分析
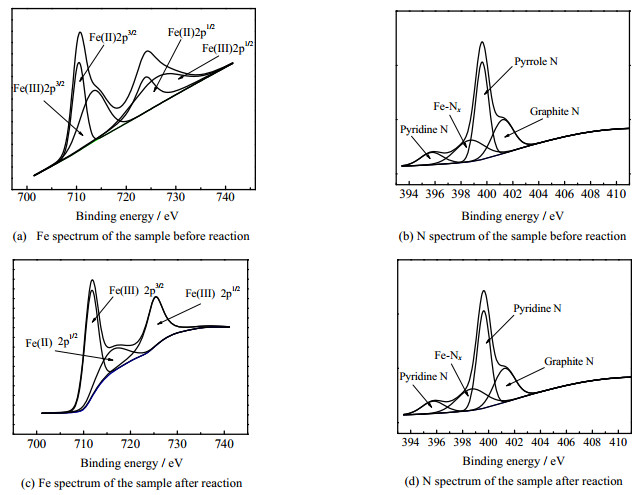
利用XPS对样品Fe-N-C的表面元素相对含量和价态进行了表征,如图 3所示。反应前样品中的Fe、N和C这3种元素质量分数分别为20.6%、3.9%和75.5%;反应后的样品中Fe、N和C这3种元素质量分数分别为4.56%、6.83% 和88.6%,其中,Fe的质量分数减少说明样品中的Fe参与了氧化体系催化过程。图 3(a)和(c)对Fe2p可以拟合成4个峰,结合能在709.2、722.8 eV对应的是Fe(Ⅱ),711.2、724.8 eV对应的是Fe(Ⅲ),反应后样品表面的Fe(Ⅱ)和Fe(Ⅲ)的质量分数比例w(Fe(Ⅱ)): w(Fe(Ⅲ))=0.259,反应前样品中的w(Fe(Ⅱ)): w(Fe(Ⅲ))=0.786,说明样品的w(Fe(Ⅱ))比例有所下降,归因于Fe(Ⅱ)参与了氧化体系中自由基的生成[24]。从图 3(b)和(d)中可以看出,N1s光谱拟合成4个峰,结合能为401.4、400.2、399.0、398.6 eV时分别对应着石墨氮、吡咯氮、Fe-Nx和吡啶氮,其中石墨氮和吡啶氮是sp2杂化,吡咯氮是sp3杂化[25],从图中可以看出在反应前后的样品中都有Fe-Nx存在,有研究证明Fe-Nx是Fe、N共掺杂催化材料的主要活性位点[26],根据XPS分析,可以推断本研究所制备的Fe-N-C的主要活性位点也是Fe-Nx。
|
图 3 反应前后样品Fe-N-C的XPS光谱图 Fig.3 XPS spectra of Fe-N-C before and after reaction |
(3) XRD表征分析
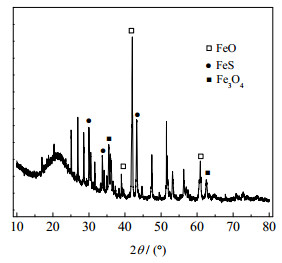
利用XRD图谱对Fe-N-C催化剂的晶体结构进行验证,如图 4所示,在衍射角2θ=29.95°、33.69°和43.20°处出现了明显的FeS特征峰,在2θ=36.07°、41.90°和60.74°处出现了明显的FeO特征峰,而Fe3O4的特征峰出现在2θ=35.44°和62.55°处。XRD衍射峰峰型尖锐,峰宽较窄,说明合成的Fe-N-C催化剂具有较高的结晶度[27]。根据Scherrer公式D=Kλ/βcos θ,D为颗粒直径,nm;K为Scherrer常数,K=0.89;λ为波长,nm;λ=0.154 17 nm;β为衍射峰高度一半时的宽度;θ为衍射角。计算得出Fe-N-C复合材料粒径约为90 nm,与SEM图的估算粒径基本一致,说明材料分散性较好,没有团聚现象发生。
|
图 4 Fe-N-C的XRD图 Fig.4 XRD patterns of Fe-N-C |
(4) BET表征分析
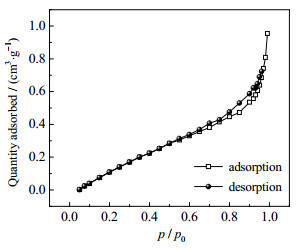
样品Fe-N-C的比表面积和孔径分布跟材料的吸附和催化性能密切相关,在热力学温度为77.35 K条件下Fe-N-C的氮气吸附-脱附等温线和孔径分布曲线如图 5所示。根据IUPAC分类,图 5中表现为典型的具有H3型滞后环的IV型等温线,H3型滞后环出现在相对压力p/p0=0.6~1.0,其在高压端吸附量大,通常认为是片状粒子堆积形成的狭缝孔[28]。相对压力越高,吸附量越大,表现出有孔填充。此外,由图可知Fe-N-C的孔径分布主要集中在3~10 nm,以介孔为主。材料密集丰富的介孔结构,提供了许多活性位点,有利于Fe-N-C的吸附和催化[29]。BET测试样品Fe-N-C的比表面积高达600.752 m2·g−1,孔体积为0.659 32 cm3·g−1,平均孔径为6.532 nm,样品有较高的比表面积、孔容和孔径,可以提供更多的表面活性位点,有利于目标污染物的吸附和扩散[30]。
|
图 5 Fe-N-C的BET图 Fig.5 BET curves of Fe-N-C |
(1) 催化剂质量浓度
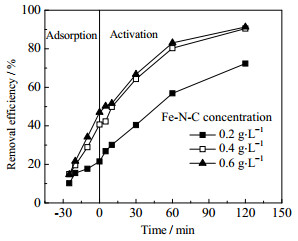
在水温为25 ℃,TC初始质量浓度为40 mg·L−1,PS质量浓度为0.04 g·L−1,初始pH=7时,考察催化剂Fe-N-C质量浓度对TC降解效果的影响,结果如图 6所示。由图 6可知,当催化剂质量浓度由0.2增加至0.4 g·L−1时,TC的降解率与降解速率都明显提高,在反应完成时,降解率由72.3% 提升至90.5%,这是由于增加催化剂质量浓度,使催化活性位点数目增多,提升了其对PS的活化速率,在反应过程中产生了更多的SO4−·,从而导致了TC降解率的提高;继续增加催化剂质量浓度由0.4增加至0.6 g·L−1时,TC的降解率与降解速率都逐渐趋于平缓,在反应150 min时,降解率仅提高至91.3%,这可以归因于质量浓度为0.4 g·L−1的催化剂已经能够提供足量的活性位点来活化体系中的PS,反应达到饱和,且过量Fe-N-C的加入会导致Fe2+的快速释放,消耗系统中的自由基,从而抑制污染物的去除[31]。所以,从经济高效方面考虑,本研究后续实验选择Fe-N-C催化剂质量浓度为0.4 g·L−1。
|
图 6 Fe-N-C质量浓度对TC降解效率的影响 Fig.6 Effects of Fe-N-C concentration on TC degradation |
(2) TC初始浓度
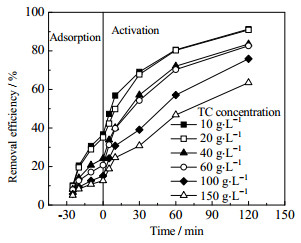
在水温为25 ℃,Fe-N-C催化剂质量浓度为0.4 g·L−1,PS质量浓度为0.04 g·L−1,初始pH=7时,考察催化剂质量浓度对TC降解效果的影响,结果如图 7所示。由图 7可知,在同样的降解条件下,随着TC初始质量浓度从10上升至150 mg·L−1,其降解率逐渐降低。当反应完成时,10和150 mg·L−1初始质量浓度的TC降解率分别为91.3%和63.5%。由此可见,TC初始质量浓度也是影响降解率的重要因素之一。在同一反应体系中,TC的初始质量浓度越高,其降解率越低。这是因为PS的浓度和催化剂质量浓度是固定的,产生的自由基浓度也是固定的,而高级氧化过程的特点之一,即是TC初始质量浓度的增加会降低TC与自由基反应的概率。此外,反应过程中产生的中间体与目标污染物之间存在竞争,边缘中间体可能会引起副反应,因此污染物浓度越高,可去除的目标污染物就越少[32]。
|
图 7 TC质量浓度对TC降解效率的影响 Fig.7 Effects of TC concentration on TC degradation |
(3) 过硫酸盐质量浓度
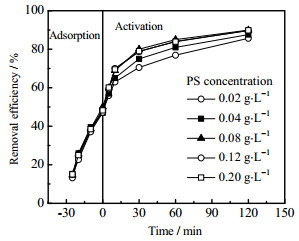
在水温为25 ℃,TC初始质量浓度为40 mg·L−1,Fe-N-C催化剂质量浓度为0.4 g·L−1,初始pH=7时,考察PS质量浓度对TC降解效果的影响,结果如图 8所示。由图 8可知,随着PS质量浓度从0.02上升至0.04 g·L−1,TC去除率从78.28% 上升至81.5%;随着PS质量浓度的增加,催化剂活化PMS产生的自由基增多,促进了降解反应。当PS质量浓度从0.04继续上升至0.08、0.12、0.20 g·L−1时,TC去除率分别下降为80.6%、80.5% 和77.8%,由此可见过高的PS质量浓度对TC降解有负面的影响,这主要是因为加入过量PS会在短时间内生成大量的自由基,而自由基相互之间会发生猝灭反应(式(1)),以及自由基会与过量的SO42−发生反应生成活性更低的SO5−·(式(2))。所以当PS投加过量时表现为TC去除率下降 [33]。因此针对此体系实验采用0.04 g·L−1的PS质量浓度为宜。
| $ {\rm{SO_4^ - \cdot + SO_4^ - \cdot \to 2SO_4^{2 - }}} $ | (1) |
| $ {\rm{SO_4^ - \cdot + HSO_4^ - \to SO_5^ - \cdot + SO_4^ - + {H^ + }}} $ | (2) |
|
图 8 PS质量浓度对TC降解效率的影响 Fig.8 Effects of PS concentration on TC degradation |
(4) 初始pH值
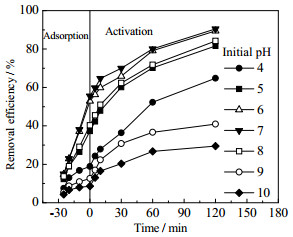
在水温为25 ℃,TC初始质量浓度为40 mg·L−1,Fe-N-C催化剂质量浓度为0.4 g·L−1,PS质量浓度为0.04 g·L−1时,考察初始pH对TC降解效果的影响,结果如图 9所示。由图 9可知,当反应完成时,初始pH值在5~8,pH对氧化体系催化降解TC的影响不显著,TC的降解率为81.6%~90.5%,均能取得理想的降解效果。当pH > 8时,TC的降解率降至40.9 %(pH=9)甚至29.5%(pH=10),这可能是由于在碱性条件下,Fe-N-C表面负电荷的增加会抑制其与PS的相互作用,从而降低TC的降解速率,且Fe3+的沉淀和氢氧化物的形成会吸附在催化剂表面,从而导致降解率下降[34-35]。结果表明,Fe-N-C + PMS体系在很宽的pH值范围内都具有很高的降解效率,证实了可以广泛应用于废水处理。
|
图 9 初始pH对TC降解效率的影响 Fig.9 Effects of initial pH on TC degradation |
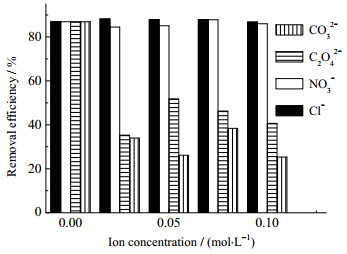
天然水体中存在着大量Cl−、NO3−、C2O42−和CO32−等阴离子,维持水体的pH平衡[36]。Cl−、NO3−、C2O42−和CO32−不同离子强度对降解效果的影响如图 6所示,控制水样水温为25 ℃,TC初始质量浓度为40 mg·L−1,Fe-N-C催化剂质量浓度为0.4 g·L−1,初始pH为7,将溶液中Cl−、NO3−、C2O42−和CO32−的浓度分别调节为0.025、0.05、0.075、0.1 mol·L−1,并设置空白对照组。预吸附30 min达到吸附平衡时,加入不同量的PS,使得PS质量浓度为40 mg·L−1,再持续反应120 min,结果如图 10所示。
|
图 10 不同离子强度对降解效果的影响 Fig.10 Effects of ion concentration on degradation |
由图 10可知,当反应完成时,在加入Cl−或NO3−的情况下,TC的降解率与空白对照组相比几乎没有区别;而在加入C2O42−和CO32−的情况下,TC的降解率由空白对照组的86%下降至35% 甚至30%。由此可见,Cl−或NO3−的存在对TC的降解并无明显影响,而C2O42−和CO32−的存在较大程度地抑制了TC的降解,可能是因为C2O42−和CO32−会与TC竞争SO4−·自由基,并且对SO4−·等自由基有淬灭作用。基本原理为体系中CO32−会发生水解,生成HCO3−,而当溶液pH=7.0时,可以认为溶液中主要以CO32−/HCO3−共同离子存在,能够与SO4−·等自由基反应生成CO3−·和HCO3·自由基,反应如式(3)、(4):
| ${\rm{ SO_4^ - \cdot + CO_3^{2 - } \to SO_4^{2 - } + CO_3^ - \cdot}} $ | (3) |
| $ {\rm{SO_4^ - \cdot + HCO_3^ - \to SO_4^{2 - } + HCO_3^{}\cdot }}$ | (4) |
CO3·和HCO3·也能够降解TC,但是其氧化能力不如SO4-·,所以表现为当加入CO32−的浓度达到一定值时,TC的降解率显著降低。一定浓度C2O42−的对TC有抑制作用原理和CO32−一样,是因为在pH=7.0时,C2O42−与SO4−·能反应生成C2O4−·,而C2O4−·的氧化能力比SO4−·弱。
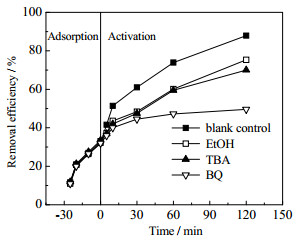
3.4 自由基淬灭实验以及反应机理活化PS过程中可能产生多种自由基,一般来说SO4−·和OH·自由基是降解有机物的主要氧化物质。利用淬灭实验可以鉴定Fe-N-C活化PS降解TC体系中的活性氧化性物质,乙醇(EtOH)是SO4−·自由基(k =1.6×107~7.7×107)和OH·自由基(k =1.2×109~2.8×109)的淬灭剂;叔丁醇(TBA)是OH·自由基(k=(3.8×108~7.6×108)和k=(3.0×109~3.9×109))的有效淬灭剂,但不适用于SO4−·自由基淬灭;O2−·自由基也是常见的活性氧化物质,对苯醌(BQ)可以作为O2−·的淬灭剂[37],结果如图 11所示。
|
图 11 自由基猝灭实验 Fig.11 Results of free radical quenching experiments |
由图 11可知,当反应完成时,在乙醇或叔丁醇存在的情况下,TC的去除率由90%分别降至75%或70%,而在对苯醌存在的情况下,TC的降解受明显抑制,去除率由90%降至50%。由此可见,反应体系中SO4−·、OH·和O2−·自由基都参与了催化反应,但O2−·自由基对TC降解的贡献大于SO4−·和OH·自由基。说明O2−·是Fe-N-C / PMS体系的主要活性氧化物质。结合反应前后催化剂样品的XPS分析提出了Fe-N-C / PMS体系可能的活化机理为:首先Fe-N-C / PMS体系中的Fe2+可以作为电子供体,通过单电子转移反应激活PMS中过氧化物键(─O─O─)的裂解,生成SO4−· (式(5)),SO4−·能够与水分子发生反应生成OH·(式(6)),PS的水解生成H2O2(式(7)),H2O2能够水解生成HO2−·(式(8)),Fe3+能够与H2O2发生反应生成HO2−·(式(9)),HO2−·的解离能就够产生O2−·(式(10))。
因此,催化剂Fe-N-C中的Fe-Nx位点控制自由基过程可能发挥主要作用,而碳基主要起到把TC吸附进入局限的空间和电子传递的作用,最终通过SO4−·、OH·和O2−·自由基将有机污染物分解成小矿化分子(如CO2、H2O)
| ${\rm{ F{{\text{e}}^{2 + }} + SO_4^{2 - } \to SO_4^ - \cdot + F{{\text{e}}^{3 + }} + SO_4^{2 - } }}$ | (5) |
| $ {\rm{SO_4^ - \cdot + {H_2}O \to SO_4^{2 - } + OH\cdot}} $ | (6) |
| $ {\rm{{S_2}O_8^{2 - } + {H_2}O \to {H_2}{O_2} + H{S_2}O_8^ - }}$ | (7) |
| $ {\rm{{H_2}{O_2} + {H^ + } \to HO_2^ - \cdot }}$ | (8) |
| $ {\rm{F{{\text{e}}^{3 + }} + {H_2}{O_2} \to F{{\text{e}}^{2 + }} + {H^ + } + HO_2^ - \cdot}} $ | (9) |
| ${\rm{ HO_2^ - \cdot \to O_2^ - \cdot + {H^ + }}} $ | (10) |
| $ {\rm{S{O}_{4}^{-}·+OH·+{O}_{2}^{-}·+TC\to 反应中间体+C{O}_{2}+{H}_{2}O }}$ | (11) |
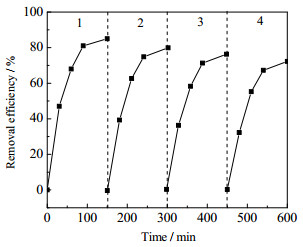
在废水处理领域催化剂的稳定性与应用成本密切相关,对降解体系的产业化应用起着至关重要的作用。通过一系列的实验考察了催化剂Fe-N-C的稳定性,将使用后的催化剂利用去离子水进行清洗,将其烘干后加入反应体系中进行重复性试验,实验结果如图 12所示。
|
图 12 催化剂的稳定性 Fig.12 Stability of Fe-N-C |
从图 12中可以看出,随着催化剂Fe-N-C使用次数的不断增加,TC降解率略微降低,循环使用4次之后降解率由85%下降至72%。这可能是由于在重复利用的过程中,残留的TC或者某些中间产物吸附在Fe-N-C表面,造成了部分活性点位的覆盖或消耗,抑制了Fe-N-C和PS之间的相互作用,导致降解效果受轻微的影响[32],但在使用第4个周期时TC降解率仍有72.8%,说明Fe-N-C的催化活性依然很高。以上结果表明Fe-N-C具有比较优异的催化稳定性,能够重复使用。
4 结论利用水热法制备了一种含过渡金属Fe的N掺杂的催化材料Fe-N-C,并对其进行了表征,研究了Fe-N-C活化过硫酸盐降解TC的影响因素,结果表明:
(1) Fe-N-C催化剂为表面粗糙、疏松多孔的不规则形状;由Fe、N和C这3种元素组成,且各元素质量分数分别为20.6%、3.9% 和75.5%;XRD衍射峰峰型尖锐、峰宽较窄,具有较高的结晶度;孔径分布主要集中在3~10 nm,以密集分布的介孔为主;
(2) 在催化剂质量浓度为0.4 g·L−1,TC初始质量浓度为40 mg·L−1,PS质量浓度为0.04 g·L−1,pH为7时TC的降解效果最佳,降解率高达90.5%,显示出了良好的处理效果;C2O42−和CO32−的存在相较Cl−或NO3−,对TC的降解有更大程度的抑制作用;
(3) 通过自由基猝灭实验可知,在整个降解体系中起主导作用的活性氧化物质为O2−·自由基,且存在着少量的SO4−·和OH·自由基;Fe-N-C经过4次循环后TC降解率依然有72.8%,表现出良好的稳定性。
| [1] |
ZHU Y, YANG Q, LU T, et al. Effect of phosphate on the adsorption of antibiotics onto iron oxide minerals: Comparison between tetracycline and ciprofloxacin[J]. Ecotoxicology and Environmental Safety, 2020, 205: 111345. DOI:10.1016/j.ecoenv.2020.111345 |
| [2] |
MA Y, LI M, LI P, et al. Hydrothermal synthesis of magnetic sludge biochar for tetracycline and ciprofloxacin adsorptive removal[J]. Bioresource Technology, 2021, 319: 124199. DOI:10.1016/j.biortech.2020.124199 |
| [3] |
马茜茜, 吴天威, 赵明月, 等. ATP@Fe3O4复合材料催化过硫酸盐降解四环素[J]. 环境工程学报, 2020, 14(9): 191-201. MA Q Q, WU T WU, ZHAO M Y, et al. ATP@Fe3O4 composite catalyzed the degradation of tetracycline by persulfate[J]. Chinese Journal of Environmental Engineering, 2020, 14(9): 191-201. |
| [4] |
QIU Y, KONG L, CHEN T, et al. Efficient adsorption of tetracycline using Cu+-modified SBA-15 and its adsorption mechanism[J]. Journal of Environmental Engineering, 2021, 147(1): 1-9. |
| [5] |
吴剑, 何东, 吴海锁, 等. 等离子体协同二氧化钛降解四环素废水研究[J]. 水处理技术, 2020, 46(12): 83-88. WU J, HE D, WU H S, et al. Study on the degradation of tetracycline wastewater by plasma and titanium dioxide[J]. Water Treatment Technology, 2020, 46(12): 83-88. |
| [6] |
王安静, 王晨, 张如玉, 等. 可见光/Fe2+/过硫酸盐法处理油田废水[J]. 高校化学工程学报, 2017, 31(5): 1232-1237. WANG A J, WANG C, ZHANG R Y, et al. Treatment of oilfield wastewater by visible light/Fe2+/persulfate process[J]. Journal of Chemical Engineering of Chinese Universities, 2017, 31(5): 1232-1237. DOI:10.3969/j.issn.1003-9015.2017.05.029 |
| [7] |
HUANG D L, ZHANG Q, ZHANG C, et al. Mn doped magnetic biochar as persulfate activator for the degradation of tetracycline[J]. Chemical Engineering Journal, 2020, 391: 123532. DOI:10.1016/j.cej.2019.123532 |
| [8] |
HE J, TANG J C, ZHENG Z, et al. Magnetic ball-milled FeS@biochar as persulfate activator for degradation of tetracycline[J]. Chemical Engineering Journal, 2020, 404: 126997. |
| [9] |
LUO H P, SHENG B, CHEN X Y, et al. Cu2+ / Cu+ cycle promoted PMS decomposition with the assistance of Mo for the degradation of organic pollutant[J]. Journal of Hazardous Materials, 2021, 411: 125050. DOI:10.1016/j.jhazmat.2021.125050 |
| [10] |
CHEN M, ZHU L, LIU S, et al. Efficient degradation of organic pollutants by low-level Co2+ catalyzed homogeneous activation of peroxymonosulfate[J]. Journal of Hazardous Materials, 2019, 371: 456-462. DOI:10.1016/j.jhazmat.2019.03.002 |
| [11] |
KOHANTORABI M, MOUSSAVI G, MOHAMMADI S, et al. Photocatalytic activation of peroxymonosulfate (PMS) by novel mesoporous Ag/ZnO@NiFe2O4 nanorods, inducing radical-mediated Acetaminophen degradation under UVA irradiation[J]. Chemosphere, 2021, 277: 130271. DOI:10.1016/j.chemosphere.2021.130271 |
| [12] |
KARIMIAN S, MOUSSAVI G, FANAEE F, et al. Shedding light on the catalytic synergies between Fe(Ⅱ) and PMS in Vacuum UV (VUV/Fe/PMS) photoreactors for accelerated elimination of pharmaceuticals: The case of metformin[J]. Chemical Engineering Journal, 2020, 400: 125896. DOI:10.1016/j.cej.2020.125896 |
| [13] |
YANG F, WANG Y, WANG Z, et al. Pivotal roles of MoS2 in boosting catalytic degradation of aqueous organic pollutants by Fe(Ⅱ)/PMS[J]. Chemical Engineering Journal, 2019, 375: 121989. DOI:10.1016/j.cej.2019.121989 |
| [14] |
SHEN M, HUANG Z, LUO X, et al. Activation of persulfate for tetracycline degradation using the catalyst regenerated from Fenton sludge containing heavy metal: Synergistic effect of Cu for catalysis[J]. Chemical Engineering Journal, 2020, 396: 125238. DOI:10.1016/j.cej.2020.125238 |
| [15] |
张守秋, 岑洁, 吕德义, 等. 纳米零价铁去除水中重金属铅, 铬离子的研究[J]. 高校化学工程学报, 2019, 33(3): 26-34. ZHANG S Q, CEN J, LYU D Y, et al. Research on the removal of heavy metal lead and chromium ions from water by nano-zero valent iron[J]. Journal of Chemical Engineering of Chinese Universities, 2019, 33(3): 26-34. |
| [16] |
WANG Y, CHI H, PU M, et al. Synthesis of iron-based metal-organic framework MIL-53 as an efficient catalyst to activate persulfate for the degradation of Orange G in aqueous solution[J]. Applied Catalysis A-General, 2018, 549: 82-92. DOI:10.1016/j.apcata.2017.09.021 |
| [17] |
PARK K, NI Z, COTE A, et al. Exceptional chemical and thermal stability of zeolitic imidazolate frameworks[J]. Proceedings of the National Academy of Sciences of the United States of America, 2018, 103(27): 10186-10191. |
| [18] |
吴坤, 孙青, 张俭, 等. 管状TiO2/层状ZnFe2O4复合材料的制备及其可见光催化性能[J]. 高校化学工程学报, 2020, 34(1): 247-254. WU K, SUN Q, ZHANG J, et al. Preparation of tubular TiO2/Layered ZnFe2O4 composite and its visible light catalytic performance[J]. Journal of Chemical Engineering of Chinese Universities, 2020, 34(1): 247-254. DOI:10.3969/j.issn.1003-9015.2020.01.031 |
| [19] |
WEI J, LIU Y, ZHU Y, et al. Enhanced catalytic degradation of tetracycline antibiotic by persulfate activated with modified sludge bio-hydrochar[J]. Chemosphere, 2020, 247: 125854. DOI:10.1016/j.chemosphere.2020.125854 |
| [20] |
WANG C H, CHAO H, KANE T, et al. Metal-organic framework-derived one-dimensional porous or hollow carbon-based nanofibers for energy storage and conversion[J]. Materials horizons, 2018, 5(3): 394-407. DOI:10.1039/C8MH00133B |
| [21] |
HUO X, ZHOU P, ZHANG J, et al. N, S-Doped porous carbons for persulfate activation to remove tetracycline: Nonradical mechanism[J]. Journal of Hazardous Materials, 2020, 391: 122055. DOI:10.1016/j.jhazmat.2020.122055 |
| [22] |
WANG Z H, JIN H H, MENG T, et al. Fe, Cu-coordinated ZIF-derived carbon framework for efficient oxygen reduction reaction and zinc-air batteries[J]. Advanced Functional Materials, 2018, 28(39): 1802596. DOI:10.1002/adfm.201802596 |
| [23] |
LIANG S, GUO H, SHEN H, et al. Ordered mesoporous carbon assisted Fe–N–C for efficient oxygen reduction catalysis in both acidic and alkaline media[J]. Nanotechnology, 2020, 31(16): 165708. DOI:10.1088/1361-6528/ab674c |
| [24] |
FENG Q, ZHOU J, LUO W, et al. Photo-Fenton removal of tetracycline hydrochloride using LaFeO3 as a persulfate activator under visible light[J]. Ecotoxicology and Environmental Safety, 2020, 198: 110661. DOI:10.1016/j.ecoenv.2020.110661 |
| [25] |
FENG L Y, LI X Y, CHEN X T, et al. Pig manure-derived nitrogen-doped mesoporous carbon for adsorption and catalytic oxidation of tetracycline[J]. Science of The Total Environment, 2020, 708: 135071. DOI:10.1016/j.scitotenv.2019.135071 |
| [26] |
LEI X, YOU M, PAN F, et al. CuFe2O4@GO nanocomposite as an effective and recoverable catalyst of peroxymonosulfate activation for degradation of aqueous dye pollutants[J]. Chinese Chemical Letters, 2019, 30(12): 2216-2220. DOI:10.1016/j.cclet.2019.05.039 |
| [27] |
刘曼, 李一兵, 王彦斌, 等. 掺铜介孔碳活化过硫酸氢盐高效降解双酚A[J]. 中国环境科学, 2017, 11: 4151-4158. LIU M, LI Y B, WANG Y B, et al. Cu-doped mesoporous carbon activated bipersulfate to efficiently degrade bisphenol A[J]. China Environmental Science, 2017, 11: 4151-4158. DOI:10.3969/j.issn.1000-6923.2017.11.018 |
| [28] |
ZHANG Y, LIU C, XU B, et al. Degradation of benzotriazole by a novel Fenton-like reaction with mesoporous Cu/MnO2: Combination of adsorption and catalysis oxidation[J]. Applied Catalysis B: Environmental, 2016, 199: 447-457. DOI:10.1016/j.apcatb.2016.06.003 |
| [29] |
陈一萍, 夏管商, 郑朝洪, 等. CNTs/PMS高级氧化体系去除水中的环丙沙星[J]. 化工进展, 2019, 38(4): 448-456. CHEN Y P, XIA G S, ZHENG C H, et al. Removal of ciprofloxacin in water by CNTs/PMS advanced oxidation system[J]. Progress in Chemical Industry, 2019, 38(4): 448-456. |
| [30] |
CHEN C, XIE M, KONG L, et al. Mn3O4 nanodots loaded g-C3N4 nanosheets for catalytic membrane degradation of organic contaminants[J]. Journal of Hazardous Materials, 2020, 390: 122146. DOI:10.1016/j.jhazmat.2020.122146 |
| [31] |
QU G, CHU R, WANG H, et al. Simultaneous removal of chromium(Ⅵ) and tetracycline hydrochloride from simulated wastewater by nanoscale zero-valent iron/copper–activated persulfate[J]. Environmental Science and Pollution Research, 2020, 27: 40826-40836. DOI:10.1007/s11356-020-10120-8 |
| [32] |
OU Y M, LI X, XU Q, et al. Heterogeneous activation of persulfate by Ag doped BiFeO3 composites for tetracycline degradation[J]. Journal of Colloid and Interface Science, 2020, 566: 33-45. DOI:10.1016/j.jcis.2020.01.012 |
| [33] |
ZHOU N, ZU J, YANG L, et al. Cobalt (0/Ⅱ) incorporated N-doped porous carbon as effective heterogeneous peroxymonosulfate catalyst for quinclorac degradation[J]. Journal of Colloid and Interface Science, 2019, 563: 197-206. |
| [34] |
LI X, YAN X, HU X, et al. Hollow Cu-Co/N-doped carbon spheres derived from ZIFs as an efficient catalyst for peroxymonosulfate activation[J]. Chemical Engineering Journal, 2020, 397: 125533. DOI:10.1016/j.cej.2020.125533 |
| [35] |
徐睿, 杨威, 杨哲, 等. 膨胀石墨负载氧化铜活化过硫酸盐用于降解盐酸四环素[J]. 环境工程, 2020, 38(2): 48-54. XU R, YANG W, YANG Z, et al. Expanded graphite supported copper oxide activated persulfate for degradation of tetracycline hydrochloride[J]. Environmental Engineering, 2020, 38(2): 48-54. |
| [36] |
刘一清, 苏冰琴, 陶艳, 等. 磁性纳米Fe3O4活化过硫酸盐降解水中磺胺甲恶唑[J]. 环境工程学报, 2020, 14(19): 2515-2526. LIU Y Q, SU B Q, TAO Y, et al. Magnetic nano-Fe3O4 activated persulfate to degrade sulfamethoxazole in water[J]. Chinese Journal of Environmental Engineering, 2020, 14(19): 2515-2526. |
| [37] |
WANG Q, WANG B, MA Y, et al. Enhanced superoxide radical production for ofloxacin removal via persulfate activation with Cu-Fe oxide[J]. Chemical Engineering Journal, 2018, 354: 473-480. DOI:10.1016/j.cej.2018.08.055 |




