近年来,国内对安全生产越来越重视,安全意识也日益提高。针对含能化合物生产过程中的热效应特征,设计有效可靠的换热器并选择合适的工艺参数以保证反应过程安全平稳地进行,是科技工作者广泛关注的一个重要课题。硝化反应是合成含能化合物的常用反应,一般情况下是一个快速的强放热过程,其热危险性主要表现为反应失控,即反应体系因反应放热而使温度升高,以致超过了反应器冷却能力的调控极限,造成反应物、产物和硝化剂的分解,生成大量气体,反应器内压力急剧升高,最后导致喷料,甚至爆炸等危险事故,对实验人员、设备等安全造成重大危害。王晓峰等[1]利用反应量热仪(RC1e)对甲苯一段半间歇硝化工艺热失控进行了研究;陈利平等[2-5]研究了硝酸甲胺、甲苯、硝基甲苯、二硝基甲苯硝化过程的热危险性;朱勇等[6-7]利用热流法测定了丁基-叠氮乙基硝胺(BuNENA)和二硝酰胺铵(ADN)合成过程的热效应;周诚等[8]利用热流法测定了1, 1-二氨基-2, 2-二硝基乙烯(FOX-7)合成过程的热效应;这些均对相应含能化合物的合成工艺安全提供了重要的指导作用。
3-硝基-1, 2, 4-三唑-5-酮(NTO)爆轰性能接近于黑索今(RDX),但感度和三氨基三硝基苯(TATB)相当,是一种综合性能优良的钝感高能炸药[9-10],在不敏感弹药领域已得到广泛应用[11-13]。目前NTO工业化生产工艺是以1, 2, 4-三唑-5-酮(TO)为原料,以质量分数为98%硝酸为硝化剂,经硝化反应后得到NTO。该工艺反应完毕后硝化液需稀释才能得到产品,从而产生大量的硝酸废液,带来较大的环境问题。针对此问题,黄新萍等[14]以质量分数为70%硝酸为硝化剂,在高温下进行硝化反应,然后直接降温过滤反应液得到NTO;该工艺硝酸滤液全部可以循环利用,提高了硝酸利用率,大大减少了废酸的产生量。这二种NTO合成工艺的关键工序均是TO的硝化反应,因此,准确测量NTO合成过程中的热效应,分析其反应过程的热危险性,对合成工艺路线的选择、合成工艺条件的控制及保证工艺安全具有极其重要的意义和特殊的价值。
本研究利用全自动反应量热器(RC1e),采用热流法测定二种NTO合成工艺中的关键反应—硝化反应过程中的反应热释放速率、传热系数和比热容等热力学数据,计算反应放热量,并对两种合成工艺的安全性进行比较和分析,以期为硝化反应器的安全设计和合成工艺安全控制提供理论基础和实验依据。
2 实验(材料与方法) 2.1 实验材料与仪器1, 2, 4-三唑-5-酮(TO),自制(按文献[3]方法合成);硝酸,质量分数为98%,工业一级;实验用水为自来水。
瑞士METTLER-TOLEDO公司全自动反应量热器(RC1e),配备2 L玻璃中压反应釜和德国Julabo公司FP52型低温循环器。
2.2 测定原理依据能量衡算,反应釜遵循热流平衡:流入=累积+流出的热量。即:
| $ {{Q}_{\text{r}}}+{{Q}_{\text{c}}}+{{Q}_{\text{stir}}}=({{Q}_{\text{a}}}+{{Q}_{\text{i}}})+({{Q}_{\text{f}}}+{{Q}_{\text{dos}}}+{{Q}_{\text{loss}}}+\ldots ) $ |
式中,Qr为化学或物理反应热量产生的速率;Qc为校准功率(插入物料内的量热器在反应前后校准时放出的热量);Qstir为由搅拌桨带进的能量(在反应物质中产生的热);Qa为反应物质的储存热量(累积);Qi为通过插入件(温度传感器、pH传感器等)储存的热量;Qf为通过反应釜壁的热流;Qdos为加料帶入的热量;Qloss为通过反应釜盖的热流(辐射或传导);Qreflux为在回流冷凝器中散发的热量;Qevap为蒸发的热量。
通过热流法测定上述各种类型的热量,可计算出反应放热速率Qr,通过式(1)积分,即可获得反应过程的总放热量。
| $ \Delta H_{\text{r}}=\int{Q_{\text{r}}\text{d}t} $ | (1) |
以1, 2, 4-三唑-5-酮(TO)为原料,经硝酸硝化后稀释得到NTO。合成工艺路线见式(2)所示。
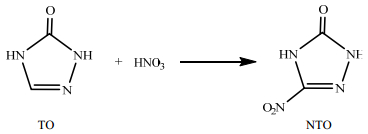
|
(2) |
(1) 方法1 (以质量分数为98%硝酸为硝化剂)
反应热测试过程:开启RC1e,设置实验流程。向2 L玻璃反应釜中加入硝酸(质量分数为98%) 667 mL,通过低温循环器使反应液降温至0℃,量热校准后分份加入268 g TO,控制加料温度为0~15℃,加完后升温至25~30℃,保温反应2 h,降温到0℃,再次量热校准后出料。
(2) 方法2(以质量分数为70%硝酸为硝化剂)
反应热测试过程:开启RC1e,设置实验流程。向2 L玻璃反应釜中加入硝酸(质量分数为70%) 667 mL,将反应液升温至60℃,量热校准后分份加入150 g TO,控制加料温度为60~65℃,加完后在60~65℃下保温反应1 h,降温到0℃,再次量热校准后出料。
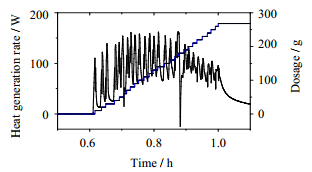
3 实验结果与讨论 3.1 硝化反应过程的热危险性分析全自动反应量热器测定两种NTO合成工艺的关键反应—硝化反应过程热释放速率曲线见图 1和图 2。
|
图 1 方法1硝化过程热流曲线 Fig.1 Heat flow curve of nitration process in process 1 |
|
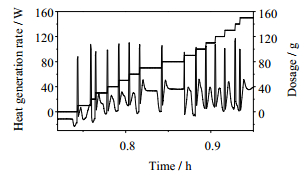
图 2 方法2硝化过程热流曲线 Fig.2 Heat flow curve of nitration process in process 2 |
两种NTO合成工艺中,由于固体加料方式为手动间歇加料,反应热释放速率曲线呈锯齿状,反应热释放属于典型的加料控制型。原料TO加入后快速反应,热量迅速释放,在热流曲线上出现一个放热峰。
由图 2可知,方法1中原料TO每次加入量为10.0 g,加料间隔时间为1 min,温升约为3.5℃,平均放热速率约为91.26 W,瞬间最高峰值甚至可达到162.84 W。由曲线可以得知,每批次原料加入后,对应的放热峰基线逐渐上移,这表明热量有部分累积,导致反应体系温度上升,其原因主要是原料加入偏快,加料间隔时间短,反应未完全进行,从而有热量积累,可以通过减少原料加入量或延长加料间隔时间来消除热量积累,增加硝化反应的安全性。随着反应进行,硝化剂被消耗,体系硝酸浓度下降,反应速率变小,基线下移,其原因主要是设定冷却介质的温度恒定,和反应体系的热交换量也基本恒定,而由于反应放热量变小,从而反应体系温度缓慢下降,但这增加了后期保温反应过程中的危险性。在保温反应过程中,仍有一次较长时间的热量释放,平均放热速率为16.30 W左右,但峰值可达到57.40 W。在反应进行到210 min后,热释放速率曲线趋近于零,反应基本进行完全。
方法2中原料TO每次加入量为10.0 g,加料间隔时间为1 min,温升约为7.9℃,平均放热速率约为101.62 W,均高于方法1,瞬间最高峰值甚至可达到117.11 W。由图 3曲线可以得知,每批次原料加入后,对应的放热峰基线波动较小,热量基本没有累积,同时,在保温阶段,仅出现一次短暂的热量释放峰。这表明高温下反应速率快,反应更完全,和方法1相比较,安全性更高。
两种NTO合成工艺中,反应热释放速率曲线表明硝化过程主要有加料和保温两个放热阶段,而且加料过程放热量均较大,但在保温阶段,方法1有热量累积,故应在加料完毕后,应继续反应10 min以上,将加料过程中累积的热量移除后再进行保温反应,这样可避免两个阶段的热量累加,有效降低反应过程的热危险性。表 1和表 2为两种方法的硝化反应传热数据。
|
|
表 1 硝化反应平均热释放速率和热释放量 Table 1 Average heat release rates and heat release capacities of the two nitration processes |
|
|
表 2 硝化反应传热数据 Table 2 Calorimetric data of the two nitration processes |
从表 1数据可看出,方法1中加料过程和保温过程的平均热释放速率分别为91.62和16.30 W,热释放量分别为79.73和39.08 kJ·mol-1,波动较大,表明反应过程难以控制。而方法2中加料过程和保温过程的平均热释放速率分别为27.55和25.46 W,热释放量分别为28.86和35.34 kJ·mol-1,波动较小,表明反应过程平稳,易于控制,工艺应更安全。
从表 2数据计算出,方法2最大热释放速率Qr max和热释放量Q分别只是方法1的49.3%和54.0%;方法2热传导系数U值为170.87 W·K-1·m-2,较方法1高出17.9%,而比热容Cpr大于方法1,这说明反应温度高,物料流动性好,方法2的热交换效率高于方法1,体系储热能力低于方法1,其结果表现为方法2的反应热能够被及时移除,热危险性更小,安全性更高。
3.2 硝化反应体系的绝热温升绝热温升(∆Tad)表示冷却失效状况下反应理论上能升高的温度,是反应过程安全评估必不可少的因素,∆Tad依据下式计算:
| $ \Delta T_{\text{ad}}=\frac{\int{Q_{\text{r}}\left( t \right)\text{d}t}}{M_{\text{r}}C_{\text{pr}}} $ | (3) |
式中,Qr为放热速率,t为反应时间,Mr为反应物料总质量,Cpr为反应体系的比热容,表示体系自身储热能量的强弱。
对于NTO硝化合成过程的硝化反应体系而言,若系统的冷却能力不足或失效,热量逐渐累积,反应温度持续升高,将导致冒料甚至爆炸等危险事故。由式(3)计算得到,方法1硝化反应体系的绝热温升为531.3 K,方法2的则为244.9 K,可见方法1硝化反应体系的反应热危险程度更高。
3.3 方法2工艺条件变化对产物收率及纯度的影响分析以70%硝酸为硝化剂和溶剂,分别考察了物料摩尔比、反应温度、反应时间对生成物收率及纯度的影响,结果见表 3、4。
|
|
表 3 投料摩尔比对收率、纯度的影响 Table 3 Effect of the molar ratio on yield and purity |
|
|
表 4 反应温度、反应时间对收率、纯度的影响 Table 4 Effect of reaction temperature and time on yield and purity |
从表 3和表 4中数据可以看出,硝酸的投料量增加,硝化能力增强,产物收率提高,纯度变化不明显。同时由于产物在体系中有一定的溶解,投料比增加导致体系增大,当因提高投料摩尔比而增加的产物量低于体系增大溶解的产物量时,收率开始降低。
反应温度升高,体系硝化能力增强,收率提高,但反应温度高于60~65℃时,收率反而开始降低,其原因可能是高温导致硝化剂损失增大。延长反应时间,对产物收率的影响不是很明显,也说明产物在反应体系中稳定。最佳的工艺条件为反应物TO与硝酸的投料摩尔比为1:6,反应温度为60~65℃,反应时间为1 h。
3.4 方法2反应液组分分析和安全性分析因方法2的硝化剂要循环利用,故其硝化滤液的稳定性也是十分重要。采用高压液相色谱法分析滤液组分为62.1%硝酸、1.0%NTO、0.3% TO和36.6%水。在室温滤液放置10天后,外观、比重、硝酸含量无明显变化。这表明方法2的硝化剂是比较稳定的,可以短时间内安全存放。
4 结论(1) 利用全自动反应量热器RC1e分别测定了用二种工艺方法合成NTO过程中的硝化反应热释放速率、热释放量、传热系数及比热容等热力学数据,结果表明方法1硝化反应过程的最大热释放速率为162.84 W,热释放量为118.81 kJ·mol-1,传热系数为144.89 W·K-1·m-2,比热容为1.72 J·K-1·g-1,反应体系的绝热温升为531.3 K,而方法2的分别为117.11 W、64.20 kJ·mol-1、170.87 W·K-1·m-2、2.01 J·K-1·g-1和244.9 K。相比之下,方法2的硝化过程热释放平稳,传热效率更高,工艺过程更加安全。
(2) 针对方法2工艺考察了物料摩尔比、反应温度、反应时间对生成物收率及纯度的影响,确定最佳的工艺条件为反应物TO与硝酸的投料摩尔比为1:6,反应温度为60~65℃,反应时间为1 h。
(3) 对方法2的硝化剂进行分析测定,结果无明显变化,表明硝化剂是比较稳定的,短期内可安全存放。
| [1] | WANG Xiao-feng(王晓峰), CHEN Wang-hua(陈网桦), XUE Yan(薛艳), et al. Runaway evaluation of semi-batch toluene mononitration in RC1e(甲苯一段半间歇硝化工艺的反应失控研究)[J]. Initiators and Pyrotechnics(火工品), 2007, 3: 18-22. |
| [2] | CHEN Li-ping(陈利平), CAI Liu-lin(蔡刘霖), PENG Jin-hua(彭金华), et al. Study on the safety synthesis of methylamine nitrate(硝酸甲胺反应过程的安全性研究)[J]. China Safety Science Journal(中国安全科学学报), 2006, 16(12): 97-102. DOI:10.3969/j.issn.1003-3033.2006.12.018. |
| [3] | CHEN Li-ping(陈利平), CHEN Wang-hua(陈网桦), LI Chun-guang(李春光), et al. Study on the hazards of semi-batch nitration process of toluene in mixed acids(混酸中甲苯半间歇硝化过程的危险性研究)[J]. China Safety Science Journal(中国安全科学学报), 2007, 17(12): 102-106. DOI:10.3969/j.issn.1003-3033.2007.12.018. |
| [4] | CHEN Li-ping(陈利平), CHEN Wang-hua(陈网桦), LI Chun-guang(李春光), et al. Thermal hazard in the process of mononitrotoluenenitration(一硝基甲苯硝化过程的热危险性)[J]. Chinese Journal of Explosives & Propellant(火炸药学报), 2008, 31(3): 36-40. DOI:10.3969/j.issn.1007-7812.2008.03.009. |
| [5] | CHEN Li-ping(陈利平), CHEN Wang-hua(陈网桦), PENG Jin-hua(彭金华), et al. Thermal hazard analysis of dinitrotoluenenitration(二硝基甲苯硝化反应的热危险性分析)[J]. Chinese Journal of Energetic Materials(含能材料), 2010, 18(6): 706-710. DOI:10.3969/j.issn.1006-9941.2010.06.022. |
| [6] | ZHU Yong(朱勇), LI Pu-rui(李普瑞), GE Zhong-xue(葛忠学), et al. Determination of heat of reaction and kinetics correlation of synthesis process of BuAENA(BuAENA合成过程中反应热的测定及动力学关联)[J]. Chinese Journal of Explosives & Propellant(火炸药学报), 2012, 32(1): 43-45. DOI:10.3969/j.issn.1007-7812.2012.01.010. |
| [7] | ZHU Yong(朱勇), WANG Yu(王玉), LIU Jian-li(刘建利), et al. Thermal effects of synthesis process of ADN(ADN合成过程的热效应)[J]. Chinese Journal of Energetic Materials(含能材料), 2012, 20(6): 735-738. DOI:10.3969/j.issn.1006-9941.2012.06.016. |
| [8] | ZHOU Cheng(周诚), ZHU Yong(朱勇), WANG Bo-zhou(王伯周), et al. Thermal hazards of nitration reaction in the synthesis of FOX-7(FOX-7合成过程中硝化反应的热危险性)[J]. Chinese Journal of Energetic Materials(含能材料), 2014, 22(1): 53-56. |
| [9] | Lee K Y, Chapman L B, Coburn M D. 3-Nitro-1, 2, 4-triazol-5-one, a less sensitive explosive[J]. Journal of Energetic Materials, 1987, 5: 27-33. DOI:10.1080/07370658708012347. |
| [10] | Beard B C, Sharma J. The radiation sensitivity of NTO (3-nitro-1, 2, 4-triazol-5-one)[J]. Journal of Energetic Materials, 1989, 7(3): 181-198. DOI:10.1080/07370658908014895. |
| [11] | Mennecy A B. 5-Oxo-3-nitro-1, 2, 4-triazole in gun power and propellant compositions: US, 5034072[P], 1991-07-23. |
| [12] | LI Yun-zhi(李运芝), ZHANG Jing-lin(张景林), ZHANG Shu-hai(张树海). Performance and application of insensitive explosives based on 3-nitro-1, 2, 4-triazol-5-one(以NTO为主体的钝感炸药的性能及应用)[J]. Journal of North University of China(中北大学学报), 2007, 28(5): 442-447. DOI:10.3969/j.issn.1673-3193.2007.05.015. |
| [13] | WANG Hong-tao (汪洪涛), ZHOU Ji-yi (周集义). Preparation, characterization and application of NTO and its salts (NTO及其盐的制备、表征与应用)[J]. Chemical Propellants and Polymeric Materials (化学推进剂与高分子材料), 2006, 4(5): 25-29, 续4(6): 28-32. http://kns.cnki.net/KCMS/detail/detail.aspx?filename=HXTJ200605006&dbname=CJFD&dbcode=CJFQ |
| [14] | HUANG Xin-ping(黄新萍), CHANG Pei(常佩), WANG Bo-zhou(王伯周), et al. Recycling use of waste acids in preparation of 3-nitro-1, 2, 4-triazol-5-one (NTO)(-硝基-1, 2, 4-三唑-5-酮(NTO)废酸的循环利用)[J]. Chinese Journal of Energetic Materials(含能材料), 2013, 21(3): 363-366. DOI:10.3969/j.issn.1006-9941.2013.03.018. |




