二氧化氮是空气中的典型污染物之一,主要来自矿物燃料的燃烧,排放会加剧空气污染,能造成酸雨、光化学烟雾以及PM2.5[1-2]等严重的环境问题。二氧化氮是一种剧毒化学品,人体吸入后会中毒,对身体造成多种损伤。另外二氧化氮在常温下可与四氧化二氮相互转化,在军事和工业用途中,通常以高浓度四氧化二氮的形式贮存,作为化学反应以及火箭燃料中做氧化剂使用[3]。目前检测二氧化氮的主要方法有:分光光度法[4]、离子色谱法[5-6]、传感器法[7-8]及差分吸收光谱法[9-10]等。分光光度法是当前应用较多的方法,是国标上检测二氧化氮的标准方法,具有准确性好、稳定性高、线性范围良好等优点,但操作步骤较多,需要使用分光光度计,很难用于现场实时检测。离子色谱法操作步骤简单、选择性好,可直接对离子进行分离和定量检测,但检测时间较长,无法进行实时监测和反馈。传感器法灵敏度高、选择性好,可长期被动检测二氧化氮,但造价昂贵,成本较高,差分吸收光谱法虽然可以同时监测多种组分,但是检测结果易受到水气和气溶胶的影响。
剂量显色片利用能产生明显颜色变化的化学反应,通过接触前后的颜色变化对有害化学物质进行现场检测,具有灵敏度高、选择性好、易于维护、体积小和运行成本低等优点,适用于工作场所低剂量二氧化氮的半定量检测。剂量显色片通过前后颜色的变化提醒作业人员进行安全防护,保护身体健康。目前国内对二氧化氮剂量显色片的相关研究较少。国标中检测二氧化氮使用的显色剂为对氨基苯磺酸和盐酸萘乙二胺。除此之外目前研究还发现了邻甲苯胺[11]、4-氨基偶氮苯[12]、二苯胺[13]、磺胺、1-萘胺、N, N-二甲基-1-萘胺、3, 3'-二甲基联苯胺[14]、N, N'-二苯基联苯胺[15]等可作为二氧化氮的显色剂。
在前期工作基础上[16],选择对氨基苯磺酸和1-萘胺作为显色剂,研究二氧化氮剂量显色片的最佳制备工艺,测试了剂量显色片的显色效果,考察剂量显色片的重复性、光稳定性和抗干扰能力,研究成果可为二氧化氮的浓度预警和半定量检测提供方法。
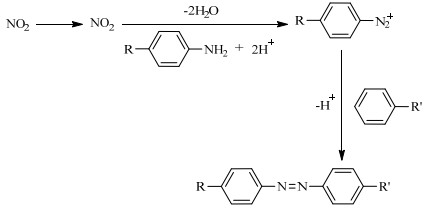
2 实验 2.1 实验原理二氧化氮的检测是利用亚硝酸根在酸性条件下与芳香族伯胺发生重氮化反应和偶联反应生成偶氮染料[17-20],产生颜色变化,显色原理如图 1所示。
|
图 1 显色原理 Fig.1 Principle of nitrogen dioxide color development |
CR-10 Plus型色差计,柯尼卡美能达控股株式会社;全自动双功能动态配气装置,山东非金属材料研究所;AB204-S型电子天平,瑞士METTLER TOLEDO公司;UV-2700型紫外可见分光光度计,日本岛津公司。
二氧化氮标准气体,205.4 mg⋅m−3,兵器工业五三所;对氨基苯磺酸,分析纯,天津市天力化学试剂有限公司;1-萘胺,分析纯,上海科丰实业有限公司;无水乙醇,分析纯,天津市富宇精细化工有限公司;乙二醇,分析纯,天津市富宇精细化工有限公司;202型中速定量滤纸,Φ12.5 mm,杭州特种纸业有限公司;氢氧化钠,分析纯,天津市天力化学试剂有限公司;实验用水为高纯水。
2.3 二氧化氮剂量显色片的制备采用单因素实验的方法确定显色剂的用量,再确定显色剂溶液的最佳pH和湿润剂的用量,得到显色剂溶液的最佳配比。将基底材料裁成直径为2.5 cm的小圆片,放入显色剂溶液中浸泡20 min,在25 ℃的烘箱中干燥10 min,密封保存待用。
2.4 二氧化氮剂量显色片性能研究根据GBZ 2.1-2007《工作场所有害因素职业接触限值化学有害因素》当中的规定,作业场所二氧化氮的平均容许质量浓度为5 mg⋅m−3,本研究选择了质量浓度为6.2 mg⋅m−3的二氧化氮气体来检验剂量显色片的显色效果,利用全自动双功能动态配气装置将质量浓度为205.4 mg⋅m−3的二氧化氮标准气体稀释至5 mg⋅m−3 (氮气为稀释气体,总体积流量为1 000 mL⋅min−1),将剂量显色片放入二氧化氮氛围中30 min。以CIE LAB色空间[21]为色度标准,颜色空间是由L、a、b三个互相垂直的轴组合成的坐标系,L表示像素的亮度,表示从纯黑到纯白,a表示从红色到绿色的范围,b表示从黄色到蓝色的范围。利用色差计测量剂量显色片前后的L、a、b的变化值ΔL、Δa、Δb,色差值ΔE可用式(1)计算得到,利用前后色差值考察剂量显色片的显色效果。
| $ \Delta E = \sqrt {\Delta {L^2} + \Delta {a^2} + \Delta {b^2}} $ | (1) |
本研究选取了4种常见材料作为基底材料:定量滤纸、玻璃纤维纸、尼龙滤膜和定性滤纸。不同基底材料反应前后的显色效果如图 2所示,由图 2可知,定量滤纸和定性滤纸在反应前后颜色变化均匀、显色效果良好,结合浸泡前后基底材料对显色剂溶液的吸收效率,最终选择了化学耐受性和负载能力更好的定量滤纸作为基底材料。

|
图 2 不同基底材料剂量显色片的显色效果
Fig.2 Color development effects with different substrate material dosages
1. quantitative filter paper 2. glass fiber filter paper 3. nylon filter membrane 4. qualitative filter paper |
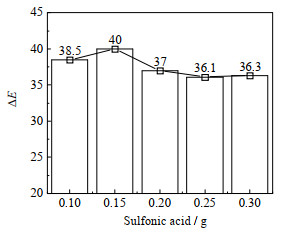
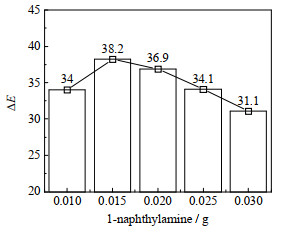
在50 mL显色剂溶液中固定1-萘胺的用量为0.02 g,在对氨基苯磺酸的质量分数为0.2%~0.6% 时研究其用量对色差的影响[22-23],结果如图 3所示,由图 3可知,对氨基苯磺酸的最佳用量为0.15 g;在1-萘胺的质量分数为0.02%~0.06% 时研究其用量对色差的影响,结果如图 4所示,由图 4可知,1-萘胺的最佳用量为0.015 g。
|
图 3 对氨基苯磺酸的用量对色差的影响 Fig.3 Effects of p-aminobenzenesulfonic acid dosage on chromatic aberration |
|
图 4 1-萘胺的用量对色差的影响 Fig.4 Effects of 1-naphthylamine dosage on chromatic aberration |
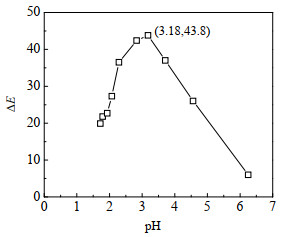
为了研究溶液pH对显色效果的影响,研究显色反应的最佳pH条件,本研究采用了浓度为0.1 mol⋅L−1的盐酸和氢氧化钠溶液对显色剂溶液的pH进行调节,溶液pH对色差的影响如图 5所示。
|
图 5 溶液pH对色差的影响 Fig.5 Effects of solution pH on chromatic aberration |
由图 5可知,随着显色剂溶液pH值的增大,剂量显色片的色差呈现先增大后减小的趋势,在pH值为3.18时剂量显色片的色差最大,经测定溶液初始pH值为2.52,最后加入了氢氧化钠溶液调节溶液的pH,用量为4 mL。
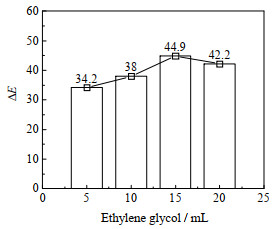
3.4 湿润剂的用量为了保证剂量显色片良好的显色效果,延长剂量显色片的使用时间,需要在显色剂溶液中加入一定量的湿润剂。乙二醇是一种可以与水互溶的有机溶剂,低毒,常常作为湿润剂使用,因此本研究选择了乙二醇作为湿润剂为显色反应提供湿润条件。乙二醇的用量对色差的影响如图 6所示。由图 6可知,乙二醇的最佳用量为15 mL。
|
图 6 乙二醇的用量对色差的影响 Fig.6 Effects of ethylene glycol dosage on chromatic aberration |
综上所述,显色剂溶液的最佳配比为:0.15 g对氨基苯磺酸、0.015 g 1-萘胺、4 mL氢氧化钠溶液和15 mL乙二醇,用纯水定容至50 mL。
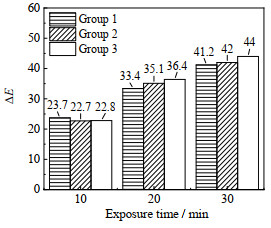
3.5 剂量显色片的性能研究 3.5.1 重复性将不同批次、相同条件下制备的剂量显色片放入二氧化氮氛围中,在10、20、30 min时取出记录色差变化,结果如图 7所示。
|
图 7 不同批次的剂量显色片的色差变化 Fig.7 Variation of chromatic aberration of different sample batches |
由图 7可知,不同批次的剂量显色片在相同的时间内显色效果相差不大,3组剂量显色片色差值的相对偏差均在5%以内,表明剂量显色片的重复性良好。
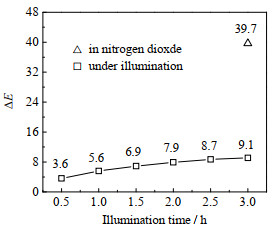
3.5.2 光稳定性将剂量显色片放置在紫外线指数(ultra violet index,UVI)为6的室外环境下,每隔0.5 h利用色差计记录色差变化,3 h后放入二氧化氮氛围中30 min,结果如图 8所示。
|
图 8 不同光照时间下剂量显色片的色差变化 Fig.8 Variation of chromatic aberration under different illumination times |
由图 8可知,随着光照时间的延长,剂量显色片的色差缓慢增大,3 h后色差值达到9.1;将剂量显色片放入二氧化氮氛围后,剂量显色片有明显的色差变化,色差值达到39.7,实验结果表明,光照会对剂量显色片产生一定的影响,但不影响剂量显色片对二氧化氮的响应,剂量显色片未失效,因此剂量显色片具有较好的光稳定性。
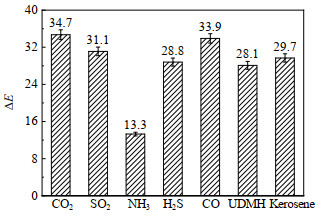
3.5.3 抗干扰能力选择二氧化碳、二氧化硫、氨气、硫化氢、一氧化碳、偏二甲肼气体和煤油挥发气体作为干扰气体(质量浓度均为205.4 mg⋅m−3),将剂量显色片放入干扰气体和二氧化氮的混合氛围中30 min,剂量显色片的色差变化如图 9所示。
|
图 9 不同干扰气体氛围下剂量显色片的色差变化 Fig.9 Variation of chromatic aberration under different interfering gas atmospheres |
由图 9可知,剂量显色片在不同干扰气体的作用下显色效果出现了一定的差异,氨气会对剂量显色片的显色效果产生较大影响,原因可能是氨气会导致显色反应的pH增大,使显色效果变差,这印证了3.3节的实验结果。其余干扰气体对剂量显色片的显色效果影响差别不大,因此剂量显色片具有较好的抗干扰能力,应注意在使用过程中避免大量接触碱性气体。
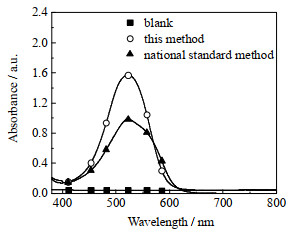
3.6 与国标方法比较利用对氨基苯磺酸和盐酸萘乙二胺在相同的条件下配制显色剂溶液,并制备剂量显色片。分别将2种方法制备的显色剂溶液和剂量显色片放入二氧化氮氛围中30 min,利用紫外可见分光光度计测量2种显色剂溶液的UV-vis吸收曲线,结果如图 10所示。2种剂量显色片的显色效果如图 11所示。
|
图 10 UV-vis吸收曲线对比 Fig.10 Comparison of UV-vis absorption curves |

|
图 11 剂量显色片的显色效果对比 Fig.11 Comparison of chromogenic effects of different samples |
利用色差计测量2种剂量显色片的前后色差分别为41.4和34.1,结合图 10和11可知,相较于对氨基苯磺酸和盐酸萘乙二胺,对氨基苯磺酸和1-萘胺作为显色剂在可见光区的吸收强度更大,在相同条件下制备的剂量显色片显色效果更好。剂量显色片可通过直观的颜色变化检测二氧化氮,缩短了检测的时间,提高了检测效率,作业人员可直接佩戴在身上,对二氧化氮进行实时检测和预警。
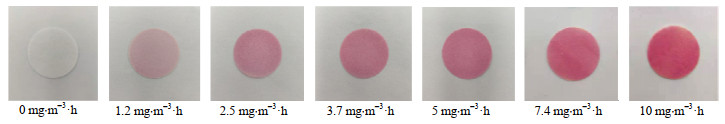
3.7 比色色阶的确定国标上规定作业场所二氧化氮的平均容许质量浓度为5 mg⋅m−3,以此为标准,考察2 h内二氧化氮剂量显色片的显色效果,制作了比色色阶,结果如图 12所示。
|
图 12 比色色阶 Fig.12 Chromatic scales obtained in the study |
(1) 本研究选择对氨基苯磺酸和1-萘胺作为显色剂,采用单因素实验的方法,确定了显色剂溶液的最佳配比:0.15 g对氨基苯磺酸、0.015 g1-萘胺、4 mL氢氧化钠溶液和15 mL乙二醇,用纯水定容至50 mL。
(2) 本研究采用定量滤纸作为基底材料制备了二氧化氮剂量显色片,利用色差计和紫外可见分光光度计对剂量显色片的显色效果和性能指标进行研究,结果表明剂量显色片对二氧化氮的响应速度快、显色效果好,并具有良好的重复性、较好的光稳定性和抗干扰能力。
(3) 剂量显色片可通过直观的颜色变化判断个人所受到的二氧化氮剂量,可作为特殊工作场所或应急条件下个人所接受剂量的预警和半定量检测。
| [1] |
JOHN J C S, CHAMEIDES W L, SAYLOR R. Role of anthropogenic NOx and VOC as ozone precursors: A case study from the SOS nashville/middle tennessee ozone study[J]. Journal of Geophysical Research: Atmospheres, 1998, 103(D17): 22415-22423. DOI:10.1029/98JD00973 |
| [2] |
PENG H, LI F, HUA Z, et al. Highly sensitive and selective room-temperature nitrogen dioxide sensors based on porous graphene[J]. Sensors and Actuators B: Chemical, 2018, 275: 78-85. DOI:10.1016/j.snb.2018.08.036 |
| [3] |
李进华, 孙兆懿. 四氧化二氮胶体饱和蒸气压的测试及分析[J]. 火炸药学报, 2007(1): 74-77. LI J H, SUN Z Y. Measurement and analysis of saturated vapor pressure of nitrogen tetroxide colloid[J]. Journal of Explosives and Explosives, 2007(1): 74-77. DOI:10.3969/j.issn.1007-7812.2007.01.021 |
| [4] |
韩国萍, 戴永生. 盐酸萘乙二胺分光光度法测定大气中二氧化氮浓度[J]. 环境与发展, 2018, 30(4): 127-128. HAN G P, DAI Y S. Determination of nitrogen dioxide concentration in atmosphere by spectrophotometry with naphthalene ethylenediamine hydrochloride[J]. Environment and Development, 2018, 30(4): 127-128. |
| [5] |
刘德琴. 离子色谱法测定大气降水中的硫酸根和硝酸根离子[J]. 环境研究与监测, 2018, 31(4): 30-32. LIU D Q. Determination of sulphate and nitrate ions in precipitation by ion chromatography[J]. Environmental Research and Monitoring, 2018, 31(4): 30-32. |
| [6] |
金梅, 陈琨, 李海英. 简析环境监测中离子色谱法的应用[J]. 环境研究与监测, 2020, 33(1): 57-59. JIN M, CHEN K, LI H Y. A brief analysis of the application of ion chromatography in environmental monitoring[J]. Environmental Research and Monitoring, 2020, 33(1): 57-59. |
| [7] |
GHASHGHAEE M, GHAMBARIAN M. Defect engineering and zinc oxide doping of black phosphorene for nitrogen dioxide capture and detection: quantum-chemical calculations[J]. Applied Surface Science, 2020, 523: 146527. DOI:10.1016/j.apsusc.2020.146527 |
| [8] |
YONG Y, SU X, CUI H, et al. Two-dimensional tetragonal GaN as potential molecule sensors for NO and NO2 detection: A first-principle study[J]. ACS Omega, 2017, 2(12): 8888-8895. DOI:10.1021/acsomega.7b01586 |
| [9] |
蔡小舒, 李树荣, 付敬业, 等. 差分吸收光谱法监测NO2浓度技术研究[J]. 工程热物理学报, 2003(2): 351-353. CAI X S, LI S R, FU J Y, et al. Study on measuring concentration of NO2 with DOAS method[J]. Journal of Engineering Thermophysics, 2003(2): 351-353. DOI:10.3321/j.issn:0253-231X.2003.02.051 |
| [10] |
AL JALAL A A, AL BASHEER W, GASMI K, et al. Measurement of low concentrations of NO2 gas by differential optical absorption spectroscopy method[J]. Measurement, 2019, 146: 613-617. DOI:10.1016/j.measurement.2019.07.022 |
| [11] |
COLIN F, SHEPHERD P D, CARTER T J N, et al. Development of a piezo-optical chemical monitoring system for nitrogen dioxide[J]. Sensors and Actuators B: Chemical, 1998, 51(1/2/3): 244-248. |
| [12] |
BRADFORD A, DRAKE P L, WORSFOLD O, et al. An improved azo chromophore for optical NO2 sensing[J]. Physical Chemistry Chemical Physics, 2001, 3(9): 1750-1754. |
| [13] |
RAKOWSKI R F. Colorimetric dosimeter for nitrogen dioxide: US, 3574552 [P]. 1971-04-13.
|
| [14] |
OH I H. A low-cost system for measuring ppb-level NO2[J]. Contributions to Tobacco & Nicotine Research, 2005, 21(7): 390-401. |
| [15] |
STANFORD E C, PLANTZ C A. Determination of nitrogen dioxide: US, 2963351 [P]. 1960-12-06.
|
| [16] |
YAO X, ZHANG G, LIU B, et al. Direct detection of 1, 1-dimethylhydrazine in water samples based on formation of gold nanoparticles[J]. Materials Research Express, 2019, 6(6): 065057. DOI:10.1088/2053-1591/ab103c |
| [17] |
BALASUBRAMANIAN N, VIJANTHIMALA R. Spectrophotometric determination of nitrogen dioxide after fixing it as nitrite[J]. International Journal of Hygiene and Environmental Health, 1987, 33(4): 212-213. |
| [18] |
SUNITA S, GUPTA V K. Extractive photometric determination of nitrite in polluted water in ppm level using 4-nitroaniline and guaiacol[J]. International Journal of Environmental Analytical Chemistry, 1987, 19(1): 11-18. |
| [19] |
NAIR J. GLIPTA V K. A rapid spectrophotometric determination of nitrogen dioxide in air using new absorbing reagent[J]. Atmospheric Environment, 1981, 15(1): 107-108. DOI:10.1016/0004-6981(81)90132-3 |
| [20] |
FLAMERZ S, BASHIR W A. Spectrometric determination of nitrite in water[J]. Analyst, 1981, 106(1259): 243-247. DOI:10.1039/an9810600243 |
| [21] |
MELGOSA M. Testing CIELAB-based color-difference formulas[J]. Color Research & Application, 2000, 25(1): 49-55. |
| [22] |
NAKANO N. Development of a monitoring tape for nitrogen dioxide in air[J]. Analytica Chimica Acta, 1996, 321(1): 41-45. |
| [23] |
NAGASHIMA K, NAKANO N. Improvement of a monitoring tape for nitrogen dioxide in air[J]. Talanta, 1999, 49(2): 305-308. |




