2. 西北大学 化工学院,陕西 西安 710069;
3. 长庆油田第一采气厂,陕西 榆林 718500
2. College of Chemical Engineering, Northwest University, Xi'an 710069, China;
3. The First Gas Plant, Changqing Oilfield, Yulin 718500, China
天然气脱硫的方法很多,一般分为化学溶剂法、物理吸收法、化学-物理溶剂法、直接转化法和分子筛法、膜分离法等,其中,化学溶剂法中的醇胺法是目前最常用的天然气脱硫方法,而N-甲基二乙醇胺作为醇胺法的代表,具有选择性高、溶剂消耗少、节能效果显著、价格低廉等诸多优点,其水溶液在高压、低温下能够有效吸收硫化氢、二氧化碳等酸性组分,并在低压、高温下将这些酸性组分解吸出来,从而实现天然气的脱硫净化[1, 2]。然而,在N-甲基二乙醇胺的不断循环过程中,由于它的抗污染能力较差,极易降解、变质并导致装置出现溶液脱硫效率降低、产品气气质不合格以及系统发泡、设备腐蚀、管线堵塞等一系列严重问题[3~5],因此,针对上述问题,为保证天然气净化装置高效、稳定运行,对失活脱硫溶液中各污染物进行定性定量分析[6~8],明确N-甲基二乙醇胺的失活原因[9]并探讨其动力学行为[10~16]是十分必要和迫切的。
本文首先利用X射线衍射仪、离子色谱仪和气质联用仪分别对失活的N-甲基二乙醇胺脱硫溶液中固体悬浮物、热稳定性盐和有机物等污染物的组成进行了检测,以期找出导致N-甲基二乙醇胺失活的主要原因;然后,通过自行设计搭建的脱硫溶液失活评价装置探讨了这些因素在不同含量下对N-甲基二乙醇胺失活度的作用规律与影响大小;最后,借助动态热重法对N-甲基二乙醇胺在连续升温条件下的降解机理进行了研究,并通过数据拟合建立了降解过程的动力学模型,为后续N-甲基二乙醇胺脱硫溶液的净化或更换提供科学、可靠的理论依据和数据来源。
2 实验材料及方法 2.1 试剂和材料失活的N-甲基二乙醇胺脱硫溶液,由长庆油田第一采气厂提供,其作业气层位于奥陶系顶部风化壳盐酸盐岩中,属下奥陶统马家沟组上部五段,气质为高碳硫比天然气,其值一般介于90~160;氢氧化钾、甲基磺酸、硫化亚铁、硫酸铁、四氧化三铁、碳化铁、氯化钠、氯化钾、氯化钙、氯化镁、硫酸钠、草酸钠、氟化钠、N-甲基二乙醇胺、三甘醇、甲醇、N, N-二甲基乙醇胺、乙二醇、N-甲基乙醇胺、三甲胺、1, 4-二甲基哌嗪,分析纯,天津市科密欧化学试剂有限公司产品;氮气、硫化氢、二氧化碳,分析纯,济宁协力特种气体有限公司产品。
2.2 固体悬浮物检测采用日本RIGAKU株式会社D/MAX-2400型粉末X射线衍射仪。钼靶片,锆滤波片,管压46 kV,管流150 mA,氮气氛,扫描速度8°×min-1,扫描范围3~90°,步进宽度0.02°×步-1。
2.3 热稳定性盐检测采用美国DIONEX公司ICS-3000离子色谱仪。阴离子分析柱为AS11-HC,淋洗液为氢氧化钾溶液,阳离子分析柱为CS12A,淋洗液为甲基磺酸溶液,淋洗液流量1.5 mL×min-1,柱温30 ℃,进样量25 μL。
2.4 有机物检测采用美国AGILENT科技有限公司5973-6890气质联用仪。气相色谱条件:色谱柱为HP-50+毛细管柱,进样口温度270℃,分流比1:50,柱流速1 mL×min-1,程序升温,初始柱温140℃,保持2 min,以25℃×min-1升至210℃,保持2 min;质谱条件:EI离子源,电子轰击能量70 eV,离子源温度230 ℃,离子阱温度250℃,扫描范围40~650 amu,自动扫描。
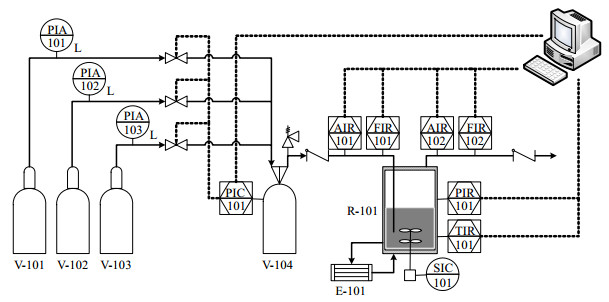
2.5 脱硫溶液失活评价脱硫溶液失活评价装置主要由溶液吸收系统、温度控制系统、压力控制系统、气体供给系统、在线分析系统和数据采集系统组成,如图 1所示。根据脱硫溶液的实际工况选择溶液吸收系统的工作温度为28 ℃,工作压力为5.4 MPa,有效容积为300 mL,内置磁力搅拌器和鼓泡吸收管,利用温度控制系统对它的温度进行控制,控温范围为5~95℃,恒温波动不大于0.05℃,通过前、后背压阀控制它的压力,控压范围为0~10 MPa,精度可达±0.1 MPa。分别将PT100型温度变送器、3051TA型压力变送器、LXI-B型气体流量计以及EC9820型二氧化碳在线分析仪、EC9852型硫化氢在线分析仪经数据采集系统与微型计算机相连,对整个装置的运行状况进行监视和调整。
|
图 1 脱硫溶液失活评价装置图
Fig.1 Schematic diagram of the apparatus for desulfurized solution inactivation evaluation
V-101: nitrogen cylinder V-102: hydrogen sulfide cylinder V-103: carbon dioxide cylinder V-104: mixing gas cylinder R-101: high-pressure reactor E-101: super thermostat water bath |
该装置以高纯氮气模拟现场天然气,以高纯硫化氢和高纯二氧化碳模拟天然气中的酸性组分,硫化氢与二氧化碳按1:120体积比混合均匀后以鼓泡方式将其缓慢通入新鲜N-甲基二乙醇胺脱硫溶液以及含有不同污染物的脱硫溶液中,污染物的加入种类与含量范围则根据失活脱硫溶液污染物组成分析结果来确定,通过取样口实时在线采集、分析吸收前后气体中的酸性组分含量,待吸收时间大于20 min后,当吸收前后的酸气含量基本不变时,即可停止实验。每个实验平行做3次,根据差量法得到脱硫溶液的失活度ψ,其具体计算公式如下:
| $ \psi = \frac{{\sum {\left( {{c_{i0}}{q_\text{V}}_0t-\int_0^t {{c_i}{q_\text{V}}\text{d}t} } \right)}-\sum {\left( {c_{i0}^{^\prime }q_\text{V}^{^\prime }t'-\int_0^{t'} {c_i^{^\prime }q_\text{V}^{^\prime }\text{d}t'} } \right)} }}{{\sum {\left( {{c_{i0}}{q_\text{V}}_0t - \int_0^t {{c_i}{q_\text{V}}\text{d}t} } \right)} }} \times 100\% $ | (1) |
式(1)中,组分i为硫化氢或二氧化碳;ci0、ci0′为在空白实验和掺杂实验条件下吸收前气体中组分i的摩尔分数;ci、ci′为在空白实验和掺杂实验条件下吸收后t、t′时刻气体中组分i的摩尔分数;qV0、qV0′为在空白实验和掺杂实验条件下吸收前t、t′时刻气体的摩尔流量,单位为mol×min-1;qV、qV′为在空白实验和掺杂实验条件下吸收后t、t′时刻气体的摩尔流量,单位为mol×min-1。
在借助脱硫溶液失活评价装置测定不同组成、不同含量下污染物对脱硫溶液失活度作用规律的基础上,使用MINITAB 15.1对上述实验数据进行多因素方差分析,通过计算各污染物的离差平方和、自由度、平均平方、统计检定值和概率来研究各污染物组成及含量对脱硫溶液失活性能的影响大小[17]。
2.6 脱硫溶液降解测定采用瑞士METTLER-TOLEDO集团TGA/DSC1同步热分析仪。称取20 mg左右样品加入有封盖的铝坩埚中,从0℃升温至300℃,升温速度5℃×min-1,氮气或氧气气氛;通过IBM SPSS Statistics 19.0对脱硫溶液降解过程的动力学模型进行拟合计算,得到它的降解级数、指前因子、表观活化能和相关系数等。
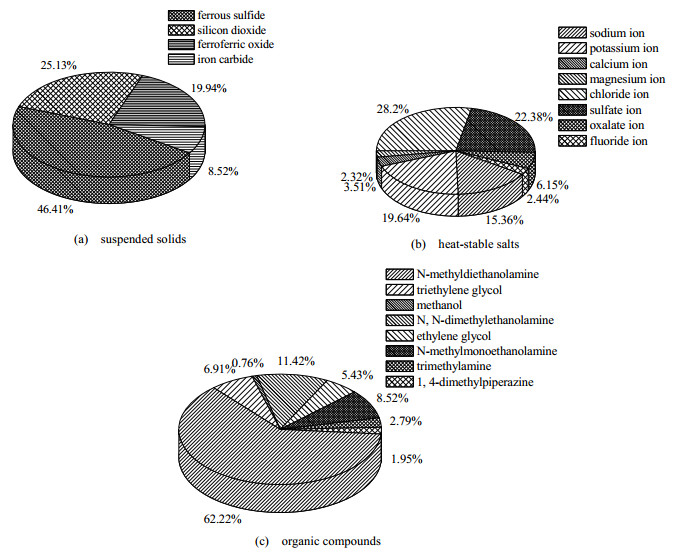
3 实验结果与讨论 3.1 失活脱硫溶液中污染物组成分析及其对脱硫溶液失活度影响影响脱硫溶液脱硫效率的因素很多,如工况条件、溶液配方、有效浓度与体系pH值等,国内外相关学者已对其进行了大量研究并取得了一定成果[18~20],但有关污染物组成及含量对于脱硫效率的影响,特别是对于失活性能的影响报道较少,因此,本文采用X射线衍射仪、离子色谱仪和气质联用仪对失活脱硫溶液中的固体悬浮物、热稳定性盐和有机物等污染物进行了测定,其组成分析结果如图 2所示。
|
图 2 失活脱硫溶液中污染物的质量百分数 Fig.2 Mass percentage of contaminations in inactive desulfurized solutions |
由图 2可知,在该失活脱硫溶液中,固体悬浮物主要含有FeS、SiO2、Fe3O4和Fe3C,尤以含硫化合物居多,故硫化氢和游离水共存下的Fe-H2S-H2O体系电化学腐蚀产物是固体悬浮物的主要来源。热稳定性盐以Na+、K+、Ca2+、Mg2+以及Cl-、SO42-、C2O42-、F-为主,它们大多来自原料气中携带的高矿化度地层水。有机物则包括N-甲基二乙醇胺、三甘醇、甲醇、N, N-二甲基乙醇胺、乙二醇、N-甲基乙醇胺、三甲胺与1, 4-二甲基哌嗪,其中,N-甲基二乙醇胺为失活脱硫溶液的主要组成,占有机物总质量的62.22%;三甘醇、甲醇分别是上游天然气开采、集输过程中常用的热力学抑制剂和脱水吸收剂;而N, N-二甲基乙醇胺、乙二醇、N-甲基乙醇胺、三甲胺、1, 4-二甲基哌嗪均属于N-甲基二乙醇胺的降解产物[21]。虽然上述有机物组成分析结果表明在失活脱硫溶液中仍然存在大量的N-甲基二乙醇胺有效成分,但是鉴于脱硫溶液的作用机理实质上为N-甲基二乙醇胺与硫化氢、二氧化碳解离产生的质子发生液膜控制的多步可逆反应,因此当该脱硫溶液被固体悬浮物、热稳定性盐和有机物所污染时,若污染物与N-甲基二乙醇胺形成热稳定物质并在解吸条件下无法分解再生,则此酸碱反应过程将受到抑制和阻断,被质子化的脱硫溶液亦会逐渐丧失活性,不能与酸性组分正常反应,从而直接导致其脱硫性能较新鲜溶液显著降低甚至失活。
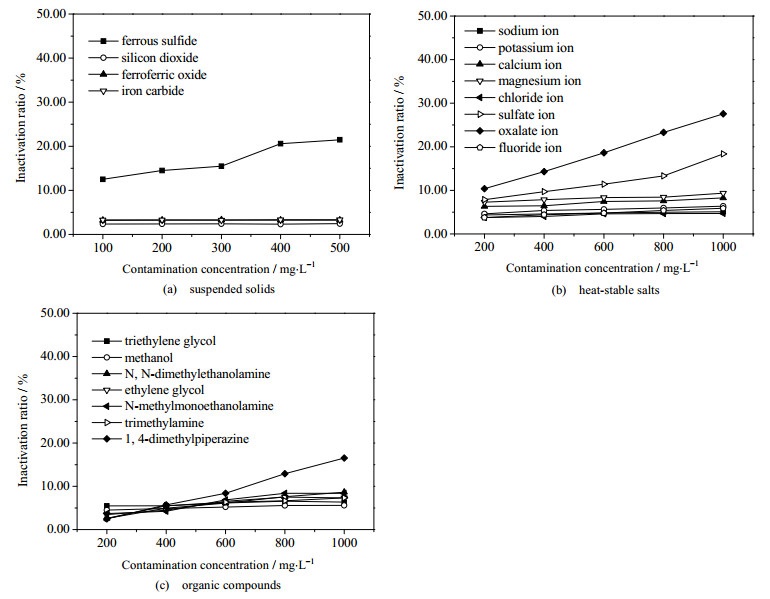
各污染物在不同含量下对脱硫溶液失活度的作用规律如图 3所示。采用MINITAB 15.1对以上实验数据进行多因素方差分析,其影响大小见表 1。
|
图 3 各污染物在不同含量下对胺脱硫溶液失活度的作用规律 Fig.3 Effects of contaminant concentration on the inactivation of desulfurized solutions |
| 表 1 各污染物在不同含量下对胺脱硫溶液失活度的影响大小 Table 1 Effects of contamination concentration on the inactivation of desulfurized solutions |
根据图 3以及表 1中脱硫溶液中各污染物的平方和SS、自由度DF和均方MS的分析结果可见,除SiO2、Fe3O4和Fe3C以外的各污染物的统计检定值F均大于临界值F0.01(4, 10)=5.99,其概率p亦全部小于临界值0.01,说明它们对脱硫溶液的失活都表现出一定的促进作用。其中,C2O42-对脱硫溶液失活的影响最为显著,其余污染物的影响程度由大到小依次为SO42- > 1, 4-二甲基哌嗪 > N-甲基乙醇胺 > FeS > N, N-二甲基乙醇胺 > 乙二醇 > 三甲胺 > Na+ > K+ > F- > Mg2+ > Ca2+ > Cl- > 甲醇 > 三甘醇。由于SiO2、Fe3O4和Fe3C的统计检定值F小于临界值F0.05(4, 10)=3.48,且概率p大于临界值0.05,故对脱硫溶液失活基本无影响。因此,为了确保N-甲基二乙醇胺的脱硫效果良好,必须严格限制脱硫溶液中的FeS、C2O42-与1, 4-二甲基哌嗪为代表的固体悬浮物、热稳定性盐和有机物等污染物的含量,从而有效避免由于其含量过高而导致的脱硫溶液失活现象。
需要说明的是,在实际生产中,脱硫溶液在进入再生塔之前必须首先进入脱硫溶液过滤器,以除去溶液中的固体悬浮物和热稳定性盐。虽然目前常用的多级强化过滤技术和深度离子交换技术能够较好地除去脱硫溶液中的这些污染物(脱除效率最高可达99.99 %),但对于有机物,尤其是N-甲基二乙醇胺系列降解产物的脱除尚无理想方法[22~24],因此本文下面从N-甲基二乙醇胺降解机理及其动力学的角度对脱硫溶液展开研究,从源头上避免失活现象发生,确保脱硫溶液吸收与再生效果良好。
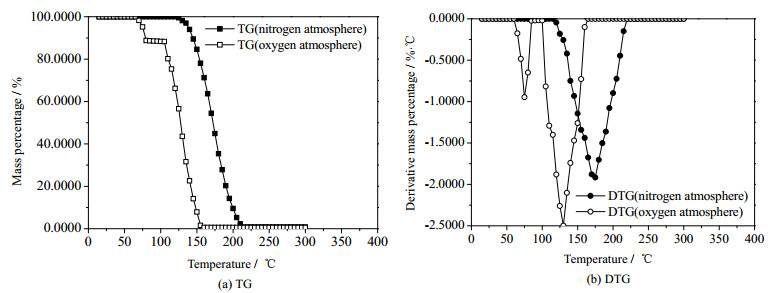
3.2 脱硫溶液的降解机理研究导致脱硫溶液降解的原因很多,一般可分为化学降解、热降解和氧化降解三种。由于N-甲基二乙醇胺是叔胺,既不会与硫化氢或二氧化碳生成噁唑烷酮一类降解产物,也不会与氧硫化碳、二硫化碳等有机硫发生不可逆反应,即基本不存在化学降解问题,故本文利用同步热分析仪仅对N-甲基二乙醇胺在连续升温条件下的热降解和氧化降解过程进行了研究,其TG和DTG曲线如图 4所示。
|
图 4 脱硫溶液在不同气氛下的TG和DTG曲线 Fig.4 TG and DTG curves of desulfurized solutions under different gas atmosphere |
设初始质量为m0的N-甲基二乙醇胺发生降解反应,在某一时刻τ时质量变为m,最终质量为m∞,根据图 4中不同时刻的质量百分数η即可得到其降解度
| $ \psi = \frac{{{m_0}-m}}{{{m_0}-{m_\infty }}} = \frac{{1-\frac{m}{{{m_0}}}}}{{1 - \frac{{{m_\infty }}}{{{m_0}}}}} = \frac{{1 - \eta }}{{1 - {\eta _\infty }}} $ |
由图 4(b)可知,对于在氮气气氛下的热降解过程来说,N-甲基二乙醇胺经历的是一步质量损失过程,初始降解温度为120℃左右,在175 ℃时降解速率达到最大值,降解度为55.13 %,到240℃以后,曲线趋于平缓,由图 4(a)可见其质量百分数仅为0.76 %,表明基本上降解完毕。而对于氧化降解过程来说,在氧气气氛下,N-甲基二乙醇胺的降解过程分两步完成,第一步从65~85℃,降解度为11.34%,第二步从100~160℃,降解度为87.79%,可见空气中的氧可使N-甲基二乙醇胺的初始降解温度明显降低、稳定性变差。综上所述,使用氮气对N-甲基二乙醇进行保护是十分必要的,同时还必须严格控制脱硫溶液的再生温度,确保其不高于120℃。
对于脱硫溶液降解过程来说,它的降解速率可用下式表示:
| $ {\upsilon _\text{d}} = \frac{{\text{d}\psi }}{{\text{d}\tau }} = {k_\text{d}}P(\psi ) $ | (2) |
| $ {k_\text{d}} = A\text{exp}(-\frac{{{E_a}}}{{RT}}) $ | (3) |
式(2)中,υd为降解速率,单位为min-1;ψ为降解度;τ为降解时间,单位为min;kd为降解速率常数,单位为min-1;P(ψ)为降解机理函数,可表示为P(ψ)=(1-ψ)n,在此假设降解级数n=1;A为指前因子,单位为min-1;Ea为表观活化能,单位为kJ×mol-1;R为理想气体常数;T为温度,单位为K。
引入升温速率β,β=dT/dt为一定值,则式(2)变为
| $ \frac{{\text{d}\psi }}{{1-\psi }} = \frac{1}{\beta }A\text{exp}(-\frac{{{E_\text{a}}}}{{RT}})\text{d}T $ | (4) |
对式(4)两边同时积分可以得到积分式:
| $ \int_0^\psi {\frac{{\text{d}\psi }}{{1-\psi }}} = \frac{A}{\beta }\int_{{T_0}}^T {\text{exp}(-\frac{{{E_\text{a}}}}{{RT}})\text{d}T} $ | (5) |
由于初始温度T0较低,降解速率很小,可忽略不计,故式(5)可写为
| $ \int_0^\psi {\frac{{\text{d}\psi }}{{1-\psi }}} = \frac{A}{\beta }\int_0^T {\text{exp}(-\frac{{{E_\text{a}}}}{{RT}})\text{d}T} $ | (6) |
令
| $ \frac{A}{\beta }\int_0^T {\text{exp}(-\frac{{{E_\text{a}}}}{{RT}})\text{d}T} = \frac{{A{E_\text{a}}}}{{\beta R}}\int_\infty ^\zeta {(-\frac{{\text{exp}(-\zeta )}}{{{\zeta ^2}}})\text{d}\zeta } $ | (7) |
当
| $ \text{ln}\frac{1}{{1-\psi }} = \frac{{A{E_\text{a}}}}{{\beta R}}Q(\zeta ) $ | (8) |
将Doyle温度积分近似式lnQ(ζ)=-5.3308-1.0516ζ代入式(8)得
| $ \text{ln}(\text{ln}\frac{1}{{1-\psi }}) = \text{ln}\frac{{A{E_\text{a}}}}{{\beta R}}-5.3308-1.0516\frac{{{E_\text{a}}}}{{RT}} $ | (9) |
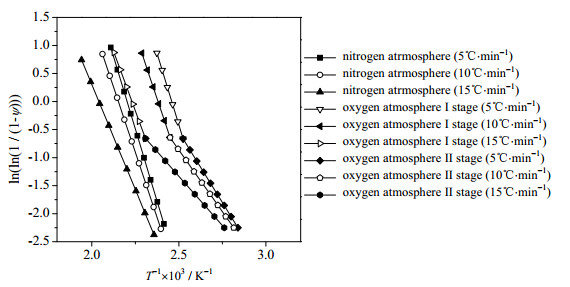
将ln (ln (1/(1-ψ)))对1/T作图并进行线性回归拟合,如图 5所示,通过其斜率和截距即可得到脱硫溶液降解模型中的指前因子A、表观活化能Ea等动力学参数以及相关系数r,计算结果见表 2。
|
图 5 脱硫溶液降解动力学模型的拟合计算 Fig.5 Fitting results of the degradation kinetic model for the desulfurized solutions |
| 表 2 脱硫溶液降解动力学参数与相关系数 Table 2 Kinetic parameters and correlation coefficients for the degradation of desulphurized solvents |
由图 5、表 2可知,对于脱硫溶液降解过程来说,氮气和氧气气氛中各阶段拟合曲线的相关系数r均在0.98以上,拟合计算结果与实验结果吻合良好,因此假设降解级数n=1是合理的;同时,由于N-甲基二乙醇胺在氧气气氛下第Ⅰ阶段的表观活化能远远小于氮气气氛下的值,因此,其更容易发生氧化降解。除此之外,随着升温速率由5℃×min-1提高至15℃×min-1,氮气和氧气气氛下的降解表观活化能均有所减小,这表明升温速率提高会加剧N-甲基二乙醇胺的降解,从而导致脱硫溶液失活。
4 结论(1) 造成脱硫溶液失活的污染物主要由固体悬浮物、热稳定性盐和有机物组成。随着脱硫溶液中各污染物含量的不断增加,FeS、Na+、K+、Ca2+、Mg2+、Cl-、SO42-、C2O42-、F-、三甘醇、甲醇、N, N-二甲基乙醇胺、乙二醇、N-甲基乙醇胺和三甲胺以及1, 4-二甲基哌嗪对溶液失活都表现出一定的促进作用,其影响程度由大到小依次为C2O42- > SO42- > 1, 4-二甲基哌嗪 > N-甲基乙醇胺 > FeS > N, N-二甲基乙醇胺 > 乙二醇 > 三甲胺 > Na+ > K+ > F- > Mg2+ > Ca2+ > Cl- > 甲醇 > 三甘醇,而SiO2、Fe3O4和Fe3C则基本无影响。
(2) N-甲基二乙醇胺热降解经历的是一步质量损失过程,而其氧化降解过程则分两步完成。空气中的氧可使它的初始降解温度明显降低、稳定性变差。为了防止N-甲基二乙醇胺发生降解,须尽量避免氧气窜入系统中,造成脱硫溶液氧化失活,并严格控制脱硫溶液的再生温度,确保其不高于120℃。
(3) 对于脱硫溶液降解过程来说,当假设降解级数n=1时,N-甲基二乙醇胺在氮气和氧气气氛中各阶段拟合计算结果与实验结果吻合良好,其相关系数均在0.98以上,表明该假设准确、合理。同时,由于N-甲基二乙醇胺在氧气气氛下第Ⅰ阶段的表观活化能远远小于氮气气氛下的值,因此,其更容易发生氧化降解。除此之外,随着升温速率由5℃×min-1提高至15℃×min-1,氮气和氧气气氛下的降解表观活化能均有所减小,这表明升温速率提高会加剧N-甲基二乙醇胺的降解,从而导致脱硫溶液失活。
| [1] | WANG Yu-dong(王遇冬), WANG Deng-hai(王登海) . Research and application of amine-gas desulphrization techniques in Changqing gas field(胺法脱硫技术在长庆气田的应用与研究)[J]. Natural Gas Industry(天然气工业) , 2002, 22 (6) : 92-96. |
| [2] | WANG Deng-hai(王登海), WANG Yu-dong(王遇冬), DANG Xiao-feng(党晓峰) , et al. Gas desulphrization and decarbonation by solution with MDEA formula in Changqing gas field(长庆气田天然气采用MDEA配方溶液脱硫脱碳)[J]. Natural Gas Industry(天然气工业) , 2005, 25 (4) : 154-156. |
| [3] | WU Xin-min(吴新民), KANG Xiao-yu(康宵瑜) . Study on the influencing factors and foaming mechanism of MDEA desulphrization solution(甲基二乙醇胺(MDEA)脱硫溶液发泡影响因素和机理研究)[J]. Natural Gas Chemical Industry(天然气化工) , 2008, 33 (6) : 31-36. |
| [4] | WU Jin-qiao(吴金桥), WU Xin-min(吴新民), ZHANG Ning-sheng(张宁生) , et al. Study on foaming reasons of MDEA desulphrization solution in second gas purification plant of Changqing gas field (2)-foaming reason and counter-measures(长庆气田第二净化厂MDEA脱硫溶液发泡原因(Ⅱ)-发泡原因及处理措施)[J]. Natural Gas Industry(天然气工业) , 2005, 25 (4) : 171-174. |
| [5] | Alhseinat E, Pal P, Ganesan S , et al. Effect of MDEA degradation products on foaming behavior and physical properties of aqueous MDEA solutions[J]. International Journal of Greenhouse Gas Control , 2015, 37 (11) : 280-286. |
| [6] | GAO Ming-ming(高明明), TIAN Pan-pan(田盼盼), ZHAO Huan-juan(赵欢娟) , et al. Determination of methyldiethanolamine content in amine solution(胺液中N-甲基二乙醇胺含量的测定)[J]. Natural Gas Chemical Industry(天然气化工) , 2015, 40 (1) : 71-74, 88. |
| [7] | LI Shu-xin(黎曙新), CHENG Wen-hu(成文虎), CHEN Jun-hua(陈军华) , et al. Rapid analysis of methyldiethanolamine decarburizing agent by gas chromatography(GC方法快速分析N-甲基二乙醇胺脱碳剂)[J]. Petrochemical Technology(石油化工) , 2012, 41 (11) : 1317-1321. |
| [8] | LIU Xue-rui(刘学蕊) . The content determination of diethanolamine (DEA) and methyldiethanolamine (MDEA) in the mixed amines of natural gas desulfurization solution:capillary gas chromatography(混合胺溶液中二乙醇胺和甲基二乙醇胺含量的测定-毛细管柱气相色谱法)[J]. Natural Gas Industry(天然气工业) , 2012, 32 (5) : 74-77. |
| [9] | SUN Jiao(孙姣), SUN Bing(孙兵), JI Chun-yan(姬春彦) , et al. Introduction of amine liquid pollution in natural gas desulfurization process and purification technology(天然气脱硫过程的胺液污染问题及胺液净化技术研究进展)[J]. Chemical Industry and Engineering Progress(化工进展) , 2014, 33 (10) : 2771-2777. |
| [10] | Davoudi M, Safadoust A R, Mansoori S A A , et al. The impurities effect on thermal degradation and corrosivity of amine[J]. Journal of Natural Gas Science and Engineering , 2014, 19 (6) : 116-124. |
| [11] | Abukashabeh A S, Alhseinat E, Al-asheh S , et al. Thermophysical properties of fresh and lean thermally degraded N-methyldiethanolamine[J]. Journal of Natural Gas Science and Engineering , 2014, 19 (7) : 317-323. |
| [12] | Fredriksen S B, Jens K J . Oxidative Degradation of Aqueous Amine Solutions of MEA, AMP, MDEA, Pz:A Review[J]. Energy Procedia , 2013, 37 (11) : 1770-1777. |
| [13] | ZHANG Jian-qiu(张剑秋), TIAN Tao(田涛), DENG Wu-yan(邓舞艳) , et al. Degradation and kinetics of DGEBA/EDA epoxy resin in ionic liquids(离子液体中双酚A缩水甘油醚/乙二胺环氧树脂的降解工艺和动力学)[J]. Journal Chemical Engineering of Chinese Universities(高校化学工程学报) , 2015, 29 (3) : 709-715. |
| [14] | LIAO Hui-wei(廖辉伟), PAN Ya-mei(潘雅妹), ZHOU Yuan(周远) . Degradation and kinetics of DGEBA/EDA epoxy resin in ionic liquids(烟酸锶[Sr (C6H4NO2)2·3H2O]的热解动力学)[J]. Journal Chemical Engineering of Chinese Universities(高校化学工程学报) , 2014, 28 (3) : 472-476. |
| [15] | GUAN Guo-qiang(关国强), LIU Xu(刘旭), CHEN Lie-qiang(陈烈强) , et al. Kinetics of thermal decomposition of decabromodiphenyl ether and interaction with polystyrene in pyrolysis(十溴二苯醚热解动力学及在聚苯乙烯中的热解行为)[J]. Journal of Chemical Industry and Engineering(化工学报) , 2012, 63 (11) : 3537-3545. |
| [16] | WANG Zhe(王哲), YANG Xin(杨鑫), CHEN Lie-qiang(吴清海) , et al. The isothermal melt crystallization kinetics of nylon 612(磺化聚芳醚酮砜的热降解动力学)[J]. Polymeric Materials Science and Engineering(高分子材料科学与工程) , 2011, 27 (2) : 99-106. |
| [17] | LI Yun-yan(李云雁), HU Chuan-rong(胡传荣) . Experiment Design and Data Processing(试验设计与数据处理)[M]. Beijing(北京): Chemical Industry Press(化学工业出版社), 2011. |
| [18] | WU Chun-lei(吴春雷), YANG Chun-ping(杨春平), HE Hui-jun(何慧军) , et al. Performance of absorption removal of H2S from FCC dry gas using Fe/Zn-TMS system(Fe/Zn-TMS体系吸收去除催化裂化干气中H2S的性能)[J]. Acta Scientiae Circumstantiae(环境科学学报) , 2014, 34 (8) : 1942-1948. |
| [19] | XU Fei (徐飞). Study on the foaming origin and mechanism of MDEA natural gas desulphurization solution (天然气脱硫用吸收剂MDEA溶液起泡成因及机理研究) [D]. Daqing (大庆): Northeast Petroleum University (东北石油大学), 2014. |
| [20] | WANG Jun-feng (王军峰). Analysis and studies on the failure mechanism of desulfurization solution of natutal gas purifeation plant (天然气净化装置脱硫溶液失效机理分析及研究) [D]. Xi'an (西安): Xi'an Shiyou University (西安石油大学), 2014. |
| [21] | Pal P, Abukashabeh A S, Al-asheh S , et al. Role of aqueous methyldiethanolamine (MDEA) as solvent in natural gas sweetening unit and process contaminants with probable reaction pathway[J]. Journal of Natural Gas Science and Engineering , 2015, 24 (5) : 124-131. |
| [22] | YAN Zhao(闫昭), HUANG Chang-meng(黄昌猛), JIA Hao-min(贾浩民) , et al. The synthesis selection of amine filter in natural gas purification(天然气净化处理中的胺液综合过滤选用)[J]. Petrochemical Industry Application(石油化工应用) , 2012, 31 (1) : 87-91. |
| [23] | LIN Xiao-hong(林霄红), YUAN Zhang-yong(袁樟永) . Application of amipur technology for removing heat-stable salts from amine solution in amine sweetening unit(用AmiPur胺净化技术去除胺法脱硫装置胺液中的热稳定性盐)[J]. Petroleum Processing and Petrochemicals(石油炼制与化工) , 2004, 35 (8) : 21-25. |
| [24] | Simone G De Ávila , Marco A Logli , Jivaldo R Matos . Kinetic study of the thermal decomposition of monoethanolamine, diethanolamine, triethanolamine (TEA) and methyldiethanolamine (MEA, DEA, MDEA)[J]. International Journal of Greenhouse Gas Control , 2015, 42 (11) : 667-671. |




