2. 浙江大学衢州研究院, 浙江 衢州 324000
2. Institute of Zhejiang University-Quzhou, Quzhou 324000, China
随着美国页岩气技术的突破,丰富低价的轻烃资源引起了人们的关注,因此裂解原料大幅度从石脑油转向轻烃,产生了丁二烯的缺口[1]。另外,随着我国西气东输工程顺利实施,天然气已然成为燃气的重要来源,碳四各组分不再适合作为燃气,因此高附加值的碳四利用成为研究热点[2]。碳四各组分是蒸气裂解以及催化裂化过程的副产物[3],其中催化裂化工艺中正丁烷含量占一定比例[4],开发利用正丁烷脱氢制取丁二烯的技术,对碳四烷烃资源的高效利用具有重要意义。正丁烷氧化脱氢制取烯烃技术适应当前我国对绿色化工过程的要求。但目前对正丁烷脱氢仍缺乏系统有效的研究。
当丁烷氧化脱氢反应发生时,催化剂表面和近表面处的晶格氧被消耗,催化剂体相的晶格氧因与表面晶格氧存在较大的浓度差而迁移至催化剂表面。反应时在空气氛围下,空气中的氧气会占据催化剂表面和近表面处的氧空位,同时被还原的金属被氧化成初始状态,随着表面氧空位被补充,表面的晶格氧和体相的晶格氧存在浓度差,氧原子将进一步迁移占据体相中的氧空位,这就是反应过程中的氧移动[3]。Ni基催化剂是目前使用较为广泛的一类催化剂,其对于烷烃氧化脱氢反应表现出较高的烯烃选择性,但反应活性不高。在反应过程中,催化剂上产生氧缺陷,镍元素从Ni2+还原成Ni0态,来源于气相氧的O2−供应到氧空位上,使得催化剂再生。因此提高Ni催化剂上的氧移动性,会极大增加催化剂的催化活性[5-7]。近年来,Ni基催化剂在低碳烃(C2,C3)氧化脱氢反应中得到广泛应用[8-9]。Li等[10]以十二烷基硫酸钠(SDS)为模板,尿素为水解控制剂制备介孔NiO,该催化剂具有优异的结构效应和表面特性,在高丙烷转化水平下对丙烯具有更高的选择性。Wu等[11]使用溶胶-凝胶法制备Ni-Zr-O催化剂用于乙烷氧化脱氢, 由于Zr的分离效应,抑制了乙烯的深度氧化,乙烯的选择性增加。除了Ni基催化剂外,其他金属氧化物催化剂对烷烃转化也有优良的催化效果。Arndt等[12]使用负载型ZnO催化剂用于烷烃转化,结果表明,负载型ZnO催化剂是低碳烷烃氧化转化的合适催化剂,但存在易烧结的缺点。
提升催化剂的氧移动性是提高丁烷氧化脱氢催化性能的关键,组分添加是提升相关催化剂氧移动性的关键[13-17]。本研究采用溶胶凝胶法制备了一系列NiZnx(x=0、0.5、1、3、5) 双金属催化剂。通过改变Zn含量来提升Ni基催化剂的氧移动性,形成的Ni-Zn-O固溶体结构还能改善ZnO催化剂易烧结的缺点,发挥了Ni与Zn之间的协同作用。通过X射线衍射(XRD),N2吸脱附曲线和电感耦合等离子体原子发射光谱(ICP-OES)表征了催化剂的结构与形貌;通过H2-TPR、TPRO和XPS表征了催化剂的氧容量与氧补充速率,深入探究了NiZnx催化剂在丁烷氧化脱氢的性能与氧移动性之间的关联。
2 实验方法 2.1 催化剂制备采用溶胶-凝胶法制备Ni-Zn-O双金属催化剂,将已知量的六水合硝酸镍(Ni(NO3)2·6H2O)、六水合硝酸锌(Zn(NO3)2·6H2O)和一水合柠檬酸(C6H8O7·H2O)分别溶解在蒸馏水中,随后将柠檬酸溶液加入含有镍和锌前体的溶液中,在70 ℃下搅拌混合2种前体溶液,得到溶胶,后将其过夜放置,陈化得到湿凝胶,再在120 ℃烘箱内干燥12 h,得到海绵状绿色粉末。干燥后的样品置于流动空气气氛下的管式炉中,在800 ℃下焙烧3 h,焙烧后的样品即为NiZnx双金属催化剂,其中x为Zn元素相对于Ni元素的物质的量比,值为0、0.5、1、3、5。
2.2 催化剂表征XRD谱图通过X′ Pert PW3050/60型X射线衍射仪得到,二倍角范围为10°~80°,步长为0.02°。氮气吸脱附曲线在Micromeritics ASAP2020型物理吸附仪上测定,催化剂的比表面积和孔容通过Brunauer Emmett and Teller (BET)方程计算得到。通过ICP-OES测定催化剂的元素含量,仪器型号为Agilent 720ES。XPS谱图通过Thermo Scientific K-Alpha型仪器得到,放射源为Al Kα (电子能量hν = 1 486.6 eV),最终结果用C 1s = 284.6 eV校正。氢气程序升温还原(H2-TPR)在Micromeritics AutoChem Ⅱ 2920型化学吸附仪上测试,将0.05 g样品置入U型管,首先在200 ℃下通入50 mL⋅min−1的Ar,预处理1 h,待降到室温后,再切换为30 mL⋅min−1的10% H2/Ar(10%为体积分数)进行程序升温还原,温度为100~900 ℃,升温速率为10 ℃⋅min−1。程序升温氧化还原(TPRO)在Micromeritics AutoChem Ⅱ 2920型化学吸附仪上测试,将0.1 g样品置入U型管,首先在440 ℃下通入10 mL⋅min−1的丁烷进行1 h的预处理,然后通入30 mL⋅min−1的He降到室温,最后通入30 mL⋅min−1的10% O2/He(10%为体积分数)混合气进行程序升温氧化,温度为100~600 ℃,升温速率为10 ℃⋅min−1,出口尾气外接质谱检测,型号为Hiden QIC‒20。热重分析在NETZSCH TG 209 F1 Libra型仪器上进行,将积炭后的催化剂先在100 ℃下干燥脱水2 h,然后进行分析,温度为50~800 ℃,升温速率为10 ℃⋅min−1,并记录样品的失重曲线。
2.3 催化剂性能评价催化剂的性能评价在固定床反应器上进行,不锈钢反应管的内径为8 mm。反应前,催化剂先在550 ℃下空气和氮气的混合气流下预处理0.5 h,反应温度为440 ℃,反应气组成为正丁烷、空气和氮气,其中正丁烷、空气、氮气的物质的量比为1:5:6,总空速为每克催化剂14 400 mL⋅h−1。反应尾气通过奇阳GC‒9860气相色谱在线检测分析,计算公式如下:
| $\begin{aligned} A_{\text {total }}= & A_{n \text {-butane }} \times f_{n \text {-butane }}+A_{\text {isomers }} \times f_{\text {isomers }}+A_{\mathrm{CO}_2} \times f_{\mathrm{CO}_2}/4+A_{\text {butene }} \times f_{\text {butene }}+ \\ & A_{\text {cracked products }} \times f_{\text {cracked products }}+A_{\text {butadiene }} \times f_{\text {butadiene }} \end{aligned}$ | (1) |
| $C_{n \text {-butane }}=\frac{T-A_{n \text {-butaine }} f_{n \text {-butane }}}{T} \times 100 \%$ | (2) |
| $S_{\text {butadiene }}=\frac{A_{\text {butadiene }} f_{\text {butadiene }}}{T-A_{n \text {-butane }} f_{n \text {-butane }}} \times 100 \%$ | (3) |
式中:
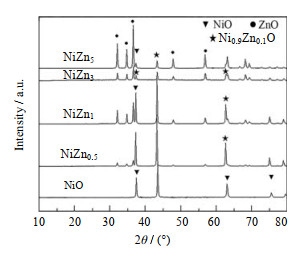
图 1为NiZnx催化剂的XRD谱图,从图可以看到在衍射角2θ为37.3°、43.4°、63.0°、75.6°、79.6°处有特征峰,与标准卡片(JCPDS No.75-0197)对照可知为NiO晶相。在31.8°、34.5°、36.3°、47.6°、56.7°、63.0°、66.5°、68.1°、69.3°、72.8°、77.2°处有特征峰,与标准卡片(JCPDS No.75-0576)对照可知为ZnO晶相。在37.1°、43.2°、62.7°、75.2°、79.2°处有特征峰,与标准卡片(JCPDS No.75-0270)对照可知为Ni0.9Zn0.1O晶相。对比NiO-NiZn5发现,随着Zn的加入,ZnO晶相的衍射峰强度增强,说明其含量逐渐增大;对比NiZn0.5-NiZn5发现,有Ni0.9Zn0.1O晶相形成,但Ni0.9Zn0.1O晶相对应的衍射峰强度逐渐下降,说明随着Zn含量的增加,该相含量逐渐减少。NiZn0.5样品含有最多的Ni0.9Zn0.1O晶相。
|
图 1 NiZnx催化剂的XRD谱图 Fig.1 XRD patterns of NiZnx catalysts |
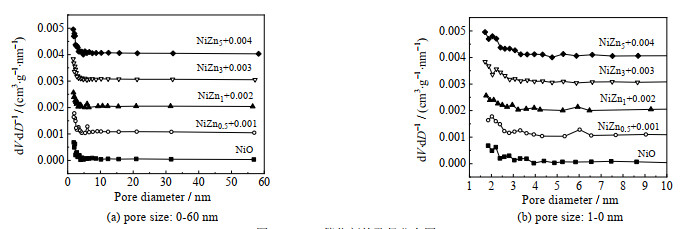
表 1为NiZnx催化剂的原子比、BET比表面积SBET和孔容。从中可以看到,NiZnx催化剂的实际原子比与理论值基本一致,表明不同Zn含量的NiZnx催化剂均被成功合成。通过物理吸附仪得到样品的比表面积和孔容,其中比表面积为2.4~3.3 m2⋅g−1,孔容为0.008~0.013 cm3⋅g−1。催化剂的孔径分布如图 2所示,图中dV⋅dD−1为单位孔径下的孔容积。Ni-Zn金属氧化物作为一种无孔材料,存在少量的介孔,不存在微孔。
|
|
表 1 NiZnx催化剂的元素组成,比表面积和孔容 Table 1 Atomic ratio, BET surface area, total pore volume of NiZnx catalysts |
|
图 2 NiZnx催化剂的孔径分布图 Fig.2 Pore size distributions of NiZnx catalysts obtained by BJH calculations |
表 2为NiZnx催化剂的性能考评结果,其中DH表示脱氢产物,包含1, 3-丁二烯、1-丁烯、2-丁烯。纯NiO催化剂在用于正丁烷氧化脱氢反应时,由于结焦严重,几乎没有催化性能。随着催化剂中Zn含量的逐渐添加,脱氢产物选择性先增大后减小,在Zn与Ni物质的量比n(Zn): n(Ni)=0.5:1时,正丁烷转化率及脱氢产物的选择性最大,分别为11.8% 与26.4%。而在n(Zn): n(Ni)= 5:1时,由于正丁烷转化率非常低,脱氢产物的选择性出现暂时的反弹,这与文献[18]的报道类似。结合XRD表征可知,催化性能与催化剂中Ni0.9Zn0.1O晶相含量呈正相关,说明Ni0.9Zn0.1O晶相有利于烷烃活化。催化性能与ZnO结晶度呈负相关,原因可能是较高的结晶度会抑制晶格氧的流动,从而抑制选择性氧化的进行,降低反应的转化率。
|
|
表 2 NiZnx催化剂的催化性能和产物分布 Table 2 Catalytic performance and product distribution of NiZnx catalysts |
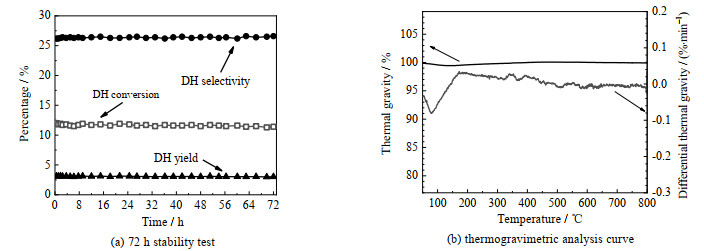
表 2还包含了不同Zn含量的NiZnx催化剂的产物分布。1, 3-丁二烯,1-丁烯的收率随Zn的添加而提高,但其增幅随Zn含量的增加先增大后减少。副反应燃烧产物CO2的收率在n(Zn): n(Ni)=1:1时最大,为7.8%。同时,在该系列催化剂上丁烷的裂解反应也很明显,裂解产物包含甲烷、乙烷、乙烯、丙烷与丙烯,加入Zn元素后,催化剂上存在较多的裂解活化中心位,进一步调控Zn的含量或者Zn氧化物的结构,是提高产物收率的一种途径[19-20]。图 3(a)为催化性能最好的NiZn0.5样品的稳定性考评,连续反应72 h后该样品的活性几乎不变,表现出了优良的稳定性。图 3(b)为NiZn0.5样品反应72 h后的热重分析结果,升温前后样品质量几乎不变,说明加入Zn后催化剂的抗结焦能力大大增强。
|
图 3 NiZn0.5样品的稳定性评价和积炭分析 Fig.3 Stability test and thermogravimetric analysis of NiZn0.5 sample |
正丁烷氧化脱氢反应是一种复杂的平行‒连串反应,影响该反应发生到生成目标产物有许多因素,其中最重要的是催化剂上的氧移动能力,可以通过H2-TPR、TPRO以及XPS来表征这一性质。对于遵循Mvk机理的烃类氧化脱氢反应,催化活性与H抽离速率有关[21],也依赖于活性位点的再氧化速率[3],催化剂的可还原性将会影响反应过程中催化剂氧化还原循环的速率。表 3为NiZnx催化剂的H2-TPR表征的还原温度和H2消耗量。对于NiO,H2-TPR低温峰对应催化剂表面较高价态NiO1+δ的还原,高温峰则对应体相NiO的还原[11]。在纯NiO中添加Zn,还原温度升高,表明Zn与Ni存在阳离子之间的强相互作用,但随着Zn含量逐渐增多,催化剂还原温度的差异逐渐变小,此时充当可还原性的活性物质种类差别不大。NiZn0.5催化剂的还原温度最低,为475.4 ℃。一般来说,催化剂还原温度越低,活性物质更容易还原,表明其表面氧质消耗的速率越快,反应过程中还原-氧化的循环速率也越快,并且NiZn0.5催化剂消耗的氢气量最大,表明该催化剂具有的可还原性的活性物质含量最大,此结果与XRD表征一致。Ni0.9Zn0.1O作为反应的活性物质,NiZn0.5样品的Ni0.9Zn0.1O晶相对应的衍射峰强度最高,消耗的氢气量也最大。随着Zn含量的提高,Ni0.9Zn0.1O晶相衍射峰强度逐渐减弱,催化剂的氢气消耗量也逐渐减小。
|
|
表 3 NiZnx催化剂TPR中H2消耗量 Table 3 H2 consumption of NiZnx catalysts in TPR measurements |
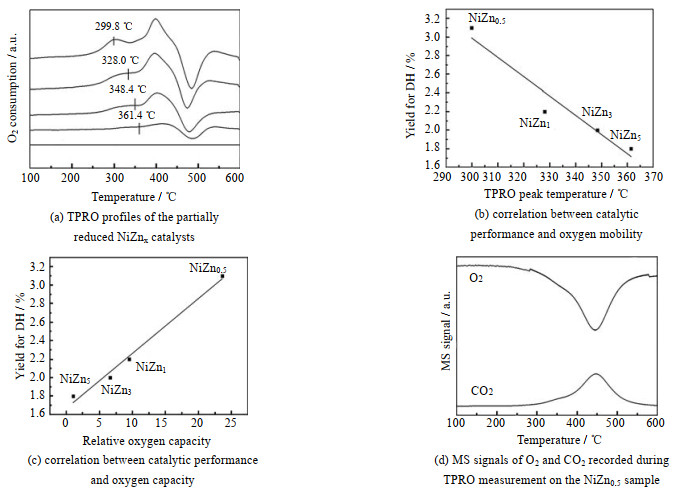
图 4(a)为NiZnx催化剂的TPRO曲线。其中的低温峰是催化剂的再氧化峰,其峰温决定了催化剂中氧的再生能力,催化剂再氧化温度越低,其越容易被氧化,氧移动性越好[13-16],同时,该低温峰的峰温和峰面积分别体现了反应过程中的氧补充速率和催化剂的氧容量,较低的TPRO峰温和较大的TPRO峰面积分别对应较高的氧补充速率和较大的氧容量。纯NiO催化剂在反应过程中结焦严重,几乎没有催化性能。为了与其他催化剂的氧移动性能进行对比,这里把纯NiO催化剂的氧消耗量为0。图 4(b)将TPRO低温峰的峰温与催化性能相关联,在Zn含量(摩尔分数)为0.5时,催化剂的TPRO峰温最低,为299.8 ℃,此时催化剂的催化活性最好。然而随着Zn含量逐渐增多,催化剂的TPRO峰温也越来越高,催化剂的性能愈加下降。图 4(b)表明,在该反应体系的整个氧移动过程(消耗‒迁移‒补充)中,气相氧转变为晶格氧的补充速率是影响催化效果的关键。
|
图 4 NiZnx催化剂的TPRO表征 Fig.4 TPRO characterizations of NiZnx catalysts |
考虑到纯NiO易结焦而NiZnx双组分催化剂表现出稳定的催化性能,说明对于双组分催化剂,当前原料中的氧气与正丁烷进料比例,足以防止由于焦炭沉积导致的催化剂失活,同时,从图 4(a)可知,不同NiZnx催化剂低温峰面积存在较大的差异,因此,需要将催化性能与催化剂的氧容量相关联。图 4(c)显示了DH收率与NiZnx催化剂的相对氧容量之间的相关性。相对氧气容量定义为催化剂的TPRO低温峰面积与NiZn5样品的低温峰面积之比,在Zn含量为0.5时,催化剂的氧容量最高,此时催化剂的性能最好。随着Zn含量增多,催化剂的氧容量也越来越小,催化性能愈加下降。由图 4(c)可知,催化活性随催化剂氧容量的增加而增加,氧容量(参与反应的催化剂中的氧量)在正丁烷氧化脱氢反应起始阶段起重要作用。具有高氧补充速率且高氧容量的催化剂,在反应过程中显示出较高的催化性能和稳定的催化活性。
TPRO谱图中的氧消耗分为低温区和高温区,分别对应低温峰和高温峰。图 4(d)是NiZn0.5催化剂的TPRO-MS信号曲线。图中明显发现既有氧的消耗,又有二氧化碳的生成。一般来说,在低温区,氧气的消耗不伴随有二氧化碳生成,而在高温区,氧气的消耗与二氧化碳的生成是相对应的[3]。此低温区中氧消耗与催化剂中金属价态变化有关系,氧气消耗的同时,金属也被氧化至初始状态;而高温区氧消耗主要用来消除表面积炭。因为在正丁烷预处理催化剂阶段,没有氧气进料,正丁烷与表面氧反应后,催化剂表面产生了积炭。
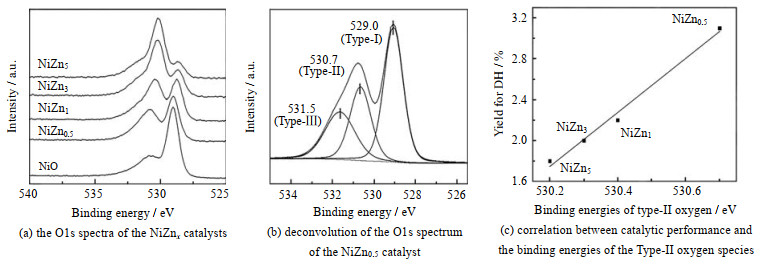
通过XPS进一步探究了催化剂表面氧的性质,并与氧移动性能关联。图 5(a)为NiZnx催化剂的O1s谱图,其中NiZn0.5样品的O1s谱图分峰结果如图 5(b)所示,催化剂表面有3种不同的氧,按结合能由高到低分别为第Ⅲ类、第Ⅱ类、第Ⅰ类氧。第Ⅰ类是催化剂表面上的强结合氧,第Ⅲ类氧物种是催化剂表面的弱结合氧,第Ⅱ类为与丁烷氧化脱氢活性密切相关的活性氧[13-16]。第Ⅱ类氧的结合能大小是影响催化剂的氧移动性强弱的关键因素。第Ⅱ类氧的结合能越大,说明该活性氧越活泼,催化剂的氧移动性越强。对NiZnx催化剂O1s谱图分别进行分峰处理,获得的三类氧结合能大小如表 4所示。NiZnx催化剂的第Ⅱ类氧结合能大小存在明显差异,将表 4中第Ⅱ类氧结合能的大小与催化性能作关联图,如图 5(c)所示。在Zn含量为0.5时,催化剂的第Ⅱ类氧结合能最大,此时催化剂的性能最好,这与TPRO表征结果一致。
|
图 5 NiZnx催化剂的XPS表征 Fig.5 XPS spectra of NiZnx catalysts |
|
|
表 4 NiZnx催化剂上各类氧物种的结合能 Table 4 Binding energies of the oxygen species on NiZnx catalysts |
采用溶胶凝胶法制备NiZnx双金属催化剂,通过H2-TPR、TPRO和XPS表征发现,Zn元素的引入增强了催化剂的氧移动性,增大了催化剂的氧容量并提高了催化剂上的氧补充速率,因此提高了丁烷氧化脱氢的反应活性。具有高氧补充速率并且高氧容量的催化剂还显示出稳定的催化活性,因为气相氧更容易填补反应期间产生的氧空位。双组分催化剂还克服了NiO单组分催化剂易结焦的缺点。在Zn含量为0.5时,正丁烷转化率及脱氢产物的选择性最高,分别为11.8% 与26.4%。
| [1] |
黄杰, 郑哲楠, 罗英武. 嵌段型丙烯腈-丁二烯-苯乙烯树脂的制备与性能[J]. 高校化学工程学报, 2022, 36(5): 757-765. HUANG J, ZHENG Z N, LUO Y W. Preparation and properties of acrylonitrile-butadiene-styrene resins based on block copolymers[J]. Journal of Chemical Engineering of Chinese Universities, 2022, 36(5): 757-765. |
| [2] |
林春光. 正丁烷应用方案研究[J]. 辽宁化工, 2015, 44(7): 827-829. LIN C G. Research on utilization of butane[J]. Liaoning Chemical Industry, 2015, 44(7): 827-829. |
| [3] |
万超. 丁烯氧化脱氢制丁二烯铋钼基催化剂研究[D]. 杭州: 浙江大学, 2015. WAN C. Study on bismuth molybdenum-based catalysts for oxidative dehydrogenation of 1-butene to 1, 3-butadiene [D]. Hangzhou: Zhejiang University, 2015. |
| [4] |
冯锁贵, 王普光, 封银昌, 等. 炼厂碳四综合利用方案比选研究[J]. 石油化工设计, 2011, 28(2): 27-29. FENG S G, WANG P G, FENG Y C, et al. Comparison and selection of comprehensive utilization methods of refinery C4[J]. Petrochemical Design, 2011, 28(2): 27-29. |
| [5] |
JERMY B R, ASAOKA S, AL-KHATTAF S. Influence of calcination on performance of Bi–Ni–O/gamma-alumina catalyst for n-butane oxidative dehydrogenation to butadiene[J]. Catalysis Science & Technology, 2015, 5(9): 4622-4635. |
| [6] |
葛善海, 刘长厚, 范煜, 等. V-Mg-O催化剂上丁烷氧化脱氢动力学研究[J]. 高校化学工程学报, 2001, 15(3): 230-235. GE S H, LIU C H, FAN Y, et al. Kinetic study of the oxidative dehydrogenation of butane over V-Mg-O catalyst[J]. Journal of Chemical Engineering of Chinese Universities, 2001, 15(3): 230-235. DOI:10.3321/j.issn:1003-9015.2001.03.005 |
| [7] |
JERMY B R, AJAYI B P, ABUSSAUD B A, et al. Oxidative dehydrogenation of n-butane to butadiene over Bi–Ni–O/γ-alumina catalyst[J]. Journal of Molecular Catalysis A: Chemical, 2015, 400: 121-131. DOI:10.1016/j.molcata.2015.01.016 |
| [8] |
HERACLEOUS E, LEMONIDOU A A. Ni–Me–O mixed metal oxides for the effective oxidative dehydrogenation of ethane to ethylene-Effect of promoting metal Me[J]. Journal of Catalysis, 2010, 270(1): 67-75. DOI:10.1016/j.jcat.2009.12.004 |
| [9] |
BERGER-KARIN C, RADNIK J, KONDRATENKO E V. Mechanistic origins of the promoting effect of tiny amounts of Rh on the performance of NiOx/Al2O3 in partial oxidation of methane[J]. Journal of Catalysis, 2011, 280(1): 116-124. DOI:10.1016/j.jcat.2011.03.010 |
| [10] |
LI J H, WANG C C, HUANG C J, et al. Mesoporous nickel oxides as effective catalysts for oxidative dehydrogenation of propane to propene[J]. Applied Catalysis A: General, 2010, 382(1): 99-105. DOI:10.1016/j.apcata.2010.04.034 |
| [11] |
WU Y, GAO J, HE Y M, et al. Preparation and characterization of Ni-Zr-O nanoparticles and its catalytic behavior for ethane oxidative dehydrogenation[J]. Applied Surface Science, 2012, 258(11): 4922-4928. DOI:10.1016/j.apsusc.2012.01.120 |
| [12] |
ARNDT S, UYSAL B, BERTHOLD A, et al. Supported ZnO catalysts for the conversion of alkanes: About the metamorphosis of a heterogeneous catalyst[J]. Journal of Natural Gas Chemistry, 2012, 21(5): 581-594. DOI:10.1016/S1003-9953(11)60407-6 |
| [13] |
WAN C, CHENG D G, CHEN F Q, et al. Characterization and kinetic study of BiMoLax oxide catalysts for oxidative dehydrogenation of 1-butene to 1, 3-butadiene[J]. Chemical Engineering Science, 2015, 135: 553-558. DOI:10.1016/j.ces.2014.08.020 |
| [14] |
WAN C, CHENG D G, CHEN F Q, et al. Effects of zirconium content on the catalytic performance of BiMoZrx in the oxidative dehydrogenation of 1-butene to 1, 3-butadiene[J]. Journal of Chemical Technology & Biotechnology, 2016, 91(2): 353-358. |
| [15] |
WAN C, CHENG D G, CHEN F Q, et al. The role of active phase in Ce modified BiMo catalysts for oxidative dehydrogenation of 1-butene[J]. Catalysis Today, 2016, 264: 180-184. DOI:10.1016/j.cattod.2015.06.029 |
| [16] |
WAN C, CHENG D G, CHEN F Q, et al. Oxidative dehydrogenation of 1-butene over vanadium modified bismuth molybdate catalyst: an insight into mechanism[J]. RSC Advances, 2015, 5(53): 42609-42615. DOI:10.1039/C5RA04925C |
| [17] |
王炼, 万超, 程党国, 等. NiZnCe复合氧化物的制备及其催化氧化正丁烷脱氢性能[J]. 化工学报, 2021, 72(1): 534-542. WANG L, WAN C, CHENG D G, et al. Preparation of NiZnCe composite oxide and its catalytic performance for dehydrogenation of n-butane[J]. CIESC Journal, 2021, 72(1): 534-542. |
| [18] |
BATIOT C, HODNETT B K. The role of reactant and product bond energies in determining limitations to selective catalytic oxidations[J]. Applied Catalysis A: General, 1996, 137(1): 179-191. DOI:10.1016/0926-860X(95)00322-3 |
| [19] |
CHEN F Q, HAO J, YU Y Y, et al. The influence of external acid strength of hierarchical ZSM-5 zeolites on n-heptane catalytic cracking[J]. Microporous and Mesoporous Materials, 2022, 330: 111575. DOI:10.1016/j.micromeso.2021.111575 |
| [20] |
LEE H, JUNG J C, KIM H, et al. Effect of pH in the preparation of ZnFe2O4 for oxidative dehydrogenation of n-butene to 1, 3-butadiene: Correlation between catalytic performance and surface acidity of ZnFe2O4[J]. Catalysis Communications, 2008, 9(6): 1137-1142. DOI:10.1016/j.catcom.2007.10.023 |
| [21] |
ZHAI Z, WANG X, LICHT R, et al. Selective oxidation and oxidative dehydrogenation of hydrocarbons on bismuth vanadium molybdenum oxide[J]. Journal of Catalysis, 2015, 325: 87-100. DOI:10.1016/j.jcat.2015.02.015 |




