内切-β-葡聚糖酶是纤维素酶的主要组成之一,具有重要的工业应用价值[1]。里氏木霉(Trichoderma reesei)是生产纤维素酶的常用菌种,由该菌生产的内切-β-葡聚糖酶适用于酸性反应体系,其最适作用pH为4.8,当反应温度高于50℃ 时酶活力迅速下降[2]。这一特性大大限制了该酶在棉织物水洗整理、废纸脱油墨、制浆造纸、含酶洗洁剂以及环保等领域中的广泛应用[3~6]。
由刺糙青霉(Penicillium echinulatum)所产的内切-β-葡聚糖酶的pH作用范围广,且热稳定性好[7, 8]。但野生型刺糙青霉的产酶水平低,发酵成本高,不适于工业化生产[9]。近年来,采用里氏木霉生产异源重组蛋白方面的研究方兴未艾,利用里氏木霉的强启动子Pcbh1 (纤维二糖水解酶I启动子) 及信号肽,可以实现外源基因的高效表达和胞外分泌[10],丝状真菌作为外源基因表达的宿主系统,还可以简化表达产物的分离提取,这方面的研究工作具有良好的发展前景[11, 12]。
本文将刺糙青霉内切-β-葡聚糖酶基因经过密码子优化后,插入里氏木霉强启动子Pcbh1(及其信号肽)和终止子Tcbh1之间,并以pCAMBIA1300为载体构建重组质粒,进一步通过根瘤农杆菌介导转化技术,将重组质粒导入里氏木霉的分生孢子中,并成功实现了目的基因的高效表达与胞外分泌。因此本研究对于新型纤维素酶制剂的研究开发及其工业化应用具有重要的促进作用。
2 材料与方法 2.1 菌株和质粒 2.1.1 菌株大肠杆菌 (Escherichia coli DH5α)、里氏木霉 (Trichoderma reesei ZU-02[13])、根癌农杆菌 (Agrobacterium tumefaciens AGL-1) 均为本实验室保存菌株。
2.1.2 质粒pMD18-T simple vector和pUC18均购自Takara公司;pDESTR (含潮霉素磷酸转移酶基因,Genbank:AB218275.1) 和pCAMBIA1300均为实验室保存质粒。
2.2 培养基 2.2.1 种子培养基(g⋅L-1) 葡萄糖15,酵母抽提物 20,(NH4)2SO4 2.5,KH2PO4 6,MgSO4 0.8,CaC12 1.0。
2.2.2 筛选培养基(g⋅L-1) 马铃薯(去皮)200,葡萄糖20,琼脂20,潮霉素B 0.1,头孢霉素0.2。
2.2.3 复筛培养基(g⋅L-1) 羧甲基纤维素钠20,(NH4)2SO4 5,KH2PO4 15,MgSO4 0.8,CaC12 0.6,FeSO4⋅7H2O 0.005,MnSO4 ⋅H2O 0.0016,ZnSO4⋅7H2O 0.0014,CoCl2⋅6H2O 0.0037,潮霉素B 0.1,琼脂粉 18。
2.2.4 产酶培养基(g⋅L-1) 乳糖40,蛋白胨5,(NH4)2SO4 2.8,KH2PO4 4,MgSO4⋅7H2O 0.6,CaCl2 0.6,FeSO4⋅7H2O 0.005,MnSO4⋅H2O 0.0016,ZnSO4 ⋅7H2O 0.0014,CoCl2 ⋅6H2O 0.0037。
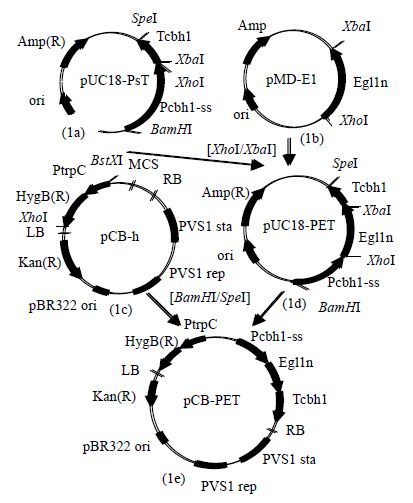
2.3 目的基因Egl1n的制备从基因文库中调取刺糙青霉内切-β-葡聚糖酶Egl1的基因序列 (GenBank: FJ998421),在氨基酸序列不改变的前提下,根据里氏木霉的密码子偏好,通过生物信息学软件(DNA2.0 Tool)对Egl1的基因序列进行密码子优化,并在该序列的上下游分别引入限制性内切酶XhoI /XbaI的切割位点,将密码子优化后的基因序列标记为Egl1n。采用ABI 3900型高通量DNA合成仪合成Egl1n基因,并克隆至载体pMD18-T,构建成pMD-E1质粒 (图 1)。
|
图 1 重组载体pCB-PET 的构建图谱 Fig.1 Construction of recombinant vector pCB-PET |
以里氏木霉基因组DNA为模板,根据Genbank报道的序列设计引物,分别扩增纤维二糖水解酶I启动子Pcbh1 (包含cbh1信号肽序列) 和终止子Tcbh1序列,将PCR产物连接到pMD18-T simple vector,进一步将Pcbh1和Tcbh1序列依次插入PUC18的BamH I和Spe I位点,构建得到质粒PUC18-PsT。
以质粒 pDESTR为模板,根据GenBank报道的序列设计PCR引物,通过PCR获得构巢曲霉色氨酸合成基因的启动子(PtrpC) 和潮霉素B磷酸转移酶基因 (HygB)。将PCR产物连接到pMD18-T simple vector,插入到pCAMBIA1300载体XhoI和BstXI位点,构建得到含潮霉素抗性筛选标记的农杆菌介导载体pCB-h。
以XhoI和XbaI分别双酶切质粒pUC18-PsT和pMD-E1,将Egl1n基因片段以T4连接酶连接至pUC18-PsT信号肽和终止子之间,得到重组质粒pUC18-PET。
以BamHI和SpeI分别双酶切pCB-h和pUC18-PET,进一步将含启动子和终止子的Egl1n基因插入到pCB-h的多克隆位点 (MCS) 中,得到重组质粒pCB-PET。质粒pCB-PET含潮霉素筛选标记和Egl1n基因,可用于农杆菌介导转化。
2.5 Egl1n基因序列的PCR检测根据Egl1n基因序列设计PCR上游引物(5'→3'):CCTCCTGCTTCCCGCTCC;下游引物(5' 3'):CAGGCACTGGGAGTAGTAGT。
PCR反应条件:94℃ 预变性10 min,30 次扩增循环 (94℃×1 min、52℃×1 min、72℃×1 min 30 s),72℃ 延伸 10 min。
2.6 根瘤农杆菌介导 (Agrobacterium tumefaciens-mediated transformation,AMT) 转化里氏木霉将重组质粒pCB-PET用冻融法转入根瘤农杆菌AGL-1,具体操作步骤见参考文献[14]。
2.7 里氏木霉基因组DNA的提取取重组里氏木霉菌体培养液4000 r⋅min-1离心10 min收集菌体,用无菌水反复洗涤,离心并干燥。用液氮快速研磨至粉状,取100 mg菌丝粉末置于1.5 mL的离心管,加入400 μL的真菌基因组提取液 (50 mmol⋅L-1 Tris-HCl;150 mmol⋅L-1 NaCl;100 mmol⋅L-1 EDTA) 震荡混匀;加入50 μL 10% SDS,震荡混匀后65℃水浴1 h;加入等体积的酚/氯仿/异戊醇 (25 : 24 : 1),震荡混匀后离心;取上层水相加入0.65倍体积的异丙醇,4℃ 沉淀30 min;离心弃上清,用70% 乙醇洗涤两次,干燥后用适量无菌水溶解,加RNA酶(终浓度为0.1 μg⋅μL-1) 37℃处理1 h。
2.8 转化子的复筛用切割器分别在转化子菌落上切取直径为0.3 cm的菌块,每个转化子取3块转接到复筛平板培养基上,30℃ 培养2~3 d,定时观察,记录菌落生长直径,从中选出生长速率快,菌落直径大的转化子。
2.9 重组转化子产酶试验将斜面菌种接种到液体种子培养基中,30℃,200 r⋅min-1摇瓶培养48 h后转接至产酶培养基,250 mL摇瓶装液量50 mL,接种量10% (v/v),28℃,200 r⋅min-1振荡培养[18],定时取样检测上清液的内切-β-葡聚糖酶活力。每个转化子做三个平行摇瓶产酶实验。
2.10 SDS-PAGE蛋白电泳将发酵液于10000~12000 r⋅min-1离心5 min,取上清液进行蛋白质电泳。采用的聚丙烯酰胺浓度为12%,染色液为0.1%的考马斯亮蓝R-250,脱色液配方为甲醇:水:乙酸 (2:7:1)。
2.11 内切-β-葡聚糖酶活力测定以1% 羧甲基纤维素钠 (CMC) 溶液为底物,加入0.5 mL适当稀释的酶液,于设定的温度、pH值条件下反应一定时间后,采用DNS法 (3,5-二硝基水杨酸法)[19]测定上清液中的还原糖。一个酶活力单位为标准反应条件下1 h内生成1 mg还原糖所需的酶量,以U⋅mL-1表示。
2.12 酶液的最适反应pH值及pH稳定性测定最适pH试验:用缓冲液配制不同pH (4.0、4.5、5.0、5.5、6.0、6.5、7.0、7.5、8.0、8.5、9.0、9.5、10.0、10.5和11.0) 的CMC底物溶液,取酶液分别测定不同pH条件下的内切-β-葡聚糖酶活力,酶反应温度为60℃。
pH稳定性试验:将酶液分别在pH值为4.0、4.5、5.0、5.5、6.0、6.5、7.0、7.5、8.0、8.5、9.0、9.5、10.0、10.5和11.0,60℃条件下保温60 min后,再在60℃、pH 8.0条件下测定内切-β-葡聚糖酶活力。
2.13 酶液的最适反应温度及温度稳定性测定最适温度试验:将酶促反应温度设为30、35、40、45、50、55、60、65和70℃,分别测定试样在pH 8.0时的内切-β-葡聚糖酶活力。
温度稳定性试验:将酶液分别在温度为30、35、40、45、50、55、60、65和70℃ 的水浴中,pH 8.0,保温2 h后,再在60℃、pH 8.0条件下测定内切-β-葡聚糖酶活力。
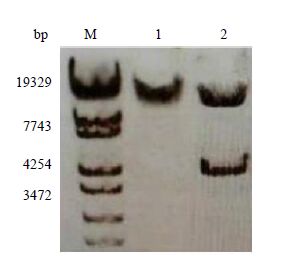
3 结果与讨论 3.1 重组载体pCB-PET的验证分析重组质粒经SpeI单酶切获得大小约为14.6 kb的条带,经SpeI/BamHI双酶切分别得到4.2 kb和10.4 kb条带 (图 2),分别与Egl1n基因表达盒 (Pcbh1+Egl1n+Tcbh1)、pCB-PET载体的片段大小相符。
|
图 2 重组质粒pCB-PET 的酶切验证 Fig.2 Enzyme digestion of recombinant plasmid pCB-PET M: DNA Marker 1: plasmid pCB-PET digested by SpeI 2: plasmid pCB-PET digested by SpeI and BamHI |
前期研究工作已经探明:采用根瘤农杆菌介导技术,可将外源基因顺利导入里氏木霉细胞[20, 21]。本项目将里氏木霉分生孢子预萌发3 h后再进行介导转化试验,发现共培养时间可由原来的48 h缩短至36 h;转化子在潮霉素抗性培养基上的培养时间从原来的4~6 d缩短至2 d,转化效率可提高约20倍以上。
在含潮霉素B的筛选培养平板上挑取获得226个重组里氏木霉转化子,进一步采用复筛培养基进行复筛试验 (表 1),试验结果显示:30℃培养3 d后,菌落直径达到4.0 cm以上的有5个转化子。由于所采用的复筛培养基中羧甲基纤维素为唯一碳源,转化子在含潮霉素B的培养平板上的生长速率与其内切-β-葡聚糖酶的表达水平呈正相关。将复筛中选出5个优良转化子依次编号为T1-T5。
| 表 1 里氏木霉转化子的复筛试验结果 Table 1 Screening results of the T. reesei transformants |
将筛选得到的5个转化子在PDA培养基上各传代培养10个批次,分别提取转化子和原始菌株基因组,利用2.5节所述方法进行目的基因PCR检测。
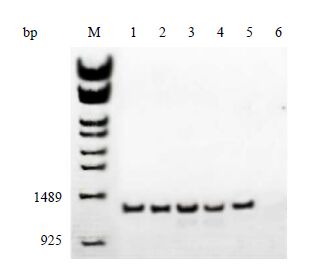
结果5个转化子的基因组都可以扩增得到大小约为1.2 kb的目的基因 (Egl1n) 条带 (见图 3),而对照菌株的PCR结果没有出现相应的条带。进一步对PCR扩增基因片段进行测序,结果表明:该基因全长为1161 bp,编码含387个氨基酸的成熟肽;同GenBank的核苷酸 序列比较分析显示,同源性可以达到98%,而氨基酸序列的同源性达到100%。说明目的基因Egl1n已整合到里氏木霉染色体上并且遗传稳定。
|
图 3 里氏木霉转化子染色体DNA 中目的 基因Egl1n 的PCR 检测结果 Fig.3 Electrophoresis of Egl1n gene obtained by PCR from chromosomal DNA of recombinant T. reesei. M: DNA Marker; 1-5: Egl1n gene from transformants 1-5 6: original strain |
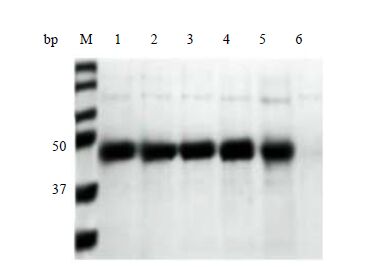
取T1-T5转化子48 h摇瓶发酵液,进行SDS-PAGE蛋白电泳,结果如图 4所示。5个重组里氏木霉转化子的电泳图谱在约41 kDa处均有明显的蛋白条带,该条带与目的基因表达蛋白的位置相符,而出发菌株在该处未出现条带。电泳试验结果表明:新型内切-β-葡聚糖酶基因在重组里氏木霉中已得到了成功表达,而且表达蛋白可分泌到胞外。
|
图 4 重组里氏木霉发酵液的SDS-PAGE 蛋白电泳 Fig.4 SDS-PAGE analysis of fermentation broth from recombinant T. reesei M: protein standard markers 1-5: recombinant T. reesei 6: original strain |
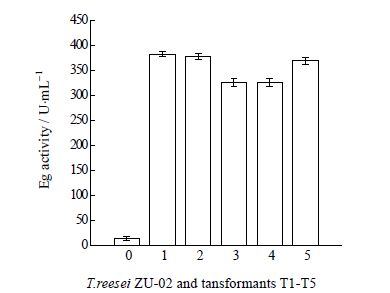
将复筛得到的5个重组里氏木霉转化子和出发菌株分别进行产酶实验,摇瓶培养48 h后,取发酵液检测内切-β-葡聚糖酶(EG) 活力,结果如图 5所示。5个转化子的碱性内切-β-葡聚糖酶活力活力与出发菌株相比都有显著提高,其中转化子T1的碱性内切-β-葡聚糖酶活力达到了382.6 U⋅mL-1,约为出发菌株的22.5倍。选取T1进行后续的酶学性质研究。
|
图 5 不同转化子摇瓶培养48 h 的碱性内切-β-葡聚糖酶活力 Fig.5 Alkali endo-β-glucanase activity of different T. reesei transformants after fermentation in shaking flasks for 48 h 0: T. reesei original strain 1~5: T. reesei transformants. Each value is mean of three replicates. Error bars indicate standard error. |
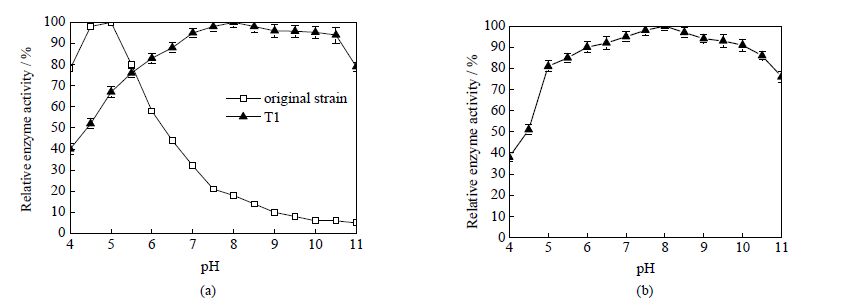
按照2.12节实验方法,对转化子T1所产酶液的最适反应pH值及pH稳定性进行研究,所有数据均重复三次,随后取平均值作图,结果如图 6所示:重组内切-β-葡聚糖酶在pH 5.0~10.5有明显的催化活性,在pH 8.0时活性最高;该酶在pH 5.0而出发菌株所产内切-β-葡聚糖酶的最适pH作用范围为4.5~5.0 (图 6(a)),属于酸性酶,当pH高于5.5时,酶活急剧下降。本研究中由重组里氏木霉生产的内切-β-葡聚糖酶在中性及偏碱性环境中有较高活力,其适用范围更广、具有良好的实际应用价值。
|
图 6 pH 值对酶的催化性能(a)及稳定性(b)的影响 Fig.6 Effects of pH value on endo-β-glucanase activity (a) and stability (b) Each value is mean of three replicates, error bars indicate standard error. |
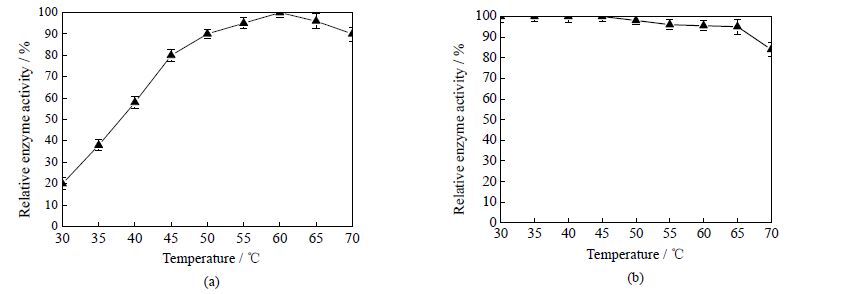
按照2.13节实验方法,对转化子T1所产酶液的最适反应温度及温度稳定性进行研究,所有数据均重复三次,随后取平均值作图,结果如图 7所示:重组内切-β-葡聚糖酶的最适反应温度为60℃,该酶具有良好的耐热性能,在温度低于65℃ 时非常稳定,即使在70℃、pH8.0条件下处理2 h,相对酶活力仍可保持在84% 以上 (图 7(b)),该特性在酶制剂的实际应用及储存过程中具有明显的竞争优势。
|
图 7 温度对酶的催化性能(a)及稳定性(b)的影响 Fig.7 Effects of temperature on endo-β-glucanase activity (a) and stability (b) Each value is mean of three replicates, error bars indicate standard error. |
本文将优化后的刺糙青霉内切-β-葡聚糖酶基因置于里氏木霉的强启动子Pcbh1及信号肽下游,以农杆菌介导转化载体pCAMBIA1300为骨架,成功构建了带有潮霉素B抗性标记的重组质粒pCB-PET。该载体可将目的基因导入里氏木霉宿主,并实现高效表达与胞外分泌。通过筛选获得了5个基因重组里氏木霉转化子。在摇瓶产酶条件下,发酵48 h酶活力最高的一株转化子(T1)碱性内切-β-葡聚糖酶活力提高至出发菌株的22.5倍,成功实现了碱性内切-β-葡聚糖酶基因在里氏木霉中的高效表达。由重组里氏木霉生产的新型内切-β-葡聚糖酶最适作用pH为8.0,最适反应温度为60℃,具有pH作用范围广,耐碱、耐高温特性,该酶在棉织物生物整理、制浆造纸等领域中具有重要的应用价值。
| [1] | Saloheima M, Pakula T . The cargo and the transport system:secreted proteins and protein secretion in Trichoderma reesei (Hypocrea jecorina)[J]. Microbiology , 2012, 158 (1) : 46-57 DOI:10.1099/mic.0.053132-0 |
| [2] | Heikinheimo L, Buchert J, Miettinen-Oinonen A . Treating denim fabrics with Trichoderma reesei cellulases[J]. Textile Research Journal , 2000, 70 (11) : 969-973 DOI:10.1177/004051750007001106 |
| [3] | Bhat M K . Cellulases and related enzymes in biotechnology[J]. Biotechnology Advances , 2000, 18 (5) : 355-383 DOI:10.1016/S0734-9750(00)00041-0 |
| [4] | Miettinen-Oinonen A, Londesborough J, Joutsjoki V . Three cellulases from Melanoarpus Albomyces with applications in the textile industry[J]. Enzyme and Microbial Technology , 2004, 34 (1) : 332-341 |
| [5] | Zhang Y H P, Himmel M E, Mielenz J R . Outlook for cellulose improvement:screening and selection strategies[J]. Biotechnology Advances , 2006, 24 (5) : 452-481 DOI:10.1016/j.biotechadv.2006.03.003 |
| [6] | Kumar R, Singh S, Singh O V . Bioconversion of lignocellulosic biomass:biochemical and molecular perspectives[J]. Journal of Industrial Microbiology and Biotechnology , 2008, 35 (5) : 377-391 DOI:10.1007/s10295-008-0327-8 |
| [7] | Dillon A J P, Zorgi C, Camassola M . Use of 2-deoxyglucose in liquid media for the selection of mutant strains of Penicillium echinulatum producing increased cellulase and β-glucosidase activities[J]. Applied Microbiology and Biotechnology , 2008, 70 (6) : 740-746 |
| [8] | Camassola M, De Bittencourt L R, Shenem N T . Characterization of the cellulase complex of Penicillium echinulatum[J]. Biocatalysis and Biotransformation , 2004, 22 (5-6) : 391-396 DOI:10.1080/10242420400024532 |
| [9] | Rau M, Heidemann C, Pascoalin A M . Application of cellulases from Acrophialophora nainiana and Penicillium echinulatum in textile processing of cellulosic fibres[J]. Biocatalysis and Biotransformation , 2008, 26 (5) : 383-390 DOI:10.1080/10242420802249430 |
| [10] | Wang B B, Xia L M . High efficient expression of cellobiase gene from Aspergillus niger in the cells of Trichoderma reesei[J]. Bioresource Technology , 2011, 102 (6) : 4568-4572 DOI:10.1016/j.biortech.2010.12.099 |
| [11] | Kiiskinen L L, Kruus K, Bailey M . Expression of Melanocarpus albomyces laccase in Trichoderma reesei and characterization of the purified enzyme[J]. Microbiology-Sgm , 2004, 150 (9) : 3065-3074 DOI:10.1099/mic.0.27147-0 |
| [12] | Liu T, Wang T H, Li X . Improved heterologous gene expression in Trichoderma reesei by cellobiohydrolase I gene (cbh1) promoter optimization[J]. Acta Biochimica et Biophysica Sinica , 2008, 40 (2) : 158-165 DOI:10.1111/abbs.2008.40.issue-2 |
| [13] | Xia L M, Shen X L . High-yield cellulase production by Trichoderma reesei ZU-02 on corn cob residue[J]. Bioresource Technology , 2004, 91 (3) : 259-262 DOI:10.1016/S0960-8524(03)00195-0 |
| [14] | Jyothishwaran G, Kotresha D, Selvaraj T . A modified freeze-thaw method for efficient transformation of Agrobacterium tumefaciens[J]. Current Science , 2007, 93 (6) : 770-772 |
| [15] | Sun W L, Liu L X, Hu X L . Generation and identification of DNA sequence flanking T-DNA integration site of Trichoderma atroviride mutants with high dichlorvos-degrading capacity[J]. Bioresource Technology , 2009, 100 (23) : 5941-5946 DOI:10.1016/j.biortech.2009.06.031 |
| [16] | Michielse C B, Hooykaas P J J, Vanden Hondel C A . Agrobacterium-mediated transformation of the filamentous fungus Aspergillus awamori[J]. Nature Protocols , 2008, 3 (10) : 1671-1678 DOI:10.1038/nprot.2008.154 |
| [17] | Jyothishwaran G, Kotresha D, Selvaraj T . A modified freeze-thaw method for efficient transformation of Agrobacterium tumefaciens[J]. Current Science , 2007, 93 (6) : 770-772 |
| [18] | HUANG Zhen-yan(黄振艳), XIA Li-ming(夏黎明) . Study on the soluble inducer for cellulase production derived from glucose by glucosylase(利用葡萄糖转苷酶制备纤维素酶可溶性诱导物的研究)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报) , 2009, 23 (2) : 270-274 |
| [19] | Miller G L . Use of dinitrosalicylic acid reagent for the determination of reducing sugar[J]. Analytical Chemistry , 1959, 31 (3) : 426-428 DOI:10.1021/ac60147a030 |
| [20] | Jin X, Xia L M . Heterologous expression of an endo-b-1,4-glucanase gene from the anaerobic fungus Orpinomyces PC-2 in Trichoderma reesei[J]. World Journal of Microbiology and Biotechnology , 2011, 27 (12) : 2913-2920 DOI:10.1007/s11274-011-0774-7 |
| [21] | Fang H, Xia L M . Heterologous expression and production of Trichoderma reesei cellobiohydrolase II in Pichia pastoris and the application in the enzymatic hydrolysis of corn stover and rice straw[J]. Biomass and Bioenergy , 2015, 78 (1) : 99-109 |




