氯酚类化合物是一类重要的化工原料,被广泛用于制造杀虫剂、除草剂、防腐剂等。在传统的造纸工业中,运用含氯漂白技术也会产生大量氯酚类化合物[1]。氯酚类化合物在环境中分布广泛,检出率较高,具有高毒性、生物积累性,且较难被自然降解,严重危害环境安全和人类健康[2~4]。2, 4, 5-三氯酚是一种典型的氯酚类物质,其本身可用作除草剂,也可用于生产农药等化工产品,用量较大,且毒性强,在土壤环境中持久性较强,对人类和环境安全构成严重威胁。世界健康组织已正式提出2, 4, 5-三氯酚等氯酚类物质具有致癌性和致突变性[5],因此由其引发的环境污染问题已不容忽略。
漆酶(Laccase,EC 1.10.3.2)是一类多铜氧化酶,属于蓝色多铜氧化酶家族,能利用分子氧在自由基催化机制作用下,氧化酚类和非酚类的物质。由于漆酶底物谱宽泛,仅利用氧气作为最终电子受体,无需辅因子或过氧化物协助,作为一种环境友好型催化剂,漆酶在有机污染物治理方面具有很好的应用潜能[6-7]。但漆酶的氧化还原电势较低,难以直接作用氧化还原电势较高的底物,且部分底物受空间位阻效应影响,漆酶难以直接催化氧化。
小分子介体物质可通过电子传递或氢原子转移机制,进一步拓展漆酶对难降解物质的催化能力和作用范围[8-10]。常用的人工合成介体包括1-羟基苯并三唑(HBT)、2, 2-联氮-二(3-乙基-苯并噻唑-6-磺酸)二铵盐(ABTS)、紫脲酸等。在实际应用过程中虽然合成介体能够有效促进漆酶作用底物,但由于其高昂的合成费用和潜在的毒性,难以实现规模化应用。天然介体是木质素自然降解过程中产生的一些小分子酚类物质及其衍生物,如丁香醛、乙酰丁香酮、香草醛、香草乙酮、对香豆酸、芥子酸等均可有效促进漆酶作用潜能,且对环境污染风险小[10-11]。从现有研究来看,天然介体的催化降解效果与人工合成介体相当,在某些领域甚至要优于合成介体[12-15]。
漆酶的生产方式主要有液态发酵与固态发酵两种,相较于液态发酵,利用固态发酵具有以下优点[1, 16]:操作简便且能耗低;能直接利用农业废弃物及粮食加工业下脚料,原料成本低;生产过程所需耗水量低,后续产生废水量少等优势。农作物秸秆是重要的可再生资源,但长期以来未能得到有效应用,任由其在自然条件下发生腐解效率低下,且易引发病虫害,而直接进行秸秆焚烧将造成严重的环境污染问题[17-18]。利用秸秆进行固态发酵,能有效解决由其过量堆积引起的环境问题,所产漆酶亦可用于后续环境污染治理。
本实验室在前期工作中,已将来源于血红密孔菌(Pycnoporus sanguineus)耐热性漆酶基因导入到里氏木霉分生孢子中,获得了高产漆酶的重组里氏木霉[19]。该重组里氏木霉具有强启动子Pcbh1及信号肽,可以实现外源基因的高效表达和胞外分泌[20-21]。此外,丝状真菌作为外源基因表达的宿主系统,还可以简化表达产物的分离提取[22-23]。本文利用重组里氏木霉转化子固态发酵产漆酶,考察了5种介体物质对漆酶降解2, 4, 5-三氯酚反应的影响,构建适宜的漆酶-介体反应体系,并通过优化反应条件,得到2, 4, 5-三氯酚降解反应进程,为漆酶在氯酚类污染物治理方面的应用奠定了坚实的基础。
2 实验材料和方法 2.1 材料 2.1.1 菌种重组里氏木霉(Trichoderma reesei Z-08)为本实验室构建并保藏[19]。
2.1.2 试剂2, 4, 5-三氯酚(2, 4, 5-TCP)标品购自Aladdin、香草醛(vanillin)、丁香醛(syringaldehyde)、丁香酸(syringic acid)、1-羟基苯并三唑(HBT)、2, 2-联氮-二(3-乙基-苯并噻唑-6-磺酸)二铵盐(ABTS)购自生工生物工程(上海),其余试剂均为分析纯。
2.1.3 含2, 4, 5-TCP污染土壤浸出液的制备2, 4, 5-TCP污染土壤取自浙江绍兴郊区某农田,利用含φ=5%甲醇的柠檬酸-磷酸氢二钠缓冲液(50 mmol·L-1,pH 4.6)对土壤进行抽提,所获抽提液重复超声3次,每次持续5 min,震荡15 min后4 000 r·min-1下离心,收集上清液,过滤,即得含2, 4, 5-TCP的污染土壤浸出液,测得其中2, 4, 5-TCP含量为59.7 mg·L-1,后续实验即在此浸出液基础上进行。
2.2 培养基PDA斜面培养基(g·L-1):马铃薯200,葡萄糖20,琼脂粉20。
固态发酵培养基(g/100 g培养基):氨水预处理后水稻秸秆70,麸皮25,(NH4)2SO4 2.5,尿素0.5,KH2PO4 0.5,CuSO4 0.025,调节含水率至70%。
2.3 固态发酵产漆酶及漆酶制备将重组里氏木霉接种到PDA斜面上,30 ℃培养5 d后取出。用20 mL无菌水从PDA斜面上洗下里氏木霉的孢子,制成孢子悬浮液,以10%(v/w)接种量转接至固态培养基,30 ℃,静置培养,每隔2 d取样,测定酶活力及秸秆降解率,得到固态发酵产酶及降解进程。
发酵完成后,每5 g酶曲,加入100 mL水,室温下浸泡24 h,于6 000 r·min-1下离心8 min,收集上清液,过滤,即得粗酶液,置于4 ℃下保存备用。
2.4 不同介体对漆酶降解2, 4, 5-TCP的影响2, 4, 5-TCP降解反应在试管中进行,包含5 mL 2, 4, 5-TCP污染的土壤浸出液(pH 4.6),漆酶用量为0.2 IU·mL-1,考察终浓度为0.2 mmol·L-1的5种介体(香草醛、丁香醛、丁香酸、HBT、ABTS)及未添加介体对漆酶降解2, 4, 5-TCP反应的影响,并以添加等量灭活后漆酶为对照,60 ℃,80 r·min-1下震荡反应2 h后利用HPLC法测定2, 4, 5-TCP含量,计算降解率。
2.5 漆酶-丁香醛系统对2, 4, 5-TCP的降解漆酶-丁香醛系统对2, 4, 5-TCP降解实验在试管中进行,包含5 mL 2, 4, 5-TCP污染的土壤浸出液,考察不同漆酶用量,丁香醛用量,温度,pH对漆酶降解2, 4, 5-TCP反应的影响,得到最适反应条件,并在最适反应条件下,每隔30 min取样,得到反应进程。
2.6 分析测定方法漆酶活力测定按照文献[24]方法进行:以ABTS为底物,利用分光光度计测定反应体系在420 nm处前2 min吸光值的变化值,每分钟反应1 μmol ABTS定义为一个漆酶活力单位(IU·mL-1)。
滤纸酶活力(代表纤维素酶的总活力)测定采用国际纯化学与应用化学联合会推荐的方法[25]。以6 cm×1 cm Whatman No.1滤纸条为底物, 取0.5 mL适当稀释的酶液,在总反应体系为1.5 mL,pH为4.6的柠檬酸缓冲体系下,50 ℃,80 r·min-1,震荡反应30 min后,利用DNS (3, 5-二硝基水杨酸)法[26]测定还原糖含量。在标准反应条件下,每分钟生成1 μmol葡萄糖(以还原糖计)所需的酶量,定义为一个滤纸酶活力(FPA)国际单位(IU·g-1)。
秸秆失重率计算,记录接种前固态基质重量为w0,发酵完成后, 向固态基质中加入适量比例水,浸泡24 h后,于6 000 r·min-1下离心8 min,收集离心底部固态基质,105 ℃干燥至恒重量,记为w。
固体发酵的失重率计算:
| $ \text{失重率=}\frac{({{w}_{0}}-w)}{{{w}_{0}}}\times 100% $ |
其中w0为固态发酵前固态基质重量,w为固态发酵后剩余固态基质重量。
2, 4, 5-TCP检测:向5 mL反应体系中加入等体积甲醇,促使反应体系中2, 4, 5-TCP充分溶解,吸取1 mL样品,过0.45 μm水膜, 利用高效液相色谱仪(Agilent 1200, USA)进行检测,测定时以甲醇/水(φ=85/15)为流动相,采用Eclipse XDB-C18(150 mm×4.6 mm×5 μm)色谱柱,流速1.0 mL·min-1,柱温30 ℃;检测波长220 nm,进样量20 μL。以2, 4, 5-TCP标准品绘制标准曲线,采用外标法定量。
2, 4, 5-TCP降解率计算:
| $ \text{降解率}\text{=}\frac{{{C}_{0}}-C}{{{C}_{0}}}\times 100% $ |
其中C0为降解反应前2, 4, 5-TCP的浓度,C为降解反应后2, 4, 5-TCP的浓度。
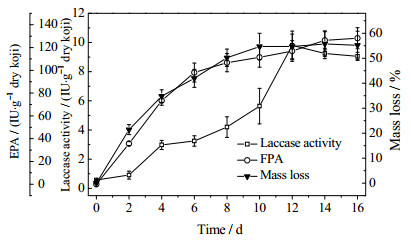
3 结果与讨论 3.1 固态发酵产漆酶进程以水稻秸秆为原料,采用重组里氏木霉进行固态发酵,结果如图 1所示。重组里氏木霉能够在水稻秸秆基质中快速生长,并分泌纤维素酶和漆酶。至发酵第12 d,漆酶和纤维素酶(FPA)活力分别达到10.12和116.96 IU·g-1,秸秆失重率为54.73%。由重组里氏木霉产生的纤维素酶可以在秸秆降解中继续发挥重要作用,而漆酶可在土壤有机污染物治理方面发挥其特有的性能。
|
图 1 固态发酵产酶及秸秆降解进程 Fig.1 Profiles of enzyme production and straw degradation during solid-state fermentation |
利用重组里氏木霉对水稻秸秆进行快速降解,不仅有利于秸秆还田,增加土壤肥力,还可以促进土壤有机污染物的降解,具有良好的推广应用前景。
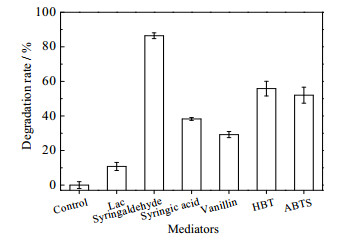
3.2 不同介体对漆酶降解2, 4, 5-TCP的影响研究了多种介体对漆酶降解2, 4, 5-TCP的影响,实验结果如图 2所示,2, 4, 5-三氯酚在实验周期内自身不会发生降解作用,单独利用漆酶降解效果不明显。添加丁香醛能显著促进漆酶降解2, 4, 5-TCP,降解率可达86.42%,添加丁香酸和香草醛也能促进2, 4, 5-TCP降解,但降解率未能超过40%。人工合成介体HBT和ABTS虽然也能促进2, 4, 5-三氯苯酚降解,降解率可达55.82%和52.01%。LISOV等利用漆酶对多氯酚进行转化试验后,发现添加介体HBT能够显著提高漆酶作用效果[27]。虽然利用合成介体能拓展漆酶作用范围及效率,但通常合成介体的稳定性较差,使用成本较高,且具有潜在毒性,会产生某些毒副产物,造成漆酶失活及环境污染[28-29]。丁香醛是木质素自然降解过程中产生的衍生物,利用天然介体丁香醛可有效避免上述缺陷,无污染环境风险,且使用成本较低,漆酶-丁香醛系统可实现对2, 4, 5-TCP的有效降解,更具实际应用价值。
|
图 2 不同介体对漆酶降解2, 4, 5-TCP的影响 Fig.2 Effects of different mediators on 2, 4, 5-TCP degradation by laccase |
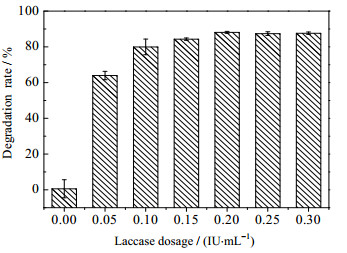
考察漆酶用量对2, 4, 5-TCP降解反应影响,在丁香醛用量均为0.2 mmol·L-1的条件下,改变反应体系中漆酶用量(0~0.3 IU·mL-1),测定2, 4, 5-TCP降解率,实验结果如图 3所示,漆酶在2, 4, 5-TCP降解中起关键作用,2, 4, 5-TCP降解率随漆酶用量增加而提高,当漆酶用量达到0.2 IU·mL-1时,2, 4, 5-TCP降解率达到87.59%,后续进一步提高漆酶用量,此时漆酶用量已不再是反应限制因素,2, 4, 5-TCP降解率虽仍有上升,但促进效果不明显。
|
图 3 不同漆酶用量对漆酶-丁香醛系统降解2, 4, 5-TCP的影响 Fig.3 Effects of laccase dosage on 2, 4, 5-TCP degradation by the laccase-syringaldehyde system |
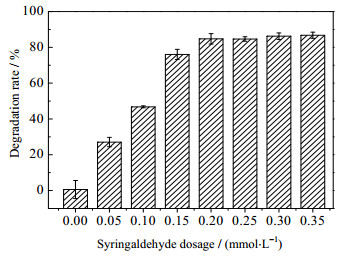
考察反应体系中丁香醛用量对2, 4, 5-TCP降解率的影响,调节反应体系中丁香醛用量(0~0.35 mmol·L-1),在漆酶用量0.2 IU·mL-1,60 ℃,80 r·min-1下,振荡反应2 h,测定2, 4, 5-TCP降解率,结果如图 4所示。丁香醛用量对反应体系影响显著,单独使用漆酶,即丁香醛用量为0 mmol·L-1时,对2, 4, 5-三氯酚降解效果不明显。在0~0.2 mmol·L-1随着丁香醛用量提高,2, 4, 5-TCP降解率逐渐提高,当丁香醛添加量达到0.2 mmol·L-1时,体系中2, 4, 5-TCP降解率为86.75%,能够实现2, 4, 5-TCP的高效降解。KAZUHITO等利用杂色云芝菌(Coriolus versicolor)所产漆酶对多种氯酚类污染物进行降解实验时,发现单独添加漆酶无法对2, 4, 5-TCP发生作用,添加芥子酸可促进漆酶发挥作用,但降解率不足30%[30],与之相较,利用重组漆酶-丁香醛系统能够实现对2, 4, 5-TCP的高效修复。
|
图 4 不同丁香醛用量对漆酶-丁香醛系统降解2, 4, 5-TCP的影响 Fig.4 Effects of syringaldehyde dosage on 2, 4, 5-TCP degradation by the laccase-syringaldehyde system |
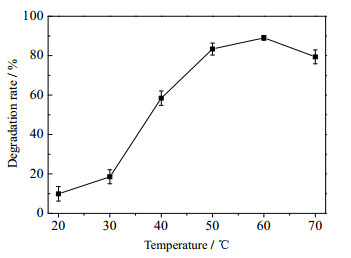
温度对漆酶活性及酶促反应速率均有影响,因此本实验对反应体系温度进行探究,在不同温度下(30~70 ℃),分别测定2, 4, 5-TCP降解率,实验结果如图 5所示,在30~60 ℃,随着温度的逐渐升高,降解率逐渐上升,60 ℃时降解率最高为89.03%,进一步提高温度,漆酶酶活受到高温抑制,降解率有所下降,但漆酶-丁香醛系统能够在较宽温度范围内实现对2, 4, 5-TCP的有效降解,具有较高实际应用价值。
|
图 5 不同温度对漆酶-丁香醛系统降解2, 4, 5-TCP的影响 Fig.5 Effects of temperature on 2, 4, 5-TCP degradation by the laccase-syringaldehyde system |
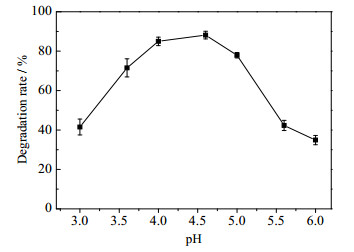
反应体系的pH值会影响酶的空间结构和稳定性,进而影响酶的活力及酶与底物之间的相互作用速率[31]。为探究最适的反应pH,本试验将反应体系的pH分别调节为3.0~6.0,在漆酶用量0.2 IU·mL-1,丁香醛用量0.2 mmol·L-1,60 ℃,80 r·min-1下,振荡反应2 h,测定2, 4, 5-TCP降解率。实验结果如图 6所示,重组里氏木霉产漆酶对2, 4, 5-TCP的最适降解pH为4.6,降解率可达88.14%。当pH在3.6~5.0时,漆酶-丁香醛系统对2, 4, 5-TCP均具有较好的降解效果,降解率维持在70%以上,具有较好的pH适应性,可以有效简化pH调节的工序。
|
图 6 不同pH对漆酶-丁香醛系统降解2, 4, 5-TCP的影响 Fig.6 Effects of pH on 2, 4, 5-TCP degradation by the laccase-syringaldehyde system |
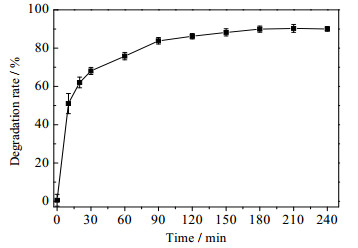
综合漆酶-丁香醛体系对2, 4, 5-TCP降解影响因素探究结果,确定最适反应条件为pH4.6,60 ℃,丁香醛用量0.2 mmol·L-1,漆酶用量0.2 IU·mL-1,80 r·min-1。在该条件下,对2, 4, 5-TCP降解进程进行跟踪,每隔30 min取样测定降解率,结果如图 7所示。随着反应进行,2, 4, 5-TCP降解率逐渐升高,60 min降解率即达到75.83%,180 min后降解率为90.11%。AEPPLI等利用Cl和C同位素标记分析探究多种氧化还原酶对多氯酚降解机理时发现,漆酶可通过自由基机制促使2, 4, 6-三氯酚发生脱氯及氧化反应,形成对应的2, 6-二氯对苯醌,达到降解的目的[32]。陈曦等利用漆酶对2, 4-二溴酚和2, 4, 6-三溴酚进行反应动力学研究时发现,底物能够在漆酶作用下形成自由基,这些自由基之间发生C-C键或C-O键耦合,形成卤代联苯醚类似物,随后会在漆酶作用下进一步发生脱卤作用,进而降低毒性[33]。XU等利用漆酶对卤代联苯醚(十溴二苯醚)作用时,也发现漆酶能够产生脱卤作用,使毒性得到降低[34]。在本实验中所构建的漆酶丁香醛降解2, 4, 5-三氯酚体系中,漆酶先与介体丁香醛之间发生作用,产生丁香醛自由基,该自由基通过与2, 4, 5-三氯酚发生作用形成对应的酚氧自由基。一方面,该酚氧自由基发生电子重排,进一步在4号位发生脱氯及氧化作用形成对应的苯醌类物质。另一方面,2, 4, 5-三氯酚所形成的自由基之间亦可能会发成C-C键及C-O键的耦合形成高卤代中间物,但该中间产物稳定性较差,既可能会进一步受到漆酶作用,又将在自然界中被生物体内酶作用形成低卤代物,达到降解脱毒的最终目的[35-36]。
|
图 7 漆酶-丁香醛系统降解2, 4, 5-TCP进程 Fig.7 Profile of 2, 4, 5-TCP degradation by the laccase-syringaldehyde system |
利用固态发酵产漆酶及微量丁香醛,用生物修复法降解土壤污染物2, 4, 5-TCP,既能有效解决由水稻秸秆堆积引起的环境污染问题,又可显著减少漆酶生产成本,操作简便易行,且后续应用过程中可将固态发酵产漆酶与土壤中污染物修复过程进行耦合,在快速降解秸秆过程中,利用所产漆酶对土壤中有机污染物进行同步修复,进一步降低应用成本,具有较高的应用前景。
4 结论利用重组里氏木霉以水稻秸秆为基质进行固态发酵,第12 d秸秆失重率可达54.73%,滤纸酶及漆酶活力分别可达116.96和10.15 IU·g-1,可实现重组里氏木霉高产漆酶。
天然介体丁香醛可以很好的替代人工介体ABTS、HBT,促进重组漆酶高效降解2, 4, 5-TCP。对漆酶-丁香醛降解体系的进一步研究表明,当漆酶用量0.2 IU·mL-1,丁香醛用量0.2 mmol·L-1,pH 4.6,60 ℃,反应180 min后2, 4, 5-TCP降解率可高达90.11%。
研究结果为废弃农作物秸秆的综合利用及土壤污染物2, 4, 5-TCP的高效降解提供指导。
| [1] |
TARTAKOVSKY B, MANUEL M F, BEAUMIER D, et al. Enhanced selection of an anaerobic pentachlorophenol-degrading consortium[J]. Biotechnology & Bioengineering, 2001, 73(6): 476-483. |
| [2] |
COOPER G S, JONES S. Pentachlorophenol and cancer risk: Focusing the lens on specific chlorophenols and contaminants[J]. Environmental Health Perspectives, 2008, 116(8): 1001-1008. DOI:10.1289/ehp.11081 |
| [3] |
邱纪时, 钟惠英, 祝翔宇, 等. 杭州湾南岸海水中的氯酚类化合物的污染特征及生态风险评价[J]. 海洋环境科学, 2016, 35(2): 231-237. QIU J S, ZHONG H Y, ZHU X Y, et al. Characteristics and ecological risk of selected chlorophenols in seawater of the south Hangzhou Bay[J]. Marine Environmental Science, 2016, 35(2): 231-237. |
| [4] |
钱勇兴, 李中坚, 杨彬, 等. 改性干菌吸附去除染化废水中共存污染物活性蓝13及五氯酚的研究[J]. 高校化学工程学报, 2016, 30(5): 1203-1212. QIAN Y X, LI Z J, YANG B, et al. Biosorption of reactive blue 13 and pentachlorophenol from dye wastewater using treated Pseudomonas sp. bacteria[J]. Journal of Chemical Engineering of Chinese Universities, 2016, 30(5): 1203-1212. |
| [5] |
ORGANIZATION W H. Chlorophenols other than pentachlorophenol[M]. Geneva: World Health Organization, 1989.
|
| [6] |
KUDANGA T, NYANHONGO G S, GUEBITZ G M, et al. Potential applications of laccase-mediated coupling and grafting reactions: A review[J]. Enzyme and Microbial Technology, 2011, 48(3): 195-208. DOI:10.1016/j.enzmictec.2010.11.007 |
| [7] |
吴坤, 闵航, 朱显峰, 等. 杂色云芝漆酶的分离、纯化和酶学特性研究[J]. 高校化学工程学报, 2003, 17(2): 173-179. WU K, MIN H, ZHU X F, et al. Purification and properties of laccases from Coriolus versicolor[J]. Journal of Chemical Engineering of Chinese Universities, 2003, 17(2): 173-179. DOI:10.3321/j.issn:1003-9015.2003.02.011 |
| [8] |
BAIOCCO P, BARRECA A M, FABBRINI M, et al. Promoting laccase activity towards non-phenolic substrates: A mechanistic investigation with some laccase-mediator systems[J]. Organic and Biomolecular Chemistry, 2003, 1(1): 191-7. DOI:10.1039/B208951C |
| [9] |
CAÑAS A I, CAMARERO S. Laccases and their natural mediators: Biotechnological tools for sustainable eco-friendly processes[J]. Biotechnology Advances, 2010, 28(6): 694-705. DOI:10.1016/j.biotechadv.2010.05.002 |
| [10] |
STRONG P J, CLAUS H. Laccase: A review of its past and its future in bioremediation[J]. Critical Reviews in Environmental Science and Technology, 2011, 41(4): 373-434. DOI:10.1080/10643380902945706 |
| [11] |
CAMARERO S, IBARRA D, MARTÍNEZ M J, et al. Lignin-derived compounds as efficient laccase mediators for decolorization of different types of recalcitrant dyes[J]. Applied and Environmental Microbiology, 2005, 71(4): 1775-1784. DOI:10.1128/AEM.71.4.1775-1784.2005 |
| [12] |
CANTARELLA G, GALLI C, GENTILI P. Free radical versus electron-transfer routes of oxidation of hydrocarbons by laccase/mediator systems : Catalytic or stoichiometric procedures[J]. Journal of Molecular Catalysis B Enzymatic, 2003, 22(3-4): 135-144. DOI:10.1016/S1381-1177(03)00014-6 |
| [13] |
SPECTRUMS C. Paper pulp delignification using laccase and natural mediators[J]. Enzyme and Microbial Technology, 2007, 40(5): 1264-1271. DOI:10.1016/j.enzmictec.2006.09.016 |
| [14] |
邱卫华, 陈洪章. 木质纤维素原料中漆酶天然介体的研究进展[J]. 生物工程学报, 2014, 30(5): 726-733. QIU W H, CHEN H Z. Progress in natural laccase mediators from lignocelluloses[J]. Chinese Journal of Biotechnology, 2014, 30(5): 726-733. |
| [15] |
MURUGESAN K, YANG I H, YOUNGMO K, et al. Enhanced transformation of malachite green by laccase of Ganoderma lucidum in the presence of natural phenolic compounds[J]. Applied Microbiology and Biotechnology, 2009, 82(2): 341-350. DOI:10.1007/s00253-008-1819-1 |
| [16] |
KRISHNA C. Solid-state fermentation systems-an overview[J]. Critical Reviews in Biotechnology, 2005, 25(2): 1-30. |
| [17] |
VÄISÄNEN T, HAAPALA A, LAPPALAINEN R, et al. Utilization of agricultural and forest industry waste and residues in natural fiber-polymer composites: A review[J]. Waste Management, 2016, 54: 62-73. DOI:10.1016/j.wasman.2016.04.037 |
| [18] |
朱佳雷, 王体健, 邓君俊, 等. 长三角地区秸秆焚烧污染物排放清单及其在重霾污染天气模拟中的应用[J]. 环境科学学报, 2012, 32(12): 3045-3055. ZHU J L, WANG T J, DENG J J, et al. An emission inventory of air pollutants from crop residue burning in Yangtze River Delta Region and its application in simulation of a heavy haze weather process[J]. Acta Scientiae Circumstantiae, 2012, 32(12): 3045-3055. |
| [19] |
ZHAO J, ZENG S Q, XIA Y, et al. Expression of a thermotolerant laccase from Pycnoporus sanguineus in Trichoderma reesei and its application in the degradation of bisphenol A[J]. Journal of Bioscience and Bioengineering, 2018, 125(4): 371-376. DOI:10.1016/j.jbiosc.2017.11.010 |
| [20] |
WANG B B, XIA L M. High efficient expression of cellobiase gene from Aspergillus niger in the cells of Trichoderma reesei[J]. Bioresource Technology, 2011, 102(6): 4568-4572. DOI:10.1016/j.biortech.2010.12.099 |
| [21] |
夏颖, 赵杰, 夏黎明. 一种新型内切-β-葡聚糖酶基因在里氏木霉中的重组与表达[J]. 高校化学工程学报, 2016, 30(3): 626-632. XIA Y, ZHAO J, XIA L M. Recombination and expression of a novel endo-beta-glucanase gene from Penicillium echinulatum in Trichoderma reesei[J]. Journal of Chemical Engineering of Chinese Universities, 2016, 30(3): 626-632. |
| [22] |
KIISKINEN L L, KRUUS K, BAILEY M, et al. Expression of Melanocarpus albomyces laccase in Trichoderma reesei and characterization of the purified enzyme[J]. Microbiology-Sgm, 2004, 150(9): 3065-3074. DOI:10.1099/mic.0.27147-0 |
| [23] |
LIU T, WANG T H, LI X, et al. Improved heterologous gene expression in Trichoderma reesei by cellobiohydrolase I gene (cbh1) promoter optimization[J]. Acta Biochimica et Biophysica Sinica, 2008, 40(2): 158-165. DOI:10.1111/j.1745-7270.2008.00388.x |
| [24] |
ZENG S Q, QIN X L, XIA L M. Degradation of the herbicide isoproturon by laccase-mediator systems[J]. Biochemical Engineering Journal, 2017, 119: 92-100. DOI:10.1016/j.bej.2016.12.016 |
| [25] |
GHOSE T K. Measurement of cellulase activities[J]. Pure and Applied Chemistry, 1987, 59(2): 257-268. DOI:10.1351/pac198759020257 |
| [26] |
CHUNDAWAT S P S, BECKHAM G T, HIMMEL M E, et al. Deconstruction of lignocellulosic biomass to fuels and chemicals[J]. Annual Review of Chemical and Biomolecular Engineering, 2011, 2: 121-145. DOI:10.1146/annurev-chembioeng-061010-114205 |
| [27] |
LISOV A V, POZHIDAEVA Z A, STEPANOVA E V, et al. Conversion of polychlorophenols by laccases with 1-hydroxybenzotriazole as a mediator[J]. Applied Biochemistry and Microbiology, 2007, 43(6): 616-619. DOI:10.1134/S0003683807060087 |
| [28] |
BALDRIAN P. Fungal laccases-occurrence and properties[J]. FEMS Microbiology Reviews, 2006, 30(2): 215-242. DOI:10.1111/j.1574-4976.2005.00010.x |
| [29] |
TORRESDUARTE C, ROMAN R, TINOCO R, et al. Halogenated pesticide transformation by a laccase-mediator system[J]. Chemosphere, 2009, 77(5): 687-92. DOI:10.1016/j.chemosphere.2009.07.039 |
| [30] |
KAZUHITO I, MIHO F, KAZUO K, et al. Phenolic acids affect transformations of chlorophenols by a Coriolus versicolor laccase[J]. Soil Biology and Biochemistry, 2000, 32(1): 85-91. DOI:10.1016/S0038-0717(99)00133-9 |
| [31] |
KIM Y J, NICELL J A. Impact of reaction conditions on the laccase-catalyzed conversion of bisphenol A[J]. Bioresource Technology, 2006, 97(12): 1431-1442. DOI:10.1016/j.biortech.2005.06.017 |
| [32] |
AEPPLI C, TYSKLIND M, HOLMSTRAND H, et al. Use of Cl and C isotopic fractionation to identify degradation and sources of polychlorinated phenols: Mechanistic study and field application[J]. Environmental Science & Technology, 2013, 47(2): 790-797. |
| [33] |
陈曦.漆酶催化转化2, 4-DBP和2, 4, 6-TBP生成OH--PBDEs及其机制[D].杭州: 浙江工业大学, 2014. CHEN X. Production of OH-PBDEs from laccase-catalized oxidation of 2, 4-DBP and 2, 4, 6-TBP[D]. Hangzhou: Zhejiang University of Technology, 2014. |
| [34] |
XU G, WANG J. Biodegradation of decabromodiphenyl ether (BDE-209) by white-rot fungus Phlebia lindtneri[J]. Chemosphere, 2014, 110: 70-77. DOI:10.1016/j.chemosphere.2014.03.052 |
| [35] |
MCKINNEY M A, DIETZ R, SONNE C, et al. Comparative hepatic microsomal biotransformation of selected PBDEs, including decabromodiphenyl ether, and decabromodiphenyl ethane flame retardants in Arctic marine-feeding mammals[J]. Environmental Toxicology and Chemistry, 2011, 30(7): 1506-1514. DOI:10.1002/etc.535 |
| [36] |
MORCK A, HAKK H, ORN U, et al. Decabromodiphenyl ether in the rat: absorption, distribution, metabolism, and excretion[J]. Drug Metabolism and Disposition, 2003, 31(7): 900-907. DOI:10.1124/dmd.31.7.900 |




