亚硝酸盐通常来自于含氮的有机化合物、动物粪便、有机废物、化肥、天然沉积和硝酸盐生物转化,是饮用水、食品和环境中普遍存在的有害物质[1]。亚硝酸盐已被证实具有致癌和影响心血管功能的风险[2]。欧盟科学委员会规定,亚硝酸盐的可接受每日摄取量为0.06 mg·kg-1体重[1];根据中华人民共和国国家标准GB 2760-2014,食品中作为固色剂和防腐剂的亚硝酸盐的最高允许含量为0.15 g·kg-1[3];亚硝酸盐在水中的最大允许值为2.17 mmol·L-1[4]。因此,有必要对亚硝酸盐进行敏感检测,特别是在饮用水和食品行业。迄今为止,用于测定亚硝酸盐的方法有色谱法[5]、化学发光[6]、分光光度法[7],毛细管电泳法[8]等,但这些方法存在明显的缺陷,如不可避免的使用有毒试剂、繁琐的预处理和昂贵的设备[9];而电化学方法因其成本低、响应速度快、灵敏度高、适合于微型化和现场检测等特点而引起研究者的广泛关注[10-12]。由于在大多数传统电极上亚硝酸盐的氧化通常需要较大的过电位,加之其表面易受污染,限制了裸电极对亚硝酸盐的利用,从而降低了传感灵敏度和精度[13]。因此,为了在亚硝酸盐氧化过电位较低的情况下获得更好的电流响应,采用新型复合材料修饰电极是目前研究的热点。
近年来,石墨烯因其独特的机械柔韧性、极高的表面体积比和无与伦比的电学性能等特点成为多用途电极材料[14-16]。然而,石墨烯氧化物形式的残余氧官能团的存在使其电导率明显降低通过引入掺杂原子可有效消除团聚现象[17]。其中,硫掺杂是一种重要的掺杂手段,可有助于提高复合材料的载流子能力和电化学性能。离子液体(ionic liquid, IL)作为一种新型的绿色溶剂,具有多种独特的物理化学性质,如可调谐化学结构、宽电化学窗口、高离子导电性、良好的溶解性和生物相容性[18-19]。在电化学中,IL因其优异的离子导电性和低挥发性[20]而被广泛应用。本研究通过在硫掺杂石墨烯上自组装离子液体(1-丁基-3-甲基咪唑六氟磷酸盐)制备硫掺杂石墨烯离子液体纳米复合材料(SG-IL),构建高特异性的亚硝酸盐电化学传感器平台。借助电化学工作站进行传感机理的研究和电化学传感器性能的考察,并进行了实际样本分析。因此,该纳米复合材料可作为电化学和生物传感应用的平台。
2 实验部分 2.1 药品与仪器氧化石墨烯(graphene oxide, GO)购于青岛华高墨烯科技有限公司;1-丁基-3-甲基咪唑六氟磷酸盐(BMIMPF6)购自中国科学院兰州应用化学研究所;将0.1 mol·L-1 NaH2PO4和0.1 mol·L-1 Na2HPO4以体积比为39:61配制0.1 mol·L-1磷酸盐缓冲溶液(phosphate buffer solution, PBS)。乙腈、乙醇、亚硝酸钠和氯化钾均购自国药集团化学试剂有限公司。除另有说明外,所有化学试剂和溶剂均未经其他处理直接使用。
采用扫描电子显微镜(scanning electron microscope,SEM,JSM-6700F,JEOL)对材料进行形貌分析;采用德国BRUKER-TENSOR 27型红外光谱仪进行傅里叶变换红外光谱(fourier transform infrared spectroscopy, FT-IR)扫描;采用上海辰华仪器有限公司660E电化学工作站的经典三电极系统进行电化学测量,其中铂线作为辅助电极,银/氯化银(Ag/AgCl)作为参比电极,SG-IL/GCE作为工作电极。pH计(PHS-25)购于上海仪电科学仪器股份有限公司。除特殊说明外,所有实验操作均在室温下进行。
2.2 材料的制备 2.2.1 硫掺杂石墨烯的制备首先将氧化石墨烯(GO)与硫还原掺杂,形成硫掺杂石墨烯(sulfur-doped graphene, SG)[21],用于自组装离子液体制备硫掺杂石墨烯离子液体复合物的模板。亚硫酸氢钠(NaHSO3)用作氧化石墨烯的还原剂和硫源,实验中将50 mg GO粉末分散至50 mL水和N, N-二甲基甲酰胺(体积比3:2)的混合溶剂中,超声分散5 min,然后加入2.7 mmol NaHSO3至上述溶液中。在此之后,将反应混合物加热到60 ℃,并在该温度下保持1 h,形成硫掺杂石墨烯(理论质量分数为63.34 %)。
2.2.2 SG-IL的制备将1-丁基-3-甲基咪唑六氟磷酸盐分散于乙腈中(1 mg·mL-1),等体积(50 mL)加入到分散于无水乙醇中的SG中,超声处理1 h,即可得。
2.2.3 传感器的组装在电极修饰之前,将玻碳电极(glassy carbon electrode,GCE)在麂皮上用0.3和0.05 μm氧化铝抛光粉打磨为镜面,之后在超纯水和无水乙醇中分别超声清洗3 min,自然晾干后将超声分散均匀的不同材料分散液滴涂于干净的电极表面,分别记为SG-IL/GCE、SG/GCE、GO/GCE。
3 结果与讨论 3.1 形貌和结构表征如图 1所示为采用扫描电镜得到的GO、SG和SG-IL的表面形貌。从图中可以看出,GO为表面不规则褶皱块状结构,而对氧化石墨烯进行硫掺杂后,其为疏松多孔且规则的纳米片层结构,片层边缘处褶皱明显增多,这可能是硫掺杂石墨烯过程中产生了更多的边缘缺陷结构。当加入离子液体后,表面褶皱相应的减少且形成了三维堆叠不规则的多孔结构,很好地实现了离子液体的掺杂,从而形成硫掺杂石墨烯离子液体复合材料。

|
图 1 不同复合材料的扫描电镜图 Fig.1 SEM images of different composites |
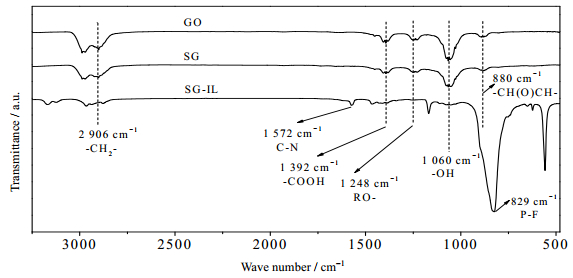
通过傅里叶变换红外光谱(FT-IR)对SG-IL复合材料进行结构表征。如图 2所示,GO在2 906、1 392、1 248、1 060、880 cm-1处出现了分别对应于─CH2─、羧基、烷氧基或醇羟基、环氧基的特征振动吸收峰。而在SG和SG-IL的谱图中,这些特征峰的强度明显减小,这说明通过对氧化石墨烯进行硫掺杂实现了有效脱氧而得到还原氧化石墨烯。离子液体加入后,在SG-IL中可以观察到对应的特征吸收峰,如1 572 cm-1对应于咪唑的芳族体系的C─N键的伸缩振动峰和827 cm-1处的P-F伸缩振动峰。这些结果进一步表明SG-IL复合材料的成功制备。
|
图 2 GO、SG和SG-IL复合材料的红外谱图 Fig.2 FT-IR spectra of GO, SG and SG-IL |
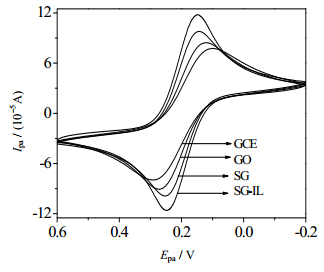
如图 3所示为不同修饰电极在含0.1 mol·L-1 KCl的5 mmol·L-1 (Fe(CN)6)3-/4-溶液中以100 mV·s-1的扫速测得的循环伏安(Cyclic voltammetry,CV)曲线,用以考察不同修饰电极的电化学性能。从图中可以看出,铁氰化物的氧化还原峰值在GCE、GO/GCE、SG/GCE、SG-IL/GCE上从低到高逐渐改变。故推测界面电导率的增加促进了铁氰化钾的电子转移,而离子液体的添加使复合物的活性位点明显增加。
|
图 3 不同修饰电极的循环伏安图 Fig.3 CV curves of different modified electrodes |
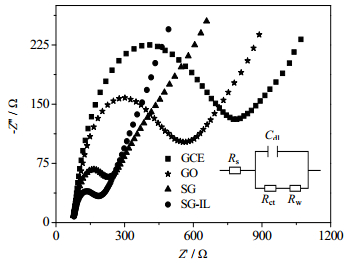
电化学阻抗谱图可以表征GCE、GO/GCE、SG/GCE和SG-IL/GCE的电子传递电阻。如图 4所示为不同修饰电极在含0.1 mol·L-1 KCl的5 mmol·L-1 (Fe(CN)6)3-/4-溶液中的电化学阻抗谱(electrochemical impedance spectroscopy,EIS)图。阻抗谱图由表示电子转移过程受扩散控制的直线部分和表示受动力学控制的半圆部分组成。从图中可以看出,与裸GCE相比,GO/GCE的半圆部分相对减小,是由于GO阻碍了氧化还原探针的电子转移。而在SG/GCE上半圆部分较小,表明硫掺杂石墨烯导电性较好,使得阻抗值显著减小。与SG/GCE不同的是,加入离子液体后阻抗值明显降低,说明离子液体的高导电性增加了电极的电化学活性。同时也表明GCE上的SG-IL薄膜可以加速电子传递过程。
|
图 4 不同修饰电极的电化学阻抗谱图 Fig.4 Nyquist plots of different modified electrodes (插图为模拟电路图) (The illustration is an analog circuit diagram) |
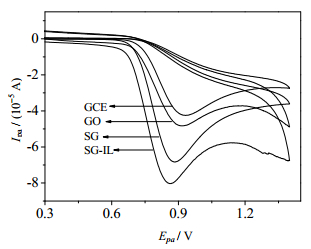
如图 5所示为不同修饰电极以扫速50 mV·s-1在0.1 mol·L-1 PBS(pH 4.0)中对2 mmol·L-1亚硝酸盐的CV响应。从图中可以看出,在所有电极系统中均观察到与亚硝酸盐电氧化相对应的单峰。在相同的电化学条件下,与裸GCE相比,涂层氧化石墨烯后,CV峰值强度有所增加;但SG/GCE较裸GCE显著增加1.62倍。而离子液体的加入,使得SG-IL/GCE的CV峰值强度进一步增加且产生最大的氧化峰。从不同电极的CVs对比曲线可以得出结论,SG及IL的存在显著地促进亚硝酸盐的电氧化过程。
|
图 5 不同修饰电极对亚硝酸盐的CV响应图 Fig.5 CV response curves of NO2- with different modified electrodes |
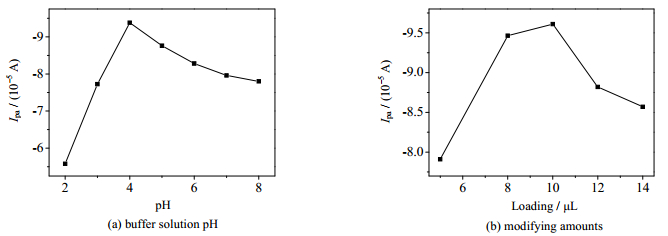
由于亚硝酸盐的氧化反应常伴随着质子的参与,因此考察PBS缓冲液的pH对亚硝酸盐电化学氧化过程的影响。如图 6(a)为缓冲液pH对2 mmol·L-1亚硝酸盐的循环伏安响应。从图中可以看出,当pH在2.0~4.0时,峰电流呈增大趋势,当pH在4.0~8.0时,峰电流呈现下降趋势,pH=4.0时峰电流达到最大值。因此pH=4.0作为后续研究的最优pH。如图 6(b)为在0.1 mol·L-1 PBS(pH 4.0)中考察电极滴涂量对2 mmol·L-1亚硝酸盐的循环伏安响应的影响。从图中可以看出,氧化峰电流在修饰量为5到14 μL之间呈现先增大后减小的变化趋势,结果显示滴涂量为10 μL时峰电流最大,故被选为最佳修饰量。
|
图 6 缓冲液pH和滴涂量对亚硝酸盐循环伏安响应的影响 Fig.6 Effects of buffer pH and modifying amounts on NO2- cyclic voltammetry response |
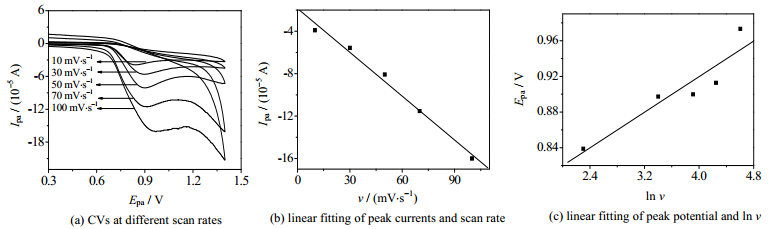
通过分析扫速的影响,研究了亚硝酸盐在SG-IL/GCE上的电化学氧化机理。如图 7(a)所示为SG-IL/GCE在含有2 mmol·L-1亚硝酸盐的0.1 mol·L-1 PBS (pH 4.0)溶液中不同扫速的循环伏安曲线。从图 7(b)中可以看出,峰电流Ipa与扫速ν是线性的,拟合线性方程是:Ipa=-0.137 85 ν-1.849 8(r=0.993 6),可知亚硝酸盐在SG-IL/GCE上的电化学氧化是受吸附控制的。图 7(c)中显示了峰电位Epa与ln ν的线性拟合结果,线性方程为:Epa=0.049 8ln ν+0.720 4(r=0.930 6),根据Laviron理论,Epa可以由Laviron方程[22]表示为
| $ {E_{pa}} = {E^0} + (RT/anF)\ln (RT{k^0}/anF) + (RT/anF)\ln v $ | (1) |
|
图 7 不同扫速的循环伏安图和线性拟合图 Fig.7 CV curves under different scan rates and related linear fitting results |
式中:T=298 K,F=96 485 C·mol-1,R=8.314 J·mol-1·k-1,根据线性方程的斜率值计算出电子传递数n约为1。因此,亚硝酸盐在SG-IL/GCE上的氧化过程是一种单电子转移过程,反应式可表示为
| $ {\rm{NO}}_{\rm{2}}^{\rm{ - }}{\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{O = NO}}_{\rm{3}}^{\rm{ - }}{\rm{ + }}{{\rm{H}}^{\rm{ + }}}{\rm{ + }}{{\rm{e}}^{\rm{ - }}} $ | (2) |
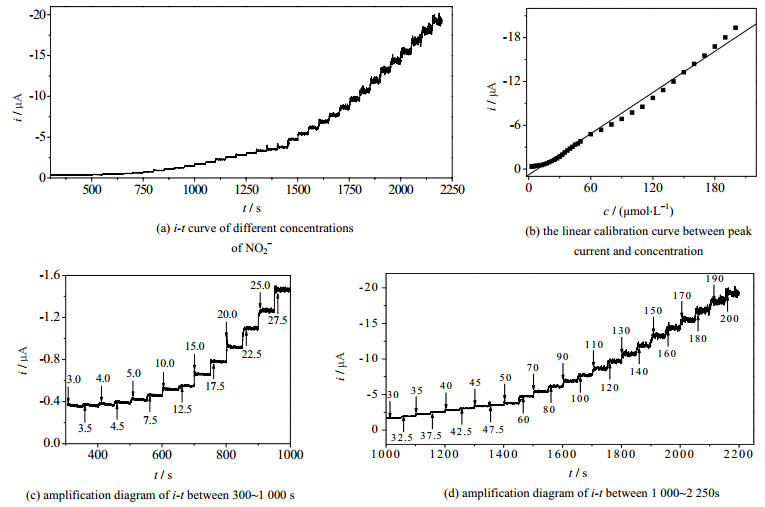
本实验采用计时电流法研究了不同浓度的亚硝酸盐在SG-IL/GCE上的响应电流变化,如图 8所示为SG-IL/GCE在0.1 mol·L-1 PBS(pH 4.0)溶液中连续加入不同浓度NO2-的电流-时间曲线和峰电流与NO2-浓度的线性关系图。从图中分析可知,随着亚硝酸盐浓度的增加,响应电流逐渐增大,且两者在3~200 μmol·L-1浓度范围内呈线性关系,线性拟合方程为i=-0.093 98c+0.790 9(r=0.995 2)。最低检测限是1.0 μmol·L-1,这一数值低于之前使用其他与石墨烯相关的材料修饰电极的报道,如表 1所示。说明用于亚硝酸盐的SG-IL/GCE的电化学传感器线性检测范围宽且明显优于为此目的而设计的材料。
|
图 8 不同浓度NO2-的电流-时间曲线、峰电流与浓度的线性拟合图及i-t放大图 Fig.8 i-t curve obtained under different NO2-concentrations; linear calibration curve of peak current and concentration; and enlarged i-t curve diagram |
|
|
表 1 不同电极对NO2-检测的比较 Table 1 Comparison of proposed sensors for NO2- detection |
为评价所构建的电化学传感器的实际性能,本实验采用电流-时间法对自来水和河水中的亚硝酸盐进行加标回收检测。如表 2所示,所有检测的相对标准偏差低于6.45%,回收率为92.46% ~ 107.04%。结果表明,SG-IL/GCE可用于实际水样中亚硝酸盐的测定。
|
|
表 2 实际水样中NO2-的检测 Table 2 NO2- detection results from water sample using the SG-IL/GCE sensor |
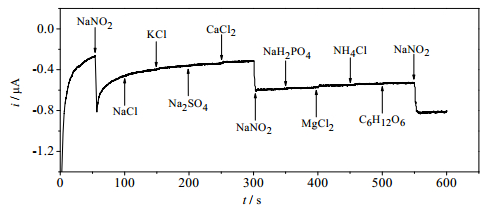
为了考察一些可能的干扰物对亚硝酸盐传感器的安培i-t时间响应的影响。为在外加均匀搅拌条件下通过连续添加NaNO2 (30 μmol·L-1)、NaCl (3μmol·L-1)、KCl (3 mmol·L-1)、Na2SO4 (3 mmol·L-1)、CaCl2 (3 mmol·L-1)、NaNO2 (30 μmol·L-1)、Na2H2PO4 (3 mmol·L-1)、MgCl2 (3 mmol·L-1)、NH4Cl (3 mmol·L-1)、葡萄糖(1.5 mmol·L-1)和NaNO2 (30 μmol·L-1)到0.1 mol·L-1 PBS(pH 4.0)中,得到安培i-t响应间隔:50 s;电压:0.72 V如图 9所示。从图中可以看出,100倍浓度的常见干扰离子如Na+、K+、SO42-、Ca2+、H2PO42-、Mg2+、NH4+和50倍浓度的葡萄糖对亚硝酸盐的检测没有明显干扰,且过程中3次间隔加入亚硝酸盐都表现出显著的电流响应,说明该传感器对亚硝酸盐有很好的选择性。将修饰电极于室温下放置10 d后对相同的亚硝酸盐溶液进行测定,发现电流变化值少于7%,说明SG-IL的稳定性较好。
|
图 9 安培i-t响应图 Fig.9 Amperometric i-t curves |
本文介绍了一种简单、方便、高灵敏度的涂有SG-IL敏感层的亚硝酸盐电化学传感器。对石墨烯进行硫掺杂及离子液体的引入使得石墨烯纳米复合材料具有较大的电活性表面积和优异的灵敏度。构建的亚硝酸盐电化学传感器的线性响应范围为3~200 μmol·L-1,最低检测限为1.0 μmol·L-1,且实际水样的检测结果较好。因此,该电化学传感器可广泛应用于实际样品中亚硝酸盐的测定。
| 符号说明: | |||
| Cdl | —界面电容,F | R | —气体常数,取值8.314 J·mol-1·K-1 |
| c | —浓度,μmol·L-1 | Rct | —电荷转移电阻,Ω |
| E0 | —形式电位,V | Rs | —溶液电阻,Ω |
| Epa | —峰电压,V | Rw | —扩散阻抗,Ω |
| F | —法拉第常数,C·mol-1 | r | —线性相关系数 |
| Ipa | —峰电流,A | T | —温度,K |
| i | —电流,μA | t | —时间,s |
| k0 | —标准速率常数 | ν | —扫描速率,mV·s-1 |
| n | —电子转移数,个 | α | —电子转移系数,不可逆电化学过程,取值0.5 |
| [1] |
MAO Y, BAO Y, HAN D X, et al. Research progress on nitrite electrochemical sensor[J]. Chinese Journal of Analytical Chemistry, 2018, 46(2): 147-156. DOI:10.1016/S1872-2040(17)61066-1 |
| [2] |
ABSALAN G, AKHOND M, BANANEJAD A, et al. Highly sensitive determination of nitrite using a carbon ionic liquid electrode modified with Fe3O4 magnetic nanoparticle[J]. Journal of the Iranian Chemical Society, 2015, 12(7): 1293-1301. DOI:10.1007/s13738-015-0594-z |
| [3] |
国家卫计委. 《食品安全国家标准包装饮用水》(GB 19298-2014)、《食品安全国家标准食品添加剂使用标准》(GB 2760-2014)等37项食品安全国家标准发布[J]. 饮料工业, 2014(12): 46-47. National health and family planning commission. 37 national food safety standards were issued, including national food safety standard for packaged drinking water (GB 19298-2014) and national food safety standard for the use of food additives (GB 2760-2014)[J]. Beverage industry, 2014(12): 46-47. DOI:10.3969/j.issn.1007-7871.2014.12.019 |
| [4] |
CHANG J L, ZEN J M. Disposable screen-printed edge band ultramicroelectrodes for the determination of trace amounts of nitrite ion[J]. Electroanalysis, 2010, 18(10): 941-946. |
| [5] |
FERREIRA I M, SILVA S. Quantification of residual nitrite and nitrate in ham by reverse-phase high performance liquid chromatography/diode array detector[J]. Talanta, 2008, 74(5): 1598-1602. DOI:10.1016/j.talanta.2007.10.004 |
| [6] |
YIN X, CHEN Q, SONG H, et al. Sensitive and selective electrochemiluminescent detection of nitrite using dual-stabilizer-capped CdTe quantum dots[J]. Electrochemistry Communications, 2013, 34(34): 81-85. |
| [7] |
BRU M, BURGUETE M I, GALINDO F, et al. Cross-linked poly(2-hydroxyethylmethacrylate) films doped with 1, 2-diaminoanthraquinone (DAQ) as efficient materials for the colorimetric sensing of nitric oxide and nitrite anion[J]. Tetrahedron Letters, 2006, 47(11): 1787-1791. DOI:10.1016/j.tetlet.2006.01.030 |
| [8] |
MELANSON J E, LUCY C A. Ultra-rapid analysis of nitrate and nitrite by capillary electrophoresis[J]. Journal of Chromatography A, 2000, 884(1): 311-316. |
| [9] |
JIAN J M, FU L, JI J, et al. Electrochemically reduced graphene oxide/gold nanoparticles composite modified screen-printed carbon electrode for effective electrocatalytic analysis of nitrite in foods[J]. Sensors and Actuators B, 2018, 262: 125-136. DOI:10.1016/j.snb.2018.01.164 |
| [10] |
XUE Z, FU X, RAO H, et al. A new electron transfer mediator actuated non-enzymatic nitrite sensor based on the voltammetry synthetic composites of 1-(2-pyridylazo)-2-naphthol nanostructures coated electrochemical reduced graphene oxide nanosheets[J]. Electrochimica Acta, 2018, 260: 623-629. DOI:10.1016/j.electacta.2017.11.181 |
| [11] |
ZOU C, YANG B, BIN D, et al. Electrochemical synthesis of gold nanoparticles decorated flower-like graphene for high sensitivity detection of nitrite[J]. Journal of Colloid and Interface Science, 2017, 488: 135-141. DOI:10.1016/j.jcis.2016.10.088 |
| [12] |
AHMAD R, MAHMOUDI T, AHN M S, et al. Fabrication of sensitive non-enzymatic nitrite sensor using silver-reduced graphene oxide nanocomposite[J]. Journal of Colloid & Interface Science, 2018, 516: 67-75. |
| [13] |
WANG Q H, YU L J, LIU Y, et al. Methods for the detection and determination of nitrite and nitrate:A review[J]. Talanta, 2017, 165: 709-720. DOI:10.1016/j.talanta.2016.12.044 |
| [14] |
刘艳, 牛卫芬. 石墨烯-纳米金修饰电极的制备及其对痕量铅(Ⅱ)的测定[J]. 高校化学工程学报, 2014, 28(3): 685-689. LIU Y, NIU W F. Preparation of graphene -Aunano modified electrodes and their application in trace lead(Ⅱ) detection[J]. Journal of Chemical Engineering of Chinese Universities, 2014, 28(3): 685-689. DOI:10.3969/j.issn.1003-9015.2014.03.040 |
| [15] |
马文石, 周俊文, 程顺喜. 石墨烯的制备与表征[J]. 高校化学工程学报, 2010, 24(4): 719-722. MA W S, ZHOU J W, CHENG S X. Preparation and characterization of graphene[J]. Journal of Chemical Engineering of Chinese Universities, 2010, 24(4): 719-722. DOI:10.3969/j.issn.1003-9015.2010.04.030 |
| [16] |
贺晓东, 魏作君, 刘迎新, 等. 氧化石墨烯的制备及其催化水解大豆异黄酮[J]. 高校化学工程学报, 2012, 26(1): 56-60. HE X D, WEI Z J, LIU Y X, et al. The preparation of graphene oxide and using it as catalyst for the hydrolyzation of soybean isoflavone[J]. Journal of Chemical Engineering of Chinese Universities, 2012, 26(1): 56-60. DOI:10.3969/j.issn.1003-9015.2012.01.010 |
| [17] |
李鑫, 张海洋, 朱如志, 等. 硫掺杂三维石墨烯的制备及其电化学特性研究[J]. 电子元件与材料, 2018, 37(5): 57-61. LI X, ZHANG H Y, ZHU R Z, et al. Preparation and electrochemical properties of sulfur-doped three-dimensional graphene[J]. Electronic Components and Materials, 2018, 37(5): 57-61. |
| [18] |
NIU X, YANG W, GUO H, et al. A novel and simple strategy for simultaneous determination of dopamine, uric acid and ascorbic acid based on the stacked graphene platelet nanofibers/ionic liquids/chitosan modified electrode[J]. Talanta, 2012, 99: 984-988. DOI:10.1016/j.talanta.2012.07.077 |
| [19] |
WEI D, WAKEHAM S J, NG T W, et al. Transparent, flexible and solid-state supercapacitors based on room temperature ionic liquid gel[J]. Electrochemistry Communications, 2009, 11(12): 2285-2287. DOI:10.1016/j.elecom.2009.10.011 |
| [20] |
NAGLES E, OLIMPO G B, JORGE A. C. Evaluation of the usefulness of a novel electrochemical sensor in detecting uric acid and dopamine in the presence of ascorbic acid using a screen-printed carbon electrode modified with single walled carbon nanotubes and ionic liquids[J]. Electrochimica Acta, 2017, 258: 512-523. DOI:10.1016/j.electacta.2017.11.093 |
| [21] |
BHAT S A, PANDIT S A, RATHER M A, et al. Self-assembled AuNPs on sulphur-doped graphene:A dual and highly efficient electrochemical sensor for nitrite (NO2-) and nitric oxide (NO)[J]. New Journal of Chemistry, 2017, 41(16): 8347-8358. DOI:10.1039/C7NJ01565H |
| [22] |
ZHAN T R, TAN Z W, TIAN X, et al. Ionic liquid functionalized graphene oxide-Au nanoparticles assembly for fabrication of electrochemical 2, 4-dichlorophenol sensor[J]. Sensors and Actuators B, 2017, 246: 638-646. DOI:10.1016/j.snb.2017.02.107 |
| [23] |
OJANI R, RAOOF J B, ZAMANI S. A novel and simple electrochemical sensor for electrocatalytic reduction of nitrite and oxidation of phenylhydrazine based on poly (o-anisidine) film using ionic liquid carbon paste electrode[J]. Applied Surface Science, 2013, 271(271): 98-104. |
| [24] |
SUN L P, LI H J, LI M J, et al. Simultaneous determination of small biomolecules and nitrite using an Au/TiO2/Carbon nanotube composite modified electrode[J]. Journal of The Electrochemical Society, 2016, 163(13): B567-B572. DOI:10.1149/2.0361613jes |
| [25] |
YANG Y J, LI W. CTAB functionalized graphene oxide/multiwalled carbon nanotube composite modified electrode for the simultaneous determination of ascorbic acid, dopamine, uric acid and nitrite[J]. Biosensors & Bioelectronics, 2014, 56(56): 300-306. |
| [26] |
MANI V, PERIASAMY A P, CHEN S M. Highly selective amperometric nitrite sensor based on chemically reduced graphene oxide modified electrode[J]. Electrochemistry Communications, 2012, 17: 75-78. DOI:10.1016/j.elecom.2012.02.009 |
| [27] |
WU H, FAN S H, JIN X Y, et al. Construction of a Zinc porphyrin-fullerene-derivative based nonenzymatic electrochemical sensor for sensitive sensing of hydrogen peroxide and nitrite[J]. Analytical Chemistry, 2014, 86: 6285-6290. DOI:10.1021/ac500245k |




