机动车尾气是我国空气污染的重要来源[1],2015年全国机动车排放的污染物初步核算为4532.2万吨,其中碳氢化合物(CxHy) 430.2万吨[2]。CxHy在大气中经过复杂光化学反应消耗平流层中的臭氧,导致臭氧层破坏,同时与空气中的NOx等发生光化学反应产生有机气溶胶和O3等,导致光化学烟雾[3],引起雾霾问题。另外CxHy通常具有三致性[4],对人体健康构成威胁。所以对机动车尾气中CxHy的控制迫在眉睫。
常见处理机动车尾气CxHy的方法有催化氧化法[5],它具有催化效果好的特点,但需要使用贵金属催化剂和较高的催化温度[6, 7]。对比传统技术,低温等离子体技术具有低温条件下有效去除污染物、反应速度快、污染物种类适应性强、装置简单等优点,因此近年来此方面的研究逐渐成为热点[8~10]。在低温等离子体中,高能电子轰击气体分子(如N2和O2)分离后,会产生活性粒子,如氧原子和其他自由基(不同的反应条件下产生不同自由基),CxHy均可被这些活性物质氧化分解成CO2和H2O等无害物质[11]。研究表明[12~14]:单独使用低温等离子体虽然对CxHy具有较高的脱除效率,但存在能量利用率低、矿化率不高等问题。而等离子体与催化剂结合,能够充分发挥等离子体和化学催化的协同作用,提高CxHy的脱除率和矿化率。
贵金属催化剂(Pd、Ag、Pt)被认为是降解有机污染物的最佳催化剂之一[15~17],它们能促进催化剂表面氧化性基团的产生,从而促进CxHy的氧化。如Tang等[16]采用两段式等离子体催化系统,在Ag基催化剂作用下,能量密度为60 J·L-1时能完全将甲苯去除;Rahimpour等[17]利用一段式等离子催化系统降解苯甲醚,单独等离子体作用时,苯甲醚转化率只有43%,而等离子体与Pt/Al2O3催化剂协同作用时,其转化率提高到了80%。
长链烷烃在柴油车尾气组成中占有重要比例。Liu等[18]对珠三角柴油车尾气成分谱分析发现,比例最高的VOCs成分依次为丙烯、乙烯、正癸烷、正十一烷等。类似的,区家敏等[19]研究表明正十一烷、苯、正十二烷、乙烯、正癸烷、异丁烷等是轻型柴油车尾气排放中所占比例最高的成分。而长链烷烃在汽油车尾气中一般比例较低[20],所以相对于苯系物(在柴油车和汽油车尾气中均占有重要比例),长链烷烃(如正癸烷、正十一烷、正十二烷)可作为一般柴油车尾气的标志物。本文选取正癸烷作为典型的柴油车尾气模拟物,开展柴油车尾气的净化研究。基于作者之前的相关研究[21~23],本研究在等离子体场中引入了三种不同贵金属催化剂(Pd、Ag、Pt),对正癸烷(C10)进行处理,研究等离子体协同三种不同贵金属催化剂对C10的降解特性,并就其中催化效果最好的Pt/Al2O3展开深入研究,探讨了催化剂负载量、C10初始浓度、反应温度、能量密度对C10去除率和COx选择性的影响,为高效去除柴油车尾气中CxHy提供理论基础。
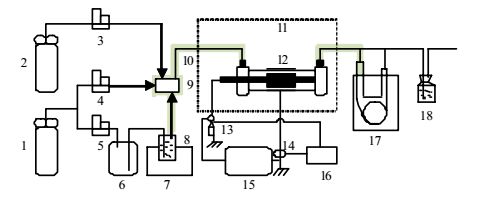
2 实验装置与方法DBD等离子体去除正癸烷的实验装置流程如图 1所示。其由四部分构成:配气(模拟气体发生)系统、反应(DBD放电)系统、放电解析(电压电流采集)系统和产物分析系统。氧气钢瓶流出的O2由质量流量计1 (MF1)控制流量,氮气钢瓶流出的N2分为两路,一路由质量流量计2 (MF2)控制流量,另一路由质量流量计3(MF3)控制较小的流量以吹脱静置在25℃水浴中的正癸烷溶液。三路气体在混合器中充分混合,通过调节各自的流量配制成一定浓度的正癸烷模拟气体。模拟气体总流量为200 mL·min-1,其中O2流量为20 mL·min-1,N2流量180 mL·min-1。模拟气体通入放置在管式电阻炉里(由可控硅温度控制器控制反应温度)的DBD反应器(放电间隙1.3 mm、放电长度100 mm),经DBD反应器处理后的气体一路通入在线气相色谱仪(3420,北京北分瑞利分析仪器)的毛细管柱和FID检测器检测反应前后的正癸烷浓度和P-N柱及TCD检测器检测产物CO、CO2的浓度。另一路排空。脉冲电源(HV-10-08,扬中科泰)给DBD反应器提供高压。电压探头(P6015A,Tektronix)和电流探头(TCP0030, Tektronix)分别用于采集放电电压和电流的波形信号,通过示波器(DPO 3032,Tektronix)转换成相应的数字信号记录保存,用于计算功率。
|
图 1 实验装置示意图 Fig.1 Schematic diagram of the experimental setup 1. N2 steel bottle 2. O2 steel bottle 3. mass flowmeter 1 4. mass flowmeter 2 5. mass flowmeter 3 6. buffer 7. water bath 8. bubbler 9. mixer 10. temperature controller 11. oven 12. DBD reactor 13. voltage prober 14. current probe 15. pulse power supply 16. oscilloscope 17. gas chromatograph 18. exhaust absorption bottle |
实验中填满放电间隙的贵金属催化剂分别为Pd/Al2O3、Ag/Al2O3和Pt/Al2O3,均由等体积浸渍法制备所得。
放电能耗是影响C10去除的重要因素,脉冲电源输出功率计算方法为:
| $P = f\sum\limits_i {\left( {\frac{{{V_{_{i + 1}}} + {V_{_i}}}}{2}} \right)\left( {\frac{{{I_{_{i + 1}}} + {I_{_i}}}}{2}} \right)\left( {{t_{_{i + 1}}} - {t_i}} \right)} $ | (1) |
其中,P是电源输出功率,W;f是脉冲频率,Hz;ti+1和ti为一个脉冲时间里示波器采样点时刻,s;Vi+1和Vi分别为放电时间ti+1和ti时刻脉冲电源放电电压,V;Ii+1和Ii分别ti+1和ti时刻脉冲放电电流,A。
能量密度根据式(2)计算:
| ${\rm{ED}} = \frac{{60P}}{F}$ | (2) |
其中,F是总气体流量,L·min-1。
C10去除率、CO和CO2的选择性是评价等离子体催化效果的重要依据,分别根据式(3)~(5)计算。
| $X = \frac{{{C_0} - C}}{{{C_0}}} \times 100\% $ | (3) |
式中:X为ClO去除率,C0为放电前DBD反应器出口C10浓度,mg·m-3;C为放电后DBD反应器出口C10浓度,mg·m-3。
| ${S_{{\rm{co}}}} = \frac{{[{\rm{CO}}]}}{{{C_0} \times X \times 10}} \times 100\% $ | (4) |
| ${S_{{\rm{c}}{{\rm{o}}_{_{\rm{2}}}}}} = \frac{{[{\rm{C}}{{\rm{O}}_{\rm{2}}}]}}{{{C_0} \times X \times 10}} \times 100\% $ | (5) |
式中:S为选择性,%;[CO]和[CO2]分别为C10分解产物CO、CO2的浓度,mg·m-3。
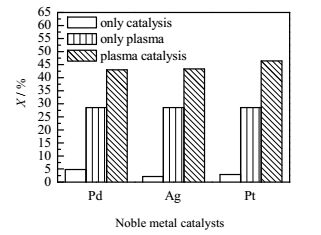
3 结果与讨论 3.1 贵金属催化剂种类对C10去除的影响本实验条件为贵金属催化剂的负载浓度1%(wt),C10的浓度1270 mg·m-3,反应温度100℃,能量密度100 J·L-1。图 2反映了了贵金属催化剂种类(Pd、Ag、Pt)对C10去除影响,具体揭示了单独热催化、单独等离子体以及等离子体催化三种情况下C10的去除性能。结果表明:只有催化作用时(无放电),三种贵金属催化剂对C10的去除率都在5%以下,这表明此时化学催化性能并没有很好体现。而单独等离子体(无催化剂)的去除效果要远好于单独催化,其对C10的去除率达到28.5%;将等离子体与贵金属催化结合后,C10去除率又有了明显提高,其中Pt催化剂效果最好,总的降解效率为46.4%,Pd、Ag催化剂次之,为43%左右;显然,等离子体催化作用明显大于单独等离子体作用与单独化学催化作用之和。这是因为将催化剂置于放电区域,能够充分发挥等离子体和化学催化的协同作用,例如等离子体强化催化剂的低温活性[8]以及催化剂促进放电的强度和均匀度[24]。
|
图 2 贵金属催化剂对C10转化率的影响 Fig.2 Effects of noble metal catalysts on C10 conversion |
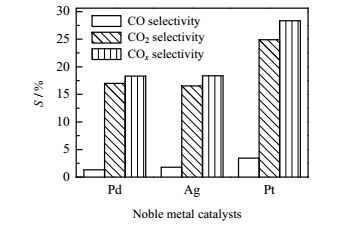
图 3反映了等离子体催化对C10降解产物COx选择性的影响。结果表明:在三种不同贵金属催化剂中,CO选择性都很小,最大仅为4%左右(Pt催化剂)。不同贵金属催化剂的CO2选择性比CO要大得多,Pt/Al2O3催化剂的CO2选择性最大,达到了24.9%。这说明贵金属催化剂Pt/Al2O3的加入促进了CO向CO2的转化[25],使C10得到深度降解。综合三种不同贵金属催化剂对C10去除率和COx选择性分析,Pt对C10的降解效果最好。
|
图 3 贵金属催化剂对COx选择性的影响 Fig.3 Effects of noble metal catalysts on COx selectivity |
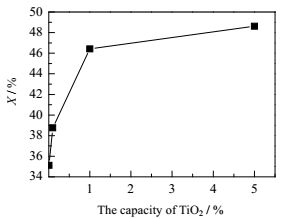
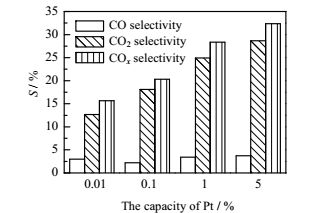
在能量密度为100 J·L-1,反应温度100℃,C10的初始浓度1270 mg·m-3的条件下,考察不同Pt负载量(0.01%、0.1%、1%、5%)对C10去除率以及COx选择性的影响,结果如图 4和图 5所示。从图 4中可知,随着Pt负载量的增加,C10的去除率随之增加,但是增加的趋势逐渐变缓。当负载量从0.01%增加到1%时,C10去的除率从35.1%提高到46.4%,而继续增加负载量到5%时,C10的去除率只从46.4%提高到48.6%。由此说明,Pt负载量对C10去除发挥着重要作用,并存在着一个相对适宜的负载量。从图 5的结果来看,COx选择性增加趋势与去除率增加趋势一致,当负载量从0.01%增加到1%时,COx选择性从15.6%提高到28.4%,而后继续增加负载量至5%,COx选择性仅提高4%。但Pt负载量的增加并没有引起CO选择性大的变化,而CO2选择性则有了比较大提高。从负载量0.01%至5%,CO选择性基本保持在4%以下,但CO2选择性从12.7%提高到28.6%,这说明Pt催化剂有助于CO深度氧化生成CO2。
|
图 4 Pt负载量对C10去除率的影响 Fig.4 Effects of Pt loading amount on C10 conversion |
|
图 5 Pt负载量对COx选择性的影响 Fig.5 Effects of Pt loading amount on COx selectivity |
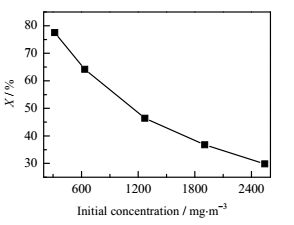
在能量密度为100 J·L-1,温度100℃,Pt负载量1%(wt)时,考察不同C10初始浓度对C10去除率以及COx选择性的影响,结果如图 6和图 7所示。从图 6中可知,随着初始浓度的增加,去除率减小,当初始浓度从317.6增加至2540.8 mg·m-3时,去除率由77.5%减小至29.8%。这是因为能量密度一定时,产生的电子、离子、原子等活性物质是确定的,虽然随着C10初始浓度增加去除量有所增加,但总的来说去除率降低了。
|
图 6 初始浓度对C10去除率的影响 Fig.6 Effects of initial concentrations on C10 conversion |
|
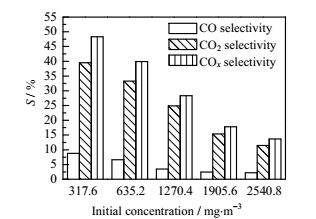
图 7 初始浓度对COx选择性影响 Fig.7 Effects of initial concentrations on COx selectivity |
从图 7中可得,随着初始浓度的增加,COx选择性也减小,当初始浓度从317.6 mg·m-3上升到2540.8 mg·m-3时,COx选择性从48.3%下降到13.6%,其中CO选择性从8.8%下降到2.2%,CO2选择性从39.5%下降到11.4%。说明由于反应过程催化氧化不彻底,C10并未完全转化为COx,所以COx选择性随着初始浓度的增加而降低,特别是CO2选择性的变化,从39.5%降低到11.4%,而CO选择性变化较小。
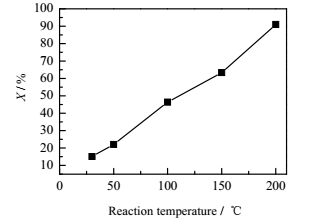
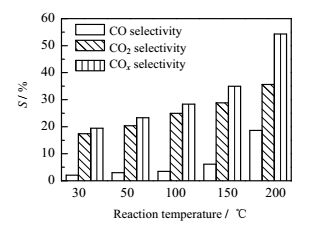
3.4 反应温度对C10去除的影响在能量密度为100 J·L-1,初始浓度1270 mg·m-3,Pt负载量1%(wt)时,考察不同反应温度对C10去除率以及COx选择性的影响,结果如图 8和图 9所示。从图 8和图 9中可知,随着反应温度的增加,去除率随之增加,COx选择性也随之增加。当反应温度从30℃上升到200℃时,去除率从15.1%上升到90.9%,COx选择性从19.4%增加到54.2%,其中CO选择性从2.0%上升到18.6%,CO2选择性从17.4%上升到35.6%。这是因为放电过程中产生的活性粒子如O和OH自由基与C10反应过程是吸热的,所以提高温度有助于增加反应速率[26];同时提高温度能够增加折合电场强度,折合电场强度是影响放电区域电子能量的重要因素,在一定条件下,折合电场强度的增加能够提高电子能量,有利于C10去除率的提高,并有利于COx生成;另外,反应温度的提高,有助于化学催化反应的进行,从而促进催化剂表面的氧化反应[27]。
|
图 8 反应温度对C10去除率影响 Fig.8 Effects of reaction temperatures on C10 conversion |
|
图 9 反应温度对COx选择性影响 Fig.9 Effects of reaction temperatures on COx selectivity |
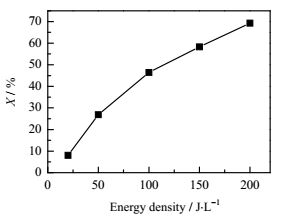
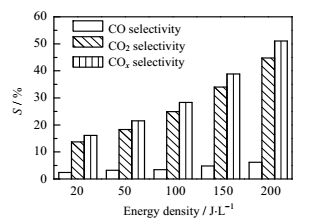
能量密度是影响等离子体放电过程中有机物去除最重要的因素。在反应温度为100℃,初始浓度1270.4 mg·m-3,Pt负载量1%(wt)时,考察不同能量密度对C10去除率以及COx选择性的影响,结果如图 10和图 11所示。从图 10和图 11中可知,能量密度的增加有利于C10的降解和COx生成,当能量密度从20上升到200 J·L-1,C10去除率从8.0%上升到69.3%,COx选择性从16.1%上升到51.0%,其中CO选择性从2.4%上升到6.2%,CO2选择性从13.7%上升到44.8%。究其原因,能量密度的增加,等离子体场中高能电子和活性基团等活性物质的数量会随之增加,即活性物质与C10碰撞的机会也就增多,有利于C10的氧化,最终导致去除的C10增多,同时去除的C10更多的向CO、CO2转化,导致COx明显上升。
|
图 10 能量密度对C10去除率影响 Fig.10 Effects of energy densities on C10 conversion |
|
图 11 能量密度对COx选择性影响 Fig.11 Effects of energy densities on COx selectivity |
(1) 等离子体催化作用明显大于单独等离子体作用与热催化作用之和,这是由于等离子体催化的协同作用而导致的。
(2) Pt/Al2O3催化剂对C10催化氧化效果优于Pd/Al2O3、Ag/Al2O3,同时Pt催化剂能够更好提高COx选择性。
(3) 初始浓度的增加不利于C10去除率和COx选择性的提高,而催化剂负载量、能量密度和反应温度的增加都有利于C10去除率和COx选择性的提高,实验中C10去除率最大可达91%,COx选择性最大为54.3%。
(4) 贵金属Pt在等离子场中有助于CO向CO2转化,导致C10催化氧化过程中转化生成了更多的CO2而使CO保持较低稳定的浓度。
符号说明:
| C | -放电前DBD反应器出口C10浓度,mg·m-3 | Ii+1 | - ti+1时刻脉冲放电电流,A |
| C0 | -放电后DBD反应器出口C10浓度,mg·m-3 | P | -放电注入功率,W |
| ED | -能量密度,J·L-1 | ti | -一个脉冲时间里示波器i采样点时刻,s |
| F | -气体流量,L·s-1 | ti+1 | -一个脉冲时间里示波器i+1采样点时刻,s |
| f | -脉冲频率,Hz | Vi | - ti时刻脉冲放电电压,V |
| Ii | -ti时刻脉冲放电电流,A | Vi+1 | - ti+1时刻脉冲放电电压,V |
| [1] | Wu Y, Zhang S J, HaoJ M, et al. On-road vehicle emissions and their control in China:a review and outlook[J]. Science of the Total Environment , 2017, 574: 332-349. DOI:10.1016/j.scitotenv.2016.09.040. |
| [2] | Ministry of environmental protection of the people's Republic of China (中华人民共和国环境保护部). China vehicle environmental management annual report (中国机动车环境管理年报)[R]. 2016. |
| [3] | Chen H L, Lee H M, Chen S H, et al. Removal of volatile organic compounds by single-stage and two-stage plasma catalysis systems:a review of the performance enhancement mechanisms, current status, and suitable applications[J]. Environmental Science & Technology , 2009, 43(7): 2216-27. |
| [4] | Vandenbroucke A M, Mora M, Jiménez-Sanchidrián C, et al. TCE abatement with a plasma catalytic combined system using MnO2 as catalyst[J]. Applied Catalysis B:Environmental , 2014, 156-157(9): 94-100. |
| [5] | Wang Y F, Zhang C B, Yu Y B, et al. Ordered mesoporous and bulk Co3O4 supported Pd catalysts for catalytic oxidation of o-xylene[J]. Catalysis Today , 2015, 242(1): 294-299. |
| [6] | Monteiro R A R, Lopes F V S, Silva A M T, et al. Are TiO2-based exterior paints useful catalysts for gas-phase photo oxidation processes? A case study on n-decane abatement forair detoxification[J]. Applied Catalysis B:Environmental , 2014, 147(14): 988-999. |
| [7] | Varjani S J. Microbial degradation of petroleum hydrocarbons[J]. Bioresource Technology , 2017, 223: 277-286. DOI:10.1016/j.biortech.2016.10.037. |
| [8] | Durme J V, Dewulf J, Leys C, et al. Combining non-thermal plasma with heterogeneous catalysis in waste gas treatment:a review[J]. Applied Catalysis B:Environmental , 2008, 78(3-4): 324-333. DOI:10.1016/j.apcatb.2007.09.035. |
| [9] | WU Zu-liang(吴祖良), ZHENG Xin-dan(郑欣丹), XIE De-yuan(谢德援), et al. Naphthalene degradation by dielectric barrier discharge coupling catalyst(介质阻挡放电协同催化萘降解)[J]. High Voltage Engineering(高电压技术) , 2016, 42(8): 1-7. |
| [10] | Feng F D, Zheng Y Y, Shen X J, et al. Characteristics of back corona discharge in a honeycomb catalyst and its application for treatment of volatile organic compounds[J]. Environmental Science & Technology , 2015, 49(11): 6831-6837. |
| [11] | Luengas A, Barona A, Hort C, et al. A review of indoor air treatment technologies[J]. Reviews in Environmental Science and Bio/Technology , 2015, 14(3): 499-522. DOI:10.1007/s11157-015-9363-9. |
| [12] | Li Y Z, Fan Z Y, Shi J W, et al. Modified manganese oxide octahedral molecular sieves M'-OMS-2(M'=Co, Ce, Cu) as catalysts in post plasma-catalysis for acetaldehyde degradation[J]. Catalysis Today , 2015, 256: 178-185. DOI:10.1016/j.cattod.2015.02.003. |
| [13] | Delagrange S, Pinard L, Tatibouët J M. Combination of a non-thermal plasma and a catalyst for toluene removal from air:manganese based oxide catalysts[J]. Applied Catalysis B:Environmental , 2006, 68(3-4): 92-98. DOI:10.1016/j.apcatb.2006.07.002. |
| [14] | Wang L, He H, Zhang C B, et al. Effects of precursors for manganese-loaded γ-Al2O3 catalysts on plasma-catalytic removal of o-xylene[J]. Chemical Engineering Journal , 2016, 288: 406-413. DOI:10.1016/j.cej.2015.12.023. |
| [15] | Lee H, Lee D H, Song Y H, et al. Synergistic effect of non-thermal plasma-catalysis hybrid systemon methane complete oxidation over Pd-based catalysts[J]. Chemical Engineering Journal , 2015, 259: 761-770. DOI:10.1016/j.cej.2014.07.128. |
| [16] | Tang X J, Feng F D, Ye L L, et al. Removal of dilute VOCs in air by post-plasma catalysis over Ag-based composite oxide catalysts[J]. Catalysis Today , 2013, 211(4): 39-43. |
| [17] | Rahimpour M R, Jahanmiri A, Rostami P, et al. Upgrading of anisole in a catalytic pulsed dielectric barrier discharge plasma reactor[J]. Energy & Fuels , 2013, 27(12): 7424-7431. |
| [18] | OU Jia-min(区家敏), FENG Xiao-qiong(冯小琼), LIU Yu-cong(刘郁葱), et al. Source characteristics of VOCs emissions from vehicular exhaust in the Pearl River Delta region(珠江三角洲机动车挥发性有机物排放化学成分谱研究)[J]. Acta Scientiae Circumstantiae(环境科学学报) , 2014, 34(4): 826-834. |
| [19] | Liu Y, Shao M, Fu L L, et al. Source profiles of volatile organic compounds (VOCs) measured in China:Part Ⅰ[J]. Atmospheric Environment , 2008, 42(25): 6247-6260. DOI:10.1016/j.atmosenv.2008.01.070. |
| [20] | GAO Shuang(高爽), JIN Liang-mao(金亮茂), SHI Jian-wu(史建武), et al. VOCs emission characteristics and emission factors of light-duty gasoline vehicles with bench test(轻型汽油车VOCs排放特征和排放因子台架测试研究)[J]. China Environmental Science(中国环境科学) , 2012, 32(3): 397-405. |
| [21] | YAO Shui-liang(姚水良), LU Hai-quan(陆海全), WU Zu-liang(吴祖良). Decomposition of n-decane with dielectric barrier discharges(介质阻挡放电分解正癸烷)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报) , 2015, 29(4): 978-984. |
| [22] | Jin Q, Jiang B Q, Han J Y, et al. Hexane decomposition without particle emission using a novel dielectric barrier discharge reactor filled with porous dielectric balls[J]. Chemical Engineering Journal , 2015, 286: 300-310. |
| [23] | Yao S L, Weng S, Jin Q, et al. Mechanism of decane decomposition in a pulsed dielectric barrier discharge reactor[J]. IEEE Transactions on Plasma Science , 2016, 44(11): 2660-2666. DOI:10.1109/TPS.2016.2573641. |
| [24] | Thevenet F, Sivachandiran L, Guaitella O, et al. Plasma-catalyst coupling for volatile organic compound removal and indoor air treatment:a review[J]. Journal of Physics D Applied Physics , 2014, 47(22): 224011. DOI:10.1088/0022-3727/47/22/224011. |
| [25] | Li J, Han S T, Bai S P, et al. Effect of Pt/g-Al2O3 catalyst on nonthermal plasma decomposition of benzene and byproducts[J]. Environmental Engineering Science , 2011, 28(6): 395-403. DOI:10.1089/ees.2010.0084. |
| [26] | Vandenbroucke A M, Morent R, De G N, et al. Non-thermal plasmas for non-catalytic and catalytic VOC abatement[J]. Journal of Hazardous Materials , 2011, 195(195): 30-54. |
| [27] | Mohanty S, Das A K, Das S P. DBD non-thermal plasma for decomposition of volatile organic compounds[J]. Chemical Science Review and Letters , 2015, 4(15): 889-911. |




