聚羧酸减水剂(PCE)作为水泥基材料广泛使用的化学外加剂,微观分子结构决定其应用性能[1-2]。使用含有活性端基的聚乙烯醇大单体与不饱和羧酸类小单体通过水溶性自由基聚合或酯化接枝聚合制备PCE时,不同共聚单体选择、投料比变化、长侧链的空间位阻作用会使聚合物组成不均,得到化学组成、支链数量和构象各不相同的共聚物[3-6]。为获得预计结构的共聚物,使用活性聚合[7]控制共聚物的主链长度,固定大单体的分子量控制共聚物支链长度,而共聚物支链密度及其分布则由共聚物组成、竞聚率控制[8],在这种情况下研究大单体的共聚合活性十分必要。影响大单体竞聚率的因素有端基的化学性质,大单体与增长链的相容性,大单体的相对分子量,均聚、共聚的转化率,溶剂效应等。有学者认为大单体聚合活性与端基小单体相同[9],实际上大单体长链结构,由于自身的位阻作用会相互排斥,且随着聚合的进行,这种大单体与聚合链的不相容性会增加,阻止聚合物链的活性中心向大单体的可聚合端靠近,从而影响大单体的聚合活性[10]。虽然已有取代基对烷基自由基向烯烃加成的影响[11],也有许多涉及大分子单体的共聚反应研究报道[9],但有关聚羧酸减水剂用大单体的活性研究还十分不足。本文对比研究了端基分别为异丁烯、异戊烯、乙烯乙基醚的3大单体在自由基共聚条件下的共聚合活性,从取代基的电子效应和极性效应角度,分析不同结构的端基对大单体共聚合活性和共聚物组成可能产生的影响。另外,对比分析了3种大单体在共聚过程中转化率、大单体在共聚物中组成与时间的变化关系,共聚物组成与转化率的变化关系,单体单元的链段分布,从而解释大单体共聚合活性对共聚物侧链数量、侧链密度、侧链分布的影响。
2 实验(材料与方法) 2.1 实验材料与仪器丙烯酸(AA):分析纯,天津福晨化学试剂厂;甲基烯丙基聚乙二醇醚(MAPEG)、异戊烯基聚乙二醇醚(IPEG):纯度 > 99%,相对分子量2 400,联泓化工有限公司;乙氧基乙烯基聚乙二醇醚(VEPEG):纯度 > 99%,相对分子量3 000,上海东大化学有限公司;过硫酸铵(APS):分析纯,天津福晨化学试剂厂;对苯二酚:分析纯,天津市光复精细化工研究所。美国Waters1525型高效液相色谱仪(HPLC);美国Waters凝胶渗透色谱仪(PL-GPC50)。
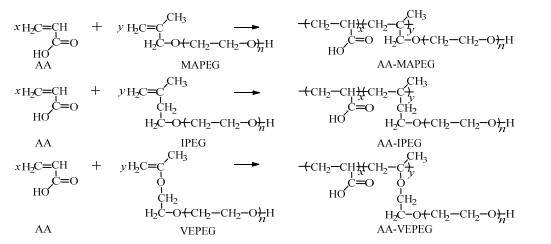
2.2 共聚物的制备3种聚醚大单体结构及与AA共聚反应方程式如图 1所示。研究3种大单体竞聚率时,将四口反应器放在50 ℃的恒温水浴锅中,按表 1设定的单体投料比(f1为大单体初始投料摩尔分数),先将大单体及适量的去离子水加入四口反应器中搅拌30 min,待大单体完全溶解后,依次加入AA和APS 1 g,通过自由基共聚制成固体质量分数为40% 的减水剂。在该温度下反应一定时间取样,加入2种单体总质量的0.01% 的对苯二酚终止反应,所得产物为低转化率下的共聚物。表 1中m为质量。
|
图 1 3种大单体与丙烯酸共聚反应方程式 Fig.1 Copolymerization reaction of three macromonomers |
|
|
表 1 竞聚率实验的单体投料质量 Table 1 Monomer dosages in the monomer reactivity ratio tests |
研究3种共聚物组成变化时,选取大单体与AA的初始投料摩尔比为1:1和1:4,按照表 2中的配方,采用与竞聚率计算相同的一次性加料方式聚合,每间隔10 min终止取样,研究3个体系大单体转化率-时间(C-t)、大单体在共聚物中组成-时间(F1-t)、以及F1-C变化情况。
|
|
表 2 大单体与丙烯酸投料摩尔比为1:1和1:4时共聚物组成实验单体用量 Table 2 Monomer dosages in the copolymer composition tests (feed molar ratio of macromers to AA = 1:4 and 1:1 |
AA含量的HPLC测定条件:柱温30 ℃,紫外检测波长205 nm,流动相为0.05 mol·L-1的H3PO4(用NaOH调pH = 7)-甲醇(体积比为92:8)溶液,体积流量为1.0 mL·min-1。HPLC测试溶液浓度控制在100×10-5mol·L-1左右,采用HPLC测定聚合体系中剩余的AA峰面积,根据丙烯酸标线计算AA剩余量,再根据初始投料量,计算得到共聚物结构中大单体与丙烯酸的摩尔比。
将所取样品配制成浓度2.5~3.5 mg·mL-1的待测溶液,GPC凝胶色谱柱温30 ℃,流动相为0.1 mol·L-1硝酸钠溶液,体积流量为1 mL·min-1,实验前记录大单体与AA投料量,通过GPC谱图中共聚物峰与大单体峰面积比,结合HPLC测试得到AA剩余量,从而计算出大单体转化率C。
大单体的1H NMR谱图测试条件:将3种大单体待测样品烘干,取30 mg溶解在氘代水中至饱和,在25 ℃、400 MHz的频率下使用德国Bruker公司AVANCE Digital 400MHz核磁共振仪测试。
3 实验结果与讨论 3.1 MAPEG、IPEG、VEPEG大单体的结构及共聚合活性 3.1.1 自由基共聚合机理大单体与AA制备PCE的自由基加成反应机理如图 2所示。自由基向单体加成时,首先是β碳上的π电子定域化,和R·反应形成σ键,然后是α碳原子上的π电子形成定域化的自由基[12]。
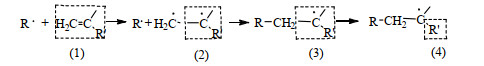
|
图 2 自由基加成机理图 Fig.2 Mechanism of free radical addition reaction |
有关烯烃取代基对其加成速率的研究已证明自由基的取代基、烯烃的β号位取代基和α号位取代基对自由基加成速率都有影响[13];β位是自由基进攻的位置,β位取代基的极性效应和位阻效应会影响加成速率,如果是使烯烃稳定的取代基对加成速率没有附加影响;α位不被进攻,α位取代基对加成速率影响很弱且只体现在极性效应方面。因此通过1H NMR核磁共振谱图比较3种大单体双键β位氢原子的化学位移来说明取代基产生的电子效应。当取代基的供电子效应越强,双键上H的电子云密度越大,核外电子对电子核的屏蔽作用增强,核磁共振吸收会向高场(低频)移动,化学位移减少。
3.1.2 3种大单体的化学结构差异MAPEG、IPEG、VEPEG 3种大单体的侧链均为聚乙烯醇,而端基分别为异丁烯、异戊烯、乙烯乙基醚。MAPEG和IPEG类大单体中双键的取代基团甲基、亚甲基具有供电子诱导效应,甲基还有超共轭效应;VEPEG大单体中氧原子与双键直接相连,电负性较强的氧原子对双键具有吸电子诱导效应,但是氧的孤对电子与双键上活动的π电子会形成更强的p-π供电子共轭效应。
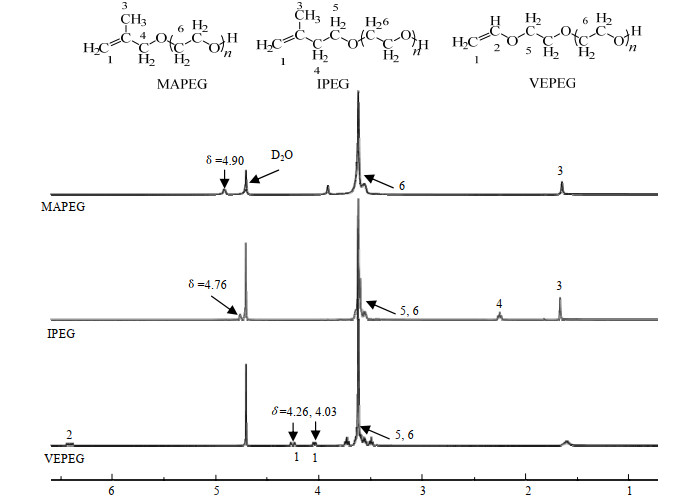
根据3种大单体的结构确定其中处于不同化学环境的氢原子化学位移的范围,从而在1H NMR谱图进行标峰,3种大单体中氢的化学位移值如图 3所示,3种大单体双键β位碳上的氢原子的化学位移为:MAPEG(4.90),IPEG(4.76),VEPEG(4.26、4.03),证明VEPEG大单体的取代基对β位碳原子的供电子效应更强,其聚合活性也应该有所不同。
|
图 3 MAPEG、IPEG、VEPEG大单体的1H NMR谱图 Fig.3 1H NMR spectra of MAPEG, IPEG and VEPEG macromers |
根据前线轨道理论[14],LUMO是最低未占分子轨道,HOMO是最高占据分子轨道,SOMO是自由基的单电子占据轨道。当自由基连有供电子基团(亲核性自由基),更容易与有吸电子基团的烯烃加成,因为SOMO-LUMO对加成反应起主导作用,供电基团使自由基SOMO轨道能级增加,从而使SOMO与LUMO之间的能级差减小,反应速率增加;反之当自由基连有吸电子基团(亲电性自由基),更易与有供电子基团的烯烃加成。
PCE合成过程产生的自由基主要有3种,分别是引发剂过硫酸铵产生初级自由基(SO4·),丙烯酸自由基(AA·)和大单体自由基(VEPEG·)。根据前线轨道理论可以推测:在链引发阶段,SO4·自由基为亲核性自由基,初级自由基引发VEPEG和AA形成单体自由基时,具有吸电子基团的AA更容易被引发形成AA·,VEPEG大单体被引发形成单体自由基的速率低于MAPEG和IPEG大单体;在链增长阶段,丙烯酸自由基是亲电性自由基,VEPEG大单体中双键所连基团产生的供电性比MAPEG和IPEG大单体更强,所以VEPEG大单体与丙烯酸自由基的加成速率高于MAPEG和IPEG,VEPEG单体自由基与AA单体的加成速率也高于MAPEG自由基和IPEG自由基。
大单体竞聚率计算过程可参照文献[15]。通过YBR法计算3种大单体的竞聚率测试结果如表 3所示(大单体为M1,丙烯酸为AA)。MAPEG-AA和IPEG-AA共聚体系单体竞聚率数值也十分接近;而VEPEG-AA共聚体系中用来表征大单体活性、丙烯酸活性的竞聚率数值rM1和rAA都高于MAPEG-AA、IPEG-AA共聚体系,再次证明端基会对大单体的共聚合活性产生较大的影响。丙烯酸竞聚率的倒数1/rAA=k21/k22可以间接表示3个大单体与丙烯酸自由基加成的活性(k21、k22分别为共聚过程中AA共聚、均聚链增长速率)。VEPEG-AA共聚体系的1/rAA数值最小,但MAPEG和IPEG被引发剂引发可以形成较稳定的叔碳自由基,VEPEG被引发剂引发形成活性更高的仲碳自由基,且VEPEG中氧原子与双键直接相连使双键电子云偏转增强,最终在与AA反应时VEPEG大单体具有更高的共聚合活性。
|
|
表 3 MAPEG-AA、IPEG-AA和VEPEG-AA共聚体系单体竞聚率 Table 3 Monomer reactivity ratios of MAPEG-AA, IPEG-AA and VEPEG-AA copolymerization systems |
大单体的共聚合活性不仅影响共聚反应速率,还会对共聚物的组成起着决定性的作用。选取2组不同的初始投料比(f1=0.20,f1=0.50,即M1与AA物质的量比n(M1): n(AA)= 1:4,n(M1): n(AA)=1:1)研究大单体转化率C、大单体在共聚物中的组成F1变化情况。
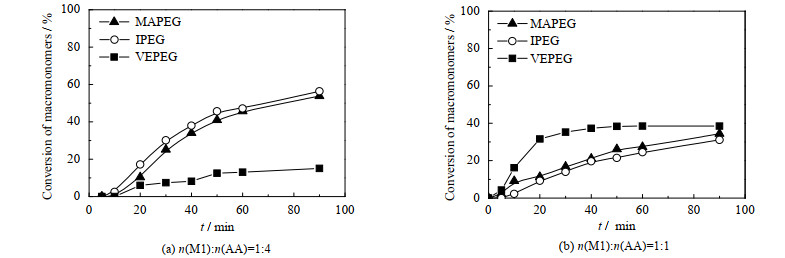
3.2.1 大单体共聚合活性对共聚合速率的影响图 4表明,在投料比n(M1): n(AA)为1:4和1:1时,3个体系中C随t变化情况明显不同。图 4(a)中f1=0.2,随着t的增加,MAPEG和IPEG大单体转化率先快速增加,在50 min后转化率增长缓慢,VEPEG大单体转化率始终为缓慢增加趋势;而图 4(b)中f1=0.5,VEPEG大单体的转化率先快速增加,在20 min后转化率增长缓慢,MAPEG和IPEG大单体的转化率却始终呈现缓慢增加的趋势;相同反应时间t,当f1=0.2时IPEG大单体转化率略高于MAPEG,VEPEG大单体转化率始终最低;而当f1=0.5时MAPEG大单体转化率略高于IPEG,VEPEG大单体转化率始终最高。
|
图 4 2种投料情况下MAPEG、IPEG、VEPEG转化率随时间变化曲线 Fig.4 Profiles of MAPEG, IPEG and VEPEG conversion under two feed ratios |
因此,随着共聚体系单体投料比f1的变化,VEPEG-AA共聚体系的大单体转化率与MAPEG-AA和IPEG-AA共聚体系变化趋势相反。降低f1 (f1=0.2),MAPEG和IPEG大单体表现出更快转化速率和更高转化率,而VEPEG大单体表现出缓慢转化速率和低转化率;提高f1 (f1=0.5),MAPEG和IPEG大单体表现出较慢共聚速率和较低转化率,而VEPEG大单体表现出较快共聚速率和更高转化率。由此可预见,当使用VEPEG作为大单体制备PCE时,需采用与MAPEG和IPEG类常用单体不同的配方组合、和聚合工艺控制参数,以提高大单体的转化率和获得理想的产品性能。
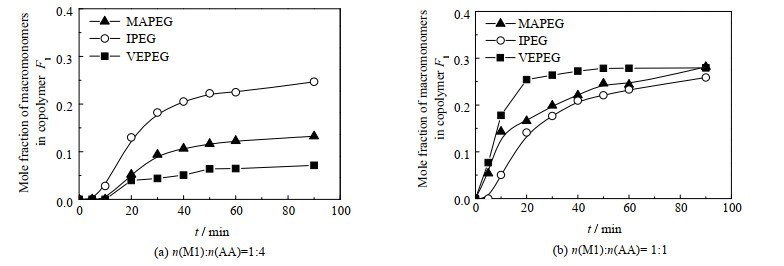
3.2.2 MAPEG-co-AA、IPEG-co-AA、VEPEG-co-AA共聚物侧链密度图 5中大单体在共聚物中组成F1随时间t变化曲线与图 4转化率C变化情况一致。但在二元共聚时,由于2个共聚单体活性和竞聚率不同,除恒比点外共聚物的组成并不等于单体组成,且共聚物组成会随转化率变化。大单体共聚形成PCE的长侧链结构,因此对比3个共聚体系中F1随着C变化情况,可以理解3种共聚物侧链密度的随着大单体转化率的变化情况。
|
图 5 2种投料比情况下MAPEG、IPEG、VEPEG在共聚物中组成随时间变化曲线 Fig.5 Profiles of MAPEG, IPEG and VEPEG compositions in copolymer under two feed ratios |
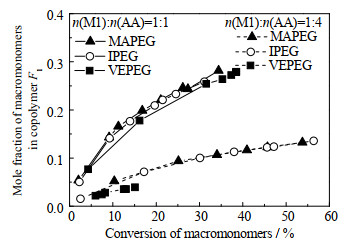
与大单体种类和单体投料比例无关,3个共聚体系中随着共聚反应的进行和大单体转化率C提高,F1逐渐提高,即形成共聚物的侧链密度逐步增加,如图 6所示。在2种投料比下,MAPEG-AA和IPEG-AA共聚体系的F1-C曲线几乎完全重合,而VEPEG-AA体系中F1-C曲线始终处于另外2条曲线的下方,说明在这2种投料比情况下,MAPEG-co-AA与IPEG-co-AA共聚物的侧链密度基本相同,而VEPEG-co-AA共聚物侧链密度始终较低;但随着f1的增加,VEPEG-AA体系的F1-C曲线与另外2条曲线的差值明显缩小,3种共聚物的侧链密度趋向于差异变小。
|
图 6 2种投料比3种大单体在共聚物中组成随转化率变化曲线 Fig.6 Profiles of MAPEG, IPEG and VEPEG compositions in copolymer as a function of conversion rate under two feed ratios |
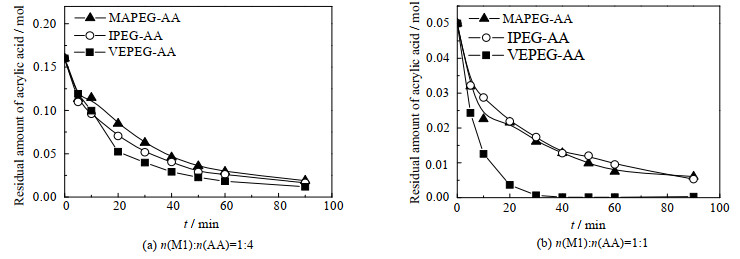
从3个体系中C、F1的变化情况与AA剩余量(见图 7)关系可以看出,随着共聚体系内AA剩余量减少,大单体的转化率增长缓慢。因为大单体的自聚倾向很弱甚至不能自聚,当AA剩余量很少不足以与大单体继续共聚反应,共聚反应终止。另外,在2种投料比情况下,VEPEG-AA共聚体系中AA消耗比其他2个体系更快,与3.1.3节部分VEPEG大单体自由基与AA单体有更高反应速率的结论一致。需要说明的是本部分实验采用一次加料方法,且为了使共聚过程放缓,从而放大3种单体反应活性的差异,加入的引发剂量较少,所以此时3种大单体转化率整体都低。
|
图 7 MAPEG-AA、IPEG-AA和VEPEG-AA共聚体系中AA剩余量 Fig.7 Residual amounts of AA in MAPEG-AA, IPEG-AA and VEPEG-AA copolymerization systems |
大单体活性和共聚过程决定了PCE共聚物中2种单体的链段分布情况,从而对PCE的性能有着至关重要的影响,为表征PCE链段结构的变化情况,利用竞聚率和概率论方法[16]计算出3种共聚体系在9组投料比下的链段分布参数如表 4所示。3种大单体、AA的链段序列分布根据公式p(xM1)=P11x-1(1-P11)、p(xAA)=P22x-1(1-P22) (p(xM1)是链段长为x的M1链段数占M1总链段数的百分比)计算并绘制如图 8所示。
|
|
表 4 MAPEG-AA、IPEG-AA、VEPEG-AA共聚体系链段分布参数 Table 4 Chain segment distribution parameters of MAPEG-AA, IPEG-AA and VEPEG-AA copolymerization systems |
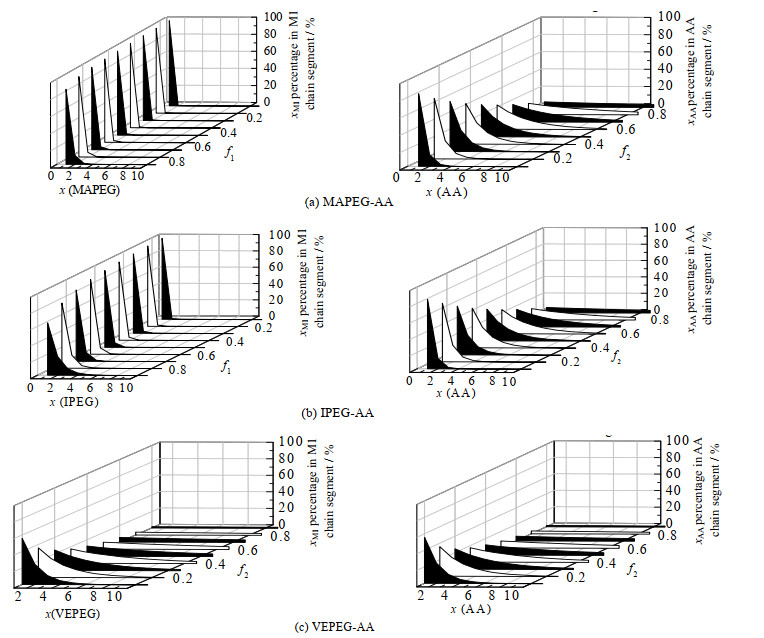
图 8为3种大单体和丙烯酸单体的链段分布情况。在所有初始投料比情况下,大单体还有丙烯酸都是长度为1的链段概率最高,链段长度增加概率值降低,下降幅度受单体活性、初始投料比等因素的影响。
|
图 8 3个共聚体系MAPEG、IPEG、VEPEG和AA单体的链段分布 Fig.8 Chain segment distribution of MAPEG, IPEG, VEPEG and AA monomers in three copolymerization systems |
3种大单体在不同投料比情况下始终表现出较窄链段分布,表现为链段长度多集中在10以内,而3个体系中丙烯酸的链段长度可达到100以上(在丙烯酸初始投料比f2接近1时)。
初始投料摩尔分数f1、f2的增加,使相应单体能形成更长的链段,从而使该单体的链段分布变宽,这反映了单体在共聚过程中的自增长倾向。根据图 8中3种大单体的链段范围可以看出VEPEG大单体自增长倾向稍高于MAPEG和IPEG大单体,且3种大单体的自增长倾向远低于丙烯酸。表 4中3个共聚体系中大单体的平均链段长度NM1始终远小于丙烯酸的平均链段长度NAA,也说明3种大单体的自增长倾向远低于丙烯酸。在MPEG-AA和IPEG-AA共聚体系中NM1始终小于1.6,而VEPEG-AA共聚体系NM1可增加到3.07,再次说明VEPEG的自增长倾向高于MAPEG和IPEG单体。
3.3.2 MAPEG-co-AA、IPEG-co-AA、VEPEG-co-AA共聚物侧链分布大单体活性和共聚过程的差异导致3种共聚物侧链分布的不同。在不同投料比情况下获得的共聚物,其侧链分布情况可以由大单体和AA的链段分布情况表示,当f1 < 0.3(f2 > 0.7)时,3种大单体链段长度集中在2以内,AA链段的分布则十分宽(链段长度可达为100),这时PCE的结构为大单体以一个单体单元的链段随机插入AA单体形成的主链中,但VEPEG-AA共聚体系的AA链段更长,这说明VEPEG大单体转化要消耗更多AA单体,共聚过程结果也证明在f1=0.2时VEPEG大单体的转化消耗更多AA,但转化率低于MAPEG和IPEG。
随着f1增加,大单体的链段分布变宽,AA的链段分布变窄,当0.3 < f1 < 0.9(0.1 < f2 < 0.7)时,MAPEG-AA和IPEG-AA共聚体系的AA最长链段在10左右,VEPEG-AA共聚体系的AA链段长度大于10,但是VEPEG大单体链段长度也比MAPEG和IPEG单体长,此时共聚合过程是VEPEG单位消耗更多的AA单体,但自身的转化率也迅速提高。
4 结论本文通过对比具有不同端基的3种聚醚大单体的共聚合活性和共聚合过程,研究端基对大单体共聚合活性及共聚物微观结构的影响。
1H NMR谱图和竞聚率结果证明端基会对单体共聚合活性产生较大的影响。3种大单体与丙烯酸进行自由基加成反应时,VEPEG大单体共聚合活性更强。随初始投料比f1的变化,VEPEG-AA共聚体系的大单体转化率与MAPEG-AA和IPEG-AA共聚体系变化趋势相反,在相同的聚合时间里VEPEG-AA共聚体系中AA的消耗量也更多。大单体活性和共聚过程的差异导致3种共聚物侧链分布的不同,但随着f1的增加3种共聚物侧链密度差异变小。由此可预见,当采用VEPEG作为大单体制备PCE时,需要采用与常用的MAPEG和IPEG不同的配方组合和聚合工艺控制参数,以提高大单体的转化率和获得理想的产品结构和性能。
| [1] |
王子明. 聚羧酸系高性能减水剂-制备、性能与应用[M]. 北京: 中国工业出版社, 2009: 1-20. WANG Z M. Polycarboxylic superplasticizer-Preparation, properties and applications[M]. Beijing: China Industry Press, 2009: 1-20. |
| [2] |
李慧群, 姚燕, 王子明. 异戊烯基聚氧乙烯醚分子量对聚羧酸超塑化剂单体序列结构的影响[J]. 硅酸盐学报, 2019, 47(2): 201-206. LI H Q, YAO Y, WANG Z M. Influence of molecular mass of isoprenyloxy polyethylene glycol on monomer sequence in polycarboxylate superplasticizers[J]. Journal of the Chinese Ceramic Society, 2019, 47(2): 201-206. |
| [3] |
PLANK J, LI H Q, ⅡG M, et al. A microstructural analysis of isoprenol ether-based polycarboxylates and the impact of structural motifs on the dispersing effectiveness[J]. Cement Concrete Research, 2016, 84(7): 20-29. |
| [4] |
HADJICHRISTIDIS N, PISPAS S, PITSIKALIS M, et al. Graft copolymers, encyclopedia of polymer science and technology[M]. New York: Wiley, 2002.
|
| [5] |
ANNA M Z, THOMAS J, CHRISTOPHER B K A. Detailed investigation of the free radical copolymerization behavior of n-butyl acrylate macromonomers[J]. Macromolecules, 2011, 44(17): 6691-6700. DOI:10.1021/ma201345m |
| [6] |
NIKOS H, MARINOS P, HERMIS I, et al. The strength of the macromonomer strategy for complex macromolecular architecture: molecular characterization, properties and applications of polymacromonomers[J]. Macromolecular Rapid Communications, 2003, 24(17): 979-1013. DOI:10.1002/marc.200300050 |
| [7] |
LIU X, GUAN J N, LAI G H, et al. Performances and working mechanism of a novel polycarboxylate superplasticizer synthesized through changing molecular topological structure[J]. Journal of Colloid and Interface Science, 2017, 504: 12-24. DOI:10.1016/j.jcis.2017.05.025 |
| [8] |
REGHUNADHAN N C P, CHAUMONT P, CHARMOT D. Copolymerization behaviour of pentadiene-functional macromonomers obtained by free radical addition-fragmentation[J]. Polymer, 1999, 40(8): 2111-2119. DOI:10.1016/S0032-3861(98)00417-0 |
| [9] |
HIRANO T, ZETTERLUND P, YAMADA B. Macromonomer preparation by radical polymerization and copolymerization of the unsaturated tetramer of methyl acrylate[J]. Polymer Journal, 2003, 35(6): 491-500. DOI:10.1295/polymj.35.491 |
| [10] |
PARASKEVI D, PANAGIOTIS B, MARINOS P. Radical copolymerization of 2-vinyl pyridine and oligo(ethylene glycol) methyl ether methacrylates: Monomer reactivity ratios and thermal properties[J]. European Polymer Journal, 2011, 47(4): 762-771. DOI:10.1016/j.eurpolymj.2010.09.032 |
| [11] |
CITTERIOA, ARNOLDI A, MINISCI F. Nucleophilic character of alkyl radicals. 18. Absolute rate constants for the addition of primary alkyl radicals to conjugated olefins and 1, 4-benzoquinone[J]. The Journal of Organic Chemistry, 1979, 44(15): 2674-2682. DOI:10.1021/jo01329a017 |
| [12] |
BERND G. Formation of C-C bonds by addition of free radicals to alkenes[J]. Angewandte Chemie International Edition, 1983, 22(10): 753-764. DOI:10.1002/anie.198307531 |
| [13] |
BERND G., Meister J. Steric effect in the addition of alkyl radical to alkenes[J]. Angewandte Chemie International Edition, 1981, 20(11): 967-967. |
| [14] |
FUKUI K, FUJIMOTO H. Frontier orbitals and reaction paths: Selected papers of Kenichi Fukui[M]. Singapore: World Scientific, 1997.
|
| [15] |
王子明, 尹东杰, 毛倩瑾. 异丁烯醇聚氧乙烯醚与丙烯酸的竞聚率及共聚物链段分布[J]. 高分子材料科学与工程, 2018, 34(2): 19-23. WANG Z M, YIN D J, MAO Q J. Reactivity ratio of isobutyl alcohol ethoxylates with acrylic acid and the segment distribution of copolymer[J]. Polymer Materials Science and Engineering, 2018, 34(2): 19-23. |
| [16] |
KELEN T, TÜDOTILDES F. Analysis of the linear methods for determining copolymerization reactivity ratios.i. a new improved linear graphic method[J]. Journal of Macromolecular Science: Part A-Chemistry, 1975, 9(1): 1-27. DOI:10.1080/00222337508068644 |




