醋酸乙烯-乙烯(VAE)共聚乳液,是醋酸乙烯乳液(白乳胶)的乙烯内增塑产品,具有优良的可塑性、耐水性、不易脆裂等特点,是一种广泛应用于工业生产、木材、纸张以及涂料等行业的水基型胶黏剂[1]。VAE乳液本身无毒,但由于传统工业生产中通常采用H2O2/次硫酸盐甲醛加合物作为引发体系,而次硫酸盐加合物会造成乳液终产物中有游离甲醛残留,因此间接对人体和环境造成危害[2, 3]。D-异抗坏血酸钠(SoE)是食品行业中常见的保鲜剂,具有优良的还原性能以及价格低廉,对环境和人体无害[4]。将SoE作为还原剂应用于乳液聚合氧化还原引发体系,鲜有报道。本文以叔丁基过氧化氢(TBHP)为氧化剂,D-异抗坏血酸钠(SoE)为还原剂,Fe2+ 为引发助剂,采用半连续聚合工艺考察TBHP-Fe2+-SoE氧化还原体系对VAE乳液的聚合动力学并与传统H2O2/次硫酸盐甲醛加合物体系进行对比,初步探究了该体系对VAE乳液聚合的影响。
2 实验部分 2.1 实验原料醋酸乙烯(VAc,聚合级):广西广维化工有限责任公司,经40℃ 减压蒸馏处理并置于阴凉处备用;乙烯(Ethylene,聚合级):南京德士蓝科技有限公司;次硫酸锌合甲醛(ZFS,分析纯):上海斯百全化学有限公司;抗坏血酸(AsAc,分析纯):上海试四赫维化工有限公司;十二烷基磺酸钠(SDS,分析纯),硫酸亚铁(FeSO4·7H2O),过氧化氢(H2O2,分析纯),聚乙二醇-400(PEG-400,分析纯):广东西陇化工股份有限公司;D-异抗坏血酸钠(SoE,分析纯):江西百勤异VC钠有限公司;叔丁基过氧化氢(TBHP,分析纯),吐温-20(Tween-20,分析纯),吐温-40(Tween-40,分析纯):阿拉丁(中国)试剂;聚乙烯醇-205(PVA-205,平均聚合度500,醇解度88%,分析纯):日本可乐丽株式会社;以上试剂除VAc均为直接使用。
2.2 乳液聚合实验采用半连续乳液聚合工艺,其反应装置如图 1所示。

|
图 1 半连续工艺制备VAE 乳液反应装置图 Fig.1 Experimental setup for the preparation of VAE emulsion 1. C3H4 streel cylinder 2. sample bottle 3. autoclave 4. piezometer 5. constant flow pump for VAc 6. constant flow pump for TBHP solution 7. programmable logic controller 8.TBHP solution 9. VAc monomer 10. heat exchanger |
将PVA-205、PEG-400、Tween-20、Tween-40、SDS、还原剂加入适量去离子水中于30℃ 并在氮气保护下充分溶解后与初始VAc单体、FeSO4溶液同时加入至高压反应釜中。高压釜密封后用乙烯(1 MPa)置换3次以清除釜内残留氧气,之后将釜内乙烯压力升至聚合压力3.0 MPa并设定搅拌转速为500 r⋅min-1进行预乳化处理30 min。待预乳化处理完成后将釜内温度升至反应所需温度并连续加入氧化剂溶液,5 min后连续加入VAc单体,给定聚合时间2 h,聚合完成后于保温30 min,之后泄压、出料。所用基础聚合配方为:PVA-205,10.0 g;PEG-400,10.0 g;Tween-20,3.0 g;Tween-40,1.0 g,SDS,1.0 g;去离子水,200 g;FeSO4(0.05 %(wt) 水溶液),5.0 g;初始VAc单体,175.0 g;连续VAc单体,150 g;氧化剂溶液,100 g。
2.3 分析与测试采用称量法测定转化率。定时从反应釜中取出适量乳液样品(约1 g)置于样品瓶内并滴加少量浓度为0.2%(wt) 的对苯二酚水溶液,在130℃ 烘箱内烘干至恒重。具体计算公式如下:
| $X(t)=\frac{{{W}_{T}}(t)(S(t)-C)(1-{{R}_{E}}(t))}{{{W}_{VAc}}(t)}$ |
其中,
固定实验所用氧化剂与还原剂摩尔浓度之比为2:1,引发助剂Fe2+ 摩尔浓度(以总VAc投入量为基础,下同)为1.5×10-5 mol⋅L-1,还原剂与引发助剂采用间歇进料,氧化剂采用连续进料。考察了TBHP-Fe2+-SoE引发体系与H2O2-Fe2+-ZFS引发体系在质量浓度为0.125%(wt)、0.250%(wt)、0.500%(wt),并分别在60和80℃时对VAE乳液聚合速率的影响。
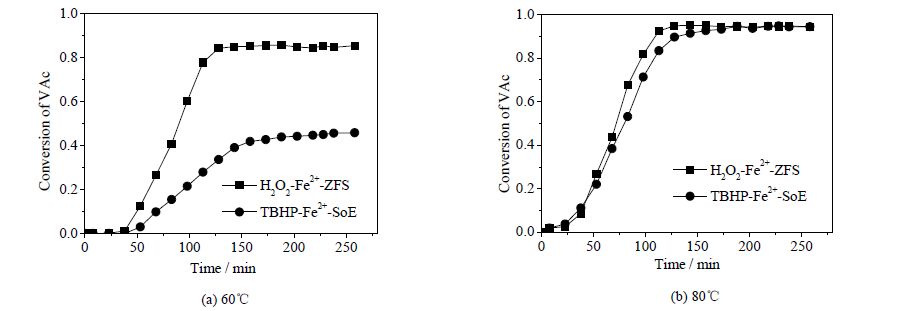
当引发体系浓度为0.125%(wt),TBHP-Fe2+-SoE引发体系与H2O2-Fe2+-ZFS引发体系分别在温度为60和80℃条件下反应,所得VAc单体转化率随反应时间的变化结果如图 2所示。由图 2可知,两种乳液引发聚合体系均较符合Smith-Ewart动力学模型。由图 2(a)可见,当反应温度为60℃时,TBHP-Fe2+-SoE体系对反应的引发效率明显低于 H2O2-Fe2+-ZFS体系,TBHP-Fe2+-SoE体系下的系统聚合速率以及总转化率偏低。由图 2(b)可见,当控制反应温度为80℃ 时,从体系聚合速率以及所得总转化率可知,TBHP-Fe2+-SoE体系的引发效率得到显著提升。虽然在乳液聚合恒速阶段过程中TBHP-Fe2+-SoE体系下的聚合速率仍略低于H2O2-Fe2+-ZFS体系,但是在乳液聚合减速阶段过程中TBHP-Fe2+-SoE体系下的聚合速率高于H2O2-Fe2+-ZFS体系,两者最终所得总转化率相近。
|
图 2 引发体系浓度为0.125%(wt)时转化率随反应时间的变化曲线 Fig.2 Profiles of conversion as a function of time with the redox concentration of 0.125%(wt) |
当引发体系浓度为0.25%(wt),TBHP-Fe2+-SoE引发体系与H2O2-Fe2+-ZFS引发体系分别在温度为60和80℃条件下反应,所得VAc单体转化率随反应时间的变化结果如图 3所示。由图 3(a)可见,当反应温度为60℃时,H2O2-Fe2+-ZFS体系下的聚合速率及所得总转化率均明显高于TBHP-Fe2+-SoE体系。由图 3(b)可见,当反应温度为80℃时,TBHP-Fe2+-SoE的引发效率相对于60℃ 时得到显著提高,同时略高于同等反应条件下的H2O2-Fe2+-ZFS体系。

|
图 3 引发体系浓度为0.25%(wt)时转化率随反应时间的变化曲线 Fig.3 Profiles of conversion as a function of time with the redox concentration of 0.25%(wt) |
当引发体系浓度为0.5%(wt),TBHP-Fe2+-SoE引发体系与H2O2-Fe2+-ZFS引发体系分别在温度为60和80℃条件下反应,所得VAc单体转化率随反应时间的变化结果如图 4所示。由图 4(a)可见,当反应温度为60℃时,TBHP-Fe2+-SoE体系的引发效率仍低于H2O2-Fe2+-ZFS体系,同时,该体系在聚合反应进行到约200 min之后引发效率明显降低并接近停滞,而外部VAc单体还在以恒定流速不断加入至反应体系中,以至于体系总VAc单体转化率出现下降趋势。由图 4(b)可见,当控制反应温度为80℃时,TBHP-Fe2+-SoE体系引发效率明显提高,聚合速率和体系最终总转化率提升并高于H2O2-Fe2+-ZFS体系。

|
图 4 引发体系浓度为0.5%(wt)时转化率随反应时间的变化曲线 Fig.4 Profiles of conversion as a function of time with the redox concentration of 0.5%(wt) |
由图 2至图 4所得曲线可知,当反应温度为60℃ 时,对于不同的引发剂体系浓度,TBHP-Fe2+-SoE体系的引发效率均明显低于H2O2-Fe2+-ZFS体系,而当反应温度为80℃ 时,TBHP-Fe2+-SoE体系的引发效率增长明显,且该体系下的单体最终转化率接近甚至高于H2O2-Fe2+-ZFS体系。将图 2至图 4所得曲线进行对比,两种引发体系的引发效率在两种温度下均随着引发体系浓度的增大呈现先增大后降低的趋势。这是由于氧化剂以及还原剂的进料方式不同引起的,氧化剂水溶液在反应过程中采用连续进料方式,而还原剂采用反应前一次性间歇进料方式。还原剂不仅可以与连续加入的氧化剂发生氧化还原反应产生具有引发活性的自由基,还可以与自由基发生进一步反应而使自由基失活。当引发体系浓度处于低浓度时反应体系中还原剂存在较少,因而对氧化还原反应产生的自由基影响较低,随着引发剂体系浓度的升高,单位时间内因氧化还原反应产生的自由基数量增大,进而对聚合反应的速率和最终总转化率的提高有促进作用。而当引发体系浓度升高到一定数值时,反应体系中还原剂浓度过大,进而造成体系中自由基大量失活,最终导致引发体系 效率下降。TBHP是一种既亲水又具有油溶性的氧化剂,其通过氧化还原反应所得到的自由基ButO·既能直接进入乳液胶核中引发反应又能通过在水相中被单体分子捕获而成长为足够疏水的单体自由基再进入胶核中引发反应[5~7]。而H2O2作为一种亲水型氧化剂,其对于乳液聚合的引发主要通过生成单体自由基来形成[7, 8]。当乳液聚合反应进入第三阶段即减速期时,单体液滴完全消失,此时未反应的单体分子主要存在于已形成的乳胶粒中[9],因而只能通过亲油型自由基ButO·直接进入乳胶粒继续引发反应,这也解释了80℃下TBHP-Fe2+-SoE体系在减速期的聚合速率以及最终VAc单体总转化率要略高于H2O2-Fe2+-ZFS体系的原因。
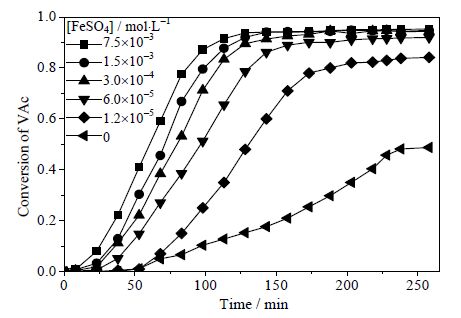
3.2 TBHP-Fe2+-SoE引发体系中各组分对VAE乳液聚合动力学的影响通过半连续式乳液聚合工艺,设定TBHP-Fe2+-SoE引发体系浓度为单体总质量的0.125%,氧化剂TBHP与还原剂SoE摩尔配比为2:1,反应温度为80℃,其他条件相同时,考察TBHP-Fe2+-SoE引发体系中Fe2+ 浓度对VAE乳液聚合动力学的影响,所得VAc单体转化率与反应时间的关系曲线如图 5所示。由图 5可知,Fe2+ 浓度对VAc单体最终转化率以及反应速率有显著的影响,体系中Fe2+ 浓度越大则聚合反应速率越高,最后所得VAc单体转化率也越高,反应前期的诱导期和成核时间也越短。但是随着Fe2+浓度成倍的增加,聚合反应速率以及总VAc单体转化率增加的越来越不明显。当Fe2+ 浓度为0时,聚合速率明显降低,所得总VAc单体转化率也维持在较低水平,小于50%。
|
图 5 Fe2++ 浓度对VAE 乳液聚合动力学的影响 Fig.5 Effects of Fe2++ concentration on VAE polymerization kinetics (redox concentration = 0.125%, oxidant/reductant ratio = 2/1) |
设定TBHP-Fe2+-SoE引发体系浓度为单体总质量的0.125%,Fe2+ 浓度为3.0×10-4 mol⋅L-1,反应温度为80℃,其他条件相同,考察体系中氧化剂TBHP与还原剂SoE摩尔配比对VAE乳液聚合动力学的影响,所得VAc单体转化率与反应时间的关系曲线如图 6所示。由图 6可知,随着TBHP与SoE摩尔配比的升高,反应聚合速率以及最终总VAc单体转化率也逐渐升高,这同样是因为体系中存在的过量还原剂会进一步与自由基反应而引起自由基失活,从而降低了引发效率。但是,这并不意味着还原剂SoE的含量越低越好,由图可知,当给定SoE物质的量为0时,聚合反应进行的十分缓慢,体系引发效率低下,其主要原因在于体系中微量Fe2+消耗完全之后引发反应及聚合物链增长所需自由基主要来源于TBHP的热分解,而TBHP在80℃下的半衰期较长(164℃下为10 h),热分解效率低,进而导致引发效率低下。

|
图 6 氧化剂与还原剂配比对VAE 乳液聚合动力的影响 Fig.6 Effects of TBHP/SoE ratio on VAE polymerization kinetics (redox concentration = 0.125%, Fe2+ concentration = 3.0×10-4 mol⋅L-1) |
将图 5和图 6所得聚合动力学曲线进行对比,可以看出,TBHP与SoE发生了氧化还原反应并产生了可引发VAE乳液聚合的自由基,这一结果也和抗坏血酸(AsAc)与TBHP发生氧化还原反应产生自由基相类似[10],但是该自由基产生方式的效率不高。在TBHP-SoE体系中引入微量的Fe2+ 可以极大地促进自由基的产生并提高反应引发效率。这是由于Fe2+ 可以快速地与TBHP发生氧化还原反应产生具有引发活性的自由基ButO·,其反应方程式[11] 如下所示。
| $F{{e}^{2+}}+B{{u}^{t}}OOH+{{H}^{+}}\to F{{e}^{3+}}+B{{u}^{t}}O\cdot +{{H}_{2}}O$ |
由反应方程式可知,Fe2+ 会被TBHP氧化为Fe3+,而由于体系中存在的SoE具有的强还原性可以将Fe3+ 再度还原为Fe2+,这样就维持了体系中Fe2+的稳定,使反应持续进行。综上,可推断TBHP-Fe2+-SoE体系的引发机理如图 7所示。自由基主要通过Fe2+ 和SoE分别与TBHP发生氧化还原反应而产生,但是在产生效率方面,Fe2+ 与TBHP要远高于SoE与TBHP。

|
图 7 TBHP-Fe2++-SoE 氧化还原体系自由基产生机理 Fig.7 Scheme of radical producing mechanism in the TBHP-Fe2++-SoE redox initiator system |
采用半连续乳液聚合工艺,设定TBHP-Fe2+-SoE引发体系浓度为单体总质量的0.125%,Fe2+ 浓度为3.0×10-4 mol⋅L-1,TBHP与SoE摩尔配比为2:1,反应温度为80℃,其他条件相同,考察TBHP进料流速对VAE乳液聚合动力学的影响,其结果如图 8所示。

|
图 8 TBHP 进料流速对VAE 乳液聚合动力学的影响 Fig.8 Effects of TBHP feeding rate on VAE polymerization kinetics (redox concentration = 0.125%, Fe2++ concentration = 3.0×10-4 mol⋅L-1, TBHP/SoE ratio = 2/1) |
由图 8中所示曲线可知,TBHP进料流速越快,其对应反应诱导期越短,成核时间越短,反应速率越高,达到减速阶段所需时间也越短。这是因为当单位时间内加入反应体系内的引发剂量增加,单位时间内产生的自由基增加,特别是在反应初期成核量增加,而聚合反应发生于生成的乳胶粒中,进而提升了反应速率[12]。
4 结 论(1) TBHP-Fe2+-SoE引发体系可以应用于VAE乳液的制备。TBHP-Fe2+-SoE引发体系在反应温度为60℃ 时引发效率较H2O2-Fe2+-ZFS体系低,但当反应温度达到80℃ 时其引发效率与H2O2-Fe2+-ZFS体系相当。同时,由于其产生的自由基具有亲油特性,在聚合反应到达减速阶段时可以直接进入乳胶粒中继续引发反应,因此在减速阶段引发的聚合速率以及最终所得VAc单体总转化率略高于H2O2-Fe2+-ZFS体系。当引发体系质量占总VAc单体质量的0.25%时,其引发效率最高。
(2) TBHP-Fe2+-SoE引发体系的引发效率随着Fe2+ 浓度的增大而升高,但升高速率逐渐放缓。升高TBHP与SoE摩尔配比对体系引发效率的提高有促进作用,但当SoE用量为0时体系引发效率骤降,说明TBHP与SoE存在一最佳配比。
(3) TBHP与SoE反应可生成具有引发活性的自由基但效率较低,在TBHP-SoE体系中引入微量Fe2+可对引发效率的提高有明显促进作用。
(4) 提高TBHP水溶液进料速率有利于提高TBHP-Fe2+-SoE引发体系的引发效率。
| [1] | LI Zi-dong(李子东), LI Guang-yu(李广宇), YU Min(于敏) . VAE emulsion and its adhesives(VAE乳液及其胶粘剂)[J]. Adhesion(粘接) , 2001, 22 (6) : 27-30 |
| [2] | MO Li-hong(莫红丽), LU Tai-rong(陆泰榕), SHI Xian-wei(石显伟) . Reduction of free formaldehyde content in VAE emulsion via FF6M reducing agent(FF6M还原剂降低VAE乳液中游离甲醛含量的研究)[J]. Technology & Development of Chemical Industry(化工技术与开发) , 2014 (1) : 20-21 |
| [3] | WU Hui-jiang(吴辉江) . Development of high solids content vinyl acetate-ethylene copolymer emulsions(高固含量醋酸乙烯-乙烯共聚乳液的研制)[J]. Adhesion(粘接) , 2003, 24 (4) : 15-17 |
| [4] | ZHANG Yong-qing(张永清) . Effect of sodium isoascorbate on the nutrient contents of fresh-cut lotus root(异抗坏血酸钠对鲜切莲藕营养成分的影响)[J]. The Food Chemistry(食品工业) , 2015, 36 (7) : 9-12 |
| [5] | Ronco L I, Minari R J, Gugliotta L M . Particle nucleation using different initiators in the miniemulsion polymerization of styrene[J]. Brazilian Journal of Chemical Engineering , 2015, 32 (1) : 191-200 DOI:10.1590/0104-6632.20150321s00003150 |
| [6] | Ronco L I, Minari R J, Vega J R . Incorporation of polybutadiene into waterborne polystyrene nanoparticles via miniemulsion polymerization[J]. European Polymer Journal , 2013, 49 (9) : 2635-2644 DOI:10.1016/j.eurpolymj.2013.06.011 |
| [7] | Rodríguez R, Barandiaran M J, Asua J M . Particle nucleation in high solids miniemulsion polymerization[J]. Macromolecules , 2007, 40 (16) : 5735-5742 DOI:10.1021/ma070525c |
| [8] | Lamb D J, Fellows C M, Gilbert R G . Radical entry mechanisms in redox-initiated emulsion polymerizations[J]. Polymer , 2005, 46 (19) : 7874-7895 DOI:10.1016/j.polymer.2005.06.078 |
| [9] | Erbil Y H . Vinyl acetate emulsion polymerization and copolymerization with acrylic monomers[M]. CRC Press: Boca Raton, 2000 . |
| [10] | Da Cunha L, Ilundain P, Salazar R . VOC formation during monomer removal by post-polymerization[J]. Polymer , 2001, 42 (2) : 391-395 DOI:10.1016/S0032-3861(00)00377-3 |
| [11] | Barton D H R, Patin H . Radical chemistry of tert-butyl hydroperoxide (TBHP). Part 2. Studies of the Fe II-TBHP mechanism[J]. New Journal of Chemistry , 1998, 22 (6) : 565-568 |
| [12] | SUN Zhi-juan(孙志娟), ZHANG Xin-ya(张心亚), JIANG Qing-mei(江庆梅) . Kinetics and nucleation mechanisum for semi-continuous emulsion polymerization of MMA/BA(MMA/BA半连续乳液聚合的动力学特征及成核机理)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报) , 2007, 21 (4) : 614-620 |




