2. 浙江医药高等专科学校,浙江 宁波 315000
2. Zhejiang Pharmaceutical College, Ningbo 315000, China
正渗透(forward osmosis,FO)是一种以膜两侧渗透压差为驱动力的新型膜分离技术,以能耗低、回收率高、分离膜不易被污染等优点,在废水处理[1]、海水淡化[2]、食品和医药[2-3]等领域具有巨大的应用潜力。通常由多孔支撑层和超薄分离层复合而成的正渗透膜是正渗透分离技术的核心之一,膜结构与性能直接影响正渗透技术的分离效率[4]。有研究通过对正渗透过程传质机理进行分析,指出支撑层内部发生的内浓差极化(internal concentration polarization, ICP),造成了正渗透实际水通量低于理论值的现象[5-6],制约了正渗透技术的进一步发展和应用。造成内浓差极化现象的原因主要是分离过程中溶质和溶剂在支撑层内的扩散受到支撑层物理结构和化学性质的限制,减小正渗透膜支撑层的结构参数S,提升支撑层的亲水性将有利于缓解内浓差极化造成的影响[7-10]。
由静电纺丝法制备的纳米纤维膜具有独特的内连通三维孔结构和高孔隙率(较小的膜结构参数),有利于膜内溶剂和溶质的扩散流动[11]。据此,Kim等[9]以静电纺丝法得到的亲水性交联聚乙烯醇纳米纤维膜为支撑层制备了水通量显著提升的正渗透膜。然而,目前以静电纺丝法得到的纳米纤维膜为支撑层制备正渗透膜,由于亲水性支撑层与分离层之间结合力较弱,在运行过程中支撑层和分离层极易剥离[12]。虽然McCutcheon等[13]发现,纳米纤维表面存在的活性基团可提升支撑层与分离层之间的结合力,但兼具静电纺丝可操作性和合适活性基团的聚合物种类较少。
本文从静电纺丝法制备聚丙烯腈纳米纤维出发,通过表面多巴胺自聚改性的方法,得到纤维表面富含邻苯二酚、氨基、亚氨基等反应活性基团的亲水性支撑层[14-15],并在此基础上通过界面聚合制备复合正渗透膜。研究多巴胺改性时间对聚丙烯腈纳米纤维支撑层物理结构和化学性质的影响,并进一步研究支撑层结构和性质对所制备的复合正渗透膜结构和性能的影响,以期为高性能静电纺丝基正渗透膜的研究提供借鉴。
2 实验部分 2.1 实验材料聚丙烯腈(polyacrylonitrile,PAN,Mw~250 000)由中国石油天然气有限公司提供;间苯二胺(MPD,99.5%)、三乙胺盐酸盐(98%),三(羟甲基)氨基甲烷(Tris,≥99.9%)和盐酸多巴胺(dopamine hydrochloride,98%)购自阿拉丁试剂(上海)有限公司;均苯三甲酰氯(TMC,98%)采购自梯希爱(上海)化成工业发展有限公司;N,N-二甲基甲酰胺(DMF,≥99.5%)、正己烷(≥99.5%)、氯化钠(≥99.5%)和硫酸铜(> 99.0%)购自国药集团化学试剂有限公司;去离子水(电导率 < 10-6 S·cm-1)由实验室自制。
2.2 正渗透膜的制备 2.2.1 聚丙烯腈纳米纤维支撑层的制备聚丙烯腈纳米纤维支撑层通过静电纺丝方法制备,静电纺丝装置由高压直流电源(DW-P303-1ACF0,东文高压电源(天津)有限公司),微量注射泵(HK-400,深圳好克光电仪器有限公司)和接收滚筒(钢制,直径105 mm)组成。具体操作方式如下:以DMF为溶剂配制质量分数为17%的PAN铸膜液;通过静电纺丝(电压:16 kV,湿度:60%,推进速度:1.0 mL·h-1,针尖内径:0.41 mm,接收端和针尖距离:20 cm,转速:8 r·min-1,收集时间:12 h)得到聚丙烯腈纳米纤维;最后于在180 ℃下热压2 h,得到聚丙烯腈纳米纤维支撑层(electrospunpolyacrylonitrile,ePAN)。
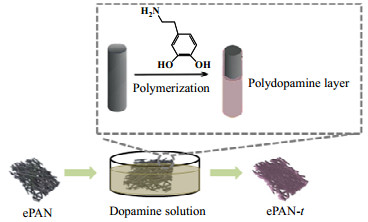
2.2.2 表面多巴胺改性聚丙烯腈纳米纤维支撑层的制备表面多巴胺改性聚丙烯腈纳米纤维支撑层制备过程如图 1所示:首先以pH=8.5的Tris-HCl缓冲液为溶剂,配制质量浓度为1.0 g·L-1的多巴胺溶液。随后将ePAN浸入上述溶液中,室温下置于敞口容器中震荡反应。经一段时间反应,将其取出并用去离子水洗去除残余的多巴胺溶液,放入60 ℃烘箱中干燥,最终得到表面聚多巴胺(polydopamine,PDA)改性的聚丙烯腈纳米纤维支撑层。将改性时间不同的支撑层命名为ePAN-t(t为多巴胺改性时间,单位h)。
|
图 1 表面多巴胺改性聚丙烯腈纳米纤维支撑层制备过程示意图 Fig.1 Schematic diagram of the preparation of PDA modified ePAN substrates |
分别以ePAN-t为支撑层,MPD为水相单体,TMC为油相单体,通过界面聚合法制备正渗透复合膜。具体操作如下:首先将质量分数为2.0%的MPD水相溶液倾倒于ePAN-t表面,浸没2 min;倒出并沥干表面多余MPD溶液后,再倒入质量分数为0.1%的TMC正己烷溶液;界面聚合反应1 min后倒出TMC溶液,将界面聚合反应后的膜置于烘箱中于60 ℃热处理8 min后得到复合正渗透膜。本研究中,将所制备的复合正渗透膜命名为TFC-t。以未改性ePAN-0为支撑层,通过同样的界面聚合法制备对照组复合正渗透膜,命名为TFC-0。
2.3 膜结构和性能表征采用扫描电镜(SEM,SU-8010,Hitachi,Japan))对样品表面形貌和结构进行测定和分析。使用全反射红外光谱仪(ATR-FTIR,Tenson 27,Bruker,Germany)测试改性前后支撑层表面特征官能团的变化。采用光学接触角测定仪(OCA20,Dataphysics,Germany)通过固定液滴法测试样品表面的水接触角,用于表征样品表面的亲疏水性。
2.4 正渗透膜性能测试采用自制正渗透测定装置评价正渗透复合膜的性能。测试条件为:有效面积7.065 cm2,温度(25±1) ℃,膜两侧流体流速0.6 L·min-1,进料液为去离子水,汲取液为不同浓度的氯化钠溶液,膜朝向为正渗透模式(FO-mode)即分离层朝向原料液侧(active layer facing feed solution,AL-FS)。正渗透膜的水通量通过单位时间内原料液侧重量的减少量计算得出,计算式为
| $ J_{\mathrm{w}}=\frac{\Delta V}{m \cdot \Delta t} $ | (1) |
式中:Jw为膜的水通量,L·m-2·h-1;Δt为测试时间,h;m为膜有效面积,m2;ΔV为透过液的体积,L。
正渗透膜的反向盐渗透通量为
| $ J_{\mathrm{s}}=\frac{\rho_{\mathrm{CF}, t} V_{\mathrm{F}, t}-\rho_{\mathrm{CF}, 0} V_{\mathrm{F}, 0}}{m \cdot \Delta t} $ | (2) |
式中:Js为膜的反向盐渗透通量,g·m-2·h-1,ρCF, t、ρCF, 0分别为t时刻原料液和初始原料液中盐质量浓度,g·L-1,VF, t,VF, 0分别为t时刻原料液和初始原料液的体积,L。
正渗透膜的纯水渗透系数A,10-5 L·m-2·h-1·Pa-1、盐渗透系数B,L·m-2·h-1和膜结构参数S,μm,参考Tiraferri等[16]提出的方法进行测定。即通过测定4种不同浓度汲取液(本研究选取浓度分别为0.3、0.6、1.0、2.0 mol·L-1的NaCl溶液)正渗透膜的纯水通量和盐反向渗透率,利用matlab最小二乘法非线性回归法拟合,得到A,B,S值。Rw2和Rs2分别为水通量和盐通量模拟值与实际值之间的拟合程度。拟合中涉及的公式如下:
| $ J_{\mathrm{w}}=A\left\{\frac{\rho_{\pi \mathrm{D}} \exp \left(-\frac{J_{\mathrm{w}} S}{D}\right)-\rho_{\pi \mathrm{F}} \exp \left(\frac{J_{\mathrm{w}}}{k}\right)}{1+\frac{B}{J_{\mathrm{w}}}\left[\exp \left(\frac{J_{\mathrm{w}}}{k}\right)-\exp \left(-\frac{J_{\mathrm{w}} S}{D}\right)\right]}\right\} $ | (3) |
| $ J_{\mathrm{s}}=B\left\{\frac{\rho_{\mathrm{CD}} \exp \left(-\frac{J_{\mathrm{w}} S}{D}\right)-\rho_{\mathrm{CF}} \exp \left(\frac{J_{\mathrm{w}}}{k}\right)}{1+\frac{B}{J_{\mathrm{w}}}\left[\exp \left(\frac{J_{\mathrm{w}}}{k}\right)-\exp \left(-\frac{J_{\mathrm{w}} S}{D}\right)\right]}\right\} $ | (4) |
| $ R_{\mathrm{w}}^{2}=1-\frac{\sum_{i=1}^{n}\left(J_{\mathrm{w}, i}^{\mathrm{EXP}}-J_{\mathrm{w}, i}^{\mathrm{CALC}}\right)^{2}}{\sum_{i=1}^{n}\left(J_{\mathrm{w}, i}^{\mathrm{EXP}}-\bar{J}_{\mathrm{w}}^{\mathrm{EXP}, n}\right)^{2}} $ | (5) |
| $ R_{\mathrm{s}}^{2}=1-\frac{\sum_{i=1}^{n}\left(J_{\mathrm{s}, i}^{\mathrm{EXP}}-J_{\mathrm{s}, i}^{\mathrm{CALC}}\right)^{2}}{\sum_{i=1}^{n}\left(J_{\mathrm{s}, i}^{\mathrm{EXP}}-\bar{J}_{\mathrm{s}}^{\mathrm{EXP}, n}\right)^{2}} $ | (6) |
式中:ρCF和ρCD分别为原料液和汲取液的质量浓度,pπF和pπD分别为原料液和汲取液侧的渗透压,105 Pa;D为25 ℃时NaCl溶质扩散系数,值为1.48×10-9 m2·s-1;k为原料液中溶质传递系数,当忽略外浓差极化的影响时,k→∞,即exp (Jw/k)值为1,n为测试总次数(本文中n = 4),Jw, iEXP,Jw, iCALC分别为第i次测试时水通量的实验值和模拟值,Js, iEXP,Js, iCALC分别为第i次测试时反向盐渗透通量的实验值和模拟值,JwEXP, n和JsEXP, n分别为n次测试所得水通量和反向盐渗透通量的实验平均值。
3 结果与讨论 3.1 表面多巴胺改性聚丙烯腈纳米纤维支撑层的制备如图 2(a)~(d)所示为表面多巴胺改性前后聚丙烯腈纳米纤维支撑层的表面SEM图片。由SEM图片可看出,所制备的支撑层均具有类似的静电纺丝法纳米纤维膜典型的网状结构(孔隙率:(70.5±2.7)%,表面孔径:(1.8±0.7) μm,且纤维形态均匀。进一步对比可见,ePAN中纤维表面较为平滑,随多巴胺改性时间的增加,纤维表面逐渐变得粗糙,并有颗粒状物质出现。从图 2(e)中也可见,支撑层的颜色随表面多巴胺改性时间的延长逐渐加深。这种纤维表面微结构的变化和支撑层宏观下颜色的改变主要是由纳米纤维表面多巴胺分子的聚合与黏附所造成。在多巴胺改性过程中,溶液中多巴胺小分子自由基会在聚丙烯腈纳米纤维表面产生黏附,并引发原位自聚合反应。随着反应时间的延长,溶液中的多巴胺单体进一步发生自聚反应,生成聚多巴胺及聚多巴胺纳米粒子并沉积于纳米纤维的表面,造成支撑层颜色的加深[17]。经多巴胺表面改性后,纳米纤维支撑层表现出优异的亲水性(图 2(f)),其水接触角由未改性前的(40.6±1.7)°下降至无法直接测得(水滴在1 s内可在支撑层表面完全铺展,接触角下降到0°)。

|
图 2 表面多巴胺改性前后聚丙烯腈纳米纤维支撑层的表面结构与表面亲水性 Fig.2 Surface morphologies and hydrophilicity of the ePAN substrates before and after PDA modification |
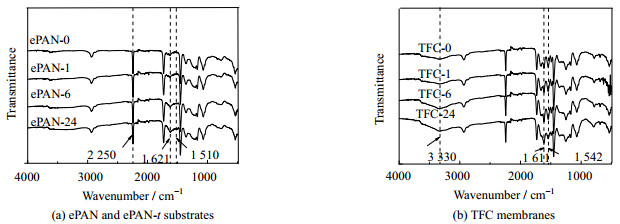
如图 3(a)所示为多巴胺改性前后支撑层的表面ATR-FTIR谱图。从图 3(a)可见,在2 250 cm-1处出现的强吸收峰,为聚丙烯腈分子中C≡N的特征吸收峰。对比未经改性的ePAN膜,多巴胺改性后的纳米纤维支撑层在3 500~3 100 cm-1处出现由多巴胺分子中酚羟基、氨基引起的伸缩振动峰;1 621和1 510 cm-1处则出现由聚多巴胺中N─H的弯曲振动和剪切振动引起的吸收峰。N─H弯曲振动和剪切振动所产生的吸收峰强度随多巴胺改性时间的延长而增强,说明纳米纤维表面聚多巴胺含量随改性时间的延长而增加。通过红外光谱分析,可以发现酚羟基、氨基等具有界面聚合反应活性的亲水基团已经成功地引入支撑层的纳米纤维表面,且随着多巴胺改性时间的延长,纳米纤维表面的聚多巴胺含量呈上升趋势,很好地符合水接触角测试的结果[18]。
|
图 3 多巴胺改性前后聚丙烯腈纳米纤维支撑层和相应正渗透膜的全反射红外光谱图 Fig.3 ATR-FTIR spectra of the substrates and corresponding FO membranes |
以不同多巴胺改性条件制备的ePAN为支撑层,通过MPD与TMC界面聚合得到的TFC正渗透膜,其表面形貌如图 4所示。界面聚合反应后,支撑层表面原有的大孔结构(图 2)均被聚酰胺分离层完整覆盖。对比表面结构较为平整的TFC-0(图 4(a)),在多巴胺改性的支撑层表面所形成的聚酰胺分离层具有更丰富的由MPD和TMC经界面聚合形成的典型的峰谷(ridge-and-valley)结构(图 4(b)~(d))。多巴胺改性在支撑层表面引入大量的极性基团(酚羟基、氨基等),极性基团的引入有利于支撑层表面MPD分子的富集[19-20],造成局部反应单体浓度的增加,导致局部反应强度的增加和更多反应热的释放,最终导致更丰富的峰谷结构的形成[21]。

|
图 4 以不同多巴胺改性膜为支撑层的复合正渗透膜表面SEM图 Fig.4 SEM images of the TFC membranes based on ePAN-0 and dopamine modified ePAN substrates |
从复合膜的红外谱图(图 3(b))可见:在1 542和1 611 cm-1有新的吸收峰出现,其中1 542 cm-1为酰胺II中N─H弯曲振动和C─N伸缩振动峰,1 611 cm-1为芳酰胺中N─H变形振动峰;而在3 330 cm-1处则出现了芳香胺中氨基伸缩振动吸收峰。上述表征进一步说明纳米纤维支撑层表面聚酰胺分离层的成功形成。由于傅里叶红外光谱仪测试厚度范围在1 μm左右,而聚酰胺的厚度通常小于1 μm,因此在复合膜的红外图谱中能观察到支撑层中特征吸收峰的存在[22]。
3.3 复合正渗透膜的结构稳定性如图 5所示为经去离子水浸泡后2类复合正渗透膜TFC-0和TFC-1的SEM图片。浸泡后,TFC-0表面的聚酰胺分离层与支撑层发生明显的剥离,这显然无法满足实际正渗透运行过程的需要。而TFC-1膜表面聚酰胺层仍保持完整,分离层与支撑层之间的稳定性表现出显著的改善。以上结果表明,未经多巴胺改性的支撑层与界面聚合所形成的聚酰胺分离层之间的结合力弱,在水中两层极易发生分离。而以多巴胺改性后的纳米纤维膜为支撑层进行界面聚合反应,所形成的复合正渗透膜的结构更为稳定。这可能是由多巴胺改性后支撑层表面所引入的酚羟基、氨基等活性基团与界面聚合单体中的酰氯基团反应[18, 23],在支撑层和聚酰胺层之间形成了共价键造成的。

|
图 5 浸泡实验后TFC-0和TFC-1的SEM图 Fig.5 Surface morphology of TFC membranes after deionized water immersion tests |
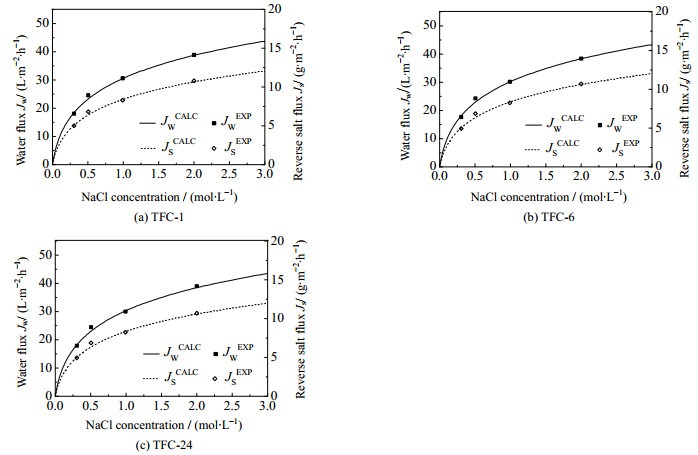
由于TFC-0膜的结构不稳定无法有效测试其性能,本文选择TFC-1、TFC-6和TFC-24为测试对象,以不同浓度的氯化钠溶液为汲取液,去离子水为进料液,测试了3组复合正渗透膜在正渗透过程中的纯水通量和反向盐渗透通量,并利用matlab最小二乘法非线性拟合,计算得到了正渗透膜的纯水渗透系数A、盐渗透系数B和膜结构参数S值,如图 6所示。3组复合膜的水通量实验值JwEXP与模拟值JwCALC之间,盐反向渗透通量的实验值JsEXP与模拟值JsCALC之间均表现出较好的拟合度,说明了测试结果的可靠性和3组复合膜运行过程中的稳定性。如表 1所示为对3种自制复合正渗透膜与2种商业化正渗透膜(HTI-CTA膜和Oasys-TFC膜)相关性能的总结。从表 1中可以看出,3种自制正渗透膜的纯水渗透系数均远高于商业化正渗透膜HTI-CTA膜,与Oasys-TFC膜相近;其盐反向渗透通量均远低于2种商业化正渗透膜。这是由于以静电纺丝法制备的纳米纤维膜为支撑层,所得复合正渗透膜具有更小的结构参数(S值),削弱了复合膜在正渗透过程中所受内浓差极化的影响。由于多巴胺改性在支撑层纤维表面形成的聚多巴胺层厚度有限,延长改性时间对支撑层的膜孔结构并无明显影响[24],对比3种自制的复合正渗透膜,其A值、B值和S值无显著差别。
|
图 6 正渗透膜水通量和反向盐渗透通量的实验值及模拟值 Fig.6 Experimental and simulated data of water flux and reverse salt flux of the TFC membranes |
|
|
表 1 复合正渗透膜和商业化正渗透膜性能的比较 Table 1 Comparison of TFC-t membranes prepared in this work with commercial membranes |
理论而言,正渗透过程中纯水通量和盐反向渗透通量将随汲取液浓度增加而线性增加[25]。但由于内浓差极化现象的存在,在实际操作过程中,随着汲取液渗透压增加,正渗透膜的纯水通量和反向盐渗透通量往往增长缓慢。从图 6中可见,本研究通过对支撑层结构和亲水性的设计与调控,降低了所制备复合正渗透膜的结构参数(S值,表 1),提升了膜的亲水性(图 2(h)),缓解了内浓差极化现象造成的影响,对提升正渗透过程中的分离性能具有一定程度的贡献。
4 结论本文研究了多巴胺对静电纺丝法制备的聚丙烯腈纳米纤维膜的改性情况,通过SEM对支撑层表面结构的观察和红外光谱对支撑层表面官能团的分析证实了聚多巴胺在ePAN表面的形成,通过水接触角实验证明了多巴胺改性有利于支撑层表面亲水性的提升。以多巴胺改性后的亲水纳米纤维膜为支撑层,通过MPD与TMC界面聚合的方法制备得到了复合正渗透膜,发现由多巴胺改性引入支撑层表面的活性基团(酚羟基、氨基等)提升了支撑层和分离层之间的稳定性。延长多巴胺改性时间对所制备的复合正渗透膜性能未造成显著影响,所制备的复合正渗透膜具有较高的水通量和较低的反向盐渗透通量,表现出良好的正渗透分离性能。所制备的复合正渗透膜的结构参数S值远小于商业化正渗透膜,有利于抑制正渗透过程中内浓差极化现象的产生。
| [1] |
LUTCHMIAH K, VERLIEFDE A R, ROEST K, et al. Forward osmosis for application in wastewater treatment: A review[J]. Water Research, 2014, 58(3): 179-197. |
| [2] |
QIN J J, LAY W C L, KEKRE K A. Recent developments and future challenges of forward osmosis for desalination: A review[J]. Desalination and Water Treatment, 2012, 39(1/2/3): 123-136. |
| [3] |
CATH T, CHILDRESS A, ELIMELECH M. Forward osmosis: Principles, applications, and recent developments[J]. Journal of Membrane Science, 2006, 281(1/2): 70-87. |
| [4] |
贾玉香, 陈立军, 李燕, 等. 正渗透过程中水和离子在碳纳米管中的传递行为研究[J]. 高校化学工程学报, 2014, 28(4): 707-711. JIA Y X, CHEN L J, LI Y, et al. Study on transport behaviours of water molecules and ions in carbon nanotube during forward osmosis process[J]. Journal of Chemical Engineering of Chinese Universities, 2014, 28(4): 707-711. |
| [5] |
KUANG W, LIU Z, YU H, et al. Investigation of internal concentration polarization reduction in forward osmosis membrane using nano-CaCO3particles as sacrificial component[J]. Journal of Membrane Science, 2016, 497(4): 485-493. |
| [6] |
GRAY G T, MCCUTCHEON J R, ELIMELECH M. Internal concentration polarization in forward osmosis: role of membrane orientation[J]. Desalination, 2006, 197(1/2/3): 1-8. |
| [7] |
PARK M, LEE J J, LEE S, et al. Determination of a constant membrane structure parameter in forward osmosis processes[J]. Journal of Membrane Science, 2011, 375(1): 241-248. |
| [8] |
YIP N Y, TIRAFERRI A, PHILLIP W A, et al. High performance thin-film composite forward osmosis membrane[J]. Environmental Science & Technology, 2010, 44(10): 3812-3818. |
| [9] |
PUGUAN J M C, KIM H S, LEE K J, et al. Low internal concentration polarization in forward osmosis membranes with hydrophilic crosslinked PVA nanofibers as porous support layer[J]. Desalination, 2014, 336(1): 24-31. |
| [10] |
HUANG L, BUI N N, MEYERING M T, et al. Novel hydrophilic nylon 6, 6 microfiltration membrane supported thin film composite membranes for engineered osmosis[J]. Journal of Membrane Science, 2013, 437(15): 141-149. |
| [11] |
SONG X, LIU Z, SUN D D. Nano gives the answer: Breaking the bottleneck of internal concentration polarization with a nanofiber composite forward osmosis membrane for a high water production rate[J]. Advanced Materials, 2011, 23(29): 3256-3260. DOI:10.1002/adma.201100510 |
| [12] |
徐佳, 唐媛媛, 高从堦. 正渗透膜支撑层结构优化的研究进展[J]. 化学进展, 2015, 27(8): 1025-1032. XU J, TANG Y Y, GAO C J. Research progress on optimizing the Structure of support layers in forward osmosis membrane[J]. Progress in Chemistry, 2015, 27(8): 1025-1032. |
| [13] |
BUI N N, LIND M L, HOEK E M V, et al. Electrospun nanofiber supported thin film composite membranes for engineered osmosis[J]. Journal of Membrane Science, 2011, 385(1): 10-19. |
| [14] |
LEE H, DELLATORE S M, MILLER W M, et al. Mussel-inspired surface chemistry for multifunctional coatings[J]. Science, 2007, 318(5849): 426-430. DOI:10.1126/science.1147241 |
| [15] |
LEE H, SCHERER N F, MESSERSMITH P B. Single- molecule mechanics of mussel adhesion[J]. Proceedings of the National Academy of Sciences of the United States of America, 2006, 103(35): 12999-13003. DOI:10.1073/pnas.0605552103 |
| [16] |
TIRAFERRI A, YIP N Y, STRAUB A P, et al. A method for the simultaneous determination of transport and structural parameters of forward osmosis membranes[J]. Journal of Membrane Science, 2013, 444(1): 523-538. |
| [17] |
HONG S, NA Y S, CHOI S, et al. Non-covalent self-assembly and covalent polymerizationco-contribute to polydopamine formation[J]. Advanced Functional Materials, 2012, 22(22): 4711-4717. DOI:10.1002/adfm.201201156 |
| [18] |
JI Y L, ANG M B M Y, HUNG H C, et al. Bio-inspired deposition of polydopamine on PVDF followed by interfacial cross-linking with trimesoyl chloride as means of preparing composite membranes for isopropanol dehydration[J]. Journal of Membrane Science, 2018, 557(1): 58-66. |
| [19] |
YAO Z K, YANG Z, GUO H, et al. Highly permeable and highly selective ultrathin film composite polyamide membranes reinforced by reactable polymer chains[J]. Journalof Colloid and Interface Science, 2019, 552(1): 418-425. |
| [20] |
YAO Z K, GUO H, YANG Z, et al. Reactable substrate participating interfacial polymerization for thin film composite membranes with enhanced salt rejection performance[J]. Desalination, 2018, 436(1): 1-7. |
| [21] |
MAX H, Y AO, Z K, YANGZ, et al. Nano-foaming of polyamide desalination membranes to tune permeability and selectivity[J]. Environmental Science & Technology Letters, 2018, 5(2): 123-130. |
| [22] |
TANGC Y, KWON Y N, LECKIEJ O. Probing the nano- and micro-scales of reverse osmosis membranes-A comprehensive characterization of physiochemical properties of uncoated and coated membranes by XPS, TEM, ATR-FTIR, and streaming potential measurements[J]. Journal of Membrane Science, 2007, 287(1): 146-156. DOI:10.1016/j.memsci.2006.10.038 |
| [23] |
ZHAO J, SU Y, HE X, et al. Dopamine composite nanofiltration membranes prepared by self-polymerization and interfacial polymerization[J]. Journal of Membrane Science, 2014, 465(1): 41-48. |
| [24] |
BERNSMANN F, BALL V, ADDIEGO F, et al. Dopamine-melanin film deposition depends on the used oxidant and buffer solution[J]. Langmuir, 2011, 27(6): 2819-2825. DOI:10.1021/la104981s |
| [25] |
TANG C Y, SHE Q, LAY W C L, et al. Coupled effects of internal concentration polarization and fouling on flux behavior of forward osmosis membranes during humic acid filtration[J]. Journal of Membrane Science, 2010, 354(1/2): 123-133. |




