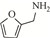
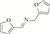
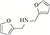
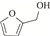
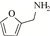
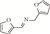
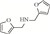
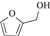
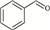
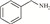
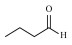
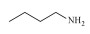
随着能源需求的不断增长,以及煤、石油和天然气等不可再生化石资源日趋消耗殆尽,绿色可再生的能源转型迫在眉睫。典型的可再生资源(如木质纤维素类生物质)转化制高附加值化学品和燃料的研究受到越来越广泛地关注[1]。木质纤维素可通过化学或生物转化制得糠醛、5-羟甲基糠醛等大宗平台化合物[2]。其中,糠醛是一种重要的呋喃化合物,可作为起始原料构建多种高附加值化学品,如糠醇[3]、2-甲基四氢呋喃[4]、糠胺[5-6]等。糠胺是合成许多药物[7]和聚酯[8]的重要组成部分,应用前景非常广阔。
糠胺由糠醛还原胺化制得。首先糠醛上的羰基与氨缩合生成亚胺,然后亚胺被还原生成糠胺。羰基与氨的缩合反应可以被酸/碱催化,甚至不需要任何催化剂。亚胺的还原目前多采用催化加氢法,在催化剂作用下直接还原为糠胺。该方法绿色环保,是生产糠胺的最佳策略。目前糠醛还原胺化制糠胺多以NH3[9-11]或氨水[12-14]作为氨源,而氨水能更稳定地控制体系中氨的浓度,应用越来越广泛。糠醛还原胺化制糠胺反应过程中存在多个竞争反应,易生成席夫碱、仲胺、高聚物等副产物,此外还存在糠醛加氢副产物和糠胺加氢副产物[15]。为提高糠胺的收率,高性能催化剂起着关键作用。目前用于糠醛还原胺化制糠胺反应的催化剂多为贵金属,如Ru[16]、Rh[17]、Pd[18]和Ir[19]等。然而,贵金属催化剂的稀缺性和高成本限制了其应用。近年来,非贵金属Ni[9]、Co[20]等也被用于催化糠醛还原胺化制糠胺。如Zhuang等[21]制备了石墨烯包覆的Co@C催化剂用于糠醛还原胺化,糠胺的收率为86.2%。本课程组[22-24]前期研究了Raney Ni催化剂,用于糠醛还原胺化制糠胺反应,糠胺的收率达到90%以上。然而,单一的非贵金属催化剂活性和重复使用性较差,为实现高收率的糠胺,通常需要苛刻的反应条件和大量的催化剂。大量研究发现,相对于单金属催化剂,添加第二金属组成双金属催化剂后,两种金属组分间存在的协同作用使得双金属催化剂具有比单金属催化剂更高的活性、选择性和稳定性[25-27]。基于此,本研究以非贵金属Ni为第一金属,添加Pd,采用共浸渍法制备NiPd/SiO2双金属催化剂,探究了该催化剂对糠醛与氨水还原胺化制糠胺的催化性能和构效关系,并优化了反应条件,考察了催化剂的稳定性和普适性。
2 实验部分 2.1 催化剂的制备采用共浸渍法制备了一系列NiPd/SiO2双金属催化剂。Ni(NO3)2 ·6H2O和PdCl2溶解于去离子水中配制成混合溶液后,将SiO2载体加入上述混合溶液中,在室温下搅拌混合均匀,并在室温下浸渍24 h后,在110 ℃干燥10 h,然后在500 ℃煅烧4 h,最后在H2气氛下500 ℃还原3 h得到NiPd/SiO2催化剂。通过改变Ni/Pd摩尔比,制备一系列NiPd(x ∶y)/SiO2催化剂,(x、y比值代表Ni、Pd金属物质的量比值)。催化剂中金属总负载量(质量分数)为5%。采用同样方法制备5%Ni/SiO2和5%Pd/SiO2催化剂作为参比催化剂。
2.2 催化剂表征X射线粉末衍射(XRD)在荷兰PA Nalytical公司的X ′Pert PRO型X射线粉末衍射仪上进行,采用CuKα辐射源(λ=0.154 05 nm),管电流为40 mA,工作电压为40 kV,扫描范围为10°~80°,扫描速率为5(°) ·min-1,步径为0.02°。透射电镜分析(TEM)在Tecnai G2 F30 S-Twin高分辨透射电子显微镜上进行。氢气程序升温还原测试(H2-TPR)在美国麦克仪器公司AutoChem Ⅱ 2910型全自动化学吸附仪上进行。样品用量为100 mg,还原气为H2和N2混合气(H2体积分数为10%~90%),流量为60 mL ·min-1,升温速率为10 ℃ ·min-1,采用热导检测器检测器(TCD)检测还原过程中的耗氢量。
2.3 催化剂评价催化剂评价在25 mL的SLM25微型高压反应釜中进行。将10 mmol糠醛、10 mL溶剂1, 4-二氧六环、0.06 g催化剂、200 μL N-甲基吡咯烷酮、20 mmol氨水(25%~28%)依次加入高压反应釜中,密封反应釜后,用H2吹扫5次,并充H2加压至2.0 MPa,然后加热至反应温度,在1 000 r ·min-1的速度下连续搅拌并保持3 h。反应结束后,将高压釜快速冷却至室温,离心分离反应混合物。固体催化剂用反应溶剂洗涤3次,如有需要可进行下一次循环使用。上层清液采用配有氢火焰离子化检测器(FID)和DB-WAX柱(30 m×0.32 mm×0.25 μm)的气相色谱仪分析,以N-甲基吡咯烷酮为内标物。
糠醛的转化率X和产物的选择性S及收率Y计算方法如式(1)~(3)。
| $ X=\frac{n_a}{n_a+n_b} \times 100 \% $ | (1) |
| $ S=\frac{m_i}{m} \times 100 \% $ | (2) |
| $ Y=X \times S $ | (3) |
式中:na为反应消耗的糠醛物质的量,nb为未反应的糠醛物质的量,mmol;mi为生成特定组分消耗的糠醛的物质的量,m为糠醛转化的总物质的量,mmol。
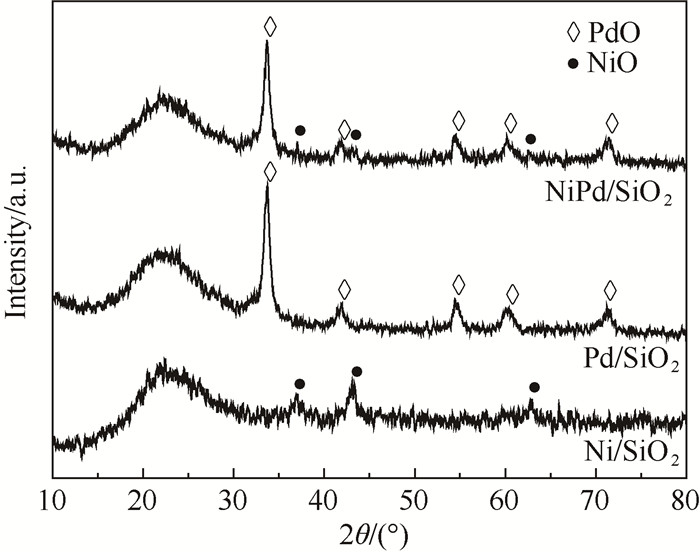
3 结果与讨论 3.1 催化剂表征结果图 1为Ni/SiO2、Pd/SiO2和NiPd/SiO2催化剂还原前样品的XRD表征结果。3种催化剂在2θ=22.5°处均出现SiO2的特征衍射峰。在Ni/SiO2中,2θ为37°、43.1°和62.9°处的峰归属于NiO[28]。Pd/SiO2的XRD图谱中在2θ=33.8°、42°、54.7°、60.12°和71.3°处的峰归属于PdO。在双金属催化剂NiPd/SiO2中,同时存在NiO和PdO的特征衍射峰,与单金属催化剂Ni/SiO2和Pd/SiO2相比,两种物种的衍射峰强度明显降低。通过谢乐方程计算得到Ni/SiO2和NiPd/SiO2中NiO纳米粒子的晶粒尺寸分别为7.3 nm和6.4 nm,Pd/SiO2和NiPd/SiO2中PdO纳米粒子的晶粒尺寸分别为10.5 nm和8.2 nm,表明双金属催化剂表面金属粒径小,分散更好。
|
图 1 不同催化剂前驱体焙烧后的XRD图 Fig.1 XRD patterns of catalyst precursors after calcination |
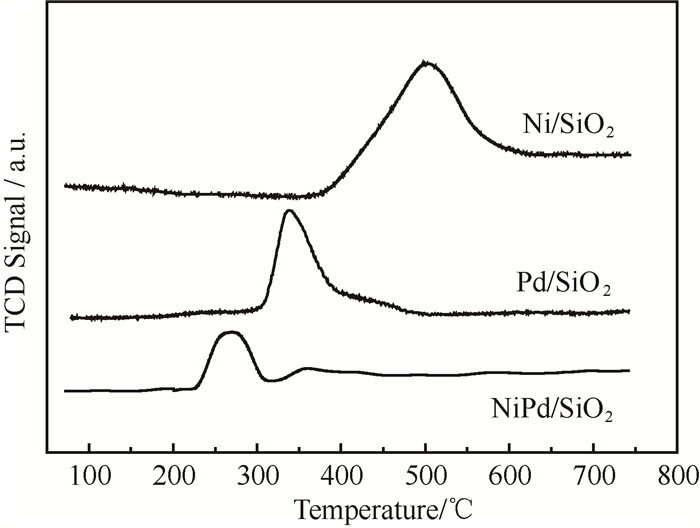
为了考察NiPd/SiO2双金属催化剂的还原性能,对焙烧后的样品进行了H2-TPR表征,并与单金属催化剂Ni/SiO2和Pd/SiO2进行了对比,结果如图 2所示。Ni/SiO2在350~550 ℃温度内有一个还原峰,归因于NiO物种的还原[29]。Pd/SiO2的TPR图中在350 ℃处有一个主还原峰,归因于PdO的还原[30]。值得注意的是,在NiPd/SiO2双金属催化剂的TPR谱图中,在220~300 ℃和300~400 ℃出现两个还原峰,分别对应NiO和PdO的还原。与两种单金属催化剂相比,NiPd/SiO2中NiO和PdO的还原温度均降低,由此可以说明Ni和Pd之间存在相互作用,催化剂中Pd的添加促进了NiO的还原,同时Ni的存在也促进了PdO的还原[31],与文献研究结果一致[32]。
|
图 2 不同催化剂的H2-TPR图谱 Fig.2 H2-TPR profiles of different catalysts |
为更好地了解NiPd/SiO2表面金属的粒径尺寸及其分散情况,对还原后的Pd/SiO2和NiPd/SiO2催化剂进行了TEM表征,结果如图 3所示,图中类球状的黑色粒子为金属纳米粒子。由图 3(a)可见,单金属催化剂Pd/SiO2上Pd纳米粒子的平均粒径为3.88±0.62 nm,图 3(b)中间距为0.227 nm的晶格条纹对应于Pd的(111)晶面。NiPd/SiO2双金属催化剂表面NiPd纳米粒子的平均粒径为3.41±0.67 nm(图 3(c)),在催化剂表面可以看到间距分别为0.202 nm和0.227 nm的晶格条纹(图 3(d)),对应于Ni(111)晶面和Pd(111)晶面[31-33],两种金属粒子紧密靠接在一起形成Ni-Pd混合相[34]。与Pd/SiO2相比,NiPd/SiO2双金属催化剂表面的金属粒径尺寸更小,且分散更均匀,表明双金属催化剂中两种金属共存促进了NiPd金属纳米粒子的分散。这有利于催化剂活性金属比表面积的增大,从而增强催化剂的催化活性。TEM表征结果与上述XRD表征结果相一致。

|
图 3 催化剂Pd/SiO2和NiPd(1 ∶4)/SiO2的TEM图 Fig.3 TEM images of Pd/SiO2 and NiPd(1 ∶4)/SiO2 catalysts |
首先探究了不同Ni/Pd摩尔比的NiPd/SiO2催化剂对糠醛与氨水还原胺化制糠胺反应的影响,结果如表 1所示。从结果可以看出,Ni/Pd摩尔比对NiPd/SiO2催化剂的活性影响较大,虽然各催化剂上糠醛基本都能完全转化,但是糠胺的选择性存在明显差异。单金属催化剂Ni/SiO2的活性很低,目标产物糠胺的选择性只有15.7%,反应物中存在大量席夫碱和其他副产物(呋喃环加氢副产物和未知高聚物)(Entry 1)。催化剂中添加Pd以后,糠胺的选择性明显增大,副产物席夫碱、呋喃环加氢副产物和未知高聚物的含量降低,说明Pd的添加提高了催化剂的活性。此结果表明,NiPd/SiO2双金属催化剂中Ni和Pd之间的协同作用有利于催化剂活性的提高。随着Pd含量增加,糠胺的选择性先增加后降低。其中Ni与Pd摩尔比为1 ∶4时,糠胺的选择性达到最高,为79.2%(Entry 7)。Pd含量进一步增加时,糠胺的选择性开始下降,副产物仲胺的含量明显增加。综合考虑,选择NiPd(1 ∶4)/SiO2进行后续研究。
|
|
表 1 不同Ni/Pd摩尔比的NiPd/SiO2上糠醛还原胺化 Table 1 Reductive amination of furfural with different Ni/Pd molar ratios using NiPd/SiO2 catalysts |
表 2为不同反应温度、氢气压力和催化剂用量等对NiPd(1 ∶4)/SiO2催化剂上糠醛还原胺化反应的影响结果。可以看出,糠醛在70 ℃即完全转化,但是此时体系中主要为席夫碱中间体,表明低温对反应不利。随着温度升高,席夫碱含量降低,糠胺选择性升高,并在130 ℃达到最大值,为91.6%(Entry 4)。进一步升高温度到150 ℃时,糠胺选择性反而大幅度下降,反应产物中出现大量呋喃环加氢副产物和未知聚合物,说明温度过高对糠胺合成不利。因此,130 ℃为最适宜的反应温度。此外,氢气压力对糠醛还原胺化制糠胺反应也有较大影响,在氢压为0.5 MPa时,席夫碱副产物较多,目标产物糠胺选择性仅有26.7%(Entry 6)。随着氢压增大,糠胺的选择性明显提高,在氢压为2 MPa时达到最大(Entry 4)。而继续增大氢压至2.5 MPa,糠胺的选择性下降至34.9%,过度加氢副产物增多(Entry 9),这说明氢压过大会导致呋喃环出现过度加氢现象。综合考虑,选择氢压为2.0 MPa继续后续研究。课题组前期研究发现[22],在还原胺化反应中,反应体系中的NH3会与H2竞争吸附在金属催化剂表面的加氢活性位点,因此催化剂的用量对反应具有较大影响。由表 2可知,随着催化剂用量的增加,糠胺的收率也明显增加(Entry 10~11),说明增加催化剂的量有助于糠醛到糠胺反应的进行,但是当用量继续增大至0.08 g时,糠胺的收率大幅下降,而过度加氢副产物含量增多(Entry 12),这说明催化剂用量过高不利于糠醛还原胺化制糠胺。综合考虑糠胺的选择性及催化剂的经济性,采用0.06 g作为该体系下最佳催化剂用量,此时糠胺选择性高达91.6%(Entry 4)。
|
|
表 2 反应温度、氢气压力和催化剂用量对糠醛还原胺化的影响 Table 2 Effects of reaction temperature, hydrogen pressure and catalyst dosage on reduction amination of furfural |
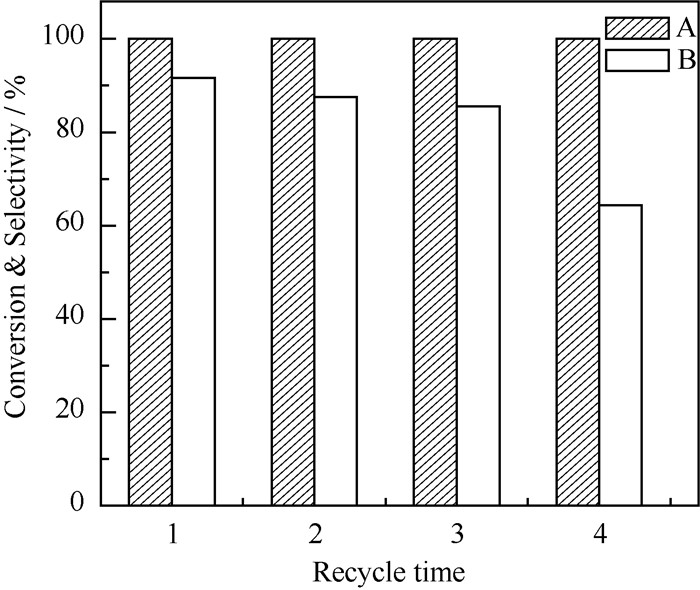
为了探究NiPd/SiO2催化剂在糠醛与氨水还原胺化反应中的稳定性,在130 ℃、2.0 MPa H2、0.06 g催化剂用量条件下,对NiPd(1 ∶4)/SiO2催化体系进行了循环实验研究。如图 4所示,NiPd(1 ∶4)/SiO2催化剂在循环使用两次后仍保留优异的催化性能,糠醛转化率为100%,糠胺选择性>90%。第4次使用时,糠醛转化率仍为100%,糠胺选择性有一定程度降低,收率为64.4%。每次重复操作过程中催化剂损失量约为3.6%。反应中催化剂活性下降的主要原因可能是在其重复使用操作过程中存在一定损失所致,此结果表明,NiPd(1 ∶4)/SiO2催化剂具有良好的稳定性。
|
图 4 NiPd(1 ∶4)/SiO2催化剂重复使用性能 Fig.4 Reusability of the NiPd(1 ∶4)/SiO2 catalyst A: Furfural conversion; B: Furfurylamine selectivity |
为了考察NiPd(1 ∶4)/SiO2催化剂的普适性,对多种醛类化合物与氨水还原胺化制伯胺类化合物进行了拓展性实验,结果如表 3所示。可以发现,在优化反应条件下,苯甲醛、脂肪醛和杂环醛均能与氨水还原胺化得到高收率的对应伯胺,收率在68%~90%。苯甲醛很容易还原胺化得到苄胺,收率高达89.4%。相比之下,脂肪醛还原胺化反应效果略差,随着碳链增加,伯胺的收率略有下降(Entry 2~4),推测其原因可能是空间位阻增加导致。含有取代基的糠醛(5-甲基-2-糠醛和5-羟甲基糠醛)也能够顺利转化为相应的伯胺,收率分别为89.8%和78.3%(Entry 5~6)。上述结果表明,NiPd/SiO2催化剂对催化醛类化合物还原胺化制伯胺反应具有良好的普适性。
|
|
表 3 醛类化合物还原胺化结果 Table 3 Results of the reductive amination of various aldehyde compounds |
采用共浸渍法制备了NiPd/SiO2双金属催化剂,用于糠醛与氨水还原胺化制糠胺。Ni和Pd之间的协同作用有利于活性金属Ni和Pd的还原,并促进了金属纳米粒子在载体表面的分散,进而有利于NiPd/SiO2双金属催化剂活性的提高。优化的催化剂NiPd(1 ∶4)/SiO2在糠醛与氨水还原胺化制糠胺反应中表现出优异的催化性能,在优化的反应条件下,糠醛转化率为100%,糠胺收率为91.6%,催化剂循环使用4次以后仍具有良好的催化性能。此外,该催化剂对多种醛与氨水还原胺化均表现出良好的催化性能。本研究对醛类化合物还原胺化制伯胺的高效催化剂的研发具有重要参考意义。
| [1] |
JI Q H, YU X J, CHEN L, et al. Comprehensive depolymerization of lignin from lignocellulosic biomass: A review[J]. Critical Reviews in Environmental Science and Technology, 2023, 53(21): 1866-1887. DOI:10.1080/10643389.2023.2190314 |
| [2] |
MIKA L T, CSÉFALVAY E, NÉMETH Á. Catalytic conversion of carbohydrates to initial platform chemicals: Chemistry and sustainability[J]. Chemical Reviews, 2018, 118(2): 505-613. DOI:10.1021/acs.chemrev.7b00395 |
| [3] |
XU C, PAONE E, RODRÍGUEZ-PADRÓN D, et al. Recent catalytic routes for the preparation and the upgrading of biomass derived furfural and 5-hydroxymethylfurfural[J]. Chemical Society Reviews, 2020, 49(13): 4273-4306. DOI:10.1039/D0CS00041H |
| [4] |
PENG Y, XU Z W, YU L, et al. Trimetallic Cu-Ni-Re/Hβ catalyst for the direct conversion of furfural to 2-Methyltetrahydrofuran[J]. Chemical Engineering Journal, 2023, 454: 139746. DOI:10.1016/j.cej.2022.139746 |
| [5] |
SAINI K, KUMAR S, LI H, et al. Advances in the catalytic reductive amination of furfural to furfural amine: The momentous role of active metal sites[J]. ChemSusChem, 2022, 15(7): e202200107. DOI:10.1002/cssc.202200107 |
| [6] |
ZOU H T, CHEN J Z. Efficient and selective approach to biomass-based amine by reductive amination of furfural using Ru catalyst[J]. Applied Catalysis B: Environmental, 2022, 309: 121262. DOI:10.1016/j.apcatb.2022.121262 |
| [7] |
PLITTA B, ADAMSKA E, GIEL-PIETRASZUK M, et al. New cytosine derivatives as inhibitors of DNA methylation[J]. European Journal of Medicinal Chemistry, 2012, 55: 243-254. DOI:10.1016/j.ejmech.2012.07.024 |
| [8] |
FROIDEVAUX V, NEGRELL C, CAILLOL S, et al. Biobased amines: From synthesis to polymers; present and future[J]. Chemical Reviews, 2016, 116(22): 14181-14224. DOI:10.1021/acs.chemrev.6b00486 |
| [9] |
SUN R Y, XIAO L F, WU W. In-situ carbon-encapsulated Ni2P@C catalysts for reductive amination of furfural[J]. Molecular Catalysis, 2024, 553: 113710. DOI:10.1016/j.mcat.2023.113710 |
| [10] |
ZHOU K, CHEN B X, ZHOU X T, et al. Selective synthesis of furfurylamine by reductive amination of furfural over Raney cobalt[J]. ChemCatChem, 2019, 11(22): 5562-5569. DOI:10.1002/cctc.201901269 |
| [11] |
YANG Y Z, ZHOU L L, WANG X C, et al. Catalytic reductive amination of furfural to furfurylamine on robust ultra-small Ni nanoparticles[J]. Nano Research, 2023, 16(3): 3719-3729. DOI:10.1007/s12274-022-4923-0 |
| [12] |
CHATTERJEE M, ISHIZAKA T, KAWANAMI H. Reductive amination of furfural to furfurylamine using aqueous ammonia solution and molecular hydrogen: An environmentally friendly approach[J]. Green Chemistry, 2016, 18(2): 487-496. DOI:10.1039/C5GC01352F |
| [13] |
GOKHALE T A, RAUT A B, BHANAGE B M. Comparative account of catalytic activity of Ru- and Ni-based nanocomposites towards reductive amination of biomass derived molecules[J]. Molecular Catalysis, 2021, 510: 111667. DOI:10.1016/j.mcat.2021.111667 |
| [14] |
SHENG M, FUJITA S, YAMAGUCHI S, et al. Single-crystal cobalt phosphide nanorods as a high-performance catalyst for reductive amination of carbonyl compounds[J]. JACS Au, 2021, 1(4): 501-507. DOI:10.1021/jacsau.1c00125 |
| [15] |
WANG H J, ZHANG Y C, LUO D, et al. Active metal dependent side reactions for the reductive amination of furfural[J]. Molecular Catalysis, 2023, 536: 112914. DOI:10.1016/j.mcat.2023.112914 |
| [16] |
DONG C L, WANG H T, DU H C, et al. Ru/HZSM-5 as an efficient and recyclable catalyst for reductive amination of furfural to furfurylamine[J]. Molecular Catalysis, 2020, 482: 110755. DOI:10.1016/j.mcat.2019.110755 |
| [17] |
CHANDRA D, INOUE Y, SASASE M, et al. A high performance catalyst of shape-specific ruthenium nanoparticles for production of primary amines by reductive amination of carbonyl compounds[J]. Chemical Science, 2018, 9(27): 5949-5956. DOI:10.1039/C8SC01197D |
| [18] |
SINGH G, KAISHYOP J, SINGH G, et al. One-Pot direct reductive amination of furfural over Pd@CNTs[J]. Molecular Catalysis, 2023, 535: 112877. DOI:10.1016/j.mcat.2022.112877 |
| [19] |
FENG H S, LIU W, PANG D H, et al. Modulation of coordination environment on atomically dispersed Ir catalysts for highly-efficient reductive amination[J]. Journal of Catalysis, 2023, 428: 115175. DOI:10.1016/j.jcat.2023.115175 |
| [20] |
YOGITA, RAO K T V, KUMAR P M, et al. Cobalt nanoparticles embedded in a nitrogen-doped carbon matrix for reductive amination of biomass-derived furfural to furfurylamine[J]. Sustainable Energy & Fuels, 2022, 6(20): 4692-4705. |
| [21] |
ZHUANG X Z, LIU J G, ZHONG S R, et al. Selective catalysis for the reductive amination of furfural toward furfurylamine by graphene-co-shelled cobalt nanoparticles[J]. Green Chemistry, 2022, 24(1): 271-284. DOI:10.1039/D1GC03578A |
| [22] |
ZHOU K, LIU H Y, SHU H M, et al. A comprehensive study on the reductive amination of 5-hydroxymethylfurfural into 2, 5-bisaminomethylfuran over Raney Ni through DFT calculations[J]. ChemCatChem, 2019, 11(11): 2649-2656. DOI:10.1002/cctc.201900304 |
| [23] |
郭珊珊, 陈娜, 魏作君, 等. Raney Ni催化生物基糠醛还原胺化合成糠胺[J]. 合成化学, 2022, 30(1): 35-41. GUO S S, CHEN N, WEI Z J, et al. Synthesis of furfurylamine by reductive amination of biomass-based furfural over Raney Ni catalyst[J]. Chinese Journal of Synthetic Chemistry, 2022, 30(1): 35-41. |
| [24] |
LIU Y X, ZHOU K, SHU H M, et al. Switchable synthesis of furfurylamine and tetrahydrofurfurylamine from furfuryl alcohol over Raney® nickel[J]. Catalysis Science & Technology, 2017, 7(18): 4129-4135. |
| [25] |
WEI R L, TANG N, JIANG L B, et al. Bimetallic nanoparticles meet polymeric carbon nitride: Fabrications, catalytic applications and perspectives[J]. Coordination Chemistry Reviews, 2022, 462: 214500. DOI:10.1016/j.ccr.2022.214500 |
| [26] |
ZHANG M, YANG J H. Selective hydrogenation of furfural: Pure silica supported metal catalysts[J]. ChemistrySelect, 2022, 7(9): e202200013. DOI:10.1002/slct.202200013 |
| [27] |
VAN DER HOEVEN J E S, JELIC J, OLTHOF L A, et al. Unlocking synergy in bimetallic catalysts by core-shell design[J]. Nature Materials, 2021, 20(9): 1216-1220. DOI:10.1038/s41563-021-00996-3 |
| [28] |
CAGLAR A, COGENLI M S, YURTCAN A B, et al. Effective carbon nanotube supported metal (M=Au, Ag, Co, Mn, Ni, V, Zn) core Pd shell bimetallic anode catalysts for formic acid fuel cells[J]. Renewable Energy, 2020, 150: 78-90. DOI:10.1016/j.renene.2019.12.104 |
| [29] |
SOSZKA E, REIJNEVELD H M, J? DRZEJCZYK M, et al. Chlorine influence on palladium doped nickel catalysts in levulinic acid hydrogenation with formic acid as hydrogen source[J]. ACS Sustainable Chemistry & Engineering, 2018, 6(11): 14607-14613. |
| [30] |
SOSZKA E, J? DRZEJCZYK M, KOCEMBA I, et al. Ni-Pd/γ-Al2O3 catalysts in the hydrogenation of levulinic acid and hydroxymethylfurfural towards value added chemicals[J]. Catalysts, 2020, 10(9): 1026. DOI:10.3390/catal10091026 |
| [31] |
PAN C, GUO Z L, DAI H, et al. Anti-sintering mesoporous Ni-Pd bimetallic catalysts for hydrogen production via dry reforming of methane[J]. International Journal of Hydrogen Energy, 2020, 45(32): 16133-16143. DOI:10.1016/j.ijhydene.2020.04.066 |
| [32] |
DOSTAGIR S K N H M D, AWASTHI M K, KUMAR A, et al. Selective catalysis for room-temperature hydrogenation of biomass-derived compounds over supported NiPd catalysts in water[J]. ACS Sustainable Chemistry & Engineering, 2019, 7(10): 9352-9359. |
| [33] |
WU J B, SHI R P, QIN Z F, et al. Selective oxidation of methanol to methyl formate over bimetallic Au-Pd nanoparticles supported on SiO2[J]. Journal of Fuel Chemistry and Technology, 2019, 47(7): 780-790. |
| [34] |
ISMAGILOV I Z, MATUS E V, KUZNETSOV V V, et al. Hydrogen production by autothermal reforming of methane over NiPd catalysts: Effect of support composition and preparation mode[J]. International Journal of Hydrogen Energy, 2014, 39(36): 20992-21006. |