2. 浙江大学 电化学储能实验室,软弱土与环境土工教育部重点实验室,浙江 杭州 310058
2. Laboratory of Electrochemistry and Energy Storage, MOE Key Laboratory of Soft Soils and Geoenvironmental Engineering, Zhejiang University, Hangzhou 310058, China
碳纤维具有碳材料强抗拉力和纤维柔软可加工性两大特征,是一种力学性能优异的新材料,在国防军工和民用方面均有广泛的应用,2020年其全球产量预计将从2015年的58000吨增长到100000吨[1]。目前碳纤维丝的主要生产工艺是以聚丙烯腈纤维为原料,经预氧化和高温碳化反应制备而得。然而聚丙烯腈分子含有26.4%氮元素,在预氧化和碳化过程中将产生含有氰化氢、氨气、腈类有机化合物的废气,是一种典型的有组织排放的含氰废气[2~4]。当高温废气降温后,废气中大分子的腈类有机物将会和其它大分子有机物以焦油形式冷凝析出附着在管道或下游设备上,造成堵塞和设备腐蚀问题,而不凝性气体含有HCN、NH3等。另外,随着我国经济的快速发展,含有腈类有机物的废气(以下称含氰废气)也逐年增加。我国制定的《国家中长期科学和技术发展规划纲要(2006~2020年)》优先主题中的“综合治污与废弃物循环利用”,特别强调了“开发非常规污染物控制技术”。
目前,工业上最常用的碳纤维尾气处理方法是燃烧法,包括直接燃烧法和催化燃烧法[4~6]。直接燃烧法工艺简单,高温废气通过直接引燃或者添加煤气辅助燃烧,将其中的有机物和HCN充分燃烧氧化。但该方法也存在燃烧温度高、产生大量NOx的缺点,后处理压力大。催化燃烧法可以降低燃烧反应的温度,文献中对于该方法的报道也局限于小分子的HCN、CH3CN和C2H3CN的催化燃烧[7, 8],常采用贵金属和过度金属为催化剂,该过程也需要严格控制氧气通入的比例以达到最佳的反应效果。
针对燃烧法的一些不足,拟尝试蒸汽催化裂解的方案进行含氰废气的处理。蒸汽裂解的氧化性较弱,可以有效避免含氮物质的深度氧化,产生NOx而导致二次污染,同时也可以避免燃烧法氧气通入带来的爆炸风险。白云石是一种天然矿石材料,主要化学成分是钙和镁的碳酸盐,经过700~900℃煅烧以后,形成了具有焦油裂解活性的CaO-MgO的复合物[9],常用于催化生物质或煤焦油裂解,如原位添加到粒料中一起裂解消除焦油,也有用于高温裂解炉后焦油的进一步处理[10~12]。煅烧后白云石具有比较好的焦油消除效果,但所需的裂解反应温度通常在700℃以上[13, 14]。当白云石颗粒负载金属镍制备Ni/白云石催化剂,其催化性能会有很大的提升[15, 16]。Sato等[17]制备了WO3改性的Ni/WO3/白云石催化剂,并用于催化含有H2S的焦油模型化合物萘的蒸汽重整,在反应温度800~850℃时,萘的转化率可达到90%以上,且在100 h的稳定性测试中有着稳定的催化活性。
碳纤维生产中产生的焦油成分非常复杂,除了含有氰基的链状、环状化合物外,还含有氰基芳环类衍生物[3]。本文针对稳定性好的氰基芳环类衍生物的蒸汽裂解,选用苯甲腈为氰基基团的模型化合物,并以白云石为载体制备了负载型镍催化剂,研究镍催化剂催化苯甲腈蒸汽裂解的催化活性,并考察了富电子体的稀土金属氧化物CeO2改性和不同温度、水碳比、空时对苯甲腈蒸汽催化裂解反应的影响。
2 实验部分 2.1 试剂六水硝酸镍、六水硝酸铈、氧化钙、氧化镁、尿素:分析纯(国药集团化学试剂有限公司);苯甲腈:分析纯(成都科龙化工试剂厂);白云石:白云石的成分分析见表 1(行唐县鑫磊矿物粉体厂)。
|
|
表 1 白云石的成分分析 Table 1 Chemical properties of the as-received dolomite |
镍基白云石催化剂采用化学沉淀法制备。首先将天然的白云石材料研磨成细粉,放到马弗炉内,在空气氛850℃下煅烧4 h,得到预处理好的白云石粉末。白云石负载金属Ni催化剂的制备方法如下:配制0.5 mol·L-1的Ni(NO3)2·6H2O和3 mol·L-1的尿素混合溶液,与一定量的煅烧好的白云石粉末一起放入圆底烧瓶中混合。将此烧瓶放入油浴锅中,在115℃温度下,搅拌回流2.5 h。沉淀好以后的混合物经过夜老化后,过滤,少量去离子水洗涤。把滤饼放在烘箱中105℃下干燥3 h。再把干燥好的滤饼研成粉末,800℃下空气氛中煅烧4 h,得到镍基白云石粉末催化剂。
CeO2改性的Ni/CeO2/白云石催化剂的制备方法与Ni/白云石催化剂类似。在催化剂前驱液中,增加0.5 mol·L-1的Ce(NO3)2·6H2O溶液组分,加入煅烧后的白云石粉末中。其它操作同Ni/白云石催化剂的合成过程一致。Ni/CaO和Ni/MgO催化剂的制备方法与Ni/白云石的制备方法相同。得到的催化剂粉末经过压片成型,再破碎筛分成20~40目的颗粒大小,供催化性能评价实验使用。本文所制备的镍基催化剂的金属镍的质量含量均控制在15%。
2.3 催化剂表征方法采用美国Thermo Fisher公司的ARLADVANT’ X IntelliPowerTM 4200 X射线荧光光谱仪(XRF),对天然矿石白云石的成分做了分析(如表 1所示)。实验用荷兰PANalytical B.V.的EmpyreanX射线衍射仪(XRD),在加速电压40 kV、电流40 mA条件下进行XRD表征,进行有关物相结构的分析。H2-TPR分析是在美国Micromeritics仪器有限公司AutoChem2920全自动化学吸附仪上进行,采用热导池检测器(TCD)检测H2浓度的变化。称取质量约0.05 g的催化剂样品,以30 mL·min-1的流速持续通入10% H2/Ar混合气进行H2程序升温还原,升温速率控制在10℃·min-1,直到900℃。记录程序升温过程中H2浓度变化的曲线,即可得到H2-TPR曲线。催化剂比表面积分析是采用美国Quantachrome公司Autosorb-IQ-C-TCD进行N2吸附脱附测试,并以BET方法计算比表面积。
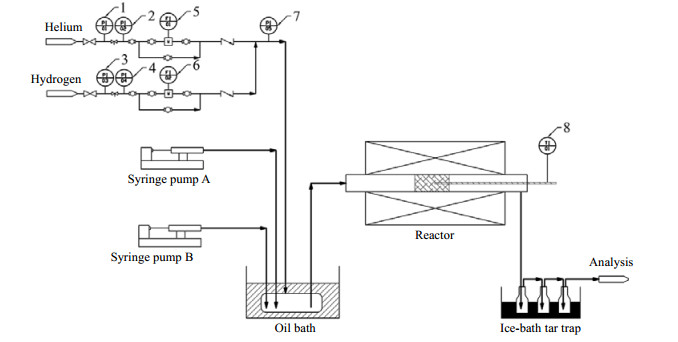
2.4 催化剂性能评价模型化合物苯甲腈的蒸汽催化裂解反应的实验装置如图 1所示。该装置由气体进料控制、液体进料控制、汽化器、反应器和产品分离收集部分组成。各气路的气体流速由质量流量计控制(D07-11C,北京七星华创电子股份有限公司)。液体进料速度是由注射泵(LSP01-1A,保定兰格恒流泵有限公司)进行控制。反应在石英管固定床反应器中进行,石英反应管内径和长度分别是8 mm和250 mm,反应管放置在高温管式炉(LTKC-05-12,杭州蓝天化验仪器厂)中,反应温度由温度控制器控制,并用K型测温热电偶进行恒温区的判定以及管式炉控温的修正。200 mg的20~40目的催化剂与600 mg相同颗粒大小的石英砂混合均匀后填充在反应管内,在催化剂床层的两端各增加5 mm高度的20~40目的石英砂,两侧再由石英棉进行固定。反应实验前,催化剂先用15% H2/N2进行还原活化,气体流量40 mL·min-1,以10℃·min-1的升温速率升到650℃,恒温60 min。活化操作完成以后,打开氦气气路,将整个反应体系吹扫成氦气氛围。将油浴汽化器的温度设定到160℃,反应器的温度设定到所需的反应温度,反应器前后的管线开启伴热带加热保温。温度稳定以后,氦气的流量控制在60 mL·min-1,苯甲腈的流速控制在1.5 μL·min-1,水的流速控制在3.0 μL·min-1,开始进行催化剂评价实验。
|
图 1 模型化合物蒸汽裂解实验装置 Fig.1 Schematic diagram of the steam cracking of model compounds 1, 2, 3, 4, 7. pressure 5, 6. flow rate 8. temperature |
经冷凝分离后出口气体中的H2、N2、CO、CH4、CO2的浓度由配有热导池(TCD)检测器的气相色谱(GC-TCD,GC-9790,浙江福立分析仪器有限公司)检测,色谱柱为TDX-01填充柱;反应尾气中的HCN浓度由配有氮磷检测器(NPD)的气相色谱(GC-NPD,GC-9790,浙江福立分析仪器有限公司)进行检测,色谱柱为AT SE-54毛细管柱。反应尾气中的NH3浓度测定是将气体中的NH3经过水吸收以后,根据国标HJ535-2009采用纳氏试剂分光光度法,在分光光度计(L5,上海棱光技术有限公司)上测定吸收液中NH4+-N的浓度。
实验中苯甲腈的转化率由出口中含碳气体产物(CO,CO2,CH4,HCN)的摩尔数除以进料中碳的摩尔数计算,见式(1)。
| $ {X_{{\rm{Benzonitrile}}}}(\% ) = \frac{{({n_{{\rm{CO - out}}}} + {n_{{\rm{C}}{{\rm{O}}_{\rm{2}}}{\rm{ - out}}}} + {n_{{\rm{C}}{{\rm{H}}_{\rm{4}}}{\rm{ - out}}}} + {n_{{\rm{HCN - out}}}}) \times 100}}{{(7 \times {n_{{\rm{Benzonitrile - in}}}})}} $ | (1) |
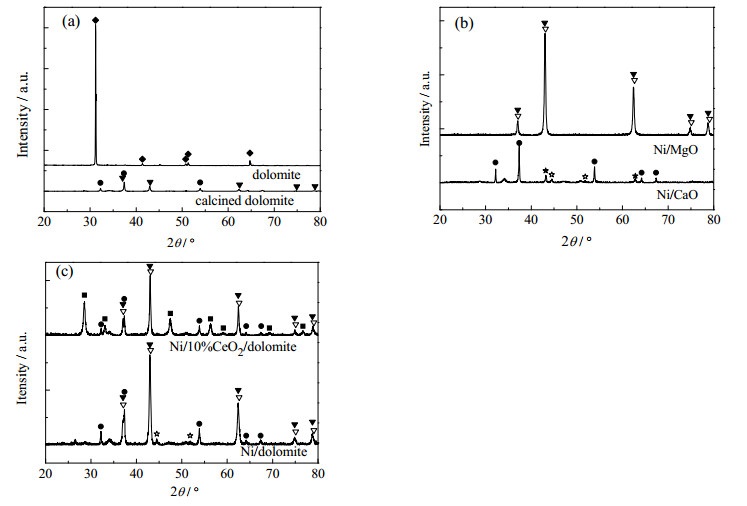
对煅烧处理前后白云石,还原后Ni/MgO、Ni/CaO、Ni/白云石、Ni/10%CeO2/白云石进行了XRD表征分析,如图 2所示。煅烧处理前后的白云石结构发生了很大的变化,处理前是钙镁碳酸盐结构的晶体,煅烧后碳酸盐相发生分解形成了CaO和MgO的复合物(图 2(a))。还原活化后的Ni/CaO催化剂的XRD图有CaO、NiO和还原态金属镍Ni峰(图 2(b)),说明在此实验的还原条件下,Ni/CaO中部分NiO得到了还原,但未被彻底还原。Ni/MgO经还原活化后的谱图中有MgO或者(Ni,Mg)O峰,而没有明显的金属镍峰,(Ni,Mg)O峰与镍镁固溶体相标准卡片(JCPDS No.34-0410)基本一致,说明Ni与氧化镁载体形成了难以还原的固溶体(Ni,Mg)O[18],或只有少量的高分散性的Ni得到了还原,但未能被XRD检测到。在Ni/白云石催化剂中,除了白云石载体中CaO、MgO、(Ni,Mg)O的峰外,也出现了还原态的金属镍峰(图 2(c))。而在CeO2改性的Ni/10%CeO2/白云石催化剂中,增加了CeO2的峰,但未发现还原态金属镍峰,说明CeO2的掺杂增强了金属镍在催化剂表面的分散度或者促进了固溶体(Ni,Mg)O的生成。
|
图 2 白云石(a),还原后的Ni/MgO、Ni/CaO(b)和还原后的Ni/白云石(c)、Ni/10%CeO2/白云石的XRD图 Fig.2 XRD spectra of dolomite (a), reduced Ni/MgO, Ni/CaO (b)and reduced Ni/dolomite, Ni/10%CeO2/dolomite(c) ◆ dolomite ●CaO ▼ MgO ■ CeO2 ▽ (Ni, Mg)O ☆ Ni ★NiO |
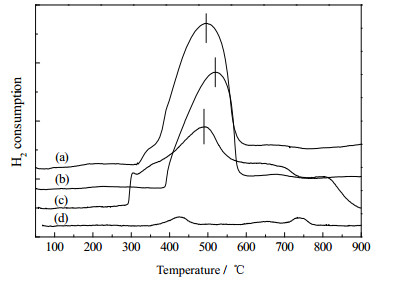
H2-TPR表征了还原前各催化剂NiO/MgO、NiO/CaO、NiO/白云石、NiO/10%CeO2/白云石的还原性能,结果见图 3。NiO/MgO的还原峰很小,且只在350~450℃和700~770℃有还原峰出现,低温区的还原峰是未与MgO形成固溶体的表层NiO的还原峰,而高温还原峰则是(Ni,Mg)O固溶体中能够被还原的NiO峰,更多的固溶体相中的NiO与MgO结合得非常稳定,难以被还原[18]。NiO/CaO的还原峰是一个很宽的峰,峰的区间从300℃一直延续到900℃,说明NiO/CaO催化剂中的金属镍分布并不均匀,颗粒大小不一,较小颗粒的NiO或者大颗粒的外层NiO则较易被还原,而大颗粒深层的NiO则较难被还原。NiO/白云石在低温还原区间(300~400℃)出现了一个肩峰,该峰可归结为催化剂表面未与载体发生相互作用呈自由态NiO还原峰[19],而在400~600℃的主还原峰区域可以归结为NiO与载体之间发生了相互作用,导致还原峰往高温方向移动。CeO2改性以后的Ni/10%CeO2/白云石催化剂只有一个主要的还原峰,且峰值向更高的温度偏移,说明CeO2的掺杂使得金属镍在催化剂的表面分散更加均匀,并加强了金属镍与载体的相互作用。而这种高分散,结构稳定的活性中心,通常有利于催化剂活性和稳定性的提升[19, 20]。
|
图 3 NiO/白云石(a),NiO/10%CeO2/白云石(b),NiO/CaO (c)和NiO/MgO (d)的H2-TPR图 Fig.3 H2-TPR profiles of NiO/dolomite(a) NiO/10%CeO2/dolomite (b), NiO/CaO (c)and NiO/MgO (d) (heating rate: 10℃·min-1, from room temperature to 900℃; 10% H2/Ar: 30 mL·min-1) |
表 2为不同镍基催化剂样品的比表面积、孔径和孔容数据。从表中可以看出,Ni/CaO的比表面积比Ni/MgO的要大(79.5 vs 52.2 m2·g-1),孔径和孔容则相反。Ni/白云石催化剂的比表面积为65.0 m2·g-1,介于Ni/CaO和Ni/MgO之间,经CeO2改性后的Ni/CeO2/白云石催化剂的比表面积有所下降,为47.8 m2·g-1。以白云石基的CaO-MgO复合物为载体的催化剂孔径都介于Ni/CaO和Ni/MgO之间,孔容都在减小。
|
|
表 2 催化剂的比表面积、孔径和孔容数据 Table 2 Surface area, pore size and pore volume of catalysts |
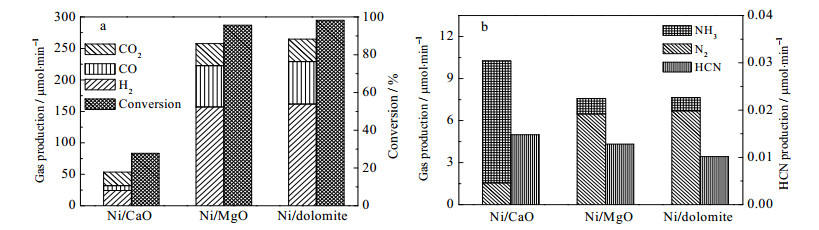
由于煅烧后白云石的主要成分是CaO-MgO,为了探究白云石作为载体的特性,首先对比研究了CaO、MgO、白云石分别作为载体时的催化性能。在蒸汽催化裂解温度为650℃时,不同载体负载镍对苯甲腈的催化转化性能和最终产品分布的实验结果见图 4。三种催化剂对于苯甲腈的转化活性由高到低的顺序为:Ni/白云石,Ni/MgO,Ni/CaO。MgO作为载体的催化活性与白云石比较接近,均远高于CaO载体的催化活性。此反应条件下,蒸汽催化裂解的最终产品有H2、N2、CO、CO2、HCN和NH3。从最终的产品分布上来看,活性最高的Ni/白云石催化剂产生的小分子气体H2、CO和CO2量最多。而含氮的产品中,Ni/白云石催化剂对于NH3和HCN的转化效果最佳,相应的产生的N2量也最多。从不同载体的对比研究可以看出,白云石中的MgO起到了良好的催化剂载体的作用,而当中的CaO并不是一种优良的载体,但可以强化吸附反应物中的水分,增大催化剂表面吸附水的浓度,从而对提升催化效果有一定的协同作用。
|
图 4 不同催化剂的催化性能对比 Fig.4 Comparison of catalytic performance between catalysts with different supporters (benzonitrile: 1.5 μL·min-1; H2O: 3 μL·min-1; He: 60 mL·min-1; catalyst amount: 0.2 g; reaction temperature: 650℃) |
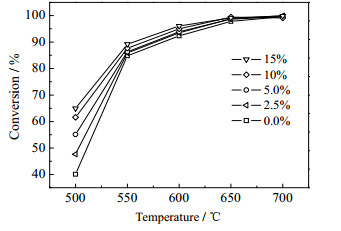
苯甲腈蒸汽催化裂解反应,需要水中的氧参与。催化剂对水的吸附、解离以及氧的顺畅传递,对于反应的稳定高效进行起到至关重要的作用。如果参与反应的氧不能及时且足够数量地传递到苯甲腈解离的物种附近参与反应,那么催化剂表面很容易产生积碳导致活性下降。CeO2是一种富电子体的稀土氧化物,它的掺杂有益于催化剂表面氧的流动性的提升,可以起到抑制积炭增长,促进反应进行的作用[21, 22]。不同CeO2添加量对于Ni/白云石催化剂在500~700℃下,催化苯甲腈蒸汽裂解的活性影响见图 5。从图中可以看出,不同催化剂体系,苯甲腈的转化率都随着反应温度和CeO2掺杂量的提高而增大。在考察的温度区间范围内,CeO2的掺杂在较高反应温条件下(650℃以上)影响并不明显,在较低反应温度条件下(550℃以下)影响较大。在反应温度为500℃时,CeO2的掺杂量从0增加到10%时,苯甲腈的转化率增加了21.1%,CeO2的掺杂量进一步增加到15%时,苯甲腈转化率仅增加了3.7%。所以,当CeO2掺杂量过高,带来的活性提升的效率会变低。后面的实验将采用Ni/10%CeO2/白云石作为催化剂,探究不同的反应条件的影响。
|
图 5 不同温度下CeO2掺杂量对催化性能的影响 Fig.5 Effects of CeO2 doping amounts on catalytic performance at different temperatures (benzonitrile: 1.5 μL·min-1; H2O: 3 μL·min-1; He: 60 mL·min-1; catalyst amount: 0.2 g) |
在500和650℃两个不同反应温度条件下,不同CeO2掺杂量对苯甲腈蒸汽催化裂解反应最终产品产率的影响的实验结果见图 6。在650℃的反应条件下,CeO2掺杂量对最终产品产率的影响较小,H2和NH3的产量会随着CeO2掺杂量的增加有减小的趋势,其它气体产品产率的变化均不大。H2产率的减小是由于CeO2在催化剂中含量的提升,表面氧的流动性增强,高温下容易与H物种化合反应而产生水[23]。在500℃的反应条件下,CeO2掺杂对苯甲腈的转化率有很大影响,最终产品产率的变化也较大,各气体产品的产率都随着CeO2掺杂量的增加而提升。从图中也可以看出,提升温度可以明显增加气体H2、CO、CO2和N2的产率,同时减少了有毒气体HCN和NH3的产率。

|
图 6 不同温度下CeO2掺杂量对催化反应最终产品产率的影响 Fig.6 Effects of CeO2 doping amounts on final product yields at 500 and 650℃ (benzonitrile: 1.5 μL·min-1; H2O: 3 μL·min-1; He: 60 mL·min-1; catalyst amount: 0.2 g) |
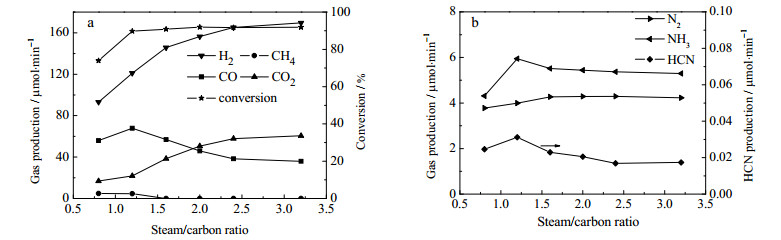
水碳比对于苯甲腈蒸汽催化裂解反应也会产生重要的影响。本实验是在570℃的反应条件下,通过调整进水流量,调节水碳比的比例在0.8~3.2范围内变化,研究苯甲腈的转化率和各气体产品分布的变化情况,实验结果见图 7。在水碳比大于1.2时候,苯甲腈的转化率稳定在91.5%左右。只有水碳比降到0.8时,转化率开始发生明显下降,原因可能是由于催化剂表面的活性中心被苯甲腈的裂解中间体覆盖,而中间体来不及与水反应,导致活性下降。这与文献中甲苯、苯的蒸汽裂解反应的结果类似[24, 25],高水碳比时,转化率并不受水蒸气量的影响,较低的水碳比,催化剂表面容易积炭而失活。苯甲腈蒸汽催化裂解最终的产品分布在水碳比大于2.4的时候,产品组成没有发生明显的变化。在水碳比降到2.4以下时,H2和CO2的产量均随着水碳比的降低而下降,CO的产量在水碳比为1.2时达到一个高点。在水碳比降到1.2时CH4被检测出,并随着水碳比的降低而增加。含氮的产品中,水碳比低于1.6时,N2的产率在呈现下降的趋势,而HCN和NH3的产率在水碳比为1.2时出现了一个高点,这可能是由于低水碳比中,催化剂活性中心被吸附的含碳中间体占据,而含碳中间体不能立刻与水蒸气发生反应,活性中心不能及时暴露出来导致催化效率在下降,影响了NH3和HCN的二次分解反应。
|
图 7 水碳比对催化反应的影响 Fig.7 Effects of the S/C ratio on catalytic performance (benzonitrile: 1.5 μL·min-1; He: 60 mL·min-1; Ni/10%CeO2/dolomite: 0.2 g; reaction temperature:570℃) |
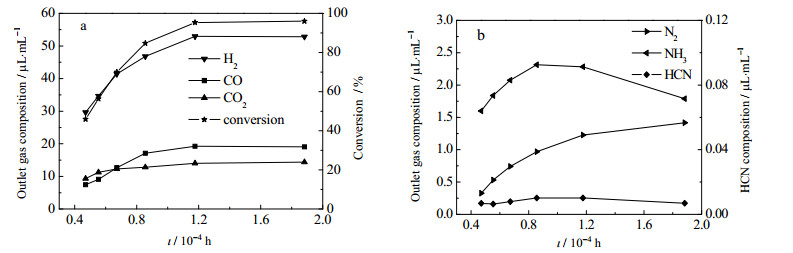
通过改变进料的流率,保持进料组成和催化剂15Ni/10%CeO2/白云石的用量不变,来考察不同空时条件下,苯甲腈在570℃蒸汽催化裂解反应的情况,实验结果见图 8。随着空时的增加,苯甲腈的转化率在增大,相应的H2、CO、CO2和N2在出口气体中的浓度都在变大。HCN和NH3的浓度趋势呈现出了一个峰形,在空时为8.6×10-5 h时,浓度出现了一个极大值。由此说明,NH3和HCN的二次分解反应需要较长的停留时间。当空时超过8.6×10-5 h,转化率的降低带来的HCN和NH3的减少效应更加明显,所以最终产品中NH3和HCN的浓度也在下降。
|
图 8 空时对反应的影响 Fig.8 Effects of space time on catalytic performance (S/C: 1.6; Ni/10%CeO2/dolomite: 0.2 g; reaction temperature: 570℃) |
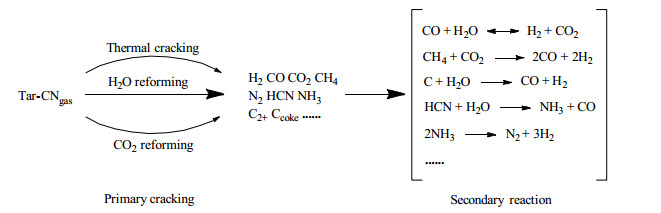
苯甲腈蒸汽催化裂解是一个复杂的反应过程,其反应历程解析如图 9所示。首先苯甲腈会发生初次裂解反应,包含了水蒸气重整反应,热裂解反应以及二氧化碳重整反应,产生了一些小分子的气体产物如H2、CO、CO2、N2、HCN、NH3、C2+以及焦炭(Ccoke)等。这些小分子的气体产物也会发生一系列的二次反应,如CO水汽变换反应,CH4和CO2重整反应、Ccoke和H2O的气化反应、HCN水解反应、NH3分解反应等。在不同的反应条件下,各反应进行的程度会不一样,从而影响到最终产物的分布。
|
图 9 苯甲腈蒸汽催化裂解反应历程图示 Fig.9 Reaction processes of catalyzed steam cracking of benzonitrile |
(1) 白云石中的MgO可在催化剂Ni/白云石中形成了稳定的(Ni,Mg)O固溶体相,是一种良好的载体成分。而白云石中的CaO可以改善催化剂的还原性能,在苯甲腈的蒸汽催化裂解中,提升了转化效率。
(2) CeO2的改性,促进了金属镍在催化剂表面的分散,加强了镍与载体的相互作用,特别是提升了催化剂的低温催化活性。10%的CeO2的掺杂量表现出了一个较高的改性效率。
(3) 较高的水碳比对苯甲腈的转化率和产品分布没有明显影响,较低的水碳比则会影响明显。提升反应的温度和空时有利于苯甲腈转化率的提升,同时抑制了HCN和NH3的生成。
| [1] | Newcomb B A. Processing, structure, and properties of carbon fibers[J]. Composites Part a-Applied Science and Manufacturing , 2016, 91: 262-282. DOI:10.1016/j.compositesa.2016.10.018. |
| [2] | Frank E, Hermanutz F, Buchmeiser M R. Carbon fibers:precursors, manufacturing, and properties[J]. Macromolecular Materials and Engineering , 2012, 297(6): 493-501. DOI:10.1002/mame.v297.6. |
| [3] | WANG Hua(王华), PENG Wei-dong(彭卫东), SHI Lei(石磊), et al. The characteristics and removal method of PAN base carbon fiber carbonization tar(PAN基碳纤维碳化焦油的特性及其脱除方法)[J]. Hi-Tech Fiber & Application(高科技纤维与应用) , 2016, 41(4): 16-19. |
| [4] | LIU Li-hua(刘礼华), JI Chun-xiao(季春晓). Removal of HCN-containing exhaust gases generated from production of PAN-based carbon fibers(聚丙烯腈基碳纤维生产中氰化氢废气的脱除方法)[J]. Technology & Economics in Petrochemicals(石油化工技术与经济) , 2011, 47(1): 41-45. |
| [5] | Zhang F, Li K, Lu C, et al. Removal methods of hydrogen cyanide[J]. New Carbon Materials , 2003, 18(2): 151-157. |
| [6] | Lei J, Wang X, Zhang Q, et al. Application research of HCN removal technology in industrial waste gases[J]. Natural Gas Chemical Industry , 2016, 41(3): 82-85. |
| [7] | Zhang R, Liu N, Lei Z, et al. Selective transformation of various nitrogen-containing exhaust gases toward N2 over zeolite catalysts[J]. Chemical reviews , 2016, 116(6): 3658-721. DOI:10.1021/acs.chemrev.5b00474. |
| [8] | SHI Dong-jun (史东军). Study on selectivity catalytic combustion of containing cyanide wastes gases with mesoporous/microporous zeolites and its industrial application (介孔/微孔分子筛选择催化燃烧含氰废气研究及其工业应用) [D]. Beijing (北京): Beijing University of Chemical Technology (北京化工大学), 2016. http://cdmd.cnki.com.cn/Article/CDMD-10010-1016322495.htm |
| [9] | Gunasekaran S, Anbalagan G. Thermal decomposition of natural dolomite[J]. Bulletin of Materials Science , 2007, 30(4): 339-344. DOI:10.1007/s12034-007-0056-z. |
| [10] | Corujo A, Yermán L, Arizaga B, et al. Improved yield parameters in catalytic steam gasification of forestry residue; optimizing biomass feed rate and catalyst type[J]. Biomass and Bioenergy , 2010, 34(12): 1695-1702. DOI:10.1016/j.biombioe.2010.06.010. |
| [11] | Pinto F, Lopes H, André R N, et al. Effect of catalysts in the quality of syngas and by-products obtained by co-gasification of coal and wastes. 1. tars and nitrogen compounds abatement[J]. Fuel , 2007, 86(14): 2052-2063. DOI:10.1016/j.fuel.2007.01.019. |
| [12] | LUO Zhong-yang(骆仲泱), ZHANG Xiao-dong(张晓东), ZHOU Jin-song(周劲松), et al. Experimental study on catalytic and thermal cracking of tar from biomass pyrolysis(生物质热解焦油的热裂解与催化裂解)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报) , 2004, 18(2): 162-167. |
| [13] | Roche E, de Andrés J M, Narros A, et al. Air and air-steam gasification of sewage sludge. The influence of dolomite and throughput in tar production and composition[J]. Fuel , 2014, 115: 54-61. DOI:10.1016/j.fuel.2013.07.003. |
| [14] | Berrueco C, Montané D, Matas Güell B, et al. Effect of temperature and dolomite on tar formation during gasification of torrefied biomass in a pressurized fluidized bed[J]. Energy , 2014, 66: 849-859. DOI:10.1016/j.energy.2013.12.035. |
| [15] | Wang T J, Chang J, Wu C Z, et al. The steam reforming of naphthalene over a nickel-dolomite cracking catalyst[J]. Biomass and Bioenergy , 2005, 28(5): 508-514. DOI:10.1016/j.biombioe.2004.11.006. |
| [16] | Elbaba I F, Williams P T. High yield hydrogen from the pyrolysis-catalytic gasification of waste tyres with a nickel/dolomite catalyst[J]. Fuel , 2013, 106: 528-536. DOI:10.1016/j.fuel.2012.12.067. |
| [17] | Sato K, Fujimoto K. Development of new nickel based catalyst for tar reforming with superior resistance to sulfur poisoning and coking in biomass gasification[J]. Catalysis Communications , 2007, 8(11): 1697-1701. DOI:10.1016/j.catcom.2007.01.028. |
| [18] | Furusawa T, Tsutsumi A. Comparison of Co/MgO and Ni/MgO catalysts for the steam reforming of naphthalene as a model compound of tar derived from biomass gasification[J]. Applied Catalysis A:General , 2005, 278(2): 207-212. DOI:10.1016/j.apcata.2004.09.035. |
| [19] | Baidya T, Cattolica R J. Improved catalytic performance of CaO and CeO2 promoted Ni catalyst on gasifier bed material for tar removal from producer gas[J]. Applied Catalysis A:General , 2015, 498: 150-158. DOI:10.1016/j.apcata.2015.03.038. |
| [20] | Hou Z, Yashima T. Meso-porous Ni/Mg/Al catalysts for methane reforming with CO2[J]. Applied Catalysis A:General , 2004, 261(2): 205-209. DOI:10.1016/j.apcata.2003.11.002. |
| [21] | McCabe R W, Trovarelli A. Forty years of catalysis by ceria:a success story[J]. Applied Catalysis B:Environmental , 2016, 197: 1-1. DOI:10.1016/j.apcatb.2016.04.044. |
| [22] | Liu Z, Senanayake S D, Rodriguez J A. Elucidating the interaction between Ni and CeOx in ethanol steam reforming catalysts:a perspective of recent studies over model and powder systems[J]. Applied Catalysis B:Environmental , 2016, 197: 184-197. DOI:10.1016/j.apcatb.2016.03.013. |
| [23] | Inaba M, Murata K, Saito M, et al. Hydrogen production by gasification of cellulose over Ni catalysts supported on zeolites[J]. Energy & Fuels , 2006, 20(2): 432-438. |
| [24] | Swierczynski D, Courson C, Kiennemann A. Study of steam reforming of toluene used as model compound of tar produced by biomass gasification[J]. Chemical Engineering and Processing:Process Intensification , 2008, 47(3): 508-513. DOI:10.1016/j.cep.2007.01.012. |
| [25] | Kaisalo N, Simell P, Lehtonen J. Benzene steam reforming kinetics in biomass gasification gas cleaning[J]. Fuel , 2016, 182: 696-703. DOI:10.1016/j.fuel.2016.06.042. |




