流感是一种常见的由流感病毒引起的急性呼吸道传染病[1]。历史上曾多次发生流感大流行,如1918年发生的西班牙流感[2],1957年爆发的亚洲流感[3]和1968年出现的香港流感[4]。自1997年香港特区发现全球首例人感染高致病性H5N1禽流感病例以来,H5N1禽流感已在全球蔓延[5]。近年来人们普遍认为,由禽流感病毒引起的新流感大流行的出现只是一个时间问题[6]。接种疫苗是现阶段最为有效的预防禽流感的手段。目前禽流感疫苗主要由鸡胚工艺生产,但此工艺存在效价偏低,产能低下,质量不稳定[7]等问题。随着动物细胞培养技术的成熟,采用基于动物细胞培养技术生产禽流感疫苗的工艺以其安全性、高产能等优势,逐渐成为替代鸡胚工艺的不二选择。其中犬肾脏上皮细胞(Madin-Darby canine kidney cell, MDCK)由于表达的唾液酸转移酶水平高,利于病毒的特异性识别,故被视为最适宜用于生产禽流感疫苗的细胞之一[8]。
目前大规模培养MDCK细胞需要微载体等支持细胞贴附的基质。此种工艺成本较高且不利于后期纯化[9],因此近年来人们开始尝试利用悬浮培养的MDCK细胞生产病毒疫苗。基于MDCK细胞无血清悬浮培养生产病毒疫苗的工艺不仅能避免微载体工艺后期纯化问题,还具有操作简单,成本低廉等优点。黄锭等[10]的研究发现无血清悬浮培养体系中MDCK细胞所能达到的最大细胞密度约为5×106 cells·mL-1,是原有微载体工艺的5倍,且前者接种H1N1病毒后所获得的病毒HA滴度比后者高出约4个HA单位。
在利用MDCK细胞生产病毒疫苗过程中有诸多关键因素影响病毒HA滴度,如病毒收获时间[11]、感染复数[12]、接毒时的细胞密度[13]、培养温度[14]和TPCK-胰酶浓度[15]等。然而目前的工艺条件研究仅停留在单因素实验层面,并未对因素之间可能具有的交互作用进行探讨。
响应面是一种能考察多变量之间交互作用的统计方法,在工艺优化领域被广泛使用[16-17]本文尝试利用经过本实验室训化可进行无血清培养的MDCK细胞生产禽流感疫苗。首先通过部分析因实验筛选出对病毒HA滴度有显著影响的因素,然后利用响应面分析考察各因素之间的交互作用,对利用MDCK细胞生产禽流感疫苗过程中的多种参数进行了优化。其结果为禽流感疫苗的高效大规模工业化生产提供数据支持。
2 材料与方法 2.1 材料 2.1.1 细胞株本文所使用细胞株为犬肾上皮连续细胞系细胞,购自美国菌种保藏中心(ATCC)。由本实验室驯化成无血清悬浮细胞。
2.1.2 培养基用于悬浮培养细胞的无血清培养基SFM-001,购自上海倍谙基生物科技有限公司。
2.1.3 毒株本文所使用病毒株为H5亚型禽流感病毒株,由合作企业提供。
2.2 方法 2.2.1 细胞悬浮培养将MDCK细胞以1.0×106 cells·mL-1的接种密度接种于125 mL摇瓶中,装液量为30 mL。置于转速为130 r·min-1、37 ℃、5% CO2的培养摇床中进行。
2.2.2 细胞计数取样后以体积分数φ = 0.4%台盼蓝染色,用血球计数板计数。
2.2.3 病毒HA滴度的测定96孔微量反应板每孔各添加25 μL生理盐水,左侧第1孔加25 μL待测样品,混合均匀后,取25 μL至第2孔,相同操作依次稀释至第11孔,吸取25 μL丢弃,第12孔作为空白对照。每孔各加入25 μL的φ=1% SPF鸡红细胞悬液,然后在37 ℃温箱中静置12 min观察是否反生凝集反应。能使红细胞发生凝集的最高稀释度即为病毒HA滴度。
2.3 实验设计 2.3.1 部分析因实验设计部分析因设计是析因实验设计的一种。可通过较少的实验次数考察多个影响因素,能精确地估计出不同因素对响应值的影响。本文选取了病毒收获时间、感染复数、接毒时的细胞密度、培养温度和TPCK-胰酶浓度5个因素,进行16次实验。响应值为病毒HA滴度,自变量编码和水平因素见表 1,实验设计与结果见表 3。
|
|
表 1 部分析因实验设计因素及水平 Table 1 Factors and levels used in the fractional factorial experiment design |
|
|
表 3 部分析因实验设计及结果 Table 3 Design and results of the fractional factorial experiments |
本文在筛选出对病毒HA滴度具有显著影响的因素后,依据Box-Benhnken实验设计理论对其关键因速的条件进一步优化,并考察了因素之间的交互作用,得到最优结果。实验水平及编码见表 2,设计与结果见表 5。
|
|
表 2 BBD设计因素及水平 Table 2 Factors and levels used in the BBD design |
|
|
表 5 BBD设计与结果 Table 5 Design and results of the BBD design |
用JMP 10软件对实验结果进行统计学分析。
3 结果与讨论 3.1 影响病毒HA重要因素筛选查阅相关文献,选取A-病毒收获时间、B-感染复数、C-接毒时的细胞密度、D-培养温度和E-TPCK-胰酶浓度5个因素进行部分析因实验,分析其对病毒HA滴度的影响,结果如表 3所示。
对表 3结果进行非线性回归分析,得到回归方程:
| $ \begin{array}{l} Y = {6.562_{}}5 + 0.625A + {0.187_{}}5B + 1.75C - {0.187_{}}5D + {0.437_{}}5En\\ \;\;\;\;\;\; + 0.125AB + {0.437_{}}5AC + 0.125AE + 0.25BC + {0.312_{}}5BD + 0.25CE \end{array} $ | (1) |
该回归方程R2为0.98,表明回归模型基本能解释实验中病毒HA滴度的变化。因此根据表 4的方差分析结果,5个主效应中,病毒收获时间、接毒时细胞密度和TPCK-胰酶浓度对病毒HA滴度具有显著性影响(P < 0.05)。这是由于病毒在复制之前需要借助TPCK-胰酶活化,且增殖需要宿主细胞与时间。而感染复数、培养温度影响未达显著水平(P > 0.05)。这可能是由于病毒株增殖能力较强,少量的病毒种子足以进行大规模复制。综上所述病毒收获时间、接毒时细胞密度和TPCK-胰酶浓度是影响病毒HA滴度的主要因素。
|
|
表 4 部分析因实验结果方差分析 Table 4 Variance analysis of the fractional factorial experiments |
进一步对上述得到的3个显著因子,利用响应面分析优化其条件。结果如表 5所示。
对实验结果进行回归拟合得到回归方程:
| $ \begin{array}{l} Y = 10.33 + 0.5{X_1} + 1.625{X_2} + 0.25{X_3} - 0.125{X_1}{X_2} - 0.375{X_1}{X_3}\\ ^{\begin{array}{*{20}{c}} {}&{} \end{array}} + 0.{\rm{375}}{X_2}{X_3} - 0.854X_1^2 - 1.354X_2^2 - 0.604X_3^2 \end{array}$ | (2) |
式中:
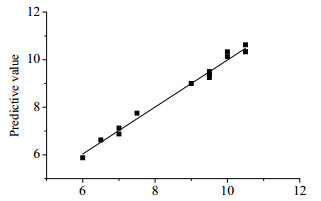
对回归模型的预测值与实际值进行比较,并对回归方程进行效应检验,结果分别见图 1和表 6。
|
图 1 实际值与预测值对比 Fig.1 Comparison of actual and predicted experimental values P = 0.000 3 RSq = 0.99 RSME = 2.887 |
|
|
表 6 响应面二次回归模型的效应检验 Table 6 Effect test of response surface quadratic regression model |
图 1为回归模型预测值与实际值对比结果,从中可以看出实际测得的病毒HA滴度与理论推测值的偏离较小,回归模型R2为0.99,方差分析的p值为0.000 3(< 0.05),说明回归方程显著。表 6为回归模型的效应检验结果,失拟项p值为0.535 2(> 0.05),失拟不显著,表明此次实验数据可用。主效应中病毒收获时间、接毒时的细胞密度效应显著,病毒收获时间和TPCK-胰酶浓度、接毒时的细胞密度和TPCK-胰酶浓度、病毒收获时间和病毒收获时间具有交互作用,此外3个因素均具有2次效应。未知因素对试验结果干扰较小,该模型可以用于病毒HA优化。
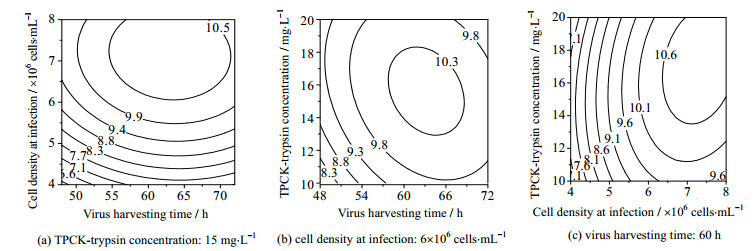
考察接毒时的细胞密度、TPCK-胰酶浓度和病毒收获时间之间相互作用对病毒HA的影响,根据回归方程拟合出的相应等高线图如图 2所示。由图 2(a)可以看出接毒时的细胞密度与病毒收获时间的交互作用并不显著。由图 2(b)可以看出等高线形状为椭圆形,表明接毒时的细胞密度与TPCK-胰酶浓度的交互作用较为显著。这是由于TPCK-胰酶有助于活化病毒提高病毒复制效率,高密度细胞接毒有助于病毒HA提高。由图 2(c)可以看出等高线形状为椭圆形,表明病毒收获时间与TPCK-胰酶浓度的交互作用较为显著。TPCK-胰酶浓度提高使病毒复制效率加快,导致收获时间提前。
|
图 2 两因素之间交互作用病毒 HA 影响的响应面等高线图 Fig.2 Response surface contour map that shows the effect of interaction between two factors on HA titer of influenza |
根据响应面的优化模型,以病毒HA滴度最大化为目标, 对实验测定数据进行优化分析。解析出病毒HA滴度最终优化结果:接毒时的细胞密度为7.28×106 cells·mL-1,TPCK-胰酶浓度为16.77 mg·L-1,病毒收获时间为62.02 h,病毒HA滴度最高可达10.94 log2 HAU·(25 µL-1)。为检验优化后工艺条件下的病毒产量与理论分析的相符合性,进行验证实验。结合实际情况,优化后的工艺实际参数为:TPCK-胰酶浓度为17 mg·L-1、接毒时的细胞密度为7.0×106 cells·mL-1、收毒时间为60 h。3次重复性实验得到的病毒HA滴度平均值为10.85 log2 HAU·(25 µL-1),与回归模型在该条件下给出的预测值(10.89 log2 HAU·(25 µL-1))仅相差2.5%,病毒HA滴度的实际值与优化预测值基本吻合, 应证了试验模型的可行性。
4 结论本文考察了基于MDCK细胞悬浮培养的禽流感疫苗病毒的生产工艺条件,从接毒时的细胞密度、接毒量、培养温度、TPCK-胰酶浓度和病毒收获时间5个因素中筛选出接毒时的细胞密度、TPCK-胰酶浓度和病毒收获时间3个显著影响因素,优化后的最优的工艺条件为:TPCK-胰酶浓度为17 mg·L-1、接毒时的细胞密度为7.0×106 cells·mL-1、病毒收获时间为60 h,在此条件下病毒HA滴度可达10.85 log2 HAU·(25 µL-1)。
| [1] |
BARDIYA N, BAE J. Influenza vaccines:recent advances in production technologies[J]. Applied Microbiology and Biotechnology, 2005, 67(3): 299-305. DOI:10.1007/s00253-004-1874-1 |
| [2] |
TRILLA A, TRILLA G, DAER C. The 1918" Spanish flu" in Spain[J]. Clinical Infectious Diseases, 2008, 47(5): 668-673. DOI:10.1086/592125 |
| [3] |
WONG, S Y. Highly pathogenic avian influenza (H5N1) in Hong Kong, 1997-2014: towards an urban biopolitical immunology[D]. Manchester: The, University of Manchester (United Kingdom), 2015.
|
| [4] |
MONDOR M, AKSAY S, DROLET H, et al. Of chickens and men: avian influenza in humans[J]. Current Molecular Medicine, 2009, 9(2): 131-51. DOI:10.2174/156652409787581565 |
| [5] |
LAI S, QIN Y, COWLING B J, et al. Global epidemiology of avian influenza A H5N1 virus infection in humans, 1997-2015: A systematic review of individual case data[J]. Lancet Infectious Diseases, 2016, 16(7): e108-e118. DOI:10.1016/S1473-3099(16)00153-5 |
| [6] |
HORIMOTO T, KAWAOKA Y. Influenza: lessons from past pandemics, warnings from current incidents[J]. Nature Reviews Microbiology, 2005, 3(8): 591-600. DOI:10.1038/nrmicro1208 |
| [7] |
GEORGE M, FAROOQ M, DANG T, et al. Production of cell culture (MDCK) derived live attenuated influenza vaccine (LAIV) in a fully disposable platform process[J]. Biotechnology & Bioengineering, 2010, 106(6): 906-917. |
| [8] |
MAHARANI U, MARSELINA T, ERNAWATI G, et al. The expression of essential components for human influenza virus internalisation in Vero and MDCK cells[J]. Cytotechnology, 2013, 1(1): 1-6. |
| [9] |
陶源, 胡又佳, 朱宝泉. 基于哺乳动物细胞培养的流感疫苗生产[J]. 世界临床药物, 2011, 32(9): 539-542. TAO Y, HU Y J, ZHU B Q. Progress in production of infl uenza vaccine by mammalian cells[J]. World Clinical Drugs, 2011, 32(9): 539-542. |
| [10] |
黄锭, 刘旭平, 赵亮, 等. MDCK细胞无血清悬浮培养法扩增流行性感冒病毒[C]//第六届全国化学工程与生物化工年会论文集.长沙: 中国化工学会, 2010: 1-5. HUANG D, LIU X P, ZHAO L, et al. Propagation of influenza virusesased on suspension culture of MDCK cells[C]// Chinese National Chemical BiochemicalEngineering Annual Meeting. Changsha: The Chemical Industry and Engineering Society of China 2010. 1-5. |
| [11] |
AGGARWAL K, JING F, MARANGA L, et al. Bioprocess optimization for cell culture based influenza vaccine production[J]. Vaccine, 2011, 29(17): 3320-3328. DOI:10.1016/j.vaccine.2011.01.081 |
| [12] |
ISKEN B, GENZEL Y, REICHL U. Productivity, apoptosis, and infection dynamics of influenza A/PR/8 strains and A/PR/8-based reassortants[J]. Vaccine, 2012, 30(35): 5253-5261. DOI:10.1016/j.vaccine.2012.05.065 |
| [13] |
BOCK A, SCHULZE-HORSEL J, SCHWARZER J, et al. High-density microcarrier cell cultures for influenza virus production[J]. Biotechnology Progress, 2011, 27(1): 241-250. |
| [14] |
YOUIL R, SU Q, TONER T, et al. Comparative study of influenza virus replication in Vero and MDCK cell lines[J]. Journal of Virological Methods, 2004, 120(1): 23-31. DOI:10.1016/j.jviromet.2004.03.011 |
| [15] |
李春艳, 肖晶, 李曦, 等. 微载体规模化培养MDCK细胞增殖H9N2亚型禽流感病毒的研究[J]. 中国人兽共患病学报, 2009, 25(12): 1149-1153. LI C Y, XIAO J, LI X, et al. Research on multiplication of the H9N2 subtype avian influenza virus in large-scale microcarrier-based MDCK cell culture system[J]. Chinese Journal of Zoonoses, 2009, 25(12): 1149-1153. DOI:10.3969/j.issn.1002-2694.2009.12.005 |
| [16] |
袁丽红, 邵辉, 顾永明, 等. 盾叶薯蓣中水解原位提取薯蓣皂甙元[J]. 高校化学工程学报, 2007, 21(3): 538-544. YUAN L H, SHAO H, GU Y M, et al. Simunaneous extraction and hydrolysis in situ for the recovery of diosgenin from Dioscorea zingiberensis[J]. Journal of Chemical Engineering of Chinese Universities, 2007, 21(3): 538-544. DOI:10.3321/j.issn:1003-9015.2007.03.032 |
| [17] |
樊铖, 展侠, 陈剑, 等. 响应面优化法在PDMS/PVDF膜制膜条件优化中的应用[J]. 高校化学工程学报, 2012, 26(3): 374-381. FAN C, ZHAN X, CHEN J, et al. Application of response surface methodology(rsm) to optimize the preparation conditions of PDMS/PVDF composite membranes[J]. Journal of Chemical Engineering of Chinese Universities, 2012, 26(3): 374-381. DOI:10.3969/j.issn.1003-9015.2012.03.003 |




