2. 石家庄学院 化工学院,河北 石家庄 050035
2. College of Chemical Engineering, Shijiazhuang University, Shijiazhuang 050035, China
雄烯二酮(4-AD)是甾体激素药物的重要中间体,可用于生产性激素、孕激素、蛋白同化激素[1],又可用于合成可的松、黄体酮和螺内脂[2]等药物。微生物转化甾醇产生雄烯二酮的发酵系统很多[3],其中分枝杆菌大豆油-水两相发酵系统因其具有较高的甾醇加入量[4]和较低的底物及产物抑制性等优点,可高效降解植物甾醇侧链产生雄烯二酮,在以植物甾醇为原料经微生物转化生产雄烯二酮的发酵系统中占有主导地位,成为目前广泛关注的热点。
正是由于采用了大豆油-水两相发酵系统,在雄烯二酮的下游提取过程中,如何分离除去大豆油成为关键性问题,所以研究雄烯二酮在含大豆油的有机溶剂体系中的溶解度对于指导工业生产实践很有意义。此外,充分了解雄烯二酮在各种不同溶剂中溶解度的变化规律,对于结晶工艺的改进至关重要。尽管如此,有关雄烯二酮溶解度的研究仅有一篇论文,潘丽军等[5]在两相发酵系统中提取分离雄烯二酮的研究中,指出不同温度、不同有机溶剂中,甾醇和雄烯二酮的溶解度问题。但所测溶剂仅有甲醇、乙醇、乙酸乙酯、正己烷这四种,种类偏少,侧重点也不同,不能满足工业生产的需求。而在含大豆油的有机溶剂体系中的溶解度等相关数据未见任何公开报道。
本研究采用固液平衡法得到饱和溶液[6, 7],用高效液相色谱法(HPLC)测定溶液中的溶解度。考虑到有机溶剂在工业生产中的可行性,溶剂选为甲醇、乙腈、丙酮、异丙醇、乙酸乙酯和乙醇这六种有机溶剂及各自的含大豆油的有机溶剂体系,最后对结果采用经验多项式方程、半经验关联模型[8]和Apelblat方程模型进行关联[9],目的在于为雄烯二酮萃取及结晶操作过程中工艺的优化提供基础数据和理论支持。
2 材料和方法 2.1 试剂和仪器试剂:4-AD工业纯品(> 98%),武汉远成共创科技有限公司;甲醇、乙腈、丙酮、异丙醇、乙酸乙酯、乙醇等,均为分析纯,天津市永大化学试剂开发中心;大豆油(食品级),益海嘉里(金龙鱼)中国有限责任公司。
仪器:岛津LC-PDA高效液相色谱分析仪,日本岛津;RE-52AA旋转蒸发仪、SHB-T循环水式真空泵,郑州长城科工贸有限公司;HH系列数显恒温水浴锅,江苏金坛安普实验仪器厂;H-1650型高速台式离心机,长沙湘仪离心机仪器有限公司;BSA-223S电子天平,梅特勒-托利多仪器(上海)有限公司;磁力搅拌器,巩义市英峪予华仪器厂;快速混匀器(SK-1),金坛市富华电器有限公司。
2.2 实验方法 2.2.1 雄烯二酮的高效液相色谱检测待测溶液经0.45 μm微孔滤膜过滤后进行高效液相色谱检测。检测条件为:Alltima C18柱(250 mm×4.6 mm);波长:254 nm;溶剂:甲醇(色谱纯);样品浓度:3.0 mg·mL-1,进样量:5 μL,流动相:甲醇:水=7:3(V/V),柱温:25℃,流速:1.5 mL·min-1。
2.2.2 雄烯二酮在不同有机溶剂中溶解度的测定采用过饱和法,在253.15、263.15、277.15、288.15、303.15和313.15 K温度下分别测定雄烯二酮在甲醇、乙醇、乙酸乙酯、丙酮、异丙醇、乙腈中的溶解度。称取过量的雄烯二酮(±0.0001 g)和一定量的有机溶剂放于试管中,盖上瓶塞放在恒温器中保持3 h,期间每30 min震荡一次,使之达到溶解平衡,最后静置30 min。用提前预热的取样器吸取上层清液,在温度高于溶解温度的操作条件下迅速用0.45 µm的微孔滤膜过滤后,经色谱级甲醇适当稀释后用外标法进行高效液相色谱分析检测其浓度。每隔一定时间测定一次,当相邻两次结果的相对误差在1%以内,即认为上清液达到了饱和状态。每组试验进行3次取其平均值。
为验证本文方法的可靠性,选择氯化钾-水体系作为标准体系进行检验,结果表明实验值与文献值[10]的平均相对误差小于0.21%。说明本方法可靠,可用于雄烯二酮溶解度的测定。
2.2.3 雄烯二酮在不同的含大豆油的有机溶剂体系中溶解度的测定在298.15 K温度下,将一定量的有机溶剂与大豆油充分混合后静置分层,上层清液即为含大豆油的有机溶剂体系,通过测定溶剂前后质量差异,结合大豆油的密度0.917 g·mL-1可确定出溶解大豆油的体积,其余方法见2.2.2节。其中,当测定温度低于298.15 K时,会有少量大豆油在试管底部析出,这时取含大豆油的上清液进行测定。
2.2.4 所配含大豆油的有机溶剂体系在不同温度下大豆油浓度的测定考虑到大豆油在低温下的溶解度较小,常规的通过蒸干溶剂测量剩余油质量的方式已不再适用,因此选择利用混合溶液密度和其浓度之间的关联间接的确定所测溶液的浓度。首先在25℃下配制一系列不同浓度(%(V),以下同)的大豆油-有机溶剂混合体系,测定其密度,建立大豆油浓度和溶液密度的关联式,然后将25℃饱和了大豆油的有机溶剂体系在不同温度下所达到平衡后,取上清液放置于25℃下,待稳定后通过测定其密度,结合上述关联式可计算出所测温度下大豆油的浓度。
3 结果与讨论 3.1 雄烯二酮在不同有机溶剂和含大豆油的有机溶剂体系中的溶解度首先测定了大豆油在298.15 K下所配饱和溶液在不同温度下的浓度S,以体积比(V/V)来表示,即在含大豆油的有机溶剂体系中:
| $ S = \frac{{\rm{大豆油的体积}}}{{\rm{有机溶剂的体积}}} $ |
结果见表 1,表中,S表示三次测量后计算结果的平均值,ε表示平均相对误差。
|
|
表 1 不同温度下有机溶剂体系中大豆油浓度列表 Table 1 Concentrations of soybean oil in organic solvents at different temperatures |
用1.2实验方法分别测定了雄烯二酮在不同有机溶剂和含大豆油的有机溶剂体系中的溶解度,以xi(摩尔分数)来表示,结果表明,乙酸乙酯和丙酮分别与大豆油互溶,故此两种体系不做后续测定。雄烯二酮在不同有机溶剂中的溶解度数据见表 2,溶解度曲线见图 1。雄烯二酮在不同的含大豆油的有机溶剂体系中的溶解度数据见表 3,溶解度曲线见图 2。表中ε表示三次测量值的平均相对误差,φ表示和有机溶剂体系相比,溶解度增加的百分比,计算公式如下:
| $ \varepsilon = \frac{1}{n}\sum\limits_{i = 1}^n {|\frac{{x_i^n - x_i^e}}{{x_i^e}}|} $ | (1) |
| $ \varphi = \frac{{x_i^s - x_i^m}}{{x_i^m}} $ | (2) |
|
|
表 2 雄烯二酮在不同有机溶剂中的溶解度数据表 Table 2 Solubility data of androstenedione in different organic solvents |
|
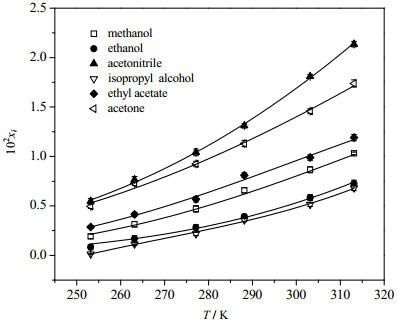
图 1 雄烯二酮在有机溶剂中的溶解度数据及回归曲线 Fig.1 Solubility and related fitting results of androstenedione in organic solvents |
|
|
表 3 雄烯二酮在不同的含大豆油的有机溶剂体系中的溶解度数据表 Table 3 Solubility data of androstenedione in different soybean-oil containing organic solvents |
|
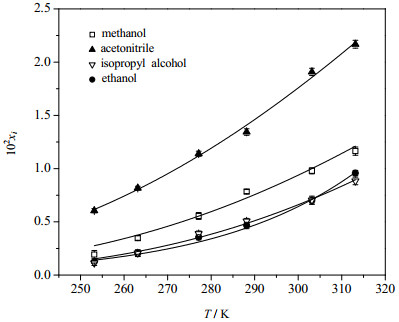
图 2 雄烯二酮在含大豆油的有机溶剂体系中的溶解度数据及回归曲线 Fig.2 Solubility and related fitting results of androstenedione in soybean-oil containing organic solvents |
式中,xin和xie分别表示溶解度测量值和平均值,xim和xis分别表示有机溶剂体系和含大豆油的有机溶剂体系中的溶解度,n表示实验次数。
实验结果表明,雄烯二酮在上述两种溶液体系中溶解度随着温度的升高而增加,呈顺溶解度趋势。因为雄烯二酮分子中含有羰基,所研究的有机溶剂均为极性溶剂,在雄烯二酮的晶体结构中分子之间的相互作用力以及雄烯二酮和有机溶剂分子之间的相互作用力主要表现为氢键、范德华力和疏水性相互作用力。雄烯二酮在纯有机溶剂当中溶解度随温度的升高而增加,证明雄烯二酮在有机溶剂中的溶解过程是一个吸热过程。更进一步可知,雄烯二酮和有机溶剂分子之间的氢键、范德华力和疏水性相互作用力等分子之间的相互作用力比雄烯二酮晶体结构中分子之间的相互作用力要弱。另外由图 1可知,有机溶剂对雄烯二酮溶解能力的大小依次为:乙腈> 丙酮 > 乙酸乙酯 > 甲醇 > 乙醇 > 异丙醇。根据相似相溶的原理,雄烯二酮会在和其极性相似的溶剂中溶解度最大,查阅相关资料,发现无论从介电常数还是溶度参数确定的溶剂极性顺序均未能符合所测结果,因此还需进一步的探索。由表 3可以看出,在相同温度下,含大豆油的有机溶剂体系中的雄烯二酮的溶解度均大于其在相应的纯溶剂中的溶解度,其中异丙醇增加的幅度最大,而乙腈增加的幅度最小。利用这些特性,在发酵过程中添加大豆油以减轻产物抑制,在提取过程中预先除去大豆油以利于分离结晶,为工业生产提供了数据支持。
3.2 雄烯二酮溶解度的关联溶解度和温度之间存在一定的关联性,以温度为唯一考察指标,并考虑到大豆油在溶剂里的溶解度很小,忽略含大豆油的有机溶剂体系在不同温度下含油量的差异,可应用以下几种方程模型进行关联。
3.2.1 多项式经验方程关联在溶剂、溶质和压力等因素一定时,溶解度由温度决定,假设溶解度是随温度连续变化的,则溶解度是可以用温度的多项式方程来表示的[11],如下:
| $ {x_i} = a + bT + c{T^2} + d{T^3} $ | (3) |
式中:xi为溶解度(摩尔分数),T为绝对温度(K),a、b、c和d是多项式经验方程参数。
由纯有机溶剂溶解度实验数据关联出的上述多项式经验方程中的参数值见表 4。由含大豆油的有机溶剂体系中溶解度数据关联到的参数值见表 5。
|
|
表 4 有机溶剂体系溶解度的多项式经验方程中的参数值 Table 4 Polynomial equation correlation parameters of androstenedione solubility in organic solvents |
|
|
表 5 含大豆油的有机溶剂体系中溶解度的多项式经验方程中的参数值 Table 5 Polynomial equation correlation parameters of androstenedione solubility in soybean-oil containing organic solvents |
表 4和表 5当中的相关系数R2都大于0.98,表明拟合方程对实验结果的拟合程度很好。而平均相对误差,由下式计算
| $ \delta = \frac{1}{N}\sum\limits_{i = 1}^N {|\frac{{x_i^{\rm{e}} - x_i^{\rm{c}}}}{{x_i^{\rm{e}}}}|} $ | (4) |
其中,δ为平均相对误差(%),xie、xic分别为溶解度实验测定值和理论计算值。
平均相对误差,表明的是由拟合方程计算出来的理论值和实验结果之间的平均相对误差,最大的平均相对误差是5.35%。总体而言,拟和效果很好,误差足够小。
3.2.2 半经验关联模型关联根据固液平衡理论和热力学原理,针对理想溶液有以下普适的溶解度方程:
| $ {\rm{ln}}({x_i}{\gamma _i}) = \frac{{\Delta {H_{\rm{m}}}}}{R}(\frac{1}{{{T_{\rm{m}}}}} - \frac{1}{T}) $ | (5) |
假设雄烯二酮溶液为理想溶液,即γ=1,则可写成如下的形式[12]:
| $ {\rm{ln}}{x_i} = A + \frac{B}{T} $ | (6) |
式中:A、B为半经验关联模型方程参数。雄烯二酮在有机溶剂和含大豆油的有机溶剂体系中的溶解度用半经验关联模型回归的结果见表 6和7。
|
|
表 6 有机溶剂体系半经验关联模型方程中的参数值 Table 6 Semi-empirical equation correlation parameters of androstenedione solubility in organic solvents |
|
|
表 7 含大豆油的有机溶剂体系半经验关联模型方程中的参数值 Table 7 Semi-empirical equation correlation parameters of androstenedione solubility in soybean-oil containing organic solvents |
表 6和表 7当中的相关系数R2都大于0.98,表明拟合方程对实验结果的拟合程度很好。而平均相对误差,最大值是5.76%。总体而言,拟和效果很好,误差足够小。
3.2.3 Apelblat方程模型关联假定溶液的焓变为温度的线性函数,依据Clausius-Clapeyron方程
| $ \int_{{x_0}}^x {{\rm{dln}}x} = \int_{{t_0}}^t {\frac{{a + bT}}{{R{T^2}}}} {\rm{d}}T $ | (7) |
进行积分得出:
| $ {\rm{ln}}x = - \frac{a}{{RT}} + \frac{b}{R}{\rm{ln}}T + \frac{a}{{R{T_0}}} - \frac{b}{R}{\rm{ln}}{T_0} - {\rm{ln}}{x_0} $ | (8) |
简化为下式[13]:
| $ {\rm{ln}}{x_i} = A + \frac{B}{T} + C{\rm{ln}}T $ | (9) |
式中:A、B和C为Apelblat方程参数。雄烯二酮的溶解度用Apelblat方程回归结果见表 8和9。
|
|
表 8 有机溶剂体系溶解度关联的Apelblat方程中的参数 Table 8 Apelblat equation correlation parameters of androstenedione solubility in organic solvents |
|
|
表 9 含大豆油的有机溶剂体系溶解度关联的Apelblat方程参数 Table 9 The Apelblat equation correlation parameters of androstenedione solubility in soybean-oil containing organic solvents |
表 8和表 9当中的相关系数R2都大于0.98,表明拟合方程对实验结果的拟合程度很好。而平均相对误差,最大值是4.05%。总体而言,拟和效果很好,误差足够小。
比较三种方程的关联结果,Apelblat方程模型的显著性最好,更能准确地计算出不同温度下雄烯二酮在不同体系下的溶解度数据。
4 结论测定了雄烯二酮在不同温度下有机溶剂和含大豆油的有机溶剂体系中的溶解度,并进行了多项式经验方程、半经验关联模型和Apelblat方程模型的建立。试验结果表明在这两种体系中雄烯二酮的溶解度都是随温度的升高而增大的。有机溶剂对雄烯二酮溶解能力的大小依次为:乙腈> 丙酮 > 乙酸乙酯 > 甲醇 > 乙醇 > 异丙醇。含大豆油的有机溶剂体系对雄烯二酮的溶解力相较于同温度下的相应纯有机溶剂更强。以上溶解度变化规律可作为工业上利用有机溶剂萃取及结晶操作的理论依据。最后用多项式经验方程、半经验关联模型和Apelblat方程模型进行关联,相关性较好。
符号说明:
|
|
| [1] | YE Li(叶丽), LI Zeng-xia(李增霞), CHEN Qian(陈倩), et al. Degradation of β-sitosterol to Androst-1, 4-diene-3, 17-dione by Mycobacterium sp(分枝杆菌降解β-谷甾醇制备雄甾-1, 4-二烯-3, 17-二酮)[J]. Fudan University Journal of Medical Sciences(复旦学报(医学版)) , 2002, 29(4): 280-283. |
| [2] | LUO Bing-hua (罗炳华). The effects of plus factors on two-phase system transform phytosterolto androstenedione (外加因子对两相系统转化植物甾醇制备雄烯二酮的影响) [D]. Hefei (合肥): Hefei University of Technology (合肥工业大学), 2009. |
| [3] | LIANG Jian-jun(梁建军), WANG Wen-jun(汪文俊). Progress of biotransforming phytosterols into androstadienedione and androstenedione by microorganisms(微生物生物转化甾体化合物生产雄烯二酮研究进展)[J]. Hubei Agricultural Sciences(湖北农业科学) , 2012, 51(7): 1309-1312. |
| [4] | JIANG Shao-tong(姜绍通), ZHAO Jun-ping(赵俊平), YANG Ying(杨英), et al. Study on transformation of phytosterol into androst-4-ene-3, 17-dione in two-phase systems(两相系统发酵转化植物街醇为雄烯二酮的研究)[J]. Food and Fermentation Industries(食品与发酵工业) , 2008, 34(6): 46-49. |
| [5] | PAN Li-jun(潘丽军), LUO Bing-hua(罗炳华), JIANG Shao-tong(姜绍通), et al. Study on extraction of androst-4-diene-17-dione from oil-water two-phase fermentation system of Mycobacterium B696(两相发酵系统中提取分离雄烯二酮的研究)[J]. Food Science(食品科学) , 2009, 30(11): 144-146. DOI:10.3321/j.issn:1002-6630.2009.11.031. |
| [6] | ZHANG Cong-liang(张从良), WANG Yan(王岩). Determination and correlation of aqueous solubilities for quinolones(喹诺酮类药物水溶解度的测定与关联)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报) , 2009, 23(1): 175-177. |
| [7] | YE Chang-shen(叶长燊), LIN Cheng(林诚), QIU Ting(邱挺). Determination and correlation of liquid-liquid equilibrium data for the ternary system of DMF-CHCl3-H2O(N, N-二甲基甲酰胺-三氯甲烷-水体系液液相平衡数据的测定与关联)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报) , 2009, 23(2): 183-186. |
| [8] | SUN Peng(孙鹏), LIU Jun-guo(刘俊果), YANG Yu-huai(杨玉淮), et al. Determination and correlation of solubilities of avermectins in different systems of alcohol-water(阿维菌素在不同醇-水溶剂体系中溶解度的测定与关联)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报) , 2010, 24(5): 735-738. |
| [9] | XU Hong-xia(许红霞), JIANG Lin-kun(姜林锟), WANG Li-sheng(王利生). Determination and correlation of solubilities of ivermectin in alcohol and alcohol-water mixture(伊维菌素在醇及醇-水混合溶剂中溶解度的测定与关联)[J]. Journal of Nanjing University of Science and Technology(南京理工大学学报) , 2014, 38(1): 173-180. |
| [10] | Pinho S P, Marcedo E A. Solubility of NaBr, and KCl in water, methanol, ethanol, and their mixed solvents[J]. Journal of Chemical and Engineering Data , 2005, 50(1): 29-32. DOI:10.1021/je049922y. |
| [11] | XIE Zhi(谢智), JI Qing-rong(季清荣), CHANG Zhi-dong(常志东). Determination and correlation of solubilities of avermectins in different solvents(Avermectin在不同溶剂中溶解度的测定与关联)[J]. Chinese Journal of Antibiotics(中国抗生素杂志) , 2006, 31(1): 42-44. |
| [12] | Wei D W, Chen L M. Solubility of 2-aminopyridinein acetone, chloroform, and ethyl acetate[J]. Journal of Chemical and Engineering Data , 2009, 54(3): 1098-1099. DOI:10.1021/je800768x. |
| [13] | Du Z X, Huang X Q, Ying H J, et al. Solubility of cytidine 5'-diphosphocholine sodium in water and different binary mixtures from(278.15 to 298.15 K)[J]. Journal of Chemical and Engineering Data , 2010, 55(2): 1000-1002. DOI:10.1021/je900465r. |




