甲醇制烯烃(MTO)技术是低碳烯烃制备的有效途径,大力发展甲醇制烯烃技术对于保障我国能源安全具有重要意义。目前,MTO技术使用的催化剂主要为SAPO-34分子筛,主要原因在于该分子筛具有小孔径、易失活等特点,对乙烯丙烯有良好的选择性。国内外对于SAPO-34催化MTO的研究主要集中在催化剂的制备和反应机理的探索上,对反应器的研究相对较少。而反应器是MTO过程的核心部分,所以开发生产能力大、产物选择性和单程转化率高、催化剂床层温控简单、床层压降小的甲醇制低碳烯烃反应器是反应器研究的主要课题。
由于MTO反应过程强放热易导致SAPO-34分子筛失活,所以目前工业生产中多采用流化床反应器,对其研究也相对成熟。Bos[1]、Soundararaja[2]、王彪[3]、郑康[4]、齐国祯等[5]对MTO反应动力学和流化床反应器进行模拟,研究操作条件对甲醇转化率和产物选择性的影响。庄亚青[6]、ChangJian等[7]采用新型多相流体模型和计算方法研究了流化床反应器中流体动力学和反应动力学行为,发现颗粒运动呈环核模型且传递效果好,进料温度、气速、水醇比对此反应影响大。
虽然工业上MTO工艺广泛采用流化床反应器,但其存在甲醇单程转化率相对较低,催化剂磨损显著以及成本高等限制,而固定床反应器结构简单操作方便,因此研究人员开展了针对固定床反应器反应过程的系列研究。胡浩等[8, 9]建立了一维MTO固定床反应器数学模型,考察催化剂装填量和床层体积对组分浓度和轴向温度分布的影响。Alwahabi等[10]对绝热和等温固定床反应器进行数值模拟,采用段间换热保证每段原料进口温度都维持在648 K,建议为保证各段转化率,催化剂的装填量应逐段增加。庄亚青等[11]开发了综合二维反应器模型来模拟MTO固定床反应器中的流动行为,应用集总反应的指数函数动力学模型进行反应过程模拟,发现甲醇转化率和催化剂失活紧密相联,且受操作条件的影响。
目前关于固定床反应器的模拟研究,特别是温度及组分浓度随反应进行的规律研究方面的文献相对较少,开展相关研究十分必要。本文利用FLUENT软件对MTO固定床反应器进行数值模拟,研究反应过程中温度、组分浓度的变化规律,探讨反应过程。
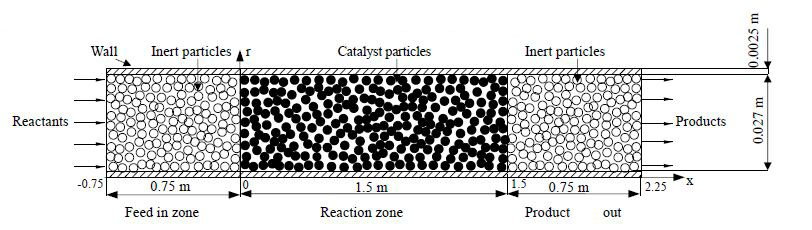
2 MTO固定床反应器模型 2.1 固定床反应器物理模型结合常用固定床反应器中反应管规格(f32 mm x2.5 mm,管长3 m)将反应管分为三个区域,见图 1。其中进料区和出料区装填惰性固体颗粒,分别进行物料的预热和产物的冷却,同时进料区具有使物料到达反应区前的流动形态稳定的功能;反应区装填活性催化剂SAPO-34,相关参数见表 1。
|
图 1 固定床反应器反应管结构模型 Fig.1 Schematic diagram of a reaction tube of the fixed-bed reactor |
| 表 1 固体催化剂参数[11] Table 1 Physical parameters of the catalyst |
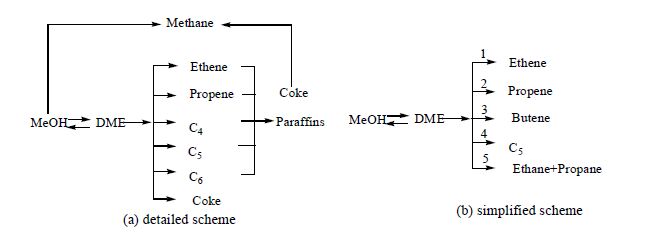
本文采用由实验得到的集总动力学模型[12],该动力学模型详细考察了反应过程中积炭对于反应过程的影响,很好地解释了反应过程中反应产物随温度、压力、积炭生成量的变化规律,具有很好的理论可靠度。Zhuang等[11]采用简化的集总反应网络对MTO固定床进行模拟,模拟的结果与文献[12]数据吻合较好,甲醇转化率和催化剂失活紧密相关,说明该动力学可靠,但其对反应过程中温度、组分浓度沿反应管轴向分布的研究较少。本文采用Zhuang等[11]验证过的简化动力学模型(参见图 2),对反应过程中温度、组分浓度的轴向变化规律,探讨反应过程。
|
图 2 集总反应网络 Fig.2 Reaction network of the whole process |
对图 2(a)的网络进行简化,采用C5代表在整体生成物中所占的质量分数相对较小的C5和C6,忽略生成质量非常小的甲烷,并以反应中主要生成的链烷烃乙烷和丙烷作为链烷烃。简化之后的反应网络见图 2(b)。
反应器采用平推流模型,表达式如下:
| $\frac{d{{X}_{i}}}{d(W/{{F}_{MeOH}})}=\overrightarrow{{{r}_{i}}}$ | (1) |
由图 2(b)的反应网络结合积炭动力学生成模型[13],得到反应动力学方程式如下:
| ${{r}_{i}}={{k}_{i}}(1-{{\varphi }_{i}}C){{p}_{A}}$ | (2) |
| ${{k}_{i}}={{k}_{i}}^{0}\exp (-{{E}_{a}}/RT)$ | (3) |
| $C=\frac{1}{{{\varphi }_{C}}}[1-\exp (-{{\varphi }_{C}}{{k}_{c}}CAMF(1-{{X}_{A}}))]$ | (4) |
| ${{K}_{C}}=1.27\exp (-6707/8.314T)$ | (5) |
| $CAMF=WHSV\times t$ | (6) |
| ${{\varphi }_{C}}=1.07\times {{10}^{-6}}{{T}^{2}}-0.00181T+0.7954$ | (7) |
甲醇制烯烃过程的传热、传质均发生在催化剂装填区,故对反应区进行多孔介质区域[14]反应模拟,对应的稳态模拟控制方程见表 2。
| 表 2 控制方程 Table 2 Control equations |
根据图 1的反应管模型与实际操作条件(气体流量0.0009 kg⋅s-1时对应的固定床空床气速1.4m⋅s-1),且反应管长径比L/D=111,确定入口为恒质量流率,壁面为恒对流传热系数。在反应区采用UDF函数添加反应源项。管外采用HTS熔盐降温。通过恒对流传热公式[16]计算可得总壁面传热系数${{K}_{fc}}$。
反应条件下对应的物性参数[17, 18]及边界条件见表 3。
| 表 3 边界条件 Table 3 Boundary condition parameters for different models |
图 3为温度698 K、水醇比为0(纯甲醇)的进料条件时不同催化剂积炭量(催化剂表面积碳失活的量与催化剂质量比)下各产物组分选择性的模拟值与实验值[13]对比。由图可见,不同物质模拟的总体误差小于5%,说明模拟值和实验值吻和良好,证明了本文所建模型的可靠性。

|
图 3 不同积碳量下生成物选择性的模拟值与实验值对比 Fig.3 Comparison between literature and simulation results of product selectivity under different coke contents |
本文主要讨论进料温度、操作压力、水醇比对甲醇转化率、反应器内温度分布、产物摩尔分率与选择性的影响。模拟条件为:进料温度673~823 K,操作压力0.2~0.5 MPa,进料水醇比0~1。
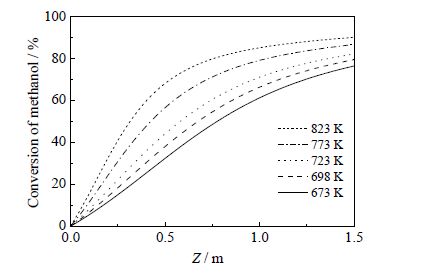
3.2.1 进料温度的影响图 4为操作压力0.3 MPa、甲醇进料水醇比为0的情况下,进料温度对反应器轴向(Z为反应区域尺寸,下同)甲醇转化率值的影响。可以发现,相同的轴向位置处,甲醇转化率随着进料温度的增大而提高;同一温度下,沿流动方向,甲醇的转化率逐渐提高。
|
图 4 不同温度下反应管轴向甲醇转化率变化 Fig.4 Axial methanol conversion profiles under different temperatures |
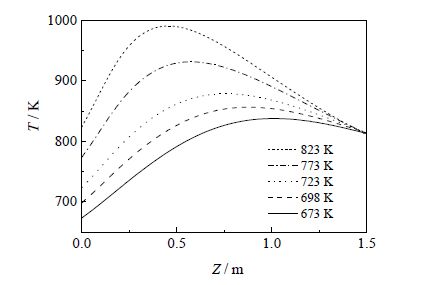
图 5为反应管内轴向温度分布情况。可以发现,随甲醇进料温度升高,反应管内温度升高,且温度峰值越靠近反应进口段。由于反应管外采用熔盐介质作为冷却介质,反应区的出口温度基本保持不变。提高进料温度,甲醇的反应速率提高,短时间内反应放出的热量多,反应管的高温区相应的前移,从而使催化剂结焦加快。
|
图 5 不同进料温度下反应管轴向温度分布 Fig.5 Axial temperature profiles of the reactor under different temperatures |
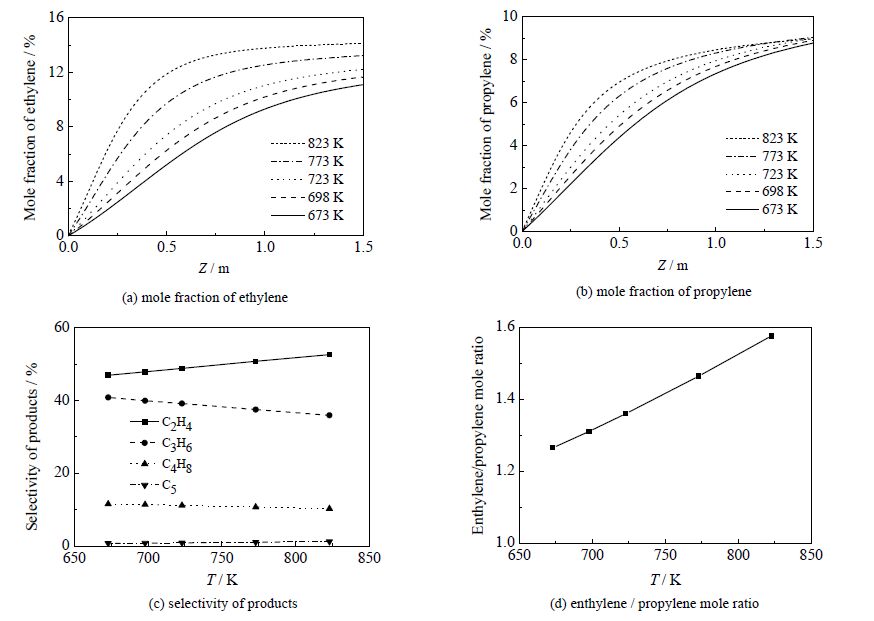
图 6为进料温度对产物摩尔分率与选择性的影响。从图 6(a,b)可以发现,在相同的轴向位置处,反应温度升高,乙烯摩尔分数增大且升高明显,而丙烯摩尔分数变化不明显(略有下降)。图 6(c)中,升高进料温度,乙烯选择性提高、丙烯选择性下降,使得乙烯/丙烯摩尔比增大(图 6(d))。由于温度升高,催化剂表面积炭量增加,催化剂孔径变小,更有利于分子相对较小的乙烯生成,抑制丙烯的生成。所以高温利于乙烯的生成,不利于丙烯的生成。由此可见,工业上可通过控制进料温度来控制产品中乙烯与丙烯的比率,达到调节产物分布的目的。但过高的温度会加速催化剂的失活,使得副产物增多。所以进料温度应适宜,本文模拟结果表明450~500℃较为合适,此时既可以保持乙烯丙烯的较高选择性,也可以有效减少催化剂的积炭量,保证生产效率。
|
图 6 温度对产物摩尔分率与选择性的影响 Fig.6 Effects of temperature on mole fraction and product selectivity |
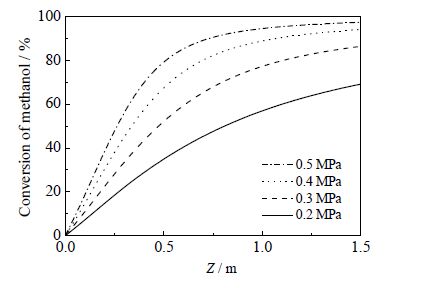
从图 7可以发现,在相同轴向位置处,升高压力使甲醇的转化率逐渐增大(后期增大趋势变缓)。这是由于压强增加,甲醇反应速率增大。但压强进一步增大,甲醇反应量一定,随着甲醇量的消耗,压强对甲醇转化率的影响就会越来越不明显。
|
图 7 不同压力下甲醇轴向转化率分布 Fig.7 Axial methanol conversion profiles under different |
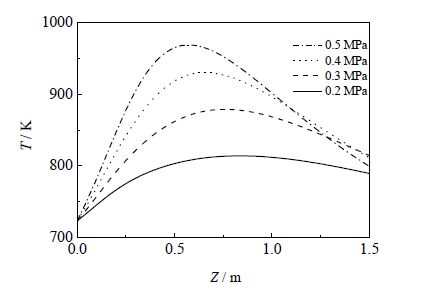
从图 8可以发现,在相同的轴向位置处,压力越高,温度升高越明显,温度峰值位置前移。这是由于压强升高导致甲醇反应速率加快,转化率升高,放出的热量更多更快,温度升高值就越大。
|
图 8 不同压力下轴向温度分布 Fig.8 Axial temperature profiles of the reactor under different |
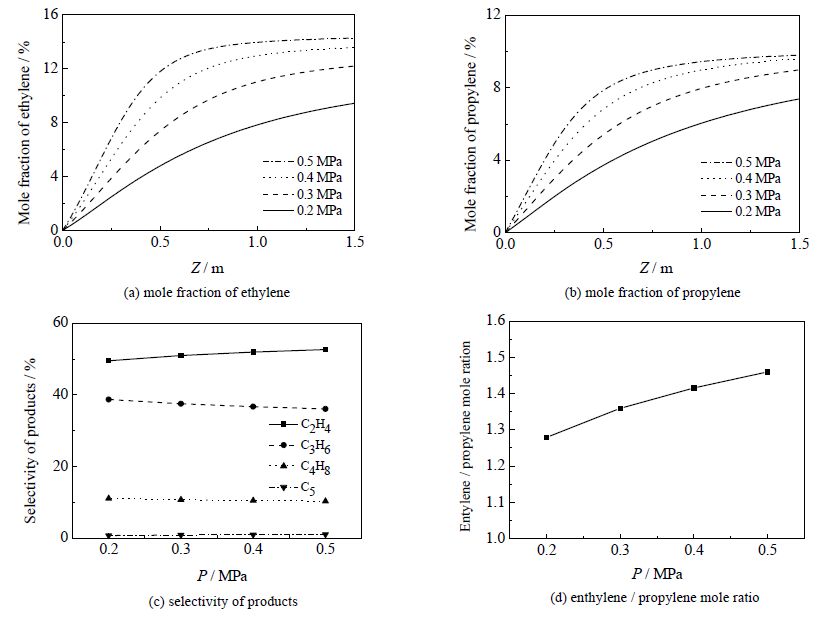
从图 9可见,在相同轴向位置处,压力提高,乙烯和丙烯的摩尔分数均增大,但压力超过0.4 MPa后,压力对两者摩尔分数的提高影响减小(图 9(a,b));乙烯选择性随压强增大略有升高,丙烯则略有下降,压力对乙烯丙烯选择性的影响并不明显(图 9(c));压力从0.2 MPa增大到0.5 MPa,乙烯/丙烯的摩尔比1.27增加到1.45(图 9(d)),该比值稍有增加,但与温度对乙烯/丙烯摩尔比的影响比较来说,该比值相对较小。
|
图 9 操作压力对产物摩尔分率和选择性的影响 Fig.9 Effects of pressure on product mole fraction and selectivity |
甲醇制烯烃工业生产中增大反应的压强可以达到更高的甲醇转化率和乙烯丙烯生成率,但压强升高对于反应器的性能提出了更高的要求。综合考虑上述因素,本文认为压力在0.3~0.4 MPa比较合适。
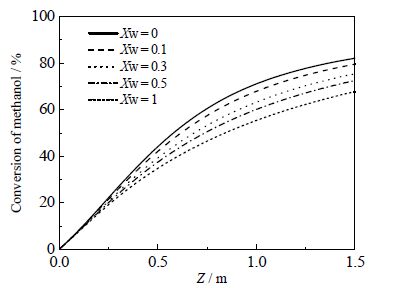
3.2.3 进料水醇比的影响由图 10,相同轴向位置处,甲醇转化率随进料水醇比的增大而减小,即水含量增加会减少甲醇转化率。主要原因在于,进料中含水量的增加不利于正向反应的进行,减小了甲醇的转化量;进料水含量的增加降低了甲醇分压,减小了甲醇的反应速率;水的加入带走反应放出的热量,使得反应的温度下降,降低甲醇反应的速率,降低甲醇的反应量。
|
图 10 水醇比对轴向甲醇转化率的影响 Fig.10 Axial methanol conversion profiles under different water to methanol ratios |
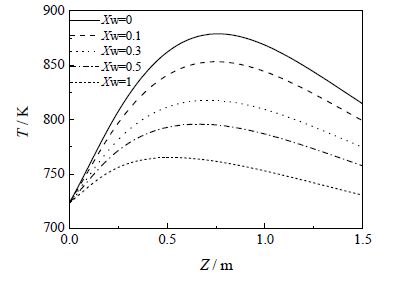
从图 11可以发现,相同轴向位置处的温度随水醇比的增大而减小,且最高温升逐渐减小。这是由于进料水醇比的增加,相同质量流量下甲醇的含量减小,甲醇的分压也减小,导致甲醇反应速率降低,反应放出热量减小。水的加入可以带走部分反应热,造成反应过程中温度升高缓慢。
|
图 11 不同水醇比下轴向温度分布 Fig.11 Axial temperature profiles of the reactor under different water to methanol ratios |
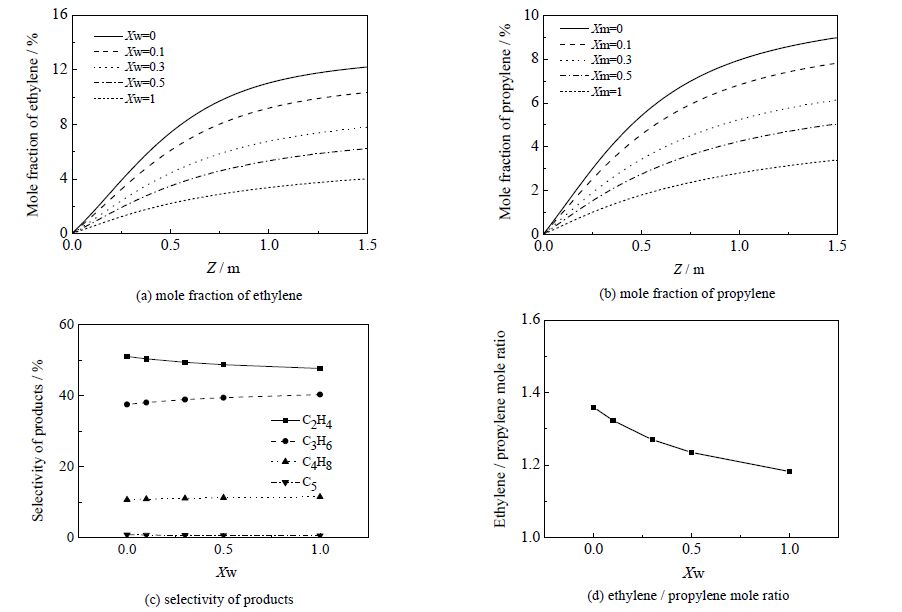
从图 12可见,相同的反应管位置处,乙烯和丙烯的摩尔分率随着进料水醇比的增大而减小(图 12a,b),进料中水含量的增加使产物明显减少,降低生成率;水醇比增大,乙烯选择性略有下降,丙烯选择性略有升高但不很明显(图 12 c),水含量的增加有利于丙烯的生成而对乙烯则起到抑制的作用;乙烯/丙烯的比率随着水醇比的增大而减小(图 12 d)。这是由于进料中水含量的增加减缓了反应过程中催化剂的积炭速率,积碳量的减小会导致催化剂孔径增大,大孔径不利于小分子乙烯的生成却对丙烯的生成有利。而水含量的增加带走了反应热,反应器内温度升高不明显,导致乙烯选择性降低和丙烯选择性提高,乙烯/丙烯比率降低。
|
图 12 水醇比对产物摩尔分率与选择性的影响 Fig.12 Effects of water to methanol ratio on product mole fraction and selectivity |
采用FLUENT软件对甲醇制烯烃过程固定床反应器进行数值模拟,讨论了进料温度、操作压力和进料水醇比对反应过程的影响,得到以下结论:
(1) 提高进料温度可提高甲醇的反应速率和转化率、乙烯的选择性,降低丙烯选择性,使产物中乙烯/丙烯摩尔比值逐渐增大。生产中可以通过调节进料温度改变产物乙烯/丙烯的摩尔比。较为合适的进料温度为723~773 K(450~500℃)。
(2) 压力升高,甲醇反应速率和转化率增大,产物中乙烯、丙烯含量均增大,但对产物选择性和乙烯/丙烯摩尔比影响不很明显。压力0.3~0.4 MPa比较合适。
(3) 水醇比增大,甲醇反应速率和转化率均减小,乙烯丙烯产量降低,乙烯选择性略有下降,丙烯选择性略有升高,乙烯/丙烯的摩尔比降低;适量水的加入有利于减缓反应过程的催化剂积炭量,延长催化剂的使用寿命。进料采用工业甲醇时,水醇比在0.5以下较为合适。
符号说明:
| b | - 管壁厚,m | ${{\widehat{R}}_{i,r}}$ | - 反应r中i组分摩尔生成速率,kmol⋅m-3⋅s-1 |
| C | - 积炭含量,%(wt) | $\mathop{S}_{f}^{h}$ | - 流体熵源项 |
| C2 | - 惯性阻力,m-1 | T | - 多孔介质温度,K |
| Cp,s | - 固体颗粒定压热容,kJ×(kmol×K)-1 | vT | - 速度矢量,m⋅s-1 |
| CAMF | - 累积进料量,gMeOH/gCat | Yi | - 组分i的质量分数 |
| dp | - 催化剂颗粒直径,m | Yv | - 湍流黏度损失,m2⋅s-2 |
| Ea | - 反应活化能,kJ×kmol-1 | e | - 床层孔隙率 |
| g | - 重力加速度,m⋅s-2 | m | - 流体黏度,Pa×s |
| Gv | - 湍流黏度,m2⋅s-1 | $\widetilde{v}$ | - 湍流动量黏度,m2⋅s-1 |
| $\overline{\overline{I}}$ | - 单位矩阵 | ${{v}^{'}}_{i,r}$ | - 第r反应中的i反应物的化学计量数 |
| $\overrightarrow{{{J}_{i}}}$ | - 组分i的扩散通量 | ${{v}^{''}}_{i,r}$ | - 第r反应中的i生成物的化学计量数 |
| ${{k}_{i}}$ | - 反应速率常数,kmol×(kg×h)-1 | ${{\eta }^{'}}_{j,r}$ | - 第r反应中的j反应物的速率指数 |
| Kc | - 初始积炭速率 | ${{\eta }^{''}}_{j,r}$ | - 第r反应中的j生成物的速率指数 |
| Kfc | - 总传热系数,W×(m2×K)-1 | rb | - 床层表观密度,kg⋅m-3 |
| ks | - 固体颗粒导热系数,W×(m×K)-1 | w | - 渗透率,m2 |
| P | - 总压,Pa | l | - 钢热导率,W×(m×K)-1 |
| PA | - 甲醇分压,Pa | $\overline{\overline{\tau }}$ | - 气相剪切力,Pa |
| r | - 反应速率,kmol×(kg×h)-1 | ji | - 失活速率常数 |
| R | - 气体常数,kJ×(kmol×K)-1 | jc | - 积炭速率常数 |
| Ri | - 质量反应速率,kg⋅m-3⋅s-1 |
| [1] | Bos A N R, Tromp P J J, Akse H N . Conversion of methanol to lower olefins. kinetic modeling, reactor simulation, and selection[J]. Industrial & Engineering Chemistry Research , 1995, 34 (11) : 3808-3816 |
| [2] | Soundararajan S, Dalai A K, Berruti F . Modeling of methanol to olefins (MTO) process in a circulating fluidized bed reactor[J]. Fuel , 2001, 80 (8) : 1187-1197 DOI:10.1016/S0016-2361(00)00182-4 |
| [3] | WANG Biao (王彪). Research of fluidized bed reactor for methanol-to-olefins process (甲醇制低碳烯烃流化床反应器的研究) [D]. Shanghai (上海): East China University of Science and Technology(华东理工大学), 2011. |
| [4] | ZHENG Kang(郑康), CHENG You-wei(成有为), LI Xi(李希) . Simulation of fluidized bed reactor for methanol to olefins (MTO) process(甲醇制烯烃流化床反应器的模拟与分析)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报) , 2012, 26 (1) : 69-76 |
| [5] | QI Guo-Zhen (齐国祯). A study on the process of methanol to olefins reaction (甲醇制烯烃(MTO)反应过程研究) [D]. Shanghai(上海): East China University of Science and Technology (华东理工大学), 2006. |
| [6] | Zhuang Y Q, Chen X M, Luo Z H . CFD-DEM modeling of gas-solid flow and catalytic MTO reaction in a fluidized bed reactor[J]. Computers & Chemical Engineering , 2014, 60 (1) : 1-16 |
| [7] | Chang J, Zhang K, Chen H . CFD modelling of the hydrodynamics and kinetic reactions in a fluidised-bed MTO reactor[J]. Chemical Engineering Research and Design , 2013, 91 (12) : 2355-2368 DOI:10.1016/j.cherd.2013.04.023 |
| [8] | HU Hao(胡浩), YING Wei-yong(应卫勇), FANG Ding-ye(房鼎业) . Mathematical simulation on multi-bed adiabatic reactor with indirect heat exchange for MTO reaction(甲醇制烯烃(MTO)多段间接换热式绝热固定床反应器的数学模拟)[J]. Journal of East China University of Science and Technology(Natural Science Edition)(华东理工大学学报(自然科学版)) , 2010, 36 (2) : 180-186 |
| [9] | HU Hao(胡浩). Reasearch of catalytic reaction engineering for methanol-to-olefin process (甲醇制烯烃MTO 催化反应工程的研究)[D]. Shanghai (上海):East China University of Science and Technology (华东理工大学), 2010. |
| [10] | Alwahabi S M, Froment G F . Conceptual reactor design for the methanol-to-olefins process on SAPO-34[J]. Industrial & Engineering Chemistry Research , 2004, 43 (17) : 5112-5122 |
| [11] | Zhuang Y Q, Gao X, Zhu Y P . CFD modeling of methanol to olefins process in a fixed-bed reactor[J]. Powder Technology , 2012, 221 (S1) : 419-430 |
| [12] | Chen D, Grønvold A, Moljord K . Methanol conversion to light olefins over SAPO-34:reaction network and deactivation kinetics[J]. Industrial & Engineering Chemistry Research , 2007, 46 (12) : 4116-4123 |
| [13] | Chen D, Rebo H P, Grønvold A . Methanol conversion to light olefins over SAPO-34:kinetic modeling of coke formation[J]. Microporous and Mesoporous Materials , 2000, 35 (4) : 121-135 |
| [14] | Gao Xi, Zhu Ya-Ping, Luo Zheng-Hong . CFD modeling of gas flow in porous medium and catalytic coupling reaction from carbon monoxide to diethyl oxalate in fixed-bed reactors[J]. Chemical Engineering Science , 2011, 66 (23) : 6028-6038 DOI:10.1016/j.ces.2011.08.031 |
| [15] | Spalart P R, Allmaras S R . A one-equation turbulence model for aerodynamic flows[J]. American Institute of Aeronautics and Astronautics Journal, , 1992, 94 |
| [16] | WANG Yun-dong(王运东), LUO Guang-sheng(骆广生), LIU Qian(刘谦) . The principle of transfer processes(传递过程原理)[M]. Beijing (北京): Tsinghua University Press Inc(清华大学出版社有限公司), 2002 . |
| [17] | WANG Song-han(王松汉) . Design handbook for petrochemical industry(石油化工设计手册)[M]. Beijing (北京): Chemical Industry Press(化学工业出版社), 2002 . |
| [18] | Shackelford J, Alexande W, Por J S K . CRC materials science and engineering handbook,[M]. New York: CRC Press Inc, 2002 . |




