2. 中国空间技术研究院北京卫星制造厂有限公司,北京 100094;
3. 上海汽车集团股份有限公司前瞻技术研究部,上海 201804;
4. 清华大学山西清洁能源研究院,山西 太原 030032
2. Beijing Spacecrafts, China Academy of Space Technology, Beijing 100094, China;
3. Advanced Technology Department, SAIC Motor Corporation Limited, Shanghai 201804, China;
4. Shanxi Research Institute for Clean Energy, Tsinghua University, Taiyuan 030032, China
近年来,环境污染问题日渐突出,氢能作为最清洁的能源之一受到广泛关注。当前,绝大部分氢气通过化石燃料制备得到,加剧了温室效应,而以可再生能源为驱动力的电解水制氢技术将电能转化为化学能,不产生废物排放,被认为是最有潜力的氢气生产途径之一[1-2]。固体聚合物电解质(solid polymer electrolyte, SPE)电解水是一种以固体聚合物作为电解质的电解水技术,具有能耗低、效率高和产氢纯度高等特点[3],能够与风电、光电设备配套使用,避免弃风弃光现象的发生,实现效率最大化。但SPE电解水高昂的制造成本制约了其工业化的步伐,其中双极板和流场成本占整个电堆成本的48%[4],因此,改进双极板对于解决成本问题有重要意义。SPE电解水电解池与质子交换膜燃料电池具有相似的组成结构,双极板在电解池和燃料电池中起传导电子、支撑膜电极的作用[5],要求其具有高电子传导率和优良的耐蚀性。金属双极板成本较低且机械性能较好,受到了研究者的关注。目前,国内外对金属双极板材料的研究主要是对价格低廉的金属基体材料表面改性。其中,磁控溅射法能够在基体表面得到致密、附着力好的膜[6-9]。耐蚀性是评估金属双极板材料的重要指标之一,耐蚀性较差的金属双极板在电解水或燃料电池的工作环境中,极易发生腐蚀溶解,致使膜层乃至基体中的金属元素以离子的形式进入水溶液中,污染膜电极,不利于系统的长久稳定运行[10]。
除材料自身性质外,SPE电解水和燃料电池内部工作环境对于双极板的耐蚀性和耐久性也有显著影响。研究发现,燃料电池内的水溶液体系中可能含有H+、SO42-、Cl-、F-、O2和H2等[11]物质。其中,氯离子会导致燃料电池的稳定性及耐久性变差[12-13],同时其对金属双极板的耐蚀性也有负面影响。氯主要源于反应气体、加湿用水、催化剂和沿海地区大气中的氯凝胶等[14-16]。
为了考察氯离子含量对金属双极板耐蚀性的影响,探究双极板腐蚀机理,本文通过磁控溅射法将Ti、Cr两种耐蚀性较好的金属以一定的比例共沉积在316L不锈钢(SS)基体上,借助电化学方法表征了其耐蚀性,测试得到了不同氯离子含量电解质溶液中材料的极化曲线和电化学阻抗谱。在此基础上,采用分子模拟软件,从分子动力学的角度对材料的腐蚀机理进行了进一步的分析。
2 实验(材料与方法) 2.1 实验材料与仪器316L不锈钢;砂纸;金相抛光剂;铂片电极、硫酸亚汞电极、电解池(天津艾达恒晟科技发展有限公司);硫酸(分析纯),氯化钾(分析纯),乙醇(分析纯),丙酮(分析纯),氧气(纯度≥99.2%)。CHI760E电化学工作站(上海辰华仪器有限公司);MSP-3200T型磁控溅射镀膜机(北京创世威纳科技有限公司);循环水泵。
2.2 实验方法使用800目、1 500目、2 000目3种型号的砂纸及金相抛光剂依次对316L不锈钢片进行打磨,直至钢片表面均匀有光泽。将钢片分别置于乙醇和丙酮中超声清洗,烘干后放置于磁控溅射仪样品架上,抽真空至1 mPa。设定氩气流量为30 sccm,工作压力为0.5 Pa,加热样品至250 ℃。选取Ti靶和Cr靶作为直流溅射靶材,设置靶功率为100 W,预溅射300 s以清洗靶材。为了细化晶粒,提高表面膜层与基体的结合力,以100 W小功率进行Ti、Cr共溅900 s,而后提高靶功率至200 W,继续溅射6 300 s,即得到双极板材料。
采用三电极体系测试材料的耐蚀性,以镀膜不锈钢为工作电极,饱和硫酸亚汞电极为参比电极,铂片为对电极,分别在室温下氧气饱和的0.5 mol·L-1硫酸溶液、10 mg·L-1 KCl+0.5 mol·L-1硫酸溶液、100 mg·L-1 KCl+0.5 mol·L-1硫酸溶液和1 000 mg·L-1 KCl+0.5 mol·L-1硫酸溶液中,测试材料的极化曲线和交流阻抗谱。
2.3 分子模拟采用Materials Studio (MS)软件[17]对材料在含氯电解质溶液中的腐蚀机理进行建模和分子动力学模拟。对于腐蚀模拟来说,腐蚀系统中包含的原子和分子个数较多,计算量较大,并且腐蚀过程主要取决于原子核的位置[18-19],综合考虑计算效果和时间成本,选用Forcite模块[20]进行模拟。由于所研究的双极板材料处于氧气饱和环境下,且Ti、Cr均为易钝化的金属,因而构建Ti-Cr-O模型。优化晶胞结构,步数为1 000。之后构建(111)晶面,将水分子、水和氢离子、氯离子、氧气分子引入体系中,再次进行结构优化。动力学模拟根据实际情况选择正则系综(NVT),通过NHL方法[21-22]控制温度为298 K,模拟步长1.00 fs,总模拟时间定为2 000 ps。
3 实验结果与讨论 3.1 电化学性能测试在316L不锈钢上沉积TiCr膜层,控制磁控溅射Ti、Cr靶功率均为200 W,在氧气饱和的0.5 mol·L-1硫酸溶液、10 mg·L-1 KCl+0.5 mol·L-1硫酸溶液、100 mg·L-1 KCl+0.5 mol·L-1硫酸溶液和1 000 mg·L-1 KCl+0.5 mol·L-1硫酸溶液中,分别对其进行极化曲线和交流阻抗谱测试。
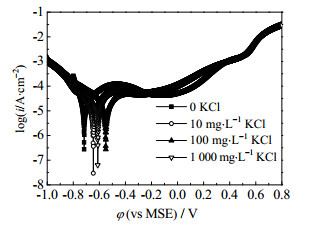
3.1.1 极化曲线测试图 1为TiCr膜层在含不同浓度氯离子的测试电解质溶液中的极化曲线。电位扫描速度为2 mV·s-1。由图 1可知,TiCr合金膜在不含氯离子的电解液中反应电流密度出现较大波动,出现明显的钝化趋势,钝化电位区间内电流密度最低约为10-4.38 A·cm-2。随着电解液中氯离子含量增加,金属的钝化电位区间逐渐变窄。当电位由负向正扫描时,在表面电化学、传质、化学和吸脱附等过程的共同作用下,极化曲线出现图 1所示走向。随着测试电位逐渐正移,到达材料的致钝电位后,材料开始钝化。比较钝化区的电流密度,发现在不含氯离子的电解质溶液中,材料的腐蚀反应电流密度最小,当KCl含量为1 000 mg·L-1时,反应电流密度最大,腐蚀反应发生速率最快,材料耐蚀性最差。可见,TiCr合金膜的耐蚀性受腐蚀介质中氯含量的影响很大,少量氯的加入也会导致材料发生显著的腐蚀。当电位高于过钝化电位后,材料钝态被破坏,进入过钝化区,腐蚀速率增加。
|
图 1 TiCr/SS在不同浓度氯离子溶液中的极化曲线 Fig.1 Potentiodynamic polarization curves of TiCr/SS in solutions with different chloride ion concentrations |
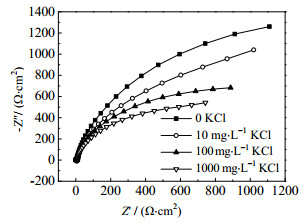
图 2所示为不同腐蚀介质中TiCr膜层在开路电位(OCP)下,振幅10 mV,0.01~106 Hz频率范围内测得的Nyquist交流阻抗谱。在测试频率范围内,谱图呈现出不完整的半圆弧。图 2表明半圆弧直径随电解液中氯离子浓度的增加而减小,即当氯离子含量增加时,材料的反应阻抗逐渐减小,更容易发生腐蚀。
|
图 2 TiCr/SS在不同浓度氯离子溶液中的交流阻抗谱图 Fig.2 EIS results of TiCr/SS in solutions with different chloride ion concentrations |
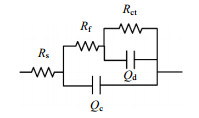
采用图 3所示等效电路图对交流阻抗谱图进行拟合,得到各电路元件参数所对应的数值如表 1所示。其中,Rs为工作电极与参比电极之间溶液的电阻;Rct为电荷转移电阻,与其对应的是电容Qd;Rf代表膜层电阻,Qc为膜电容[23-24]。
|
|
表 1 开路电位下交流阻抗谱拟合电化学参数 Table 1 EIS parameters obtained by equivalent circuits at OCP |
|
图 3 交流阻抗谱拟合电路图 Fig.3 Equivalent circuits for EIS |
由于交流阻抗谱均在氧气饱和的0.5 mol·L-1硫酸溶液中测得,因此,Rs值相差不大,但由于强电解质KCl的加入能够提高电解液的电导率,所以随着氯离子含量增加,Rs值减小,即溶液电阻减小。Rct值越大,材料发生腐蚀反应的阻抗越大,表明其耐蚀性越好。氯离子含量减少后,Rct值有明显增加,材料耐蚀性显著提高,在不含氯离子的电解液中TiCr合金膜耐蚀性最好,这与极化曲线的测试结果一致。对于KCl浓度为1 000 mg·L-1的电解液来说,其交流阻抗谱无法用图 3所示电路准确拟合,可能原因在于高浓度的氯离子对合金膜的腐蚀严重,导致材料表面状态发生较大改变。
从极化曲线和电化学阻抗谱的测试结果中不难发现,溶液中氯离子的加入能够显著影响TiCr合金膜的耐蚀性,随着氯离子浓度增加,材料耐蚀性逐渐降低,即使是少量氯离子也会对金属的耐腐蚀性能造成极大影响。因此,在燃料电池和SPE电解水电解池实际工作过程中,一定要避免混入氯离子,以免使双极板发生腐蚀溶解,影响使用寿命。为了提高燃料电池和电解池工作的稳定性,原料气体和纯水在通入反应体系之前,有必要进行氯含量的检测;反应过程中可通过定期抽检水样的方法实现对体系氯离子浓度的实时监测。
3.2 合金膜层腐蚀机理模拟为了解释TiCr合金膜在含氯电解液中耐蚀性变差的原因,采用分子模拟手段对氯离子腐蚀TiCr合金膜层的机理进行探究。
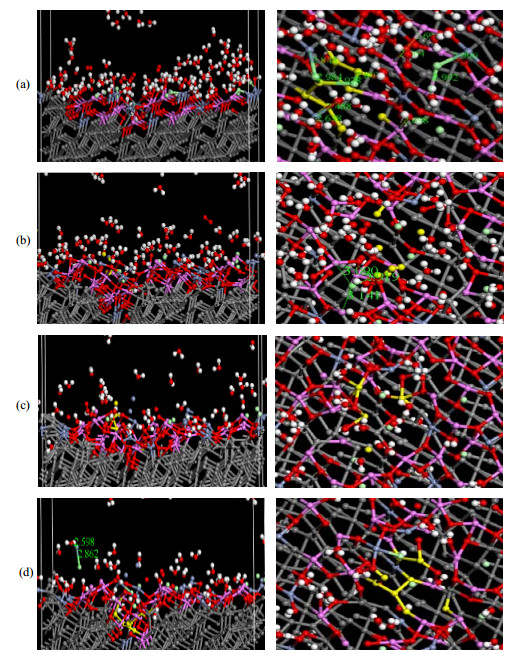
由于TiCr合金处于氧气饱和环境下,且电化学测试结果表明,金属表面发生了钝化,因而选取Ti-Cr-O作为腐蚀模拟的研究主体。实验发现,Ti-Cr-O(111)晶面上的Ti、Cr、O 3种元素能够密排在同一平面上,排列具有规律性和典型性,故以(111)晶面作为研究对象。经结构优化后,结果如图 4(a)所示。氯离子会优先吸附晶面缺陷处和缺陷附近的金属原子,并同时与临近的两个金属原子发生吸附作用,吸附距离在2.8~3.0。水分子中的氧由于电负性较大,也会与表面金属原子吸附在一起,从而造成氯离子与数量占优的水分子在晶体表面的竞争吸附。氧气分子主要分散在距晶面较远的溶液中,并未与晶面产生吸附作用,致使金属表面氧化剂缺失,当金属钝态受到破坏时,将难以实现再钝化。水合氢离子则主要聚集在氯离子周围,但晶格缺陷处没有发现氢离子的分布,猜测原因在于水合氢离子的体积较大,进入晶格缺陷需要突破较大的位阻。
|
图 4 Ti-Cr-O (111)晶面在氯离子溶液中的分子动力学模拟截图(主视图和俯视图) Fig.4 Snapshots taken from molecular dynamics simulation of Ti-Cr-O (111) surface in chloride solutions (front view and vertical view) (a) 0 ps (b) 95 ps (c) 1 000 ps (d) 2 000 ps Color code: red-O, white-H, green-Cl, purple-Ti, blue-Cr, yellow-particles around defects, grey-lower part |
对体系模型进行腐蚀动力学模拟,模拟时间共2 000 ps,截取计算过程中不同时间所对应的构型图,如图 4(a)(b)(c)(d)所示。在95 ps时,原先吸附在金属原子附近的水分子,随着时间的增加而逐渐远离金属表面。晶格缺陷附近,3个金属原子与氯的吸附距离都在3.0 Ǻ左右。1 000 ps时,钝化膜表面的金属原子和氧原子远离最优构型下的晶格位置,表面晶格变形明显,部分Cr原子脱离晶格本体,进入到水溶液中,只有缺陷处的水分子仍处于平衡位置附近,未出现明显位移。与95 ps的模拟结果相比,晶体表面聚集的水分子和氧气分子数减少,氯离子数几乎不变。2 000 ps的截图表明,动力学计算后期,Cr原子溶解进入到溶液中,但溶液中的氯离子并未随金属的溶解而远离晶面,晶体表面的氯离子数目基本保持稳定,以进入到溶液中的Cr为例,如图 4(d)所示,2 000 ps时Cr与水分子中的氧原子间距为2.598 Ǻ,与氯离子之间的距离为2.862 Ǻ,氯离子因受到晶面原子的吸引,未完全远离晶面,缺陷处的氯离子逐渐向晶格缺陷纵深处移动,与此同时缺陷处水分子数目减少。在整个模拟过程中,晶格缺陷周边的原子逐渐溶解到溶液中去,同时氯离子向缺陷内纵深方向迁移,缺陷内部的水分子数目减少,氯离子浓度增加。
根据动力学模拟结果,推测Ti-Cr-O在含氯水溶液中腐蚀的大致过程是:暴露在溶液中的金属原子首先受到氯离子的吸引,偏离原有晶格位置,在平衡位置附近振动;随着时间增加,金属原子在氯离子与水分子的共同作用下扩散到水溶液中,而氯离子受到晶体表面其他原子的吸引倾向于继续吸附在晶面上;处于晶格缺陷处的氯离子受到空间位阻和晶格内部金属原子吸引的共同作用会纵向扩散,导致缺陷底部氯离子含量增加,加速腐蚀。综合以上的分析,在导电基体上沉积金属膜层作双极板时,应该尽量避免表面缺陷的产生,防止腐蚀介质中的氯离子等活性阴离子在膜层缺陷处的大量聚集,加速金属的腐蚀。
4 结论(1) 通过磁控溅射实验在316L不锈钢上沉积TiCr膜层,在不同氯离子含量的电解质溶液中进行电化学测试,极化曲线和交流阻抗谱的表征结果显示,材料的耐蚀性随氯离子浓度的增加而降低,少量的氯离子也会加速TiCr合金膜的腐蚀。
(2) 分子模拟结果表明,电解质溶液中的氯离子会吸附在Ti-Cr-O表面,吸引其中的金属原子,促使缺陷附近的金属原子逐渐溶解,同时缺陷内的氯离子会纵向迁移,使得晶体缺陷内部活性阴离子浓度增加,加速腐蚀。
(3) 燃料电池和SPE电解水系统实际工作过程中,尽量不要混入氯离子,从而减缓双极板腐蚀速率,延长使用寿命。可通过控制原料气体和液体中氯的含量,实时监测工作产水中的氯离子浓度来避免氯对双极板的严重腐蚀。在双极板表面沉积耐蚀膜层时,应尽量避免晶格缺陷的产生,以免膜层局部腐蚀速率过快。
| [1] |
LæDRE S, KONGSTEIN O E, OEDEGAARD A, et al. Materials for proton exchange membrane water electrolyzer bipolar plates[J]. International Journal of Hydrogen Energy, 2017, 42(5): 2713-2723. DOI:10.1016/j.ijhydene.2016.11.106 |
| [2] |
倪萌, LEUNG M K H, SUMATHY K. 电解水制氢技术进展[J]. 能源环境保护, 2004, 18(5): 5-9. NI M, LEUNG M K H, SUMATHY K. Progress of hydrogen production through water electrolysis[J]. Energy Environmental Protection, 2004, 18(5): 5-9. DOI:10.3969/j.issn.1006-8759.2004.05.002 |
| [3] |
杜升飞, 余军, 吴青. SPE水电解催化剂研究进展[J]. 电源技术, 2014, 38(9): 1771-1773. DU S F, YU J, WU Q. Progress of SPE water electrolysis catalyst technology[J]. Chinese Journal of Power Sources, 2014, 38(9): 1771-1773. DOI:10.3969/j.issn.1002-087X.2014.09.056 |
| [4] |
AYERS K E, ANDERSON E B, CAPUANO C B, et al. Research advances towards low cost, high efficiency PEM electrolysis[J]. ECS Transactions, 2010, 33(1): 3-15. |
| [5] |
张军, 任丽彬, 李勇辉, 等. 质子交换膜水电解器技术进展[J]. 电源技术, 2008, 32(4): 261-265. ZHANG J, REN L B, LI Y H, et al. Technology progress of proton exchange membrane electrolyser[J]. Chinese Journal of Power Sources, 2008, 32(4): 261-265. DOI:10.3969/j.issn.1002-087X.2008.04.017 |
| [6] |
ZHANG D M, GUO L, DUAN L T, et al. Preparation of Cr-based multilayer coating on stainless steel as bipolar plate for PEMFCs by magnetron sputtering[J]. International Journal of Hydrogen Energy, 2011, 36(3): 2184-2189. DOI:10.1016/j.ijhydene.2010.10.085 |
| [7] |
ALISHAHI M, MAHBOUBI F, KHOIE S M M, et al. Electrochemical behavior of nanocrystalline Ta/TaN multilayer on 316L stainless steel: Novel bipolar plates for proton exchange membrane fuel-cells[J]. Journal of Power Sources, 2016, 322: 1-9. DOI:10.1016/j.jpowsour.2016.04.133 |
| [8] |
JAROŠ M, MUSIL J, ČERSTVY R, et al. Effect of energy on structure, microstructure and mechanical properties of hard Ti(Al, V)Nx films prepared by magnetron sputtering[J]. Surface and Coatings Technology, 2017, 332: 190-197. DOI:10.1016/j.surfcoat.2017.06.074 |
| [9] |
FENG K, LI Z G. Effect of microstructure of TiN film on properties as bipolar plate coatings in polymer electrolyte membrane fuel cell prepared by inductively coupled plasma assisted magnetron sputtering[J]. Thin Solid Films, 2013, 544: 224-229. DOI:10.1016/j.tsf.2013.03.115 |
| [10] |
SULEK M, ADAMS J, KABERLINE S, et al. In situ metal ion contamination and the effects on proton exchange membrane fuel cell performance[J]. Journal of Power Sources, 2011, 196(21): 8967-8972. DOI:10.1016/j.jpowsour.2011.01.086 |
| [11] |
LI M C, LUO S Z, ZENG C L, et al. Corrosion behavior of TiN coated type 316 stainless steel in simulated PEMFC environments[J]. Corrosion Science, 2004, 46(6): 1369-1380. DOI:10.1016/S0010-938X(03)00187-2 |
| [12] |
EHTESHAMI S M M, TAHERI A, CHAN S H. A review on ions induced contamination of polymer electrolyte membrane fuel cells, poisoning mechanisms and mitigation approaches[J]. Journal of Industrial and Engineering Chemistry, 2016, 34: 1-8. DOI:10.1016/j.jiec.2015.10.034 |
| [13] |
LI H, WANG H J, QIAN W M, et al. Chloride contamination effects on proton exchange membrane fuel cell performance and durability[J]. Journal of Power Sources, 2011, 196(15): 6249-6255. DOI:10.1016/j.jpowsour.2011.04.018 |
| [14] |
YAN W M, CHU H S, LIU Y L, et al. Effects of chlorides on the performance of proton exchange membrane fuel cells[J]. International Journal of Hydrogen Energy, 2011, 36(9): 5435-5441. DOI:10.1016/j.ijhydene.2011.01.158 |
| [15] |
MATSUOKA K, SAKAMOTO S, NAKATO K, et al. Degradation of polymer electrolyte fuel cells under the existence of anion species[J]. Journal of Power Sources, 2008, 179(2): 560-565. DOI:10.1016/j.jpowsour.2008.01.027 |
| [16] |
LI H, ZHANG S S, QIAN W M, et al. Impacts of operating conditions on the effects of chloride contamination on PEM fuel cell performance and durability[J]. Journal of Power Sources, 2012, 218: 375-382. DOI:10.1016/j.jpowsour.2012.07.003 |
| [17] |
Dassault Systèmes BIOVIA. BIOVIA Materials Studio 8.0[Z]. San Diego: Dassault Systèmes, 2014.
|
| [18] |
KHALED K F, AMIN M A. Corrosion monitoring of mild steel in sulphuric acid solutions in presence of some thiazole derivatives - Molecular dynamics, chemical and electrochemical studies[J]. Corrosion Science, 2009, 51(9): 1964-1975. DOI:10.1016/j.corsci.2009.05.023 |
| [19] |
ALLEN M P, TILDESLEY D J. Computer simulation of liquids[M]. New York: Clarendon Press, 1987.
|
| [20] |
KARASAWA N, GODDARD III W A. Acceleration of convergence for lattice sums[J]. Journal of Physical Chemistry, 1989, 93(21): 7320-7327. DOI:10.1021/j100358a012 |
| [21] |
SAMOLETOV A A, DETTMANN C P, CHAPLAIN M A J. Thermostats for "slow" configurational modes[J]. Journal of Statistical Physics, 2007, 128(6): 1321-1336. DOI:10.1007/s10955-007-9365-2 |
| [22] |
LEIMKUHLER B, NOORIZADEH E, PENROSE O. Comparing the efficiencies of stochastic isothermal molecular dynamics methods[J]. Journal of Statistical Physics, 2011, 143(5): 921-942. DOI:10.1007/s10955-011-0210-2 |
| [23] |
NAM N D, JO D S, KIM J G, et al. Corrosion protection of CrN/TiN multi-coating for bipolar plate of polymer electrolyte membrane fuel cell[J]. Thin Solid Films, 2011, 519(20): 6787-6791. DOI:10.1016/j.tsf.2011.01.207 |
| [24] |
MANI S P, RAJENDRAN N. Corrosion and interfacial contact resistance behavior of electrochemically nitrided 316L SS bipolar plates for proton exchange membrane fuel cells[J]. Energy, 2017, 133: 1050-1062. DOI:10.1016/j.energy.2017.05.086 |




