2. 浙江大学 海洋学院, 浙江 舟山 316021
2. Ocean College, Zhejiang University, Zhoushan 316021, China
生物医学[1]和海洋防污[2]等领域一直面临着蛋白质等生物大分子非特异性吸附的困境。蛋白质等在生医材料表面吸附能导致炎症、免疫等许多不良后果,严重影响患者的康复[3]。海洋设备表面易被蛋白质、微生物、动植物吸附,严重影响海洋工程设备的正常使用[4-5]。例如,船体表面的海洋生物附着造成燃耗量大幅度增加,导致经济损失和加剧环境污染[6]。先前采用释放抗生素雷帕霉素等用于生物防污[7],重金属铜等用于海洋防污[8]以抑制生物附着,但因危害环境而逐渐被取代。因此,研究环境友好型防污材料成为当下的热点。其中,携有等量正负电荷的两性离子材料具有亲水性,能在材料表面形成具有能量屏障和物理阻隔能力的水合层,因而具备环境友好的防污性能[9]。然而,该材料稳定性及防污持久性较差。在此基础上,CHEN等[10]将两性离子酯化为两性离子前体以提高其稳定性。当其暴露于水环境中,材料表面附近的酯能逐渐水解转换为具有防污性能的两性离子。随着表面水不断渗透到材料内部,侵蚀的材料表面被新水解的两性离子不断更换,因而长期具备防污性能。
为了制备具有优异防污性能的含两性离子前体材料,JI等[11]制得羧酸甜菜碱酯类似物(carboxybetaine ester,CBE)医用敷料,但其防污性能一般。HUNG等[12]制得甲基取代叔胺型羧酸甜菜碱酯(tertiary carboxybetaine ester,TCBR)生物医学材料,具有优异的防污性能。这是因为缩短了两性离子中氨基和羧基的距离,两性离子的亲水性得以增强。上述研究材料均是通过自由基共聚方式以共价键连接而制得,虽然具有良好的稳定性,但其呈现体相交联状态,在应用上有一定的局限性。继而,WANG等[13]将CBE引入聚氨酯中制得涂层类材料,具有更广阔的应用前景。然而,其耐水性差、机械强度低,存在一定的缺陷。为了实现材料同时具有强效持久的防污性能和物理性能,本文设计合成以乙基取代叔胺型羧酸甜菜碱叔丁酯(tertiary ethyl carboxybetaine t-butyl,TECBT)为两性离子前体的聚氨酯材料。TECBT水解后产生带负电的COO─基团,同时较强碱性的叔胺基团易结合氢离子带上正电荷,形成两性离子。通过憎水基体使两性离子前体的酯水解速度减慢[14],增强材料防污的长效性与耐水性。同时将寡聚四氢呋喃(polytetrahydrofuran,PTMG)引入聚氨酯材料中,进一步改良材料的物理性能[15]。最后采用ATR-IR、接触角表征水解前后聚氨酯材料化学结构、亲水性的变化;并利用蛋白质、细菌、细胞吸附实验表征聚氨酯材料的防污性能。
2 实验部分 2.1 实验材料与仪器2-(乙氨基)乙醇等原料购自TCI(日本)公司。辣根过氧化物酶标记山羊抗人IgG (HRP-IgG)和TMB显色试剂盒均购自Beyotime(上海)公司。
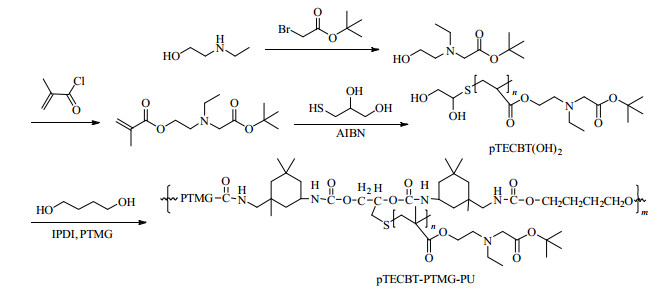
2.2 合成步骤含两性离子前体聚氨酯pTECBT-PTMG-PU的合成线路示于图 1中。最初合成两性离子前体TECBT,接着将TECBT通过自由基聚合的方法与链转移剂α-硫代甘油反应制得双羟基封端的低聚物pTECBT(OH)2,然后将pTECBT(OH)2与异佛尔酮二异氰酸酯(isophorone diisocyanate,IPDI)反应制得异氰酸根预聚体,继而加入PTMG异氰酸预聚体、扩链剂1, 4-丁二醇(1, 4-butanediol,BDO)反应制得pTECBT-PTMG-PU。最后添加交联剂IPDI固化成膜。具体步骤如下:
|
图 1 pTECBT-PTMG-PU的合成路线图 Fig.1 Synthetic route of pTECBT-PTMG-PU |
将2-(乙氨基)乙醇(1.1 eq.),缚酸剂三乙胺(1.1 eq.)溶解于适量无水二氯甲烷(CH2Cl2)中,在冰浴条件下逐滴滴入溴乙酸叔丁酯(1.0 eq.)并搅拌反应6 h。将产物分别用饱和Na2CO3及NaCl溶液萃取提纯。每次萃取后均使用薄层层析(TLC)确保产物无杂质。继而,干燥、过滤、旋蒸制得淡黄色油状化合物。将制得化合物溶解于适量无水CH2Cl2中,加入少许阻聚剂2, 6-二叔丁基对甲酚和三乙胺(1.3 eq.),冰浴条件下逐滴滴入甲基丙烯酰氯(1.2 eq.)并搅拌反应12 h。萃取、干燥、过滤、旋蒸后即得TECBT,产率约为95%。两性离子前体TECBT的结构和纯度通过核磁共振仪(Advance-400M,瑞士Bruker公司)进行1H-NMR表征。
2.2.2 pTECBT(OH)2的合成使用适量无水四氢呋喃(THF)将TECBT (3.0 eq.),α-硫代甘油(1.0 eq.),引发剂2, 2'-二氰基-2, 2'-偶氮丙烷(AIBN) (w = 0.01%)溶解。将体系用N2保护后,60 ℃油浴反应20 h。冷却至室温后,将粗产物用大量正己烷多次沉淀纯化,继而置于干燥箱中42 ℃真空过夜干燥。
2.2.3 pTECBT-PTMG-PU的合成将pTECBT(OH)2 (1.0 eq.)和IPDI (2.5 eq.)溶于无水THF中,油浴65 ℃反应2 h,得到异氰酸根封端的低分量预聚体。向体系中加入PTMG (Mn = 1 000)异氰酸根预聚体,BDO (2.0 eq.),少许催化剂二丁锡继续反应4 h。所得粗产物纯化后置于干燥箱中42 ℃真空过夜干燥。
将pTECBT-PTMG-PU溶于适量乙酸乙酯中,加入IPDI并混匀后,涂于自制的Teflon模具中,常温下使溶剂自然挥发。
2.3 聚氨酯材料的表征 2.3.1 衰减全反射红外光谱(ATR-IR)表征聚氨酯材料的化学结构通过ATR-IR (Vector22,德国Bruker公司)进行表征,扫描范围为4 000~500 cm-1,分辨率为2 cm-1,扫描次数为64次。
2.3.2 表面亲水性表征聚氨酯材料的表面亲水性通过接触角测试仪(Digidrop D-1,法国DBX公司)进行表征,均使用1000 μL螺旋盖注射器将10 μL纯水液滴滴至待测量样品的表面进行测定。
2.3.3 抗非特异性蛋白质吸附性能表征聚氨酯材料通过酶联免疫法(ELISA)测定抗蛋白质吸附能力。将样品置于较强的碱性环境饱和Na2CO3溶液中以加速样品的水解,使其检测更为便捷。具体实验步骤如下:将聚氨酯材料和聚苯乙烯(tissue culture polystyrene,TCPS)均匀剪切成边长约为5 mm正方形样品片,测量并记录各样品边长。继而置于饱和Na2CO3溶液中水解不同的时间。随后将样品用PBS缓冲溶液充分洗涤。将洗涤后的样品和TCPS置于1 mL浓度为1 μg×mL-1的模型蛋白质HRP-IgG中,置于37 ℃水平摇床振荡吸附25 min。充分洗涤样品后加入500 μL的TMB显色液。于水平摇床中振荡显色20 min后取出样品,加入1 mol×L-1的HCl溶液500 μL以终止酶活性。最后,根据酶标仪测定吸光度值(λ = 450 nm)。
2.3.4 抗细菌黏附性能表征聚氨酯材料的抗细菌黏附性能以金黄色葡萄球菌(S. aureus)为革兰氏阳性细菌模型,以大肠杆菌(E. coli)为革兰氏阴性细菌模型进行检测。
以S. aureus为例,具体实验步骤如下:将聚氨酯材料和TCPS片分别置于l×l06 cells·mL-1的S. aureus中,常温吸附2 h后使用Live/Dead®BackLight染色剂染色。充分洗涤后用荧光显微镜(Eclipse Ti-E,日本Nikon公司)在20倍镜头下观察细菌在材料表面的黏附情况。
2.3.5 抗动物细胞吸附性能表征以人脐静脉内皮细胞(HUVEC)为动物细胞模型,对聚氨酯材料的抗动物细胞吸附性能进行表征。具体实验步骤如下:将聚氨酯材料和TCPS片分别置于l×l05 cells·mL-1的HUVEC细胞中,于37 ℃,5%CO2细胞培养箱中共培养24 h后用荧光素二乙酸(FDA)染色,在20倍镜头下观察HUVEC细胞在材料表面的吸附和生长。
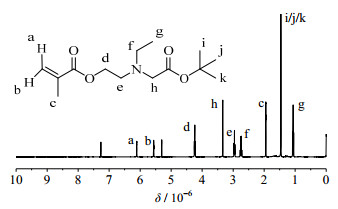
3 实验结果与讨论 3.1 聚氨酯材料的合成分析 3.1.1 两性离子前体TECBT的核磁分析实验合成的TECBT单体的1H NMR(400 MHz, CDCl3)示于图 2中。核磁结果与归属结果如下:6.11 (m,1H),5.56 (m,1H),4.24 (t,3H),3.33 (s,2H),2.96 (t,2H),2.76 (q,2H),1.94 (s,3H),1.49 (s,9H),1.10 (t,3H)。由图可知,产物杂质峰较少,杂质主要为溶剂CH2Cl2和CDCl3,表明实验所合成的TECBT较为纯净。
|
图 2 TECBT的核磁谱图(氘代氯仿) Fig.2 1H-NMR spectra of TECBT (CDCl3) |
IPDI中─NCO基团能与样品中的─OH基团反应,通过扩大聚合物的分子量以制得具有一定物理性能的聚氨酯材料。由表 1及实验观察可知,当IPDI小于4 μL·0.1 g-1时,样品分子量较小,膜片较软较黏,难脱膜具。当IPDI大于12 μL·0.1 g-1时,由于样品分子量较大,膜片较硬且易裂,难溶于溶剂进行GPC测量。当IPDI的用量为8 μL·0.1 g-1,样品分子量适中,呈现最佳的成膜和物理性能。
|
|
表 1 不同IPDI用量下pTECBT-PTMG-PU的分子量 Table 1 GPC results of pTECBT-PTMG-PU under different IPDI dosages |
通过一系列反应,选用最佳交联剂用量,制得的氨酯材料形态示于图 3中。通过观察可知,材料的成膜效果良好,呈透明状,表面致密光滑。将样品弯曲,拉伸表征说明材料具备优异的硬度、弹性等物理性能。

|
图 3 聚氨酯材料的形态图 Fig.3 Digital pictures of PU |
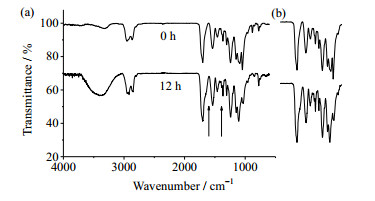
以ATR-IR表征的样品结构变化示于图 4,其中红色曲线表示水解前,蓝色曲线表示饱和Na2CO3水解12 h后。由红蓝曲线对比可知,聚氨酯材料水解后1 640和1 388 cm-1处出现两个新的吸收峰,这是因为水解后生成了COO-基团。另外,3 401 cm-1处的吸收峰明显变宽,这是由于样品水解后产生优异亲水性的两性离子导致出现结合水的峰。
|
图 4 聚氨酯材料的ATR-IR谱图
Fig.4 ATR-IR spectra of PU
(a) before and after hydrolysis (b) spectra between 2 000 cm-1 to 895 cm-1 |
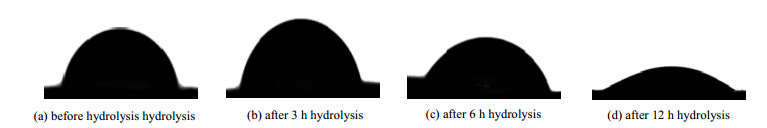
采用接触角表征不同饱和Na2CO3水解时间下聚氨酯材料的亲水性变化。由图 5可知,未水解的聚氨酯材料接触角为(81.5±1)°,水解3 h后接触角为(78.8±1)°,水解6 h后接触角为(56.4±1)°,水解12 h后接触角为(32.4±2)°。由此可知,材料在饱和Na2CO3中水解时间越长,接触角越小,亲水性越强。这是因为聚氨酯材料中越来越多的两性离子前体TECBT被水解成具有强烈亲水性的两性离子。由此说明,水解能增强聚氨酯材料的亲水性。
|
图 5 聚氨酯材料水解前后的接触角 Fig.5 Water contact angles of PU |
ELISA具备很强的灵敏度,能清晰直观地反应聚氨酯材料防污性能的变化。由图 6分析可知,未水解的样品相对蛋白质吸附量为44.78%。饱和Na2CO3水解2 h后,吸附量快速下降至0.98%。经过3 h水解后样品的相对蛋白质吸附量为0.25%,材料呈现最佳防污性能。并且水解12 h后,聚氨酯材料的相对蛋白质吸附量为1.02%,仍然非常低,表明聚氨酯材料具有优异持久的防污性能。与JI等[11]的研究相比,该材料的防污性能及长效性显著提高。与WANG等[13]的研究相比,材料的抗蛋白吸附性能得以提高。这是因为缩短了两性离子中氨基和羧基的距离,进一步提高了防污性能。

|
图 6 聚氨酯材料的相对蛋白质吸附量与水解时间的关系图,以TCPS片为基准 Fig.6 Protein adsorption as a function of hydrolysis time of PU (normalized to TCPS) |
实验采用S. aureus为革兰氏阳性细菌模型。革兰氏阳性细菌以膜蛋白等为黏附因子,故采用组织培养专用的TCPS作为对照组。图 7为TCPS和聚氨酯材料在细菌黏附染色后的荧光照片。由图可知,S. aureus在TCPS表面大量黏附,在未水解的聚氨酯材料表面仅有少量黏附,而在水解后的聚氨酯表面没有观察到细胞黏附。未水解样品中存在少量S. aureus黏附,可能是因为材料于S. aureus吸附的过程中轻微水解产生了对细菌吸附的抵抗力。这与聚氨酯材料的蛋白质抗性一致(见图 6)。而水解后样品无S. aureus吸附说明了聚氨酯材料水解后产生具有防污性能的两性离子,有效抵抗了革兰氏阳性细菌的黏附。

|
图 7 金黄色葡萄球菌表面吸附图 Fig.7 S. aureus bacterial adhesion on the surfaces |
实验选用E.coli为革兰氏阴性细菌模型。革兰氏阴性细菌以菌毛等为黏附因子,不易在TCPS等疏水性材料表面黏附,易在聚乳酸(polylactide,PLA)等亲水性材料表面黏附,故将对照组改用PLA。图 8为PLA和聚氨酯材料在细菌粘附染色后的荧光照片。由图可知,E.coli在PLA表面大量黏附,而在未水解和水解后的聚氨酯材料表面均未观察到细菌黏附。未水解样品亲水性较差,不能使E. coli黏附[16],而水解后材料的防污性能有效抵抗了革兰氏阴性细菌的黏附。

|
图 8 大肠杆菌表面黏图 Fig.8 E. coli bacterial adhesion on the surfaces |
实验采用HUVEC为动物细胞模型。图 9为TCPS和聚氨酯材料在细胞吸附染色后的荧光照片。由图可知,HUVEC在TCPS表面大量吸附,而在未水解和水解后聚氨酯表面均未观察到细胞吸附。未水解聚氨酯材料无细胞吸附可能是因为材料与细胞共培养的24 h内,其轻微水解具有的防污性能就能有效抵抗细胞的吸附。水解后细胞在聚氨酯表面没有吸附,说明了水解后聚氨酯材料能有效抵抗动物细胞的吸附。另外,水解后聚氨酯材料周边的TCPS衬底上有HUVEC吸附生长,并且细胞呈现优异生长状态的梭形。由此表明,材料具有优异的细胞相容性。良好的防污性能及细胞相容性使该材料在生物医学、海洋防污等领域具有优异的应用前景[17]。

|
图 9 HUVEC细胞吸附图 Fig.9 Typical microscopic images of HUVEC cells |
(1) 本文设计合成的两性离子前体TECBT合成简便、纯度高、产率佳,制得的聚氨酯材料具有优异的成膜效果、表面致密性、弹性等物理性能。
(2) 采用ATR-IR和接触角表征说明了聚氨酯材料水解后能形成亲水性的两性离子,具有防污性能。
(3) 防污实验表明聚氨酯材料能强效长久地抵抗蛋白质吸附。其中,饱和Na2CO3水解3 h后呈现最佳防污效果,相对蛋白质吸附量仅为0.25%。同时,聚氨酯材料能有效的抗细菌黏附和动物细胞吸附,并且具有优异的生物相容性。
| [1] |
RATNER B D, BRYANT S J. Biomaterials:Where we have been and where we are going[J]. Annual Review of Biomedical Engineering, 2004, 6(1): 41-75. DOI:10.1146/annurev.bioeng.6.040803.140027 |
| [2] |
SILVA E R, FERREIRA O, RAMALHO P A, et al. Eco-friendly non-biocide-release coatings for marine biofouling prevention[J]. Science of The Total Environment, 2019, 650: 2499-2511. DOI:10.1016/j.scitotenv.2018.10.010 |
| [3] |
GROEN N, GUVENDIREN M, RABITZ H, et al. Stepping into the omics era:Opportunities and challenges for biomaterials science and engineering[J]. Acta Biomaterialia, 2016, 34(1): 133-142. |
| [4] |
YEBRA D M, KIIL S, Dam-Johansen K. Antifouling technology-past, present and future steps towards efficient and environmentally friendly antifouling coatings[J]. Progress in Organic Coatings, 2004, 50(2): 75-104. DOI:10.1016/j.porgcoat.2003.06.001 |
| [5] |
CALLOW M E, CALLOW J E. Marine biofouling:A sticky problem[J]. Biologist, 2002, 49(1): 10-14. |
| [6] |
SCHULTZ M P. Effects of coating roughness and biofouling on ship resistance and powering[J]. Biofouling, 2007, 5(23): 331-341. |
| [7] |
CHAPMAN R G, OSTUNI E, TAKAYAMA S, et al. Surveying for surfaces that resist the adsorption of proteins[J]. Journal of the American Chemical Society, 2000, 122(34): 8303-8304. DOI:10.1021/ja000774f |
| [8] |
MA C, ZHANG W, ZHANG G, et al. Environmentally friendly antifouling coatings based on biodegradable polymer and natural antifoulant[J]. ACS Sustainable Chemistry & Engineering, 2017, 5(7): 6304-6309. |
| [9] |
CHEN S, JIANG S. An new avenue to nonfouling materials[J]. Advanced Materials, 2008, 20(2): 335-338. DOI:10.1002/adma.200701164 |
| [10] |
CHEN S, LIU L, JIANG S. Strong resistance of oligo(phosphorylcholine) self-assembled monolayers to protein adsorption[J]. Langmuir, 2006, 22(6): 2418-2421. DOI:10.1021/la052851w |
| [11] |
JI F, LIN W, WANG Z, et al. Development of nonstick and drug-loaded wound dressing based on the hydrolytic hydrophobic poly(carboxybetaine) ester analogue[J]. ACS Applied Materials & Interfaces, 2013, 5(21): 10489-10494. |
| [12] |
HUNG H, JAIN P, ZHANG P, et al. A coating-free nonfouling polymeric elastomer[J]. Advanced Materials, 2017, 29(31): 171-178. |
| [13] |
WANG G, WANG L, LIN W, et al. Development of robust and recoverable ultralow-fouling coatings based on poly(carboxybetaine) ester analogue[J]. ACS Applied Materials & Interfaces, 2015, 7(31): 16938-16945. |
| [14] |
OZCAN S, KANER P, THOMAS D, et al. Hydrophobic antifouling electrospun mats from zwitterionic amphiphilic copolymers[J]. ACS Applied Materials & Interfaces, 2018, 10(21): 18300-18309. |
| [15] |
KIM H. LEE T, HUH J, et al. Preparation and properties of segmented thermoplastic polyurethane elastomers with two different soft segments[J]. Journal of Applied Polymer Scienc, 1993, 73(2): 345-352.
|
| [16] |
CHEN X, SONG D, XU J, et al. Role and mechanism of cell-surface hydrophobicity in the adaptation of sphingobium hydrophobicum to electronic-waste contaminated sediment[J]. Applied Microbiology and Biotechnology, 2018, 102(6): 2803-2815. DOI:10.1007/s00253-017-8734-2 |
| [17] |
张娟, 林伟锋, 陈圣福. 基因传递材料聚羧酸甜菜碱酯的细胞毒性及转染研究[J]. 高校化学工程学报, 2012, 26(6): 994-1000. ZHANG J, LIN W F, CHEN S F. The cytotoxicity and the application of poly (carboxybetaine methacrylate ester) as a gene carrier[J]. Journal of Chemical Engineering of Chinese Universities, 2012, 26(6): 994-1000. |




