2. 国家复合改性聚合物材料工程技术研究中心,贵州 贵阳 550014
2. National Engineering Research Center for Compounding and Modification of Polymer Materials, Guiyang 550014, China
膜是指在一种流体相内或两种流体相之间,把流体相分成两部分的二维材料,它可以是固相或液相,被分离的流体可以是液态或者气态。膜分离技术涉及到高分子物理及化学、材料科学和化学工程等交叉学科知识,被认为是最重要的工业技术之一。相比于传统的吸附、蒸馏或萃取等分离技术,膜分离具有无可比拟的优势:1)高效,膜的孔隙结构可选择性透过某些物质,实现高效分离、提纯和浓缩等目的;2)节能,膜分离无需高能耗的投入,成本较低;3)接近室温工作温度,绝大部分膜在室温条件即可分离纯化,工作环境温和;4)绿色环保,膜分离过程极少产生环境污染物,多为对烟气、废水等物质进行纯化分离;5)工作稳定性高,一般的膜材料结构稳定,力学性能较好,且耐酸碱,具有优异的可持续工作性[1-2]。
膜通过以下两种原理实现物质的分离:(1)基于质量、体积等物理性质的不同而实现分离,比如微滤膜就是根据颗粒的大小差异从而去除0.1~5 μm的固体杂质;(2)基于物质的化学性质差异,物质通过分离膜的速度由两部分构成:进入膜表面的接触速度以及运动到另一表面的扩散速度,其中扩散速度是决定性的,被分离物质在膜中的扩散与其性质密切相关[2-3]。目前分离膜材料主要以有机基体及无机基体为主,其中无机膜材料一般有分子筛、金属氧化物、沸石、陶瓷等,存在成本高、分离性能差、自身结构缺陷、加工困难等缺点,市场应用规模较小;而有机基体膜材料市场规模大,具有成本较低,易于制造,环境稳定性好等优势[4]。纤维素是地球上含量最为丰富的天然高分子材料,具有绿色环保、可降解、储量大、机械性能优异、生物相容性等优势,一直被认为是理想的膜材料,已经引起了越来越多的关注[5-7]。文章介绍了近些年来关于纤维素基膜材料的制备以及应用方面的研究工作,重点是在水处理、气体分离、生物医用、手性拆分、电池隔膜等领域的研究进展。最后对纤维素基膜材料目前存在的问题及其发展前景做了展望。
2 水处理膜工业废水及生活污水中存在的重金属、有机染料、生物抗生素等污染物给全球水资源、环境以及人类健康造成了巨大压力,通过膜技术去除污染物,实现污水的纯化具有深远的现实意义。
刘蕾蕾等[8]制备出三醋酸纤维素(TCA)正向渗透膜,其水通量为6~7 L·(m2·h)-1,且对NaCl的截留率达到95%以上。ZHANG等[9]在碱-尿素以及碱-硫脲5种不同的溶剂体系中制备出再生纤维素膜,具有12.77~17.09 nm的类似于典型超滤膜的孔隙结构,油水实验表明截油性能达到98%,水通量恢复率在90%左右,在强酸、碱体系中浸泡一周,性能无明显变化,显示出优异的耐酸碱性能。
通过物理或者化学方式得到的复合膜同样具有优异的分离性质。李国亮等[10]制备出以涤纶网为增强基层的醋酸纤维素(CA)膜材料,亲水性较好,孔隙率达到74.2%,在pH=2~11性能稳定,水通量和截留率分别达到3.78 L·(m2·h)-1和95.65%,具有优异的循环使用性。苏林梅等[11]以CA为原料,和尿素反应得到醋酸纤维素氨基甲酸酯(CAC)膜材料,发现CAC的拉伸强度以及水通量高于CA,且随着取代度的增加,CAC的性能呈现逐步提高的趋势。NGUYEN等[12]制备出三醋酸/醋酸纤维素正向渗透膜(TCA/CA),相比于商业化的正向渗透膜,该膜具有更高的亲水性和光滑的表面,抗污染性较好,同时发现,TCA含量的增加会提高耐盐性,在废水处理及海水淡化等领域具有潜在应用价值。KIM等[13]通过聚间苯二酰胺接枝甲基丙烯酰胺对CA进行修饰,以改变超滤膜表面性质并提高抗污垢能力,修饰后的膜接触角减小,亲水性明显提高;对牛血清蛋白质的分离发现,蛋白会在该膜表面均匀覆盖,而对于纯CA膜,蛋白质则覆盖不均一,研究发现这种差异性是由于复合膜表面的酰胺基团以及较小的膜孔径对蛋白质阻抗能力优异造成的。GOETZ等[14]通过甲壳素纳米晶修饰CA,静电纺丝制备出超亲水抗油污膜,甲壳素加入后不仅显著提高了膜强度,而且会对表面结构特征产生影响,促使膜的接触角显著减小,使膜对抗牛血清蛋白与酸性污染溶液都具有很好性质。SITKO等[15]制备出氧化石墨烯-纤维素复合膜用于水中钴、镍、铜、锌、镉和铅等二价金属离子的分离,动力学实验表明金属离子在膜表面是单层分布的,是基于氧化石墨烯的含氧基团与离子的络合作用,膜对金属离子的分离能力为Pb2+ > Cu2+ > Cd2+ > Zn2+ > Ni2+ > Co2+,且膜的重复使用性较好,在分析化学领域用于痕量或超痕量金属离子分析具有潜在意义。FAN等[16]利用编织增强技术制备出醋酸纤维素中空纤维膜,添加少量聚丙烯腈,不仅可保证良好的膜界面结合,而且克服了膜长期使用存在的溶胀问题,随着聚丙烯腈含量的变化,膜拉伸强度从6.0到62.9 MPa不等,在牛蛋白过滤方面显示出同商业化PVDF膜相似的优异性能,并且可通过化学清洗恢复膜通量以实现膜的重复利用。
工业废水的排放使得水源中的硼污染呈上升趋势,对环境、水资源以及人体健康带来不可忽视的危害[17-18]。WEI等[19]通过原子转移自由基聚合(ATRP)技术在纤维素表面接枝聚甲基丙烯酸缩水甘油酯,继续和N-甲基葡糖胺反应,通过环氧烷开环得到多羟基结构。制备的膜材料具有亲水性,对硼元素最大吸附量达到0.75 mmol·g-1,原位红外检测发现羟基和叔胺是硼元素主要结合位点。ASIM等[20]以纤维素纳米晶、阿拉伯树胶为基质,利用聚乙烯醇等为交联剂制备出抗菌、抗氯、除硼性能好的多孔交联膜,最优除硼效果达到92.4%,由于阿拉伯树胶和大肠杆菌存在静电斥力,使膜的抗菌活性明显提高,阻碍了细菌在膜表面的附着。
3 气体分离膜气体分离膜是在以压力差为推动力,利用气体混合物中各组分在膜中渗透速率不同而使各组分气体分离的膜材料。其原理包含溶解扩散过程,首先气体分子与膜接触并在表面吸附溶解;然后,在膜内部扩散最终到达膜的透过侧;最后,在膜的透过侧发生解析而实现气体分离[21]。操作中不发生相变,无需使用分离试剂,具有节能、环保、高效、方便等优势[22]。
ANSALONI等[23]研究纤维素纳米纤维(CNF)膜对CO2的分离捕获能力,发现CNF膜对CO2/N2、CO2/CH4的选择性好,但对CO2的渗透性较差。为提高CO2的膜通量,将其与商业聚乙烯胺复合,发现复合膜渗透性显著增加而选择性减小,但聚乙烯胺亲水,长时间接触水汽会发生溶胀,导致综合性能下降。LU等[24]将三醋酸纤维素(TCA)膜置于单甘醇和三甘醇溶液中处理后,发现其对CH4和CO2的渗透性增加,认为是由于在醇溶液中溶胀,导致自由体积增大,促进气体的扩散;对H2S气体脱硫发现,不会类似传统膜发生塑化溶胀,其脱硫性能非常优越。LU[25]还研究了甲苯和二甲苯溶液在不同压力下对TCA膜分离性质的影响,发现在低压氛围中,对CH4和CO2的渗透性较差,但高压条件下,溶剂对膜存在塑化作用,膜的自由体积增大,渗透性提高。
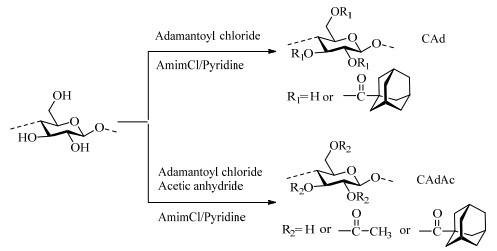
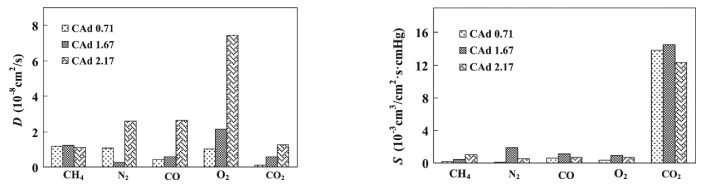
近些年来,混合基质膜(mixed matrix membrane,MMM)发展迅速,合适的聚合物及无机填料可提高膜的气体分离性,这是因为聚合物和填料之间的界面形貌对气体运输有影响,包括硅烷偶联、掺入添加剂、移植、原位聚合等方法都可提高相容性[26]。MUBASHIR等[27]在CA中掺入NH2-MIL-53(Al)金属有机框架物,发现NH2-MIL-53(Al)提高了CO2/N2以及CO2/CH4混合气体中CO2的渗透率,在掺杂量为w = 15%时,分离效果达到最优。SANAEEPUR等[28]通过硅烷化反应来修饰微型纳米沸石,再将其掺入CA膜用于CO2/N2的分离,研究发现复合膜对CO2的渗透性高于纯CA膜。SANAEEPUR等[29]又通过离子交换制备出含二价钴离子的沸石,再掺入CA中进行CO2/N2的气体分离,复合膜的形貌以及结构更加改善,当掺入w = 15%的改性沸石后,CO2的渗透率比纯CA提高了17.3%,比未经改性的沸石复合膜提高了44.4%。气体分离膜难点在于控制渗透性和选择性间的平衡,高渗透膜缺乏选择性,而好的选择性又造成渗透性差,因此通过膜材料的结构设计来实现两者的平衡具有一定挑战性。金刚烷及其衍生物作为一类具有大位阻的刚性环状基团物质,可赋予膜材料较大的自由体积,而提高膜的综合性能[30]。CHEN等[31]通过1-烯丙基-3-甲基咪唑氯盐离子液体制备出金刚烷纤维素膜(CAd)和醋酸/金刚烷混合纤维素酯膜(CAdAc),如图 1示。CAd的溶解性、热稳定性好,通过调节金刚烷的取代度可实现对自由体积拓扑结构的调控。基于气体的溶解-扩散机理,对膜进行气体分离检测,图 2为膜的扩散系数(D)和溶解度系数(S),发现随着取代度(degree of substitution,DS)的增加,膜对小分子气体如O2、CO的渗透率增加,但对大体积的分子如CH4透过率却减少,金刚烷DS = 2.17时,其渗透率达到最大,这是因为DS的增加使得分离膜的自由体积分数减小,从而阻止大体积气体的透过。
|
图 1 在AmimCl离子液中合成金刚烷纤维素(CAd)和醋酸/金刚烷混合纤维素酯(CAdAc)[31] Fig.1 Synthesis of cellulose adamantanes (CAd) and cellulose adamantane acetates (CAdAc) in AmimCl[31] |
|
图 2 CAd0.71, CAd1.67和CAd2.17的扩散系数和溶解度系数[31] Fig.2 Diffusion coefficients and solubility coefficients of CAd0.71, CAd1.67 and CAd2.17[31] |
生物医用膜要求材料具有良好的生物相容性、稳定性以及较强的机械性能,而纤维素的特殊结构完全符合生物医用膜的要求,因而在血液净化、可控释放、组织工程等方面应用广泛[32-34]。
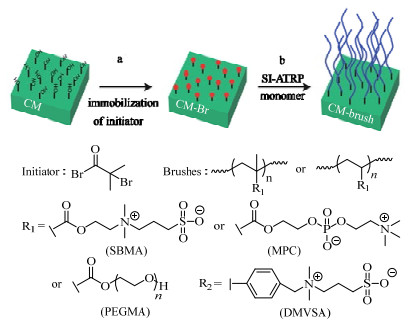
鲍方毅等[35]用壳聚糖溶液包覆法制备出透明纤维素共混膜,该膜的氧气阻隔性优异,渗透系数低于商品化乙烯-乙烯醇共聚物膜,而且对金黄色葡萄球菌具有很好的抵抗性。对纤维素基材料进行离子化修饰,也可得到高抗污染的膜。WANG等[36]首先制备出具有两性离子结构的烷氧基硅烷偶联剂,再将其和纤维素进行缩合反应得到两性化的纤维素膜材料,研究发现膜的抗污染性、血液相容性和细胞相容性较好。LIU等[37-38]通过ATRP技术对纤维素进行两性离子化表面改性(图 3所示),研究了改性前后膜的表面结构、形貌和热稳定性、蛋白质和血小板黏附等性能差异,实验发现改性后的膜具有很好的抗生物蛋白变质以及抗污染能力;对膜进行细胞毒性研究,经过7天的培养,发现在改性后的膜环境中几乎没有细胞死亡,但在初始纤维素膜环境中的细胞却发生死亡,表明两性离子化的纤维素膜具有优良的细胞相容性;细胞黏附性结果也发现在初始纤维素膜的表面会发生细胞的吸附,而在改性膜表面的细胞则会以圆形状悬浮,实验结果说明两性离子化纤维素膜具有优良的抗污染能力。
|
图 3 纤维素膜(CM)的表面改性示意图[38]
Fig.3 Schematic illustration of surface modification of cellulose membranes (CM) [38]
a. immobilization of initiator on CM surface through the esterification reaction b. grafting of zwitterionic brushes and PEGMA brush on CM through SI-ATRP |
部分贵金属具有天然生物抗菌性,和纤维素基膜材料复合后综合性质优异。FU等[39]制备出银/氧化锌修饰的纤维素纳米复合薄膜,银/氧化锌平均粒径为16.5 nm,细胞相容性较好,在3 h之内就可以实现对大肠杆菌以及金黄色葡萄球菌的灭菌。TANG等[40]探索银/氧化石墨烯复合物来修饰纤维素薄膜,SEM发现嵌入银/氧化石墨烯的膜表面具有规整的多孔结构,且对抑制金黄色葡萄球菌以及大肠杆菌的生长非常有效。ANIRUDHAN等[41]以金沉积方式制备出金修饰的纤维素基膜,皮肤刺激测试发现该膜具有很好的抗微生物生长性,适合在皮肤载药方面长期使用。
LIU等[42]采用ATRP技术将膦酸盐物质接枝到纤维素膜表面并用于蛋白质的分离,发现其对富含精氨酸的蛋白质具有选择性分离的作用,分离容量达到12 mg·mL-1,远高于聚对苯二甲酸乙二酯(PET)支撑膜,证实了膦酸酯基团以及N-(2-羟丙基)甲基丙烯酰胺是实现蛋白质强结合的关键。YU等[43]采用亲核加成方式,利用二乙烯基砜(DVS)将蛋白质和DNA等以共价键形式固定在纤维素的羟基上,经过碳寡核苷酸修饰的纤维素膜具有特异的生物活性、长期稳定性特点,在分子检测、诊断、环境监测等方面具有潜在应用。VOICU等[44]对CA功能衍生化,将丝胶固定在膜表面,该膜对牛血清蛋白和血红蛋白的保留率分别达到91%和96%,这主要是因为血红蛋白的分子结构大,容易在膜表面堆积而难以透过膜,因此保留率更高;且通过细胞毒性测试证明膜可以支持细胞的黏附和生长,且能够促进细胞增殖。
酶是保证生命体正常运转而不可缺少的物质之一。MURTINHO等[45]将过氧化氢酶、醇氧化酶、葡萄糖氧化酶固定在纤维素酯衍生物膜上,发现酶的催化活性和稳定性没有受到影响,证明纤维素酯是酶固化反应的有效支撑材料。BALDINO等[46]在CA中加入溶菌酶使其具有抗菌性,采用超临界相转化法制备膜,酶均匀分布在膜中,可作为潜在活性包装材料。SUKSAEREE等[47]利用乙基纤维素和脱蛋白天然橡胶胶乳制备出酮洛芬载药膜,其体外释放和皮肤渗透性优良,载药性较好。LIN等[48]制备出具有双面膜结构的凝胶,内层为阳离子化纤维素纳米晶(CCNC),外层为阴离子海藻酸,其形貌可控调节,内层的CCNC具有“纳米阻挡效应”和“纳米锁定效应”,可以实现药物的可控释放,在药物包装方面具有潜在意义。SOFIA和RAQEL等[49-50]以纤维素硫酸酯作为膜材料来纯化流感病毒,结果表明配体密度、膜渗透性、流速和盐浓度对分离性影响较大,在针对性疫苗生产方面具有指导作用。
5 电池隔膜锂离子电池是近年来的研究热点,它具有能量密度高、循环寿命长、自放电率低等优点,已成为数码产品、电动汽车等领域的宠儿[51-52]。隔膜材料作为电池的组件之一,不仅要保证离子的顺利通过,而且还需阻断电子的运输,其物理化学性质不仅决定了电池的结构、内阻等参数,更是影响到电池容量、循环寿命以及安全性能等特性,因此隔膜的优异关乎到电池的综合性能[53-54]。锂电池对隔膜的要求较高,需要具有如下性质:1)电子绝缘性,在电池的正、负极之间需要机械隔离;2)耐电解液腐蚀,具有较好的热、化学及电化学稳定性;3)低电阻,高离子电导率,适宜的孔隙率;4)机械性能高,耐刺穿,空间稳定性好;5)电解液浸润性好[53, 55]。市售的锂电池隔膜主要为聚乙烯、聚丙烯以及两者的复合膜,具有电化学稳定性好、膜厚度适宜等优点,然而却存在电解液浸润性差、低孔隙率、热稳定性差等缺点,而纤维素基材料的超分子结构赋予其优良的物理化学稳定性、机械性好等优点,有望成为新一代锂电池隔膜[56]。
WENG等[57]对CA水解制备出多孔的纤维素隔膜,具有随机取向、完全连通的三维纤维网状结构特征,孔隙率高达76%,电解质润湿性良好以及高电解质吸收能力,相比于商业化的聚丙烯隔膜,该多孔膜具有更高的离子电导率,较低电阻以及更好的电化学稳定性。LIAO等[58]在商业聚丙烯膜表面涂覆一层绿色环保、廉价的羟乙基纤维素来提高膜的离子导电率,与未涂覆的聚丙烯膜相比,复合膜具有优异的尺寸稳定性,高电解质吸收率,高离子电导率和更好的循环性能,可作为一种有效的方法来改性商业化隔膜。BORIBOON等[59]将二氧化钛嵌入CA中作为电池隔膜,二氧化钛嵌入CA后制备出的复合体材料的粒径大小在310 nm左右,其分解温度在300 ℃,远高于聚乙烯隔膜的220 ℃,添加的二氧化钛颗粒提高了电解质润湿性,并将锂离子转移数从0.22提高到0.62,经过30个循环周期后,其容量为79 mA·h·g-1。ZHANG等[60]以偶氮二异丁腈(AIBN)为引发剂将聚(乙二醇)甲基丙烯酸甲酯(PEGMEM)和甲基丙烯酸十八烷基酯(SMA)共聚,得到PEGMEM-co-SMA的共聚物,继续和双三氟甲烷磺酰亚胺锂(LiTFSI)以及纤维素基质混合制备出复合电解质隔膜,研究发现其电化学稳定窗口宽(> 5V vs Li/Li+)、离子导电率高以及热稳定性高达315 ℃,且电阻较低,放电容量高达156.9 mA·h·g-1;在熔点以上,共聚物的黏流性所带来的渗透作用,可保证在充放电过程中与电极表面的均匀接触。KANG等[61]采用电纺丝技术制备出CA/PVDF气凝胶复合电解质膜,研究发现CA:PVDF的质量比2:8时,其性能达到最优,强度达11.1 MPa,电解质吸收率达到768.2%,在80 ℃条件不收缩,离子导电率为2.61×10-3 S·cm-1,循环性好,容量高达204.15 mA·h·g-1,综合性能优越。
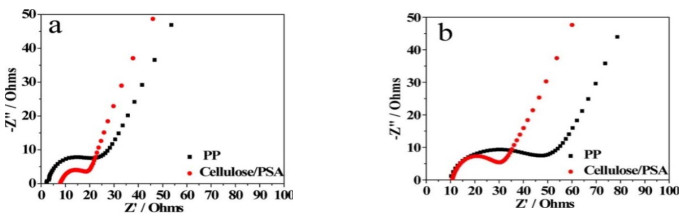
XU等[62]制备出纤维素/聚磺酰胺复合隔膜,通过SEM测试发现,采用单轴拉伸技术制备的商业PP膜表面是椭圆孔,不施加压力制备出的复合膜呈现出大尺寸且不规则的孔洞,这在电池充放电过程中是不安全的;而在施加20 MPa压力制备的膜,膜的交织孔隙减小到纳米孔,结构紧凑,有利于防止内部短路,避免电池自放电[63];纤维素/聚磺酰质量比在3:1时,机械性能强度最高达到17 MPa,此时纤维素相当于一个很好的骨架作用。与商业化的PP膜进行物理化学性质的对比,表 1中复合膜的孔隙率为66%,高于商业PP膜为55%;且复合膜的高孔隙率表面和低表面能使其透气率为60 s,远远低于商业的PP膜;膜厚度决定电解质浸没高度,在电池充放电过程中,优越的润湿性有助于电解液的填充。隔膜的热稳定性对锂离子电池的安全性起到了重要的作用,因为它们可以保持阳极和阴极分开而防止高温条件下发生短路甚至爆炸。纤维素/聚磺酰胺复合膜在200 ℃依旧可以保持原始的膜尺寸,而商业PP膜发生了热收缩,说明复合膜的热稳定性明显优于PP膜材料。对膜材料进行电性能的测试(图 4),发现以锂钴氧化物/石墨做电解质,在第一个充放电循环后,复合膜的电阻为18 Ω,略低于商业PP膜的20 Ω,而经过100个循环后,出现明显的差异,复合膜的电阻增加到30 Ω,但PP膜电阻增加较多,达到60 Ω,电池的电阻越低则电解液的吸收越高。经100个循环后其容量保持率为85%,经过电解液浸泡后,展现出1.2×10-3 S·cm-1高离子导电率,这是由于电解液和隔膜之间的协同作用决定的。
|
|
表 1 PP分离膜和纤维素/PSA复合膜的物理性质[62] Table 1 Physical properties of PP and cellulose/PSA composite membranes[62] |
|
图 4 电池(a)第一周期和(b)第100周期后测量的Nyquist图[62] Fig.4 Nyquist plots for cells measured after the (a) first cycle and (b) 100th cycle[62] |
手性分子是指化学中结构上镜像对称而又不能完全重合的分子,会形成左旋式和右旋式分子,它们物理性质相同,但化学性质却可能存在很大差异[64]。手性拆分膜因具有低能耗、环境友好、节约时间、设备简洁、可连续工作等优点,已成为手性物质分离的主流方法[65]。其制备方法主要有3种:第1种是基膜改性和修饰法,一般通过涂覆、浸渍、接枝等方式,将具有手性识别功能的物质负载到支撑层上,基膜支撑层包括聚砜、聚酰胺、纤维素等材料,识别分子主要为氨基酸类手性物质[66];第2种是直接成膜法,使用具有手性识别功能的材料,如环糊精、甲壳素、壳聚糖等天然物质,直接成膜,其最大的特点就是简单易行,但此种方法制备的膜适用范围较窄,对大部分手性物质的普适性不高[67];第3种是分子印迹法,当模板分子(印迹分子)和聚合物单体接触时,会形成多重作用点,单体通过聚合会记下这种作用,除去模板分子后,聚合物就形成与模板分子空间构型相匹配的空穴,当模板分子及其结构类似的手性物质接触分离膜时,就会发生特异性选择识别,从而将对映体拆分开来[68]。
纤维素结构天然存在大量手性碳,其本身或衍生物可直接用于手性分离。传统纤维素基手性材料是通过物理涂层的方式来制备,最早是将介孔硅胶、氧化锆等无机物嵌入纤维素基材中,其流动相多采用己烷/异丙醇以及水/乙腈等混合体系,而制备出的膜对外消旋体也有一定的分离效率[69-71]。但无法采用四氢呋喃、氯仿和丙酮等溶剂,因为会破坏纤维素衍生物的结构,后来就将纤维素衍生物固定在支架上[72],一般以两种方法来固定:第1种是将纤维素衍生物附着在固体上形成一个刷层[73];第2种是将纤维素衍生物交联[74],两种方式都需要纤维素衍生物具有功能性,但衍生化引入其它基团会改变原始的空间结构而导致手性识别能力的改变,因此控制基团在纤维素侧链上的数量和分布至关重要。
ZHAO等[75]采用CA膜来对二苯乙烯氧化物进行拆分,发现膜对反式结构的选择性好,在CA浓度为w = 30%、DMF浓度为w = 25%的丙酮浇注液中,可达到85%的拆分效果,这归因于手性碳、色散力、偶极-偶极、氢键等因素作用而实现对手性物质的识别。
ZHENG等[76]采用分子印迹法,以邻苯二酚为模板分子,加入到纤维素的DMAc/LiCl溶液中,通过控制模板分子用量来调节膜的印迹率。对二甲苯异构体进行手性拆分,发现膜对邻二甲苯具有很好的选择分离性,而对于间二甲苯以及对二甲苯的拆分较差,这是由于印迹分子和邻二甲苯的结构相似。YOSHIKAWA等[77]以谷氨酸为印迹分子制备出CA印迹膜,该膜提供了一种对氨基酸进行选择分离的方法。JIANG等[78]将硝化纤维素膜(CN)用于D-L酪氨酸的手性识别,基于主链结构上的手性碳,并有可能形成螺旋结构,促使其具有对映选择性。LI等[79]以ZrO2改性的氧化铝膜作为模板,制备出CA分子印迹膜用于对映体的分离,研究发现在w = 15%含量时,分离性质达到最优,其对扁桃酸的选择性以及渗透性远高于苹果酸和乳酸,分离因子高达35。
WANG等[80]制备出纤维素醋酸-丁酸膜(CAB)用于二苯乙烯氧化物对映体的拆分,发现在溶质浓度为w = 15%、DMF浓度为w = 30%的丙酮浇注液中,最高可实现92%手性体的分离。FLORES等[81]制备出纤维素醋酸-丙酸酯(CAP)/CA复合膜来拆分二苯乙烯氧化物对映体,不同浓度配比如表 2所示,实验发现在控制CA浓度为w = 18%不变时,随着CAP浓度从0增加到w = 8%,膜对手性物质的渗透性逐步下降,而手性拆分效果逐步增加,选择性最高可达到97%,认为是随着CAP浓度增加,膜的结构变得更加紧凑,自由体积分数减小,从而使得膜通量减小,但更加有利于膜选择性的提升;同样在控制CAP浓度不变时,膜的性能变化趋势结果也几乎一样。该研究为纤维素基手性拆分膜的基础研究提供重要参考价值。
7 展望与结论文章介绍了分离膜技术的特点,阐述了纤维素在膜领域的高值化利用,同时对近年来国内外关于纤维素基膜材料的制备、性能进行了总结,综述了其在水处理、气体分离、生物医用、手性拆分、电池隔膜等领域的应用研究进展。
膜分离是工业发展不可缺少的技术,作为一门系统的科学,对膜领域还需要更深层次的基础研究。关于纤维素基膜材料的基础研究目前仅处于发展阶段,虽然有众多报道关于纤维素基膜材料的制备、表征以及应用研究,但真正做到工业化的却寥寥无几,因此还存在很多基础问题与挑战,总结发现对纤维素基膜材料的研究重点存在以下几个方面的突破点:(1)目前关于纤维素的高值化利用大部分都是停留在一级衍生化,其衍生物主要为纤维素酯、纤维素醚、纤维素氨基甲酸酯以及纤维素杂环等物质,如何在一级衍生物的基础上继续改性制备出二级、三级等衍生物成为研究的方向,如采用点击化学可以制备出二级衍生物,因此目前需要探索有效的方式来制备纤维素多级衍生化物质用于膜材料;(2)目前纤维素膜材料的应用涉及到众多领域,在此基础上继续深化研究,探索清楚材料结构—性能之间的关系,如研发分子识别膜,开发新的制膜工艺等,探索在其它领域以及交叉学科领域的新应用。
| [1] |
VINH-THANG H, KALIAGUINE S. Predictive models for mixed-matrix membrane performance:A review[J]. Chemical Reviews, 2013, 113(7): 4980-5028. DOI:10.1021/cr3003888 |
| [2] |
STRATHMANN H. Membrane separation processes[J]. Journal of Membrane Science, 1981, 9(1): 121-189. |
| [3] |
BAKER R W, CUSSLER E L, EYKAMP W, et al. Membrane separation systems[M]. Park Ridge: Noyes Publications, 1991.
|
| [4] |
BASU S, KHAN A L, CANO-ODENA A, et al. Membrane-based technologies for biogas separations[J]. Chemical Society Reviews, 2010, 39(2): 750-768. DOI:10.1039/B817050A |
| [5] |
KONTTURI E, TAMMELIN T, OSTERBERG M. Cellulose——model films and the fundamental approach[J]. Chemical Society Reviews, 2006, 35(12): 1287-1304. DOI:10.1039/B601872F |
| [6] |
杨鹏飞. 纤维素在膜科学中的研究进展[J]. 煤炭与化工, 2009, 32(4): 9-12. YANG P F. Research progress of cellulose in membrane science[J]. Coal and Chemical Industry, 2009, 32(4): 9-12. |
| [7] |
张金明, 张军. 基于纤维素的先进功能材料[J]. 高分子学报, 2010(12): 1376-1398. ZHANG J M, ZHANG J. Advanced functional materials based on cellulose[J]. Journal of Polymer, 2010(12): 1376-1398. |
| [8] |
刘蕾蕾, 王铎, 汪锰, 等. 三醋酸纤维素正渗透膜制备过程中影响因素的研究[J]. 膜科学与技术, 2011, 31(1): 77-83. LIU L L, WANG D, WANG M, et al. Study on the influencing factors in the preparation of cellulose triacetate positive osmosis membrane[J]. Membrane Science and Technology, 2011, 31(1): 77-83. DOI:10.3969/j.issn.1007-8924.2011.01.013 |
| [9] |
ZHANG W, CHEN X, PAN J, et al. Preparation and characterization of the tolerance to acid/alkaline and anti-oil-fouling of regenerated cellulose membranes for oil-water separation[J]. RSC Advances, 2016, 6(115): 114750-114757. DOI:10.1039/C6RA18766H |
| [10] |
李国亮, 王军, 赵长伟, 等. 醋酸纤维素正渗透膜的制备及性能研究[J]. 膜科学与技术, 2017, 37(1): 92-99. LI G L, WANG J, ZHAO C W, et al. Preparation and properties of cellulose acetate positive osmosis membranes[J]. Membrane Science and Technology, 2017, 37(1): 92-99. |
| [11] |
苏林海, 陈夫山. 醋酸纤维素改性制备氨基甲酸酯超滤膜材料的研究[J]. 纤维素科学与技术, 2013, 21(2): 39-45. SU L H, CHEN F S. The study of modified cellulose acetate to carbamate as ultrafiltration membrane materials[J]. Journal of Cellulose Science and Technology, 2013, 21(2): 39-45. DOI:10.3969/j.issn.1004-8405.2013.02.006 |
| [12] |
NGUYEN T P N, YUN E T, KIM I C, et al. Preparation of cellulose triacetate/cellulose acetate (CTA/CA)-based membranes for forward osmosis[J]. Journal of Membrane Science, 2013, 433: 49-59. DOI:10.1016/j.memsci.2013.01.027 |
| [13] |
JAYALAKSHMI A, RAJESH S, KIM I C, et al. Poly(isophthalamide) based graft copolymer for the modification of cellulose acetate ultrafiltration membranes and a fouling study by AFM imaging[J]. Journal of Membrane Science, 2014, 465: 117-128. DOI:10.1016/j.memsci.2014.04.020 |
| [14] |
GOETZ L A, JALVO B, ROSAL R, et al. Superhydrophilic anti-fouling electrospun cellulose acetate membranes coated with chitin nanocrystals for water filtration[J]. Journal of Membrane Science, 2016, 510: 238-248. DOI:10.1016/j.memsci.2016.02.069 |
| [15] |
SITKO R, MUSIELAK M, ZAWISZA B, et al. Graphene oxide/cellulose membranes in adsorption of divalent metal ions[J]. RSC Advances, 2016, 6(99): 96595-96605. DOI:10.1039/C6RA21432K |
| [16] |
FAN Z, XIAO C, LIU H, et al. Structure design and performance study on braid-reinforced cellulose acetate hollow fiber membranes[J]. Journal of Membrane Science, 2015, 486: 248-256. DOI:10.1016/j.memsci.2015.03.066 |
| [17] |
TAGLIABUE M, REVERBERI A P, BAGATIN R. Boron removal from water:Needs, challenges and perspectives[J]. Journal of Cleaner Production, 2014, 77: 56-64. DOI:10.1016/j.jclepro.2013.11.040 |
| [18] |
TU K L, NGHIEM L D, CHIVAS A R. Boron removal by reverse osmosis membranes in seawater desalination applications[J]. Separation and Purification Technology, 2010, 75(2): 87-101. DOI:10.1016/j.seppur.2010.07.021 |
| [19] |
WEI Y T, ZHENG Y M, CHEN J P. Functionalization of regenerated cellulose membrane via surface initiated atom transfer radical polymerization for boron removal from aqueous solution[J]. Langmuir, 2011, 27(10): 6018-6025. DOI:10.1021/la200154y |
| [20] |
ASIM S, WASIM M, SABIR A, et al. The effect of nanocrystalline cellulose/gum arabic conjugates in crosslinked membrane for antibacterial, chlorine resistance and boron removal performance[J]. Journal of Hazardous Materials, 2018, 343: 68-77. DOI:10.1016/j.jhazmat.2017.09.023 |
| [21] |
KOROS W J, FLEMING G K. Membrane-based gas separation[J]. Journal of Membrane Science, 1993, 83(1): 1-80. |
| [22] |
PANDEY P, CHAUHAN R S. Membranes for gas separation[J]. Progress in Polymer Science, 2001, 26(6): 853-893. DOI:10.1016/S0079-6700(01)00009-0 |
| [23] |
ANSALONI L, SALAS-GAY J, LIGI S, et al. Nanocellulose-based membranes for CO2 capture[J]. Journal of Membrane Science, 2017, 522: 216-225. DOI:10.1016/j.memsci.2016.09.024 |
| [24] |
LU H T, KANEHASHI S, SCHOLES C A, et al. The impact of ethylene glycol and hydrogen sulphide on the performance of cellulose triacetate membranes in natural gas sweetening[J]. Journal of Membrane Science, 2017, 539: 432-440. DOI:10.1016/j.memsci.2017.06.023 |
| [25] |
LU H T, LIU L, KANEHASHI S, et al. The impact of toluene and xylene on the performance of cellulose triacetate membranes for natural gas sweetening[J]. Journal of Membrane Science, 2018, 555: 362-368. DOI:10.1016/j.memsci.2018.03.045 |
| [26] |
WANG M, WANG Z, ZHAO S, et al. Recent advances on mixed matrix membranes for CO2 separation[J]. Chinese Journal of Chemical Engineering, 2017, 25(11): 1581-1597. DOI:10.1016/j.cjche.2017.07.006 |
| [27] |
MUBASHIR M, YEONG Y F, LAU K K, et al. Efficient CO2/N2 and CO2/CH4 separation using NH2-MIL-53(Al)/cellulose acetate (CA) mixed matrix membranes[J]. Separation and Purification Technology, 2018, 199: 140-151. DOI:10.1016/j.seppur.2018.01.038 |
| [28] |
SANAEEPUR H, KARGARI A, NASERNEJAD B. Aminosilane-functionalization of a nanoporous Y-type zeolite for application in a cellulose acetate based mixed matrix membrane for CO2 separation[J]. RSC Advances, 2014, 4(109): 63966-63976. DOI:10.1039/C4RA08783F |
| [29] |
SANAEEPUR H, KARGARI A, NASERNEJAD B, et al. A novel Co2+ exchanged zeolite Y/cellulose acetate mixed matrix membrane for CO2/N2 separation[J]. Journal of the Taiwan Institute of Chemical Engineers, 2016, 60: 403-413. DOI:10.1016/j.jtice.2015.10.042 |
| [30] |
HATTORI Y, MIYAJIMA T, SAKAI M, et al. Synthesis and thermal characterization of novel adamantane-based polysiloxane[J]. Polymer, 2008, 49(12): 2825-2831. DOI:10.1016/j.polymer.2008.04.053 |
| [31] |
CHEN J, ZHANG J, FENG Y, et al. Synthesis, characterization, and gas permeabilities of cellulose derivatives containing adamantane groups[J]. Journal of Membrane Science, 2014, 469: 507-514. DOI:10.1016/j.memsci.2014.06.010 |
| [32] |
KLEMM D, HEUBLEIN B, FINK H-P, et al. Cellulose:Fascinating biopolymer and sustainable raw material[J]. Angewandte Chemie International Edition, 2005, 44(22): 3358-3393. DOI:10.1002/anie.200460587 |
| [33] |
TEERI T T, BRUMER H, DANIEL G, et al. Biomimetic engineering of cellulose-based materials[J]. Trends in Biotechnology, 2007, 25(7): 299-306. DOI:10.1016/j.tibtech.2007.05.002 |
| [34] |
HALIB N, AHMAD I. Nanocellulose:Insight into health and medical applications[J]. Berlin:Springer International Publishing, 2017, 1-19. |
| [35] |
鲍文毅, 徐晨, 宋飞, 等. 纤维素/壳聚糖共混透明膜的制备及阻隔抗菌性能研究[J]. 高分子学报, 2015(1): 49-56. BAO W Y, XU C, SONG F, et al. Preparation and barrier properties of cellulose/chitosan blend transparent membrane[J]. Journal of Polyme, 2015(1): 49-56. |
| [36] |
WANG P, MENG J, XU M, et al. A simple but efficient zwitterionization method towards cellulose membrane with superior antifouling property and biocompatibility[J]. Journal of Membrane Science, 2015, 492: 547-558. DOI:10.1016/j.memsci.2015.06.024 |
| [37] |
LIU P S, CHEN Q, LIU X, et al. Grafting of zwitterion from cellulose membranes via ATRP for improving blood compatibility[J]. Biomacromolecules, 2009, 10(10): 2809-2816. DOI:10.1021/bm9006503 |
| [38] |
LIU P, CHEN Q, LI L, et al. Anti-biofouling ability and cytocompatibility of the zwitterionic brushes-modified cellulose membrane[J]. Journal of Materials Chemistry B, 2014, 2(41): 7222-7231. DOI:10.1039/C4TB01151A |
| [39] |
FU F, GU J, CAO J, et al. Reduction of silver ions using an alkaline cellulose dope:Straightforward access to Ag/ZnO decorated cellulose nanocomposite film with enhanced antibacterial activities[J]. ACS Sustainable Chemistry & Engineering, 2014, 6(1): 738-748. |
| [40] |
TANG H, ZHOU W, LU A, et al. Characterization of new sorbent constructed from Fe3O4/chitin magnetic beads for the dynamic adsorption of Cd2+ ions[J]. Journal of Materials Science, 2014, 49(1): 123-133. DOI:10.1007/s10853-013-7684-z |
| [41] |
ANIRUDHAN T S, NAIR S S, SEKHAR. V C. Deposition of gold-cellulose hybrid nanofiller on a polyelectrolyte membrane constructed using guar gum and poly(vinyl alcohol) for transdermal drug delivery[J]. Journal of Membrane Science, 2017, 539: 344-357. DOI:10.1016/j.memsci.2017.05.054 |
| [42] |
LIU Z, DU H, WICKRAMASINGHE S R, et al. Membrane surface engineering for protein separations:Experiments and simulations[J]. Langmuir, 2014, 30(35): 10651-10660. DOI:10.1021/la5026119 |
| [43] |
YU A, SHANG J, CHENG F, et al. Biofunctional paper via the covalent modification of cellulose[J]. Langmuir, 2012, 28(30): 11265-11273. DOI:10.1021/la301661x |
| [44] |
VOICU S I, CONDRUZ R M, MITRAN V, et al. Sericin covalent immobilization onto cellulose acetate membrane for biomedical applications[J]. ACS Sustainable Chemistry & Engineering, 1990, 4(3): 1765-1774. |
| [45] |
MURTINHO D, LAGOA A R, GARCIA F A P, et al. Cellulose derivatives membranes as supports for immobilisation of enzymes[J]. Cellulose, 1998, 5(4): 299-308. DOI:10.1023/A:1009255126274 |
| [46] |
BALDINO L, CARDEA S, REVERCHON E. Supercritical assisted enzymatic membranes preparation, for active packaging applications[J]. Journal of Membrane Science, 2014, 453: 409-418. DOI:10.1016/j.memsci.2013.11.019 |
| [47] |
SUKSAEREE J, CHAROENCHAI L, MONTON C, et al. Preparation of a pseudolatex-membrane for ketoprofen transdermal drug delivery systems[J]. Industrial & Engineering Chemistry Research, 2003, 52(45): 15847-15854. |
| [48] |
LIN N, G ZE A, WOUESSIDJEWE D, et al. Biocompatible double-membrane hydrogels from cationic cellulose nanocrystals and anionic alginate as complexing drugs codelivery[J]. ACS Applied Materials & Interfaces, 2016, 8(11): 6880-6889. |
| [49] |
SOFIA B C, RAQUEL F A, MICHAEL W W, et al. Purification of influenza virus-like particles using sulfated cellulose membrane adsorbers[J]. Journal of Chemical Technology & Biotechnology, 2018, 93(7): 1988-1996. |
| [50] |
RAQUEL F A, FLORIAN T, LOUIS V, et al. Optimization of cell culture-derived influenza A virus particles purification using sulfated cellulose membrane adsorbers[J]. Engineering in Life Sciences, 2018, 18(1): 29-39. |
| [51] |
SCROSATI B, HASSOUN J, SUN Y K. Lithium-ion batteries. A look into the future[J]. Energy & Environmental Science, 2011, 4(9): 3287-3295. |
| [52] |
TARASCON J M, ARMAND M. Issues and challenges facing rechargeable lithium batteries[J]. Nature, 2001, 414(6861): 359-367. DOI:10.1038/35104644 |
| [53] |
ARORA P, ZHANG Z. Battery separators[J]. Chemical Reviews, 2004, 104(10): 4419-4462. DOI:10.1021/cr020738u |
| [54] |
ZHANG S S. A review on the separators of liquid electrolyte Li-ion batteries[J]. Journal of Power Sources, 2007, 164(1): 351-364. DOI:10.1016/j.jpowsour.2006.10.065 |
| [55] |
OH Y S, JUNG G Y, KIM J H, et al. Janus-faced, dual-conductive/chemically active battery separator membranes[J]. Advanced Functional Materials, 2016, 26(39): 7074-7083. DOI:10.1002/adfm.201602734 |
| [56] |
SHENG J, TONG S, HE Z, et al. Recent developments of cellulose materials for lithium-ion battery separators[J]. Cellulose, 2017, 24(10): 4103-4122. DOI:10.1007/s10570-017-1421-8 |
| [57] |
WENG B, XU F, ALCOUTLABI M, et al. Fibrous cellulose membrane mass produced via forcespinning® for lithium-ion battery separators[J]. Cellulose, 2015, 22(2): 1311-1320. DOI:10.1007/s10570-015-0564-8 |
| [58] |
LIAO H, ZHANG H, HONG H, et al. Novel cellulose aerogel coated on polypropylene separators as gel polymer electrolyte with high ionic conductivity for lithium-ion batteries[J]. Journal of Membrane Science, 2016, 514: 332-339. DOI:10.1016/j.memsci.2016.05.009 |
| [59] |
BORIBOON D, VONGSETSKUL T, LIMTHONGKUL P, et al. Cellulose ultrafine fibers embedded with titania particles as a high performance and eco-friendly separator for lithium-ion batteries[J]. Carbohydrate Polymers, 2018, 189: 145-151. DOI:10.1016/j.carbpol.2018.01.077 |
| [60] |
ZHANG J, MA C, XIA Q, et al. Composite electrolyte membranes incorporating viscous copolymers with cellulose for high performance lithium-ion batteries[J]. Journal of Membrane Science, 2016, 497: 259-269. DOI:10.1016/j.memsci.2015.09.056 |
| [61] |
KANG W, MA X, ZHAO H, et al. Electrospun cellulose acetate/poly(vinylidene fluoride) nanofibrous membrane for polymer lithium-ion batteries[J]. Journal of Solid State Electrochemistry, 2016, 20(10): 2791-2803. DOI:10.1007/s10008-016-3271-y |
| [62] |
XU Q, KONG Q, LIU Z, et al. Cellulose/polysulfonamide composite membrane as a high performance lithium-ion battery separator[J]. ACS Sustainable Chemistry & Engineering, 2014, 2(2): 194-199. |
| [63] |
ZHANG J, LIU Z, KONG Q, et al. Renewable and superior thermal-resistant cellulose-based composite nonwoven as lithium-ion battery separator[J]. ACS Applied Materials & Interfaces, 2013, 5(1): 128-134. |
| [64] |
YOSHIKAWA M, MURAKOSHI K, KOGITA T, et al. Chiral separation membranes from modified polysulfone having myrtenal-derived terpenoid side groups[J]. European Polymer Journal, 2006, 42(10): 2532-2539. DOI:10.1016/j.eurpolymj.2006.04.014 |
| [65] |
FERNANDES C, TIRITAN M, PINTO M. Chiral separation in preparative scale:A brief overview of membranes as tools for enantiomeric separation[J]. Symmetry, 2017, 9(10): 206. DOI:10.3390/sym9100206 |
| [66] |
INGOLE P G, BAJAJ H C, SINGH K. Membrane separation processes:Optical resolution of lysine and asparagine amino acids[J]. Desalination, 2014, 343: 75-81. DOI:10.1016/j.desal.2013.10.009 |
| [67] |
LIU Y, LI P, XIE L, et al. β-Cyclodextrin modified silica nanochannel membrane for chiral separation[J]. Journal of Membrane Science, 2014, 453: 12-17. DOI:10.1016/j.memsci.2013.10.064 |
| [68] |
SUEYOSHI Y, FUKUSHIMA C, YOSHIKAWA M. Molecularly imprinted nanofiber membranes from cellulose acetate aimed for chiral separation[J]. Journal of Membrane Science, 2010, 357(1): 90-97. |
| [69] |
IKAI T, YAMAMOTO C, KAMIGAITO M, et al. Immobilization of polysaccharide derivatives onto silica gel:Facile synthesis of chiral packing materials by means of intermolecular polycondensation of triethoxysilyl groups[J]. Journal of Chromatography A, 2007, 1157(1): 151-158. |
| [70] |
LUAN Y, WU J, ZHAN M, et al. "One pot" homogeneous synthesis of thermoplastic cellulose acetate-graft-poly(l-lactide) copolymers from unmodified cellulose[J]. Cellulose, 2013, 20(1): 327-337. DOI:10.1007/s10570-012-9818-x |
| [71] |
CHEN X, OKAMOTO Y, YANO T, et al. Direct enantiomeric separations of tris(2-phenylpyridine) iridium(Ⅲ) complexes on polysaccharide derivative-based chiral stationary phases[J]. Journal of Separation Science, 2007, 30(5): 713-716. DOI:10.1002/jssc.200600409 |
| [72] |
OKAMOTO Y, IKAI T. Chiral HPLC for efficient resolution of enantiomers[J]. Chemical Society Reviews, 2008, 37(12): 2593-2608. DOI:10.1039/b808881k |
| [73] |
CHANKVETADZE B, IKAI T, YAMAMOTO C, et al. High-performance liquid chromatographic enantioseparations on monolithic silica columns containing a covalently attached 3, 5-dimethylphenylcarbamate derivative of cellulose[J]. Journal of Chromatography A, 2004, 1042(1): 55-60. |
| [74] |
CHEN X, QIN F, LIU Y, et al. Synthesis of chiral stationary phases with radical polymerization reaction of cellulose phenylcarbamate derivatives and vinylized silica gel[J]. Journal of Chromatography A, 2004, 1034(1): 109-116. |
| [75] |
ZHAO M, XU X L, JIANG Y D, et al. Enantioseparation of trans-stilbene oxide using a cellulose acetate membrane[J]. Journal of Membrane Science, 2009, 336(1): 149-153. |
| [76] |
ZHENG H, YOSHIKAWA M. Molecularly imprinted cellulose membranes for pervaporation separation of xylene isomers[J]. Journal of Membrane Science, 2015, 478: 148-154. DOI:10.1016/j.memsci.2014.12.048 |
| [77] |
YOSHIKAWA M, OOI T, IZUMI J I. Alternative molecularly imprinted membranes from a derivative of natural polymer, cellulose acetate[J]. Journal of Applied Polymer Science, 1999, 72(4): 493-499. DOI:10.1002/(SICI)1097-4628(19990425)72:4<493::AID-APP5>3.0.CO;2-U |
| [78] |
JIANG Y D, ZHANG J H, XIE S M, et al. Chiral separation of D, L-tyrosine through nitrocellulose membrane[J]. Journal of Applied Polymer Science, 2012, 124(6): 5187-5193. |
| [79] |
LI H, HUANG Q, LI D, et al. Generation of a molecular imprinted membrane by coating cellulose acetate onto a ZrO2-modified alumina membrane for the chiral separation of mandelic acid enantiomers[J]. Organic Process Research & Development, 2018, 22(3): 278-285. |
| [80] |
WANG W F, XIONG W W, ZHAO M, et al. Chiral separation of trans-stilbene oxide through cellulose acetate butyrate membrane[J]. Tetrahedron:Asymmetry, 2009, 20(9): 1052-1056. DOI:10.1016/j.tetasy.2009.03.032 |
| [81] |
FLORES-LPEZ L Z, CALOCA J, ROGEL-HERN N E, et al. Development of an enantioselective membrane from cellulose acetate propionate/cellulose acetate, for the separation of trans-stilbene oxide[J]. Cellulose, 2014, 21(3): 1987-1995. DOI:10.1007/s10570-014-0252-0 |




