2. 浙江省化工研究院,浙江 杭州 310023
2. Zhejiang Research Institute of Chemical Industry, Hangzhou 310023, China
制冷被评为20世纪最重要的20项工程成就之一,与计算机、航天器和互联网并列[1]。制冷剂作为热机中用于实现能量转化的媒介物质,是传热、制冷系统的“血液”,被广泛用于家用空调、工商制冷等领域。
第一代制冷剂主要采用自然工质,如NH3、H2O、CO2、SO2、乙醚以及空气等。这些制冷剂各自存在着一些缺点,如易燃、毒性大、制冷效率低等,被更安全的第二代制冷剂所取代[2]。第二代制冷剂氯氟烃(CFCs)与氢氯氟烃(HCFCs)具有不可燃或不易燃的优点,这类制冷剂具有极佳的制冷效果以及稳定性,被广泛地使用,但其分解的氯原子会引发破坏臭氧的链式反应,造成臭氧层空洞。随着环境问题日益恶化,人们逐渐认识到这类氟氯昂制冷剂对环境所造成的巨大破坏,于1987年签署了《关于消耗臭氧层物质的蒙特利尔议定书》,通过逐步淘汰导致臭氧消耗的制冷剂来保护臭氧层。第三代制冷剂氢氟烃(HFCs)虽臭氧消耗潜能值(ODP)为零,但其全球变暖潜能值(GWP)较高。在全球变暖的严峻形势下,国际社会愈发认识到HFCs这类高GWP值的温室气体所带来的巨大危害,因而纷纷采取行动,逐步淘汰其使用,以积极应对气候变化。欧盟的《移动空调指令》(MACs)和《含氟气体法》(F-gas)规定,2011年起新车型禁用GWP值超过150的制冷剂,2017年所有汽车禁用GWP值超过150的制冷剂。美国环境保护署通过新制冷剂替代计划,积极推动环保型制冷剂的使用。同时,澳大利亚和日本也更新了其氟碳法规,限制了高GWP值的HFCs的使用。
第四代新型制冷剂主要指含氟烯烃(HFOs),其具有ODP值为零、GWP值极低等优点,其中的代表是2,3,3,3-四氟丙烯(HFO-1234yf)。HFO-1234yf的热物理性质与第三代制冷剂1,1,1,2-四氟乙烷(HFC-134a)相近,因此能够与现有的制冷系统设计良好兼容。这使得汽车制造商在采用HFO-1234yf作为替代制冷剂时,无需对系统设计进行大幅改动,从而降低了更换制冷剂的成本和难度。在2008年的普渡大学国际制冷与空调会议上,Dupont与Honeywell联合提交了一份报告,该报告深入阐述了HFO-1234yf替代HFC-134a的可行性。此外,美国汽车工程师协会对HFO-1234yf的安全性和功效进行了全面的评估,报告明确指出,HFO-1234yf具备替代HFC-134a的充分可行性。相较于HFC-134a,HFO-1234yf的环保性能更好,且完全契合汽车制冷行业中生态保护、低毒性以及防爆等关键要求。凭借这些卓越的特性,HFO-1234yf已被广泛接受并用于车载空调系统[3-4]。
目前,对HFO-1234yf的研究方兴未艾。本文综述了HFO-1234yf的合成工艺与催化剂研究的进展,比较了各类合成工艺的优缺点,分析了催化剂开发中的难点,旨在为HFO-1234yf的研究提供有益参考,推动其合成技术的进一步发展。
2 HFO-1234yf合成工艺早在20世纪60年代,Dupont公司便对HFO-1234yf制备技术开展了研究[5]。然后,在此后长达40年的时间里,HFO-1234yf的相关专利申请陷入了沉寂状态。直到2004年,受到《蒙特利尔议定书》、欧盟F-gas及MACs指令等一系列环保政策的影响,HFO-1234yf凭借其作为汽车空调制冷剂HFC-134a理想替代品的突出优势,迅速吸引了业界的广泛关注,一跃成为行业研究的热点,其专利申请也由此迈入了蓬勃发展的黄金时期[6]。
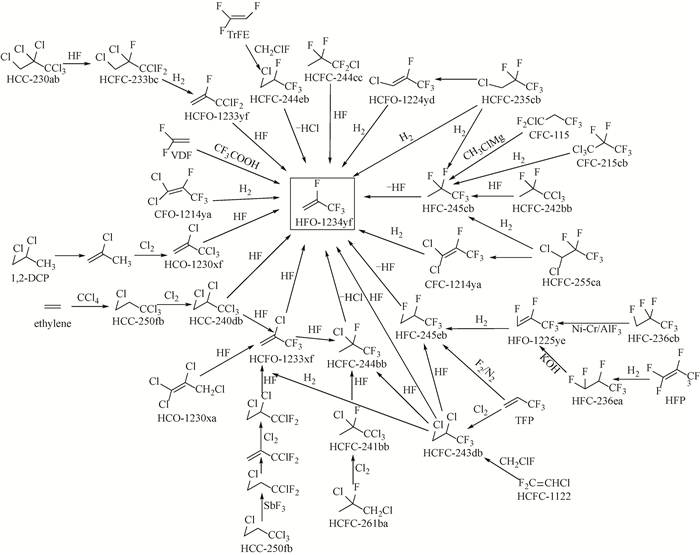
纵观20世纪60年代至今的发展历程,HFO-1234yf的制备工艺可根据起始原料碳原子数的不同,大致划分为三种主要类别,具体分类情况如表 1所示。此外,HFO-1234yf的主要合成路线展示在图 1中。
|
|
表 1 专利中涉及原料品种 Table 1 Raw material varieties involved in the patents |
|
图 1 HFO-1234yf的合成工艺 Fig.1 Synthesis process for HFO-1234yf |
以C1为原料的工艺只有一条,20世纪60年代Dupont公司[5]提出的二氟一氯甲烷(CHClF2,HCFC-22)与氯甲烷(CH3Cl,R40)在高温下热解生成HFO-1234yf。该工艺转化率仅为14.8%,且需在高温下进行,温度低于700 ℃时,几乎无HFO-1234yf生成。反应温度高及转化率低限制了此工艺的应用。
山东东岳高分子材料有限公司[7]提出将原料HCFC-22和R40预热后与900~1 000 ℃的过热水蒸气混合,在600~1 100 ℃下反应生成HFO-1234yf的工艺。该工艺采用水蒸气稀释裂解,抑制了结碳现象,但也存在能耗大、产率低等不适合工业化的缺点。
2.2 以C2为原料的工艺 2.2.1 卤代乙烷巨化公司[8]提出以五氟一氯乙烷(CF3CF2Cl,CFC-115)和格氏试剂甲基氯化镁为起始原料的工艺。该工艺先经亲核加成-消去反应,然后脱氟化氢反应两步生成HFO-1234yf,具有较高收率,两步反应总收率可达85.3%。但两步均为间歇操作,生产效率低,且反应均需大量溶剂参与,同时会产生大量废液。
2.2.2 乙烯北京宇极科技公司[9]提出乙烯(CH2=CH2)与四氯化碳首先在铁、铬、镍合金催化下,90~120 ℃调聚反应生成1,1,1,3-四氯丙烷(CCl3CH2CH2Cl,HCC-250fb);然后,HCC-250fb在FeCl3催化、0~120 ℃下,于四氯化碳溶剂中发生氯代反应生成1,1,1,2,3-五氯丙烷(CCl3CHClCH2Cl,HCC-240db);接着,HCC-240db和HF以CrF3为催化剂,在300~350 ℃下气相反应生成2-氯-3,3,3-三氟丙烯(CF3CCl=CH2,HCFO-1233xf);最后,HCFO-1233xf和HF以SbF5/AlF3为催化剂,在50~150 ℃下发生气相氟氯交换反应生成HFO-1234yf的工艺。该工艺原料价廉易得,但路线复杂,第二步反应为溶剂化反应,不利于工业化应用。
2.2.3 卤代乙烯(1) 偏氟乙烯
巨化公司[10]提出了一种以经NH4F处理的γ-Al2O3为催化剂,在300~600 ℃反应条件下,使偏氟乙烯(CF2=CH2,VDF)与三氟乙酸(CF3COOH)发生反应生成HFO-1234yf的工艺。该工艺产率较低,最高仅为27%,因此在工业化应用方面前景有限。
(2) 2-氯-1,1-二氟乙烯
浙江三美化工[11]提出以SbF3-SbF5-AlCl3/C为催化剂,在150~250 ℃下,2-氯-1,1-二氟乙烯(CF2=CHCl,HCFC-1122)与氟氯甲烷(CH2ClF,R31)调聚反应生成中间体2,3-二氯-1,1,1-三氟丙烷(CF3CHClCH2Cl,HCFC-243db),HCFC-243db通过三条不同路径生成HFO-1234yf的工艺:(a)HCFC-243db与HF在Cr2O3-Ni/C作用下反应生成HFO-1234yf,反应温度为150~340 ℃;(b)HCFC-243db在CrF3作用下,200~350 ℃脱HCl生成HCFO-1233xf,HCFO-1233xf与HF在La-Cr2O3作用下,280~350 ℃反应生成HFO-1234yf;(c)HCFC-243db先脱HCl生成HCFO-1233xf,HCFO-1233xf与HF在Zn-Cr2O3作用下,200~320 ℃反应生成2-氯-1,1,1,2-四氟丙烷(CF3CClFCH3,HCFC-244bb),HCFC-244bb在CsCl/MgF2作用下,320~380 ℃脱HCl生成HFO-1234yf。
该工艺以HCFC-1122为原料,尽管该原料对人体和环境存在潜在危害,但通过特定工艺,能够有效降低其对环境的负面影响,从而在一定程度上起到环境友好作用。此外,路径(a)工艺流程简单,且收率表现优异,可达80% 以上,这使其具备了良好的工业应用潜力。
(3) 三氟乙烯
浙江省化工研究院[12]提出三氟乙烯(CF2=CHF,TrFE)和R31在Lewis酸催化剂催化下,0~50 ℃反应生成3-氯-1,1,1,2-四氟丙烷(CF3CHFCH2Cl,HCFC-244eb),HCFC-244eb在活性炭作用下,300~350 ℃脱HCl生成HFO-1234yf的工艺。该工艺第一步为液相反应,产能有限,同时原料TrFE价格较高,且存在自聚问题,安全性差。
(4) 三氟氯乙烯
Honeywell公司[13]提出三氟氯乙烯(CF2=CClF,CTFE)与卤甲烷(氯甲烷、氟甲烷或溴甲烷)在第一反应器中650~750 ℃反应得到中间产物流,随后中间产物流与HF一同进入第二反应器,在Cr2O3或Cr2OxFy作用下,280~550 ℃反应生成HFO-1234yf的工艺。该工艺反应过程气相连续,原料CTFE易得,且转化率可达99%,HFO-1234yf选择性可到87%,但两步反应都需要较高的温度,能耗较高。
(5) 四氟乙烯
Daikin公司[14]提出四氟乙烯(CF2=CF2,TFE)与一卤代甲烷(CH3Cl、CH3Br、CH3I)在NaF、MgO或KF/CaF2催化下,450~560 ℃一步反应生成HFO-1234yf的工艺。该工艺虽然路线简单,但反应产率低,且较高温度下会发生催化热裂解反应,导致催化剂极易积碳,寿命较短。巨化公司[15]提出将TFE、一卤代甲烷与N2或水蒸气稀释气体混合预热后,无需催化剂参与,500~700 ℃下反应生成HFO-1234yf的工艺。该工艺有较好的HFO-1234yf产率,但预热温度和反应温度都较高,能耗大。
此外,巨化公司[16]提出以TFE为起始原料,经亲核加成-消去、氟气加成、脱氟化氢三步反应生成HFO-1234yf。该工艺原料TFE简单易得、总收率高,但溶剂化反应存在生产效率低、废液量大等问题。
浙江工业大学韩文锋等[17]提出TFE、固体氟源(KF、RbF或CsF)和甲基源(硫酸二甲酯)在四乙二醇二甲醚为溶剂的反应釜中,15~50 ℃下生成1,1,1,2,2-五氟丙烷(CF3CF2CH3,HFC-245cb),HFC-245cb在Cr2O3作用下,350~420 ℃气相脱HF生成HFO-1234yf的工艺。该工艺第一步收率可达93%,第二步产率可达93.3%,具有良好的工业前景。
(6) 氯乙烯
浙江三美化工[18]提出以氯乙烯(CH2=CHCl)为原料,经过调聚、脱氯化氢、氟氯交换和脱氯化氢、异构化、液相氟化,最后通过脱HCl制备出HFO-1234yf的工艺。该工艺原料价廉易得,但路线过于繁琐,且各步均在高压釜中反应,不适合工业化大规模生产。
(7) 四氯乙烯
浙江三美化工[19]提出四氯乙烯(CCl2=CCl2)与CH3Cl在负载型催化剂作用下,220~300 ℃调聚反应生成1,1,1,2,2-五氯丙烷(CCl3CCl2CH3,HCC-240ab)和2,3,3,3-四氯丙烯(CCl3CCl=CH2,HCO-1230xf);然后,HCC-240ab和HCO-1230xf与HF在金属氧化物催化剂作用下,220~400 ℃氟化反应生成HFC-245cb和HCFC-244bb;最后,HFC-245cb和HCFC-244bb在Cr催化剂作用下,200~350 ℃脱卤化氢生成HFO-1234yf的工艺。该工艺反应气相连续,有较高的HFO-1234yf收率,可达82.7%,原料四氯乙烯经济易得,反应过程连续,有较好的工业化应用前景。
2.3 以C3为原料的工艺 2.3.1 卤代丙烷(1) 1,2-二氯-2-氟丙烷
旭硝子公司[20]提出1,2-二氯-2-氟丙烷(CH2ClCClFCH3,HCFC-261ba)与Cl2在四氯化碳溶剂中,在200~400 nm紫外光照射下反应生成1,1,1,2-四氯-2-氟丙烷(CCl3CClFCH3,HCFC-241bb)后,HF氟化HCFC-241bb生成HCFC-244bb,最后HCFC-244bb脱HCl生成HFO-1234yf的工艺。该工艺存在光催化氯化效率低、光催化反应器设计复杂、设备成本高等缺点。
(2) 1,1,1-三氯-2,2-二氟丙烷
Honeywell公司[21]提出1,1,1-三氯-2,2-二氟丙烷(CCl3CF2CH2,HCFC-242bb)在SbCl5作用下,300 ℃与HF反应生成HFC-245cb,HFC-245cb在Pd/C或Pt/C作用下,450~600 ℃脱HF生成HFO-1234yf的工艺。该工艺的原料较难获得。
(3) 2,3-二氯-1,1,1-三氟丙烷
INEOS公司[22]提出HCFC-243db在Zn/Cr2O3作用下,200~370 ℃与HF反应生成1,1,1,2,3-五氟丙烷(CF3CHFCH2F,HFC-245eb),HFC-245eb再在氟化Zn/Cr2O3作用下,240~340 ℃脱HF生成HFO-1234yf的工艺。该工艺存在氟化步骤中HFC-245eb选择性低的缺点。
浙江环新氟材料[23]提出HCFC-243db和氟化剂HF混合后,预热至150~180 ℃再进入固定床中,在氟化催化剂作用下,300~550 ℃反应生成HCFC-244bb,HCFC-244bb在脱卤催化剂作用下,400~650 ℃脱HCl反应生成HFO-1234yf的工艺。该工艺路线简单,两步气相反应过程连续、稳定、易于控制,且每步均有较高转化率和选择性,工业化应用前景广阔。
(4) 1-氯-1,1,2,2-四氟丙烷
Daikin公司[24]提出在Cr基催化剂作用下,1-氯-1,1,2,2-四氟丙烷(CF2ClCF2CH3,HCFC-244cc)与HF在280~350 ℃下反应直接生成HFO-1234yf的工艺。该工艺HCFC-244cc转化率较低,最高为50.9%,且原料HCFC-244cc难以获得。
(5) 2-氯-1,1,1,2-四氟丙烷
Honeywell公司[25]提出HCFC-244bb在催化剂存在下400~500 ℃气相脱HCl生成HFO-1234yf的工艺。在采用质量分数为10% 的CsCl/MgF2催化剂时,反应效果最佳,HCFC-244bb的转化率为49.6%,HFO-1234yf的选择性为96.9%。
针对烯烃产物容易使固体酸催化剂结焦失活的问题,西安近代化学研究所张伟等[26]提出HCFC-244bb在N2、水蒸气或HF稀释气体存在下,无需催化剂,在600~750 ℃下脱HCl生成HFO-1234yf的工艺。该工艺需要将稀释气体预热至600~1 100 ℃,作为热介质加热原料HCFC-244bb,能耗较大。
(6) 1,1,1,2,2-五氟丙烷
Daikin公司[27]提出以含氟量30% ~45% (质量分数)的高氟化氧化铬为催化剂,在250~450 ℃下,HFC-245cb气相脱HF生成HFO-1234yf的工艺。该工艺HFC-245cb转化率为78.4%,HFO-1234yf选择性为99.6%,但缺点是原料HFC-245cb难获取,铬基催化剂对环境有害。浙江衢化氟化学有限公司[28]提出通过共沉淀法制备以铬为主成分,掺钴、镁、镍、锌、铝中的一种为辅助成分的氧化物催化剂。该催化剂可在较低的温度下气相催化HFC-245cb脱HF生成HFO-1234yf,延缓催化剂积碳速率,延长催化剂的寿命,但HFC-245cb转化率降低,最高为41.7%。
(7) 1,1,1,2,3-五氟丙烷
Dupont公司[29]提出HFC-245eb在相转移催化剂存在下,与KOH水溶液反应生成HFO-1234yf的工艺。该工艺HFO-1234yf选择性高,但效率低,废液多,溶剂化反应的通病限制了其应用。Honeywell公司[30]提出以Ni/C、氟氧化铬(F-Cr2O3)、Pd/C为脱卤催化剂,在300~600 ℃下,HFC-245eb脱HF生成HFO-1234yf的工艺。该工艺反应温度需高于500 ℃时才能得到较好的效果,产率可达69%,反应温度低于500 ℃时,产率迅速降低,均低于10%。同时,高温不仅导致能耗增加,还对设备提出了更高要求。
(8) 3-氯-1,1,1,2,2-五氟丙烷
Dupont公司[31]提出了3-氯-1,1,1,2,2-五氟丙烷(CF3CF2CH2Cl,HCFC-235cb)合成HFO-1234yf的三条路线。(a)一步反应催化加氢、热解脱HF:HCFC-235cb与H2在Pd/AlF3作用下,100~400 ℃反应生成HFO-1234yf。(b)两步反应,先消去再氢化:HCFC-235cb在AlF3或Cr2O3作用下,100~400 ℃脱HF生成3-氯-1,1,1,2-四氟丙烯(CF3CF CHCl,HCFO-1224yd),然后HCFO-1224yd与H2在Pd/AlF3作用下,100~400 ℃生成HFO-1234yf。(c)两步反应,先氢化再消去:HCFC-235cb与H2在Pd/AlF3作用下,100~400 ℃生成HFC-245cb,后在AlF3作用下,脱HF生成HFO-1234yf。
(9) 3,3-二氯-1,1,1,2,2-五氟丙烷
Dupont公司[32-33]提出3,3-二氯-1,1,1,2,2-五氟丙烷(CF3CF2CHCl2,HCFC-225ca)为原料制备HFO-1234yf的两条路线。(a)先氢化再消去:HCFC-225ca在钯负载多孔碳催化剂作用下,200~350 ℃气相Cl/H交换生成HFC-245cb,再在AlF3或Cr2O3作用下,300~450 ℃脱HF生成HFO-1234yf。(b)先消去再氢化:HCFC-225ca在AlF3或Al2OxFy作用下,300~450 ℃脱HF生成1,1-二氯-2,3,3,3-四氟丙烯(CF3CF CCl2,CFC-1214ya),后CFC-1214ya在Pd/AlF3或Pd/Al2OxFy作用下,125~350 ℃加氢脱氯生成HFO-1234yf。两路线均为气相连续,且操作简单,但原料HCFC-225ca难以获取,且转化率低,限制了其工业应用。
(10) 3,3,3-三氯-1,1,1,2,2-五氟丙烷
Dupont公司[34]提出以Pd/Al2O3或Pd/Al2OxFy为催化剂,在125~300 ℃下,3,3,3-三氯-1,1,1,2,2-五氟丙烷(CF3CF2CCl3,CFC-215cb)加氢脱卤生成HFC-245cb,后HFC-245cb在AlF3作用下,300~450 ℃脱HF生成HFO-1234yf的工艺。该工艺转化率低,工业化应用受限。
(11) 3-溴-1,1,1,2,2-五氟丙烷
Daikin公司[35]提出以镁、铜、铁、锌等类似金属为催化剂,在极性有机溶剂或极性有机溶剂与水混合溶液中3-溴-1,1,1,2,2-五氟丙烷(CF3CF2CH2Br)脱卤生成HFO-1234yf的工艺。该工艺产率可达87.9%,且反应条件温和,但反应过程中会产生大量废液,易造成环境污染。
(12) 1,1,1,2,2,3-六氟丙烷
Arkema公司[36]提出1,1,1,2,2,3-六氟丙烷(CF3CF2CH2F,HFC-236cb)在Ni-Cr/AlF3作用下,300~400 ℃脱HF生成1,2,3,3,3-五氟丙烯(CF3CF CHF,HFO-1225ye),然后HFO-1225ye与H2加成反应生成HFC-245eb,最后HFC-245eb同样在Ni-Cr/AlF3作用下,300~400 ℃脱HF生成HFO-1234yf的工艺。该工艺步骤繁琐,副产物较多HF,不适合工业应用。
(13) 1,2-二氯丙烷
山东联创节能新材料[37]提出1,2-二氯丙烷(CH3CHClCH2Cl,1,2-DCP)在沸石作用下,230~250 ℃脱HCl生成2-氯丙烯(CH3CCl=CH2),2-氯丙烯与Cl2在FeCl3作用下,200~220 ℃生成HCO-1230xf,HCO-1230xf与氢氟酸在SbF3或SbF5作用下,100~120 ℃于釜中反应生成HFO-1234yf的工艺。该工艺第一步转化率和选择性都较低,不适合工业化应用。
(14) 1,2,3-三氯丙烷
Arkema公司[38]提出1,2,3-三氯丙烷(CH2ClCHClCH2Cl,HCC-260da)在NaOH水溶液中液相脱HCl或在FeCl3/AC作用下气相脱HCl生成2,3-二氯丙烯(CHCl=CClCH3,HCO-1250xf);HCO-1250xf与HF在弱Lewis酸作用下,液相氟化生成HCFC-261ba;HCFC-261ba在无水条件下光氯化生成HCFC-241bb;最后HCFC-241bb在含铬催化剂作用下,反应生成HFO-1234yf的工艺。该工艺繁琐,光氯化反应效率低,不适合工业应用。
(15) 1,1,1,3-四氯丙烷
西安近代化学研究所[39]提出以氯磺酸为催化剂,在壬烷、癸烷或十二烷溶液中,0~100 ℃下HCC-250fb与SbF3液相氟化反应生成1,3-二氯-1,1-二氟丙烷(CClF2CH2CH2Cl)。在相转移催化剂作用下,1,3-二氯-1,1-二氟丙烷于氢氧化钠或氢氧化钾的水溶液中,60~150 ℃脱HCl生成3-氯-3,3-二氟丙烷(CClF2CH CH2);3-氯-3,3-二氟丙烷与Cl2在FeCl3或AlCl3作用下,30~80 ℃反应生成1,2,3-三氯-1,1-二氟丙烷(CClF2CHClCH2Cl);1,2,3-三氯-1,1-二氟丙烷与HF在氟化催化剂Fe-Mo-Mg-F作用下,200~300 ℃生成HCFO-1233xf。HCFO-1233xf与HF在氟化催化剂A-B-Al-F(A为Ni、Fe或Co中的一种,B为Sc、Y、Th、U、Pb以及Zr中的一种)作用下,250~350 ℃反应生成HFO-1234yf的工艺。该工艺虽然原料价廉易得,各步转化率、选择性均可达95% 以上,但步骤过于繁琐,且前两步用到大量的溶剂,废液量大。
(16) 1,1,1,2,3-五氯丙烷
陕西中蓝化工科技新材料有限公司及浙江省化工研究院[40]共同提出HCC-240db与HF在Fe2OxFy氟化催化剂作用下,气相依次经过210~270 ℃的第一反应区、300~380 ℃的第二反应区,联产HFO-1234yf和1,3,3,3-四氟丙烯(CF3CH CHF,HFO-1234ze)的工艺。该工艺有很好的HCC-240db转化率,但HFO-1234yf的选择性不高,且HFO-1234yf和HFO-1234ze的分离困难。
(17) 五氯环丙烷
中化近代环保化工(西安)有限公司[41]提出一种以氧化铝、氟化铝或氟氧化铝为催化剂,使五氯环丙烷(C3HCl5)与HF在300~400 ℃下进行反应联产HCFO-1233xf和HFO-1234yf的工艺。该工艺在HFO-1234yf的选择性方面表现不佳,最高选择性仅为29.59%,这很大程度上限制了其在工业化生产中的应用。
(18) 1,1,1,2,2,3-六氯丙烷
西安近代化学研究所[42]提出1,1,1,2,2,3-六氯丙烷(CCl3CCl2CH2Cl,HCC-230ab)与HF在氟化催化剂Zn-Fe-La-Mg作用下,220~260 ℃反应生成1,2,3-三氯-1,1,2-三氟丙烷(CClF2CClFCH2Cl,HCFC-233bc),然后HCFC-233bc与H2在Cu-V-Mg-F作用下,200~300 ℃反应生成3-氯-2,3,3-二氟丙烯(CClF2CF CH2,HCFO-1233yf),最后HCFO-1233yf与HF在FeF3/MgF2作用下,160~240 ℃反应生成HFO-1234yf的工艺。该工艺原料HCC-230ab简单易得,且每步均有较好的转化率和选择性,工业应用前景好。
2.3.2 卤代丙烯(1) 3,3,3-三氟丙烯
Arkema公司[43]提出3,3,3-三氟丙烯(CF3CH CH2,TFP)先在釜中氯化生成HCFC-243db,然后HCFC-243db在FeCl3、NiCl2或CrF3作用下,250~380 ℃脱HCl生成HCFO-1233xf,最后HCFO-1233xf在F-Cr2O3或AlF3作用下,150~300 ℃与HF反应生成HFO-1234yf的工艺。
巨化公司[44]提出TFP与全氟丁烷、全氟己烷、全氟辛烷及全氟萘烷中的一种溶剂于反应釜中,通入氟气体积分数为10% ~20% 的F2/N2反应生成HFC-245eb,HFC-245eb通入盛有碱液的反应釜中脱HF生成HFO-1234yf的工艺。该工艺虽然步骤相对简单,但存在一些问题,如原料氟气价格昂贵且危险性大,溶剂化反应生产效率低,产生的废液量大。
(2) 2-氯-3,3,3-三氟丙烯
Daikin公司[45]提出以氧化铬(CrOm,2<m<2.3)为催化剂,在250~450 ℃下HCFO-1233xf与HF反应生成HFO-1234yf的工艺。该工艺HCFO-1233xf转化率为12.5%、HFO-1234yf选择性为52.8%,若想获得足够的产量,则需要庞大的反应设施,设施成本和运行成本高。
针对HCFO-1233xf转化率低的问题,Daikin公司[46]后续提出以Cr为主催化剂,通过浸渍、沉淀等方法,制备掺杂V、Nb、Ta等VB族元素的Cr基催化剂。结果显示,掺Nb后Cr基催化剂HCFO-1233xf转化率为24%,HFO-1234yf选择性为67%,均略有提升,但仍不适合工业化应用。
(3) 1,3,3,3-四氟丙烯
Dupont公司[47]提出以负载过渡金属的Cr2OxFy为催化剂,在300~400 ℃下,HFO-1234ze发生异构化反应生成HFO-1234yf的工艺。该工艺HFO-1234yf选择性很差,原料HFO-1234ze本就是需要的工业产品,再做异构化处理,增加了生产成本,应用价值不大。
(4) 1,1-二氯-2,3,3,3-四氟丙烯
旭硝子公司[48]提出1,1-二氯-2,3,3,3-四氟丙烯(CF3CF CCl2,CFO-1214ya)与H2在Pd负载型催化剂作用下,150~200 ℃反应生成HFO-1234yf的工艺。该工艺原料CFO-1214ya的获取很困难。
(5) 1,2,3,3,3-五氟丙烯
Dupont公司[49]提出HFO-1225ye先在Pd/C氢化催化剂作用下,50~200 ℃与H2加成反应生成HFC-245eb,后HFC-245eb在Al2O3、氟化氧化铝(F-Al2O3)催化下,300~450 ℃反应生成HFO-1234yf的工艺。该工艺原料HFO-1225ye获取较难,限制了该工艺的应用。
(6) 六氟丙烯
Arkema公司[50]提出六氟丙烯(CF3CF CF2,HFP)在Pd/C、Pd/AlF3催化作用下加氢生成1,1,1,2,3,3-六氟丙烷(CF3CHFCHF2,HFC-236ea),HFC-236ea在氢氧化钾水溶液中脱HF生成HFO-1225ye,HFO-1225ye再在Pd/C、Pd/AlF3催化作用下加氢生成HFC-245eb,HFC-245eb最后在氢氧化钾水溶液中脱HF生成HFO-1234yf的工艺。该工艺步骤繁琐,第三步加氢反应强放热,易产生过度加氢副产物,同时高温加氢危险性高,对设备和操作人员要求高。此外,脱HF步骤均为溶剂化反应,会产生大量废液,增加后处理成本。
山东东岳高分子材料有限公司[51]提出将浸渍法制备的Ni-Cu-La2O3/Al2O3、Ni-Cu-Li2O/Al2O3负载型催化剂分别用于HFP、HFO-1225ye加氢步骤,氟化氧化铬、氟化氧化铝分别用于HFC-236ea、HFC-245eb脱HF步骤,结果显示四步反应产率均高于94%。虽然该工艺原料HFP易得、产率高,但工业应用该工艺最少需要四个独立的单元,开发这样的生产设备需要大量的经济投资。
(7) 1,1,2,3-四氯丙烯
Honeywell公司[52]提出以Cr2O3/C、FeCl3/C为催化剂,在300 ℃下,1,1,2,3-四氯丙烯(CH2ClCCl= CCl2,HCO-1230xa)与HF反应生成HCFO-1233xf,HCFO-1233xf在SbCl5/C作用下,85 ℃与HF反应生成HCFC-244bb,HCFC-244bb在Cr2O3作用下,400 ℃脱HCl生成HFO-1234yf的工艺。该工艺HCO-1230xa会聚合导致催化剂失活,使得催化剂寿命短,对工业生产不利。
此外,Honeywell公司[53]提出HCO-1230xa与HF在SbCl5催化下,150~250 ℃液相反应生成HFC-245eb,分离得到高纯HFC-245eb后,在Pd/C、Ni/C作用下250~500 ℃气相反应生成HFO-1234yf的工艺。该工艺第一步氟化有副产物CF3CHFCH2Cl、CF3CHClCH2F、CF3CHClCH2Cl、CF3CCl CH2、CF3CClFCH3等产生,导致HFC-245eb收率低,最高为59%,同时副产物多也造成分离困难。
Arkema公司[54]提出HCO-1230xa在铬催化剂作用下与HF气相催化氟化一步生成HFO-1234yf、HCFO-1233xf、HFC-245cb及HCl,分离后得HFO-1234yf的工艺。该工艺铬催化剂需在约1 MPa、350 ℃条件下与HF接触活化,对设备要求高,操作复杂,且HFO-1234yf的分离繁琐。
2.3.3 其他C3原料路线Honeywell公司[55]提出2,2,3,3,3-五氟丙醇(CF3CHFCH2OH)与甲烷先在65~80 ℃混合成气态,然后经250~450 ℃预热,最后在Pd/AC作用下,400~700 ℃反应生成HFO-1234yf的工艺。该工艺存在选择性低的不足,同时原料价格较高,没有市场竞争力。
3 催化剂体系分析以上HFO-1234yf合成工艺,C1和C2有机物一般通过调聚反应实现碳链增长生成相应的中间体,然后中间体再进行氢化、氟化、脱卤化氢等反应生成最终产物HFO-1234yf。其中,调聚、氢化、氟化、脱卤化氢等反应过程均需催化剂的参与,本小节对目前催化剂的研究进展进行介绍与评述。
3.1 HFO-1234yf制备工艺调聚催化剂调聚反应,即根据需要控制聚合反应的聚合度,特别是合成低分子质量聚合物的反应[56]。调聚法是当今工业上合成卤代烃的主要方法,该方法简单易行且经济高效。从目前相关文献看,调聚合成HFO-1234yf中间体的催化剂,主要有铁催化剂、金属盐催化剂、金属盐类负载型催化剂以及合金催化剂。
3.1.1 铁催化剂调聚合成卤代烃的铁催化剂一般以铁、二价铁盐或三价铁盐为主要活性组分,并添加磷酰基化合物、亚磷酸烷基酯类、烷基磷酸酯类和亚硫酸钠等作为结构助剂来稳定活性组分,延长催化剂寿命。
Asahara等[57]道了一种以FeCl3为主催化剂、烷基磷酸酯为助催化剂,在160 ℃和0.6~0.7 MPa下,CH2=CH2与CCl4调聚生成HCC-250fb的方法。该方法收率超90%,但FeCl3与CCl4的混溶性很差,在反应过程中会形成焦油状副产物。信越化学工业株式会社[58]提出引入乙腈至FeCl3、亚磷酸烷基酯类二元催化体系,含腈的三元催化体系与CCl4有良好的混溶性,大幅降低了焦油状副产物的产生,解决了连续化生产中管道易堵塞的问题。此外,美国孟山都公司[59]提出将金属铁加入FeCl3、亚磷酸烷基酯类二元催化体系同样可降低焦油状副产物的产生。
Honeywell公司[60]提出以铁粉代替氯化铁作为主催化剂,在85~150 ℃和0.3~0.85 MPa下,调聚生成HCC-250fb的方案,该方案CCl4单程转化率为70%,HCC-250fb选择性为95%。
以商业铁粉为主催化剂时,铁粉易在釜底沉积结块导致活性降低。同时,铁粉也难以从反应器中移除。针对这一问题,宁波巨化化工科技有限公司[61]提出在固定床反应器中,以铁粉作为主催化剂,将原料CH2=CH2及CCl4和助催化剂磷酸三丁酯或磷酸三乙酯混合物预热后同时通入反应器,反应混合物在90~110 ℃和0.95~1.20 MPa下调聚生成HCC-250fb的方案,该方案收率超过80%。中国科学院宁波材料技术与工程研究所张业新等[62]提出了采用负载型纳米零价铁催化剂代替铁粉的方法,这可以显著改善单纯市售铁粉做催化剂时容易团聚的问题,且反应结束后催化剂容易从反应釜中脱除。他们首先采用十六烷基三甲基溴化铵对有机膨润土进行改性,然后以乙醇-水混合物为溶剂,使用FeSO4 ·7H2O作为铁源进行浸渍。最后,通过NaBH4溶液还原,得到有机膨润土负载的纳米零级铁催化剂。该催化剂性能优异,HCC-250fb的收率可达95.5%。
3.1.2 金属盐类催化剂金属盐SbF5、AlF3、FeF3、CuF2、ZrCl4、HfCl4、TiCl4、AlCl3、ZnBr2、AlBr3等金属卤化物常用作调聚合成HFO-1234yf中间体的催化剂。
Belenkii等[63]提出以SbF5为催化剂,在50 ℃下,CF2=CF2与CH3F调聚反应10 h生成HFC-245cb的方法。该方法的收率为67%。类似的,Daikin公司[64]利用CF2=CF2与CH3Cl在SbF5作用下调聚生成HFC-245cb,在70 ℃下反应10 h,TFE转化率为15%,HFC-245cb选择性为63%。但是,SbF5与原料CH3Cl发生氟氯交换生成SbClxF5-x会使转化率降低。
浙江省化工研究院[12]提出以ZrCl4、HfCl4、TiCl4、AlF3、AlCl3、SbF5中至少一种为催化剂,在0~50 ℃和0.8~3.0 MPa下,TrFE与CH2ClF调聚反应5~10 h生成HCFC-244eb的方案。该方案CH2ClF转化率为76.5% ~99.8%,HCFC-244eb选择性为75.5% ~89.9%。印度SRF公司[65]提出以选自SbF5、FeCl3、FeF3、NiCl2、NiBr2、NiF2、CuF2、CuCl2、ZnCl2、ZnBr2、AlBr3、AlCl3或溴氟化铝等类似物为催化剂,催化HCFC-1122与CH2F2调聚生成HCFC-244eb,但其产率不高,仅为29%。
3.1.3 金属盐类负载型催化剂金属盐类无载体型催化剂在调聚合成卤代烃工艺中存在一定的不足之处,如反应和后处理过程中,催化剂损耗较大,催化剂回收存在一定难度。相比之下,金属盐类负载型催化剂在反应和后处理过程中损耗较小,易回收利用,使得催化剂调聚合成卤代烃的工艺由液相转化为气相成为可能。
Honeywell公司[66]提出以SbF5/AC为催化剂,在50~70 ℃和0.02~0.69 MPa的反应条件下,TFE与CH3F气相调聚生成HFC-245cb的方案,该方案的TFE转化率为35% ~39%,HFC-245cb选择性为64% ~74%。但与均相催化剂SbF5相比,活性炭负载的SbF5催化剂的反应活性较低。浙江三美化工[11]提出以SbF3-SbF5-AlCl3/C为催化剂,在150~250 ℃和0.2~0.4 MPa下,HCFC-1122与CH2ClF气相调聚生成HCFC-243db的方案。该方案的反应收率最高为90.9%。此外,浙江三美化工以Lewis酸负载型催化剂FeCl3-AlCl3/C、MgCl2-CoCl2/Al2O3、SbF5-AlCl3/C等为调聚催化剂,在220~300 ℃,0.3~0.5 MPa,500~800 h-1的反应条件下,催化CCl2=CCl2与CH3Cl调聚生成HCC-240ab。
3.1.4 合金催化剂北京宇极科技公司[9]以铁、铬、镍合金为主催化剂,二甲基甲酰胺为助催化剂,在90~120 ℃和0.3~0.8 MPa的反应条件下,CH2=CH2与CCl4调聚生成HCC-250fb。合金可做出如鲍尔环、拉西环等散堆填料装于反应管中,既起到了催化作用,同时达到改善流型和强化传热的作用。但这种方法催化剂损耗很大。
3.2 HFO-1234yf制备工艺氢化催化剂氢化是有机化合物与氢分子的反应,在HFO-1234yf制备工艺中,主要包括两种氢化反应:双键的氢化、加氢脱卤。一般的还原催化剂都可用于氢化反应,特别是活性炭上负载的Pd、Pt等,载体还可以是金属氧化物(如氧化铝)或金属氟化物。
例如,Dupont公司[49]以Pd/C为催化剂,在50~200 ℃下,催化HFO-1225ye加氢生成HFC-245eb。Arkema公司[50]以Pd/C或Pd/AlF3为催化剂,催化HFP加氢生成中间体HFC-236ea,HFO-1225ye加氢生成中间体HFC-245eb。Dupont公司[31, 33]以Pd/AlF3为氢化催化剂,催化HCFC-235cb、HCFO-1224yd或CFC-1214ya与H2反应脱卤生成HFO-1234yf,但具体的选择性和转化率未公布。
西安近代化学研究所[42]先将V2O5加到Mg(NO3)2 ·6H2O和Cu(NO3)2 ·3H2O的混合水溶液中,再加入10% 的NH4HCO3调节溶液pH约为9,分离得到沉淀后烘干焙烧,最后用HF、H2活化焙烧后的固体得到Cu-V-Mg-F催化剂。在反应温度320 ℃下,上述催化剂催化HCFC-233bc与H2反应脱卤得到HCFO-1233yf,其转化率和选择性分别为92.4% 和93.1%。
Tian等[67]以磷化镍(Ni2P、Ni12P5、NiP3)为催化剂,催化HCFC-244bb与H2反应生成HFO-1234yf。在Ni3P的表面,Ni位点和Ni3团簇不仅能够有效地吸附H2,还能通过多种机制实现H2的活化。因此,相较于Ni2P和Ni12P5,Ni3P能够生成更多的活性氢物种,表现出更高的活性及对HFO-1234yf的选择性。在反应温度300 ℃下,HCFC-244bb转化率约为42%,HFO-1234yf选择性约为88%。
3.3 HFO-1234yf制备工艺氟化催化剂氟化反应是指在有机物分子中引入氟原子的过程,通常会涉及到氢原子被氟取代和其他卤素(Cl、Br等)被氟取代的反应。氟化反应的类型可分为液相氟化和气相氟化。
3.3.1 液相氟化催化剂液相氟化法的优势是反应温度相对较低,但是其操作压力通常比较高。此方法对于合成低氟代产物比较容易控制,但对高氟代产物则较难实现。同时,其所需的催化剂量大,且不易处理。液相氟化的催化剂通常为SbCl3或SbCl5。
例如,Honeywell公司[52]以SbCl5为催化剂,在85 ℃和6.9 MPa的反应条件下,液相氟化HCFO-1233xf生成HCFC-244bb。旭硝子公司[20]以SbCl5为催化剂,在80~90 ℃和0.95 MPa的反应条件下,液相氟化HCFC-241bb生成HCFC-244bb,此过程的转化率为100%,选择性为48.3%。山东联创节能新材料[37]以SbCl3或SbCl5为催化剂,液相氟化HCO-1230xf生成HFO-1234yf。
尽管液相氟化条件较温和,但基本为液相间歇工艺,催化剂难以回收再利用,不利于大规模连续化工业应用。
3.3.2 气相氟化催化剂气相氟化方法对操作压力要求比较低,通常在常压附近,但是需要相对较高的反应温度。催化剂通常为铬、IB族、IIIB族、VIIB族、VIII族以及稀土金属、碱土金属离子中的一种或多种,按不同基体又可以分为铬基、镁基、银基和活性炭基催化剂等。具有较高活性的催化剂一般是以铬化合物为主体的组合。
例如,彭小波[68]以Cr(NO3)3 ·9H2O为铬源、Al2O3为铝源,(NH4)2CO3为沉淀剂通过共沉淀法制备了Cr2O3-Al2O3,其可以催化HCO-1230xa与HF氟化反应制备HCFO-1233xf。研究结果显示,HCO-1230xa转化率和HCFO-1233xf选择性随反应温度升高均有所提高。当Cr/Al原子比为8 ∶2时,催化剂体系表现良好,原料HCO-1230xa的转化率和产物HCFO-1233xf的选择性都能达到98%。西安近代化学研究所Mao等[69]以CrCl3为铬源,氨水为沉淀剂,通过共沉淀法制备了Cr2O3,在260 ℃下,氟化HCO-1230xa制备了HCFO-1233xf。初始HCO-1230xa转化率为100%,HCFO-1233xf选择性为98%。在反应96 h后,转化率和选择性分别降低了12.4% 和12.1%。同时作者团队探究了La和Y改性的Cr2O3的性能。研究发现,经过La改性后,催化剂表面的Cr2OxFy物种含量显著增加,且催化剂比表面积也有所提升。这使得催化剂有更高的活性和更长的使用寿命,在使用96 h后,改性后的催化剂仍然可保持其初始活性。
谢遵运[70]以Cr(NO3)3 ·9H2O为前驱体,氨水为沉淀剂,通过共沉淀法制备了Cr2O3催化剂,其可以催化HCFO-1233xf与HF氟化反应生成HFO-1234yf,HCFO-1233xf的转化率为56.2% ~63.3%,HFO-1234yf选择性为58.2% ~60.7%。随后探究了Mg、Ga、Fe、Zn、Co等助剂的影响,发现这些助剂的添加有利于提高催化剂对HFO-1234yf的选择性,但不利于活性的提高。
巨化公司[71]以碳纳米管为载体,乙醇为溶剂,加入Cr(NO3)3 ·9H2O、LaNO3、NH4F、NH3 ·H2O,通过液相沉降法制备Cr2O3-LaOF-碳纳米管催化剂,在220 ℃、常压和500 h-1空速反应条件下,氟化HCO-1230xa生成了HFO-1234yf。原料HCO-1230xa的转化率在99% 以上,HFO-1234yf的选择性在60% 以上。
Arkema公司[72]提出了Ni-Cr负载型催化剂,其中载体为氟化氧化铬、氟化氧化铝、氟化活性炭或石墨碳,其可催化HCC-240db经过两步氟化反应生成HFO-1234yf。第一步,HCC-240db先与HF发生氟化反应生成HCFO-1233xf,HCC-240db的转化率可达100%,HCFO-1233xf选择性可达98.3%;第二步,HCFO-1233xf与HF气相反应成HFO-1234yf,HCFO-1233xf的转化率为10.3%,产物HFO-1234yf选择性为71.4%。
铬基催化剂由于其原料易得、活性较高的优点,引起了世界各国科学家的研究兴趣。但铬具有毒性,可以对人造成极大伤害,特别是高价铬具有强致癌性,且在一定条件下,三价铬和六价铬可以相互转化。所以亟须寻找安全环保无害、催化活性高、使用寿命长的非铬氟化催化剂。北京宇极科技公司[73]通过浸渍法制备了负载型非铬催化剂,其由非铬离子、助剂和载体组成,其中非铬离子为钼离子和钨离子,助剂为其他金属,载体为氟化铝、氟化镁、氟氧化铝、氟氧化镁或活性炭。其催化性能优异,HCFO-1233xf转化率可达85.5%,HFO-1234yf选择性可达84.5%,且连续运行1 000 h,催化活性基本不变。
3.4 HFO-1234yf制备工艺脱卤化氢催化剂脱HX反应是较为典型的一类消除反应,反应类型可分为液相脱卤化氢和气相脱卤化氢。
3.4.1 液相脱卤化氢催化剂液相脱卤化氢反应条件温和,但缺点是属于间歇工艺,采用大量溶剂,容易产生工业废物,难以处理,环境污染严重。常用的催化剂为甲基三辛基氯化铵、氯氟化铝、三乙基硅烷及聚乙二醇等。
例如,Honeywell公司[74]以甲基三辛基氯化铵为催化剂,在40~80 ℃下,HCFC-245cb或HCFC-244eb与KOH水溶液反应脱卤化氢得到HFO-1234yf。印度SRF公司[75]以聚乙二醇为催化剂,在85 ℃下,2-溴-1,1,1,2-四氟丙烷与NaOH水溶液反应脱卤化氢得HFO-1234yf。
3.4.2 气相脱卤化氢催化剂气相脱卤化氢催化剂大都由一种主体成分和单一或多种配体成分构成,根据主体成分的差异,可分为铬基、镁基及铝基催化剂。
(1) 铬基催化剂
铬基催化剂主要以Cr2O3和CrF3为基底。由于Cr2O3和CrF3本身具有较高的催化活性,能独立作为催化剂使用,可发挥出高效的催化作用。此外,通过负载Mg、Co、Ni、Zn等活性组分,可进一步提升催化剂的反应活性及稳定性,从而拓展其在更广泛的应用场景中的潜力。
例如,Honeywell公司[76]以Cr2O3氟化后形成的Cr2OxFy催化HFC-245eb脱HF生成HFO-1234yf,在反应温度440 ℃下,HFC-245eb流量为10 g ·h-1时,HFC-245cb的转化率为78%,HFO-1234yf的选择性为43%。Arkema公司[77]提出通过焙烧CrF3 ·H2O或用HF氟化Cr2O3获得Cr2OxFy来催化HFC-245cb脱HF生成HFO-1234yf,在350 ℃和0.1 MPa反应条件下,HFC-245cb的转化率为95%,HFO-1234yf的选择性为98%。贾文志等[78]采用浸渍法制备了一系列ZnO/Cr2O3催化剂,用于催化1,1,1,3,3-五氟丙烷(CF3CH2CHF2,HFC-245fa)脱卤化氢,以联产HFO-1234ze,HFO-1234yf和3,3,3-三氟丙炔(CF3C ≡ CH)。研究发现,随着ZnO含量的逐步增加,Cr2O3的晶粒尺寸呈现增大的趋势。此外,在催化剂表面,Cr(OH)3和CrO3物种的浓度逐渐降低,而Cr2O3物种的浓度则逐渐增加,ZnO与Cr2O3之间的相互作用增强了催化剂的表面酸性,进而使得催化剂对HFO-1234yf的选择性得到了提升。当ZnO添加量为2% 时,催化剂的表面酸度最高,此时HFO-1234yf的选择性也达到了最高,为11.7%。
(2) 镁基催化剂
镁基催化剂是以MgO为基底的催化剂,其成本相对低,对环境友好。
例如,Honeywell公司[79]通过将MgO浸渍于CsCl水溶液中,烘干焙烧得到质量分数为10% 的CsCl/MgO,在5% HF/N2的气氛下,350~490 ℃处理2 h后催化HCFC-244eb脱HCl生成HFO-1234yf。在反应温度400~500 ℃,HF处理的10% CsCl/MgO催化剂原料转化率约为33%,HFO-1234yf选择性约为97%,比相同条件下10% CsCl/MgF2的活性高约60%。Mao等[80]采用初湿浸渍法制备了一系列碱性金属改性的MgO催化剂,用于催化HCFC-244bb脱卤化氢生成HFO-1234yf。KF和CsF改性降低了MgO催化剂表面酸性,酸性的降低有利于抑制脱氢氟化过程。同时,碱金属改性会抑制HCFC-244bb在转化过程中发生的氟化反应,提高了HFO-1234yf的选择性。
(3) 铝基催化剂
Al基催化剂具有比表面积大、酸性强、制备简单、价格低廉及对环境无破坏等优点,被广泛使用。
例如,Miller等[81]以AlF3为催化剂,在400 ℃和接触时间60 s的反应条件下,催化HFC-245cb脱HF生成HFO-1234yf,其转化率为98.1%,选择性为93.1%。Dupont公司[49]在425 ℃,使用HF/N2混合气氟化Al2O3获得Al2OxFy催化剂催化HFC-245eb脱HF生成HFO-1234yf。在反应温度400 ℃下,HFC-245eb转化率为98.1%,HFO-1234yf选择性为91.3%。
4 结论总结以上HFO-1234yf制备路线,高温条件和转化率低限制了C1原料的路线工业应用。
从C2原料出发的多为国内路线,C2原料经调聚得到C3中间体,后对中间体进行一系列反应来合成最终产物HFO-1234yf。浙江三美化工提出的以2-氯-1,1-二氟乙烯和氟氯甲烷为起始原料,经调聚、脱卤、氟化得到HFO-1234yf的工艺。第一步反应中HCFC-243db的收率可达90.4%,第二步反应中HCFO-1233xf的收率可达92.5%,第三步反应中HFO-1234yf的收率可达91.8%。其采用对人体和环境均有害的2-氯-1,1-二氟乙烯为原料,能对环境起到保护作用,且三步反应均有较高收率,因此有较高的工业化应用价值。
从C3原料出发的HFO-1234yf的核心制备专利几乎完全掌握在Honeywell、Dupont、Daikin、旭硝子等外国企业手中,工业化价值较高的工艺如下:(1)Arkema公司提出的以3,3,3-三氟丙烯为起始原料,经氯化、氢化、氟化得到HFO-1234yf的工艺。该工艺第一步液相釜式反应无需催化剂的参与,分离成本低,且反应效果好,3,3,3-三氟丙烯转化率可达95.3%,HCFC-243db选择性大于99%。后续氢化、氟化反应气相可连续,反应条件温和。(2)西安近代化学研究所提出的以1,1,1,2,2,3-六氯丙烷为起始原料,经氟化、氢化、氟化得到HFO-1234yf的工艺。该工艺三步均为气相反应,容易实现连续化大规模生产,且每步反应均有较高的转化率和选择性,有很好的工业应用前景。
我国是全球最大的氟化工生产国,拥有丰富的氟资源储量。此外,国内对制冷剂需求旺盛,市场容量巨大。现有的HFO-1234yf合成路线都存在一定的局限性,例如原料成本高、能耗高、步骤繁琐、反应不连续、催化剂合成制备复杂、原料转化率和目标产物选择性低等。因此,后续研究重点是(1)开发具有自主知识产权的新一代绿色高效的HFO-1234yf合成路线,降低HFO-1234yf的生产成本,加快绿色传热工质的国产化替代;(2)针对目前C2原料调聚制备HFO-1234yf路线中普遍存在的催化剂损耗大、催化剂套用次数低、产物分离纯化困难等问题,设计开发寿命长、转化率和选择性高、再生简便的调聚催化剂;(3)气相氟化、脱卤化反应中铬基催化剂的催化活性较高,但铬基催化剂会对环境造成破坏,不符合低碳环保的要求,终将面临淘汰。因此,开发高活性、高寿命、高抗炭能力非铬基催化剂刻不容缓。
| [1] |
MCLINDEN M O, HUBER M L. (R)Evolution of refrigerants[J]. Journal of Chemical & Engineering Data, 2020, 65(9): 4176-4193. |
| [2] |
ZHANG X X, LI Y Z. A review of recent research on hydrofluoroolefin (HFO) and hydrochlorofluoroolefin (HCFO) refrigerants[J]. Energy, 2024, 311: 133423. DOI:10.1016/j.energy.2024.133423 |
| [3] |
SICARD A J, BAKER R T. Fluorocarbon refrigerants and their syntheses: Past to present[J]. Chemical Reviews, 2020, 120(17): 9164-9303. DOI:10.1021/acs.chemrev.9b00719 |
| [4] |
ARORA P, SESHADRI G, TYAGI A K. Fourth-generation refrigerant: HFO 1234yf[J]. Current Science, 2018, 115(8): 1497-1503. DOI:10.18520/cs/v115/i8/1497-1503 |
| [5] |
MALEY M D. Process for preparing 2,3,3,3-tetrafluoropropene: US, 2931840A[P]. 1960-04-05.
|
| [6] |
李雄亚. 2,3,3,3-四氟丙烯(HFO-1234yf)专利统计与分析[J]. 浙江化工, 2018, 49(5): 16-19. LI X Y. Patent statistics and analysis of 2,3,3,3-tetrafluoropropene(HFO-1234yf)[J]. Zhejiang Chemical Industry, 2018, 49(5): 16-19. |
| [7] |
韩春华, 张恒, 张永明, 等. 2,3,3,3-四氟丙烯的制备方法: CN, 103833511A[P]. 2014-06-04. HAN C H, ZHANG H, ZHANG Y M, et al. Preparation method of 2,3,3,3-tetrafluoropropene: CN, 103833511A[P]. 2014-06-04. |
| [8] |
李宏峰, 徐晓波, 黄雪浩, 等. 一种2,3,3,3-四氟丙烯的制备方法: CN, 106316777A[P]. 2017-01-11. LI H F, XU X B, HUANG X H, et al. Preparation method for 2,3,3,3-tetrafluoropropene: CN, 106316777A[P]. 2017-01-11. |
| [9] |
周晓猛, 贾晓卿, 鲍鹏. 一种2,3,3,3-四氟丙烯的合成方法: CN, 102199071A[P]. 2011-09-28. ZHOU X M, JIA X Q, BAO P. Method for synthesizing 2,3,3,3-tetrafluoropropene: CN, 102199071A[P]. 2011-09-28. |
| [10] |
李宏峰, 王金明, 吴国颖. 一种偏氟乙烯为原料合成四氟丙烯HFO1234yf的方法: CN, 105111040A[P]. 2015-12-02. LI H F, WANG J M, WU G Y. Method for synthesizing tetrafluoropropene HFO1234yf with vinylidene fluoride as raw material: CN, 105111040A[P]. 2015-12-02. |
| [11] |
徐庆瑞, 王晓东, 徐煜, 等. 一种2,3,3,3-四氟丙烯的制备方法: CN, 109438170A[P]. 2019-03-08. XU Q R, WANG X D, XU Y, et al. Preparation method of 2,3,3,3-tetrafluoropropylene: CN, 109438170A[P]. 2019-03-08. |
| [12] |
刘敏洋, 于万金, 林胜达, 等. 一种两步法制备2,3,3,3-四氟丙烯的方法: CN, 115215724A[P]. 2022-10-21. LIU M Y, YU W J, LIN S D, et al. Method for preparing 2,3,3,3-tetrafluoropropene by two-step method: CN, 115215724A[P]. 2022-10-21. |
| [13] |
VAN DER PUY M. Process for the preparation of 2,3,3,3-tetrafluoropropene (HFO-1234yf): US, 20090253946A1[P]. 2009-10-08.
|
| [14] |
MASATOSHI N, ATSUSHI S, AKINARI S. Process for producing fluorine-containing propene compound: WO, 2010013576[P]. 2009-06-25.
|
| [15] |
李宏峰, 王树华, 徐晓波, 等. 一种2,3,3,3-四氟丙烯的制备方法: CN, 106008145A[P]. 2016-10-12. LI H F, WANG S H, XU X B, et al. Preparation method of 2,3,3,3-tetrafluoropropylene: CN, 106008145A[P]. 2016-10-12. |
| [16] |
李宏峰, 王树华, 徐晓波, 等. 一种用甲基氯化镁制备2,3,3,3-四氟丙烯的方法: CN, 105111038A[P]. 2015-12-02. LI H F, WANG S H, XU X B, et al. Method for preparing 2,3,3,3-tetrafluoropropene by using methyl magnesium chloride: CN, 105111038A[P]. 2015-12-02. |
| [17] |
韩文锋, 刘兵, 韦小丽, 等. 一种由四氟乙烯制备2,3,3,3-四氟丙烯的方法: CN, 114634395A[P]. 2022-06-17. HAN W F, LIU B, WEI X L, et al. Method for preparing 2,3,3,3-tetrafluoropropene from tetrafluoroethylene: CN, 114634395A[P]. 2022-06-17. |
| [18] |
徐庆瑞, 王晓东, 吴业铧, 等. 一种2,3,3,3-四氟丙烯的制备方法: CN, 109608302A[P]. 2019-04-12. XU Q R, WANG X D, WU Y H, et al. Preparation method of 2,3,3,3-tetrafluoropropene: CN, 109608302A[P]. 2019-04-12. |
| [19] |
徐庆瑞, 王晓东, 吴陈兴, 等. 一种气相连续合成2,3,3,3-四氟丙烯的方法: CN, 109438171A[P]. 2019-03-08. XU Q R, WANG X D, WU C X, et al. Gas-phase continuous synthesis method of 2,3,3,3-tetrafluoropropylene: CN, 109438171A[P]. 2019-03-08. |
| [20] |
SATOSHI K, TAKASHI O, HIDEKAZU O. Processes for producing 2-chloro-1,1,1,2-tetrafluoropropane and 2,3,3,3-tetrafluoropropene: EP, 2374782[P]. 2009-12-15.
|
| [21] |
TUNG H S, MUKHOPADHYAY S, VAN DER PUY M, et al. Method for producing fluorinated organic compounds: WO, 2007079435[P]. 2007-01-03.
|
| [22] |
SMITH J W, MCGUINESS C, SHARRATT A P. Process for the preparation of 2,3,3,3-tetrafluoropropene: US, 08552228B2[P]. 2013-10-08.
|
| [23] |
方海滔, 应永安, 吕洁, 等. 2-氯-1,1,1,2-四氟丙烷和2,3,3,3-四氟丙烯的制备方法: CN, 112778079A[P]. 2021-05-11. FANG H T, YING Y A, LYU J, et al. Preparation method of 2-chloro-1,1,1,2-tetrafluoropropane and 2,3,3,3-tetrafluoropropene: CN, 112778079A[P]. 2021-05-11. |
| [24] |
NOSE M, KARUBE D, SUGIYAMA A, et al. Process for preparing 2,3,3,3-tetrafluoropropene: WO, 2010013796[P]. 2009-07-24.
|
| [25] |
TUNG H S, WANG H Y. Preparation of fluorinated olefins via catalytic dehydrohalogenation of halogenated hydrocarbons: WO, KR20170024136A[P]. 2017-03-06.
|
| [26] |
张伟, 吕剑, 曾纪珺, 等. 2,3,3,3-四氟丙烯的制备方法: CN, 101913988A[P]. 2010-12-15. ZHANG W, LYU J, ZENG J J, et al. Preparation method of 2,3,3,3-tetrapion propylene: CN, 101913988A[P]. 2010-12-15. |
| [27] |
TAKEHIRO C, SHUN O, DAISUKE K. Method for producing fluorine-containing olefin: JP, 2015110774[P]. 2015-29-05.
|
| [28] |
张彦, 雷俊, 谭显文, 等. 一种合成2,3,3,3-四氟丙烯的催化剂及其制备方法和用途: CN, 103055843A[P]. 2013-04-24. ZHANG Y, LEI J, TAN X W, et al. Catalyst for synthesizing 2,3,3,3-tetrafluoropropene and preparation method and application thereof: CN, 103055843A[P]. 2013-04-24. |
| [29] |
RAO V N M, SIEVERT A C, NAPPA M J. Dehydrofluorination process to manufacture hydrofluoroolefins: WO, 2008030439[P]. 2007-09-05.
|
| [30] |
MUKHOPADHYAY S, NAIR H, VAN DER PUY M, et al. Method for producing fluorinated organic compounds: EP, 1943203[P]. 2012-12-19.
|
| [31] |
NAPPA M J, RAO V N M, SIEVERT A C. Processes for producing 2,3,3,3-tetrafluoropropene, a process for producing 1-chloro-2,2,3,3,3-pentafluoropropane and azeotropic compositions of 1-chloro-2,3,3,3-tetrafluoropropene with hf: WO, 2008054778A3[P]. 2008-08-14.
|
| [32] |
NAPPA M J, RAO V N M, SIEVERT A C. Processes for producing 2,3,3,3-tetrafluoropropene and/or 1,2,3,3-tetrafluoropropene: US, 20100320412A1[P]. 2010-12-23.
|
| [33] |
RAO V N M, SIEVERT A C. Process for producing 2,3,3,3-tetrafluoropropene: WO, 2008060614[P]. 2007-11-15.
|
| [34] |
NAPPA M J, RAO V N M, SIEVERT A C. Processes for producing and compositions comprising 2,3,3,3-tetrafluoropropene and/or 1,2,3,3-tetrafluoropropene: EP, 2091898[P]. 2007-10-31.
|
| [35] |
SUGIYAMA A, CHAKI T. Method for producing olefin: WO, 2008053811[P]. 2007-10-26.
|
| [36] |
PIGAMO A, DEVIC M, WENDLINGER L. Process for the preparation of fluorinated compounds: CN, 101671229[P]. 2009-09-07.
|
| [37] |
李洪国, 李俊. 2,3,3,3-四氟丙烯的合成方法: CN, 104987278A[P]. 2015-10-21. LI H G, LI J. Method for synthesizing 2,3,3,3-tetrafluoropropene: CN, 104987278A[P]. 2015-10-21. |
| [38] |
ELSHEIKH M Y, BONNET P, CHEN B B. Process for the manufacture of tetrafluoroolefins: WO, 2011130108[P]. 2011-04-08.
|
| [39] |
韩升, 吕剑, 曾纪珺, 等. 一种2,3,3,3-四氟丙烯的制备方法: CN, 115403442A[P]. 2022-11-29. HAN S, LYU J, ZENG J J, et al. Preparation method of 2,3,3,3-tetrafluoropropene: CN, 115403442A[P]. 2022-11-29. |
| [40] |
杨会娥, 任建纲, 杨刚, 等. 一种反式/顺式-HFO-1234ze和HFO-1234yf的联产制备工艺: CN, 113527049A[P]. 2021-10-22. YANG H E, REN J G, YANG G, et al. Co-production preparation process of trans/cis-HFO-1234ze and HFO-1234yf: CN, 113527049A[P]. 2021-10-22. |
| [41] |
杨刚, 许磊, 杨会娥, 等. 一种制备2,3,3,3-四氟丙烯和2-氯-3,3,3-三氟丙烯的方法: CN, 103896725A[P]. 2014-07-02. YANG G, XU L, YANG H E, et al. Preparation method of 2,3,3,3-tetrafluoropropene and 2-chloro-3,3,3-trifluoropropene: CN, 103896725A[P]. 2014-07-02. |
| [42] |
吕剑, 秦越, 马辉, 等. 一种2,3,3,3-四氟丙烯的制备方法: CN, 105753639A[P]. 2016-07-13. LYU J, QIN Y, MA H, et al. Preparation method of 2,3,3,3-tetrafluoropropene: CN, 105753639A[P]. 2016-07-13. |
| [43] |
PIGAMO A, DEVIC M, WENDLINGER L. Process for the preparation of trifluorinated and tetrafluorinated compounds: WO, 2010029419[P]. 2009-09-11.
|
| [44] |
耿为利, 周强, 王宗令, 等. 一种2,3,3,3-四氟丙烯的合成方法: CN, 105367378A[P]. 2016-03-02. GENG W L, ZHOU Q, WANG Z L, et al. Synthesis method of 2,3,3,3-tetrafluoropropene: CN, 105367378A[P]. 2016-03-02. |
| [45] |
YUKO S, KAKERU H, TAKEHIRO C, et al. Method for producing fluorine-containing alkane: JP, 2011029637[P]. 2011-02-15.
|
| [46] |
加留部大輔, 茶木勇博, 西海雅巳, など. 含フッ素オレフィンの製造方法: JP, 5888436B2[P]. 2016-03-22. KARUBE D, CHAKI T, NISHIUMI M, et al. Method for producing fluorine-containing olefin: JP, 5888436B2[P]. 2016-03-22. |
| [47] |
PETROV V A, NAPPA M J. Catalytic isomerization processes of 1,3,3,3-tetrafluoropropene for making 2,3,3,3-tetrafluoropropene: US, 20080058562A1[P]. 2008-03-06.
|
| [48] |
OKAMOTO H, SASAO Y. Processes for production of 1,1-dichloro-2,3,3,3-tetra- fluoropropene and 2,3,3,3-tetrafluoropropene: WO, 2010074254[P]. 2009-12-25.
|
| [49] |
RAO V N M, SIEVERT A C, NAPPA M J. Process to manufacture 2,3,3,3-tetrafluoropropene: WO, 2008030440[P]. 2007-09-05.
|
| [50] |
AVRIL K, COLLIER B. Method for preparing fluorine compounds: WO, 2011010025[P]. 2010-06-01.
|
| [51] |
韩春华, 张永明, 张恒, 等. 2,3,3,3-四氟丙烯的合成方法: CN, 102267869A[P]. 2011-12-07. HAN C H, ZHANG Y M, ZHANG H, et al. Synthetic method of 2,3,3,3-tetrafluoropropene: CN, 102267869A[P]. 2011-12-07. |
| [52] |
KOPKALLI H, CHIU Y, COTTRELL S A, et al. Integrated process for fluoro-olefin production: US, 2011105807[P]. 2009-11-03.
|
| [53] |
MUKHOPADHYAY S, LIGHT B A, CANTLON C L, et al. Processes for synthesis of fluorinated olefins: WO, 2009052064[P]. 2008-10-14.
|
| [54] |
ELSHEIKH M Y, BONNET P. Catalytic gas phase fluorination of 1230xa to 1234yf: WO, 2009158321[P]. 2009-06-23.
|
| [55] |
MUKHOPADHYAY S, NAIR H K, TUNG H. Catalytic conversion of hydrofluoroalkanol to hydrofluoroalkene: WO, 2006063069[P]. 2005-12-09.
|
| [56] |
杨鲁腾, 宋妍妍, 王术成, 等. 调聚反应在合成卤代烃中的应用[J]. 有机氟工业, 2017(2): 41-46. YANG L T, SONG Y Y, WANG S C, et al. Application of synthesis of halogenated hydrocarbons by telomerization reaction[J]. Organo-Fluorine Industry, 2017(2): 41-46. |
| [57] |
ASAHARA T, SATO T. Telomerization of ethylene and carbon tetrachloride[J]. Kog Kagaku Zasshi, 1971, 74(4): 703-705. DOI:10.1246/nikkashi1898.74.4_703 |
| [58] |
MINORU T, HARUO O, MITSUO U, et al. Process for the preparation of tetrachloroalkanes: US, 4243607A[P]. 1981-01-06.
|
| [59] |
WOODARD S S. Process for producing 1,1,2,3-tetrachloropropene: US, 4535194A[P]. 1985-08-13.
|
| [60] |
WANG H Y, TUNG H S, CLOSE J, et al. Synthesis of 1,1,2,3-tetrachloropropene: US, 20140221705A1[P]. 2014-08-07.
|
| [61] |
周强, 钟骏良, 夏林兵, 等. 一种1,1,1,3-四氯丙烷的连续生产方法: CN, 111056913A[P]. 2020-04-24. ZHOU Q, ZHONG J L, XIA L B, et al. Continuous production method of 1,1,1,3-tetrachloropropane: CN, 111056913A[P]. 2020-04-24. |
| [62] |
张业新, 邓艳艳, 张建, 等. 一种1,1,1,3-四氯丙烷的制备方法: CN, 114835554A[P]. 2022-08-02. ZHANG Y X, DENG Y Y, ZHANG J, et al. Preparation method of 1,1,1,3-tetrachloropropane: CN, 114835554A[P]. 2022-08-02. |
| [63] |
BELENKII G G, PETROV V A, RESNICK P R. Addition of hydrofluorocarbons to fluoroolefins: US, 06184426B2[P]. 2001-02-06.
|
| [64] |
KARUBE D, YAMASHITA T, SUGIYAMA A, et al. Process for preparing fluorine-containing propane: WO, 2010131760[P]. 2010-05-11.
|
| [65] |
IYENGAR S, CHELLAIAH M, VINAYAGAM P, et al. Preparing 1,1,1,2-tetrafluoropropene involves fluorinating trichloroethene, dehydrohalogenating 1,2-dichloro-1,1-difluoroethane, reacting difluorochloroethene with difluoromethane, and performing dehydrohalogenation: IN, 201911002026-A[P].
|
| [66] |
MUKHOPADHYAY S, TUNG H S, VAN DER PUY M, et al. Method for producing fluorinated organic compounds: US, 20190263736A1[P]. 2019-08-29.
|
| [67] |
TIAN S, MAO W, SUN P F, et al. Breakthrough synthesis of 2,3,3,3-tetrafluoropropene via hydrogen-assisted selective dehydrochlorination of 1,1,1,2-tetrafluoro-2-chloropropane over nickel phosphides[J]. Journal of Catalysis, 2020, 391: 366-377. DOI:10.1016/j.jcat.2020.08.022 |
| [68] |
彭小波. 四氯丙烯氟化合成四氟丙烯(HFC-1234yf)催化剂的研究[D]. 杭州: 浙江师范大学, 2012. PENG X B. Catalysts studies on fluorination from tetrachloropropene to tetrafluoropropene (HFC-1234yf)[D]. Hangzhou: Zhejiang Normal University, 2012. |
| [69] |
MAO W, WANG B, MA Y B, et al. Selective gas-phase catalytic fluorination of 1,1,2,3-tetrachloropropene to 2-chloro-3,3,3-trifluoropropene[J]. Catalysis Communicat ions, 2014, 49: 73-77. DOI:10.1016/j.catcom.2014.02.013 |
| [70] |
谢遵运. 2-氯-3,3,3-三氟丙烯氟化合成四氟丙烯(HFC-1234yf, HFC-1234ze)催化剂的研究[D]. 杭州: 浙江师范大学, 2013. XIE Z Y. Catalysts studies on fluorination from 2-chloro-3,3,3-trifluoropropene to tetrafluoropropene (HFC-1234yf, HFC-1234ze)[D]. Hangzhou: Zhejiang Normal University, 2013. |
| [71] |
王金明. 一种气相氟化合成2,3,3,3-四氟丙烯的催化剂的制备方法: CN, 104492496A[P]. 2015-04-08. WANG J M. Preparation method for gas phase fluorination synthesis of 2,3,3,3-tetrafluoropropylene catalyst: CN, 104492496A[P]. 2015-04-08. |
| [72] |
WENDLINGER L, BONNET P, PIGAMO A, et al. Process for the preparation of 2,3,3,3 tetrafluoropropene: WO, 2012052797[P]. 2012-04-26.
|
| [73] |
权恒道, 张呈平, 李忠, 等. 浸渍法制备钼基和钨基氟-氯交换催化剂: CN, 107126954A[P]. 2017-09-05. QUAN H D, ZHANG C P, LI Z, et al. Impregnation method prepared molybdenum-based and tungsten-based fluoride-chlorine exchange catalyst: CN, 107126954A[P]. 2017-09-05. |
| [74] |
BEKTESEVIC S, TUNG H S, WANG H Y, et al. Method for producing tetrafluoropropenes: US, 2011270000[P]. 2011-05-28.
|
| [75] |
IYENGAR S, CHELLAIAH M, ARUMUGAM T, et al. Preparation of 2,3,3,3-tetrafluoropropene, intermediate and composition thereof: WO, 2019220463A1[P]. 2019-11-21.
|
| [76] |
MUKHOPADHYAY S, BORTZ C L, LIGHT B A, et al. Process for synthesis of fluorinated olefins: US, 2009099396[P]. 2008-10-12.
|
| [77] |
ELSHEIKH M Y, BONNET P, KEELEY O C N, et al. Dehydrofluorination of pentafluoroalkanes to form tetrafluoroolefins: WO, 2011140013A8[P]. 2012-11-22.
|
| [78] |
JIA W Z, FANG X X, FANG C T, et al. Selective dehydrofluorination of 1,1,1,3,3-pentafluoropropane to synthesize tetrafl-uoropropylene and trifluoropropyne over the ZnO/Cr2O3 catalysts[J]. Chemistryselect, 2020, 5(42): 13027-13032. DOI:10.1002/slct.202002721 |
| [79] |
WANG H, TUNG H S. Process for dehydrochlorinating 1,1,1,2-tetrafluoro-2-chloropropane to 2,3,3,3-tetrafluoropropene in the presence of an alkali metal-doped magnesium oxyfluoride catalyst and methods for making the catalyst: US, 20090299107A1[P]. 2009-12-03.
|
| [80] |
MAO W, BAI Y B, WANG W, et al. Highly selective dehydrochlorination of 1,1,1,2-tetrafluoro-2-chloropropane to 2,3,3,3-tetrafluoropropene over alkali metal fluoride modified MgO catalysts[J]. Chemcatchem, 2017, 9(5): 824-832. DOI:10.1002/cctc.201601259 |
| [81] |
MILLER R N, NAPPA M J, RAO V N M, et al. Azeotrope compositions comprising 2,3,3,3-tetrafluoropropene and hydrogen fluoride and uses thereof: US, 20070100175A1[P]. 2007-05-03.
|




