2. 绍兴市质量技术监督检测院,浙江 绍兴 312366;
3. 嘉兴学院 生物与化学工程学院,浙江 嘉兴 314001
2. Shaoxing Testing Institute of Quality and Technical Supervision, Shaoxing 312366, China;
3. College of Biological, Chemical Sciences and Engineering, Jiaxing University, Jiaxing 314001, China
环己烷氧化反应是目前工业生产环己醇和环己酮(俗称KA油)的重要途径,KA油可进一步氧化生产尼龙6, 6的主要原料己二酸,环己酮也可进一步肟化制备尼龙6的主要原料己内酰胺[1]。但是,环己烷的氧化产物环己醇和环己酮更容易发生进一步氧化反应生成酸及其衍生物酯等副产物[2]。为提高原料的利用率和减少副产物的生成量,工业生产中控制环己烷的单程转化率在4%以内,以保证环己醇和环己酮的总选择性约80%;而未反应的环己烷需经分离循环使用,因此,现有环己烷液相氧化工艺的主要特点是环己烷单程转化率低、原料循环量大和过程能耗高。为提高环己烷氧化反应的单程转化率,国内外就环己烷液相氧化反应进行了多方面的研究,尤其在新催化剂开发方面做了许多尝试[3~5],而从氧化反应器的传质混合性能与反应特性耦合方面改善环己烷液相氧化反应的优化研究尚少。
微通道反应器因其具备高面积体积比[6]、高安全性[7]、优异的传质和传热性能[8, 9]等优点而受到普遍关注,并在一些强放热的液相反应[10]和气相反应[11]、快速气液相反应[12]等过程中得到了实际应用。微通道反应器在环己烷液相氧化反应中也有一些应用研究[13~16],但或因所选择的微通道反应器管径过大,或因未添加催化剂,所得实验结果都不甚理想。本文在内径为0.762 mm、总长度为20 m的微通道反应器内,以环己酮为引发剂、环烷酸钴(Ⅱ)为催化剂、纯氧为氧化剂,考察了表观液体流速、表观气体流速、反应温度、反应压力和催化剂用量等因素对环己烷转化率、主要产物浓度和选择性的影响,以期获得合适的工艺条件。
2 实验部分 2.1 实验试剂与仪器实验试剂环己烷(AR,纯度≥99.5%)、环己酮(AR,纯度≥99.5%)、无水乙醇(AR,纯度≥99.7%)、氢氧化钠(AR,纯度≥96.0%)、碘化钾(AR,纯度≥99.0%)、可溶性淀粉(AR)、五水合硫代硫酸钠(AR,纯度≥99.0%)等均购于国药集团化学试剂有限公司,氧气(99.5%)购自杭州今工特种气体有限公司,三苯基膦(CP)和氯苯(GC)购自上海晶纯试剂有限公司,实验用水为去离子二次蒸馏水。
实验主要仪器包括高压输液泵(LC-500A,杭州旭昱科技有限公司)、T型混合器(SUS-1/16,杭州旭昱科技有限公司)、气体质量流量控制器(CS200,北京七星华创电子股份有限公司)、不锈钢微通道管(0.762 mm I.D.×20 m,上海济成分析仪器有限公司)和背压阀(RW75,杭州宝研仪表有限公司)。
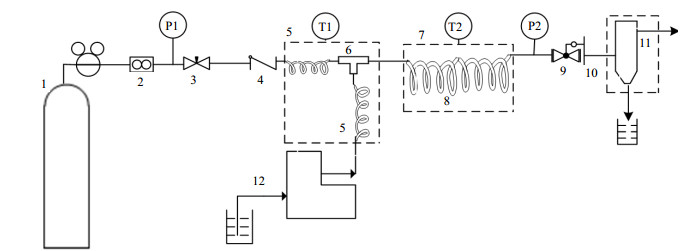
2.2 实验方法微通道反应器由内径为0.762 mm不锈钢微通道管8、等径T型混合器6、氧气预热管5、液体预热管5等构建,实验装置如图 1所示。环己烷液体(含催化剂和环己酮引发剂)采用高压输液泵12输送并控制流量;氧气由氧气钢瓶1提供、经过氧气减压阀、过滤器后由气体质量流量控制器2控制流量;氧气流经针型截止阀3、单向阀4和预热段后,进入T型混合器,与预热后的环己烷混合进入微通道反应器中进行氧化反应。微通道反应器连同前置的气、液两相预热段和T型混合器均置于恒温油浴中。反应物料流经背压阀9进入气液微分离器11进行分离,液相产物收集至产物瓶中,气相排空。气液分离器外加冷凝套。反应压力由背压阀控制,也可通过在P1处增加压力缓冲罐和P2位置改用微量调节阀控制。
|
图 1 微通道反应器装置 Fig.1 Schematic diagram of the microchannel reactor setup 1.oxygen 2. mass flow meter 3. shutoff valve 4. check valve 5. pre-heater 6. T-mixer 7. oil bath 8. stainless steel microchannel tube 9. back-pressure regulator 10. cooling system 11. micro separator 12. HPLC pumper |
产品中环己醇和环己酮通过气相色谱定量分析(Shimadzu GC-2014),色谱柱为HP-INNOWAX毛细管柱(30 m × 0.25 mm × 0.25 μm)。色谱操作条件:N2为载气,柱前压120 kPa;H255 kPa;空气50 kPa;汽化室温度280℃;检测器(FID)温度280℃;柱温为100℃(从50℃开始程序升温);分流比为50:1;氯苯为内标物;进样量为1 μL。其中环己醇含量扣除了环己基过氧化氢(CHHP)与三苯基膦还原后定向生成的量。CHHP含量用滴定法测定。除此之外,环己烷深度氧化产物是酸类化合物,主要有己二酸、丁二酸、丙二酸和戊酸等,其中己二酸占主要部分,为便于分析,这里统一指代为己二酸。己二酸含量用酸碱滴定法测定。总酯类含量用皂化结合酸式反滴定的方法测定。
反应转化率通过产品中所有生成物的摩尔量总和除以初始环己烷摩尔量计算;若以环己烷转化的摩尔量计算则会因为其易挥发性导致结果偏大。各产物选择性通过相应产物的生成量除以所有产物的摩尔量总和计算。另外,表观液体流速和表观氧气流速为以微通道截面积计算的流速,而表观停留时间(τ)为理论计算值,即τ =微通道管长度/表观流速。微通道反应器中气液两相流的实际停留时间为气液两相流动的综合影响的停留时间。
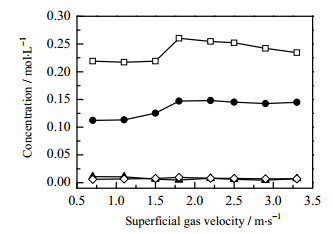
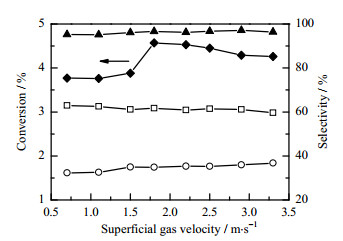
3 结果与讨论 3.1 表观气体流速的影响管式反应器中反应物的转化率取决于其在反应器内的停留时间,而环己烷液相氧化过程是一个气液相反应过程,环己烷和氧气的流速将决定反应物料在微通道中的停留时间和环己烷的转化率[14]。实验中在固定表观液体流速为0.004 m·s-1,反应温度165℃,反应压力1.4 MPa,催化剂浓度10 ppm,引发剂浓度0.2%(wt)的条件下,考察了表观氧气流速(0.70 ~3.30 m·s-1)对环己烷氧化反应的影响,结果见图 2和图 3。从图中可以看出,因中间产物CHHP在催化剂作用下易分解为环己醇和环己酮,因此CHHP浓度很低,环己烷氧化产物主要为环己醇和环己酮。环己烷转化率和各产物浓度随着气速增大呈现两个阶段的变化趋势。在氧气流速较小时,环己烷转化率和环己酮浓度随氧气流速增大而缓慢增大,而环己醇浓度几乎保持稳定;当氧气流速大于1.50 m·s-1时,环己烷转化率、环己醇和环己酮浓度均有一个突跃提高,在气速为1.80 m·s-1时达到最大值,尔后环己烷转化率和环己醇浓度随氧气流速增大而缓慢下降,而环己酮浓度几乎保持稳定。CHHP和己二酸浓度均很小,数值变化不大,己二酸变化趋势与环己酮基本相同。图 3表明,环己醇、环己酮及目标产物总选择性分别随氧气流速增大而下降和增大,但变化幅度不大。这可能与微通道内反应物料的流动型态有关。气液两相经等径T型混合器混合后进入微通道,当氧气流速较小时,微通道内气液两相呈现稳定的弹状流[17],气液两相交替流动,气体弹状流随气速增大而变长、液膜减小,但液膜变化幅度不显著,气液相界面积主要取决于液相流速,因此环己烷转化率和醇、酮浓度变化不显著;当氧气增大到一定程度,气液流型逐渐转变为弹状流-环状流,气液界面波动剧烈,相界面积大幅增加,强化了气液相间氧的传质系数[18],加快了环己烷氧化反应速度。因此可认为气液两相流型过渡转变是导致环己烷氧化转化率突跃提高的原因。氧气流速的增大也会导致环己烷停留时间逐渐减小,氧化反应时间缩短,环己烷转化率下降[15]。
|
图 2 表观气体流速对产物浓度的影响 Fig.2 Effects of superficial gas velocity on product concentration ‒□‒ cyclohexanol ‒●‒ cyclohexanone ‒▲‒ CHHP ‒◇‒ adipic acid |
|
图 3 表观气体流速对转化率和选择性的影响 Fig.3 Effects of superficial gas velocity on conversion and selectivity ‒▲‒ cyclohexanol + cyclohexanone + CHHP ‒◆‒ cyclohexane ‒□‒ cyclohexanol ‒○‒ cyclohexanone |
表观氧气流速的影响结果表明,适当增加表观气体流速可提高环己烷的转化率,且能维持较高的醇、酮及CHHP总选择性,但并非气速越大越好,保持氧气流速在气液流型转变范围内较合理。气速过大时大部分氧气未被消耗而排出,造成浪费。因此选择表观气体流速为1.80 m·s-1来进行下一步的研究。
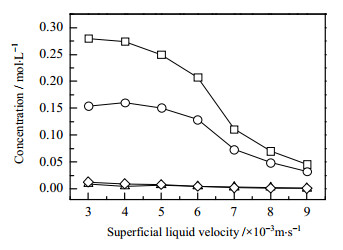
3.2 表观液体流速的影响微通道内液体流速也是影响气液相流动型态、传质特性和物流停留时间的关键因素。因此,本文在固定表观气体流速(标准状态下)为1.80 m·s-1,反应温度165℃,反应压力1.4 MPa,催化剂浓度10 ppm(以Co2+计),引发剂浓度0.2%(wt)的条件下,考察了表观液体流速(0.003 ~ 0.009 m·s-1)对环己烷氧化反应的影响,结果见图 4和图 5。从图中可以看出,环己烷氧化产物浓度和环己烷转化率随着环己烷表观流速的增大,即停留时间的缩短而下降,主要氧化产物环己醇和环己酮浓度也呈现相同变化趋势。而当环己烷表观液速较小(小于0.005 m·s-1)时变化缓慢,这可能是在表观氧气流速一定条件下,环己烷表观流速较小(小于0.005 m·s-1)时,其停留时间增长、氧化反应程度提高[13, 15];同时气液摩尔比较大,气液流型可能从弹状流-环状流逐渐转变为环状流[17],液膜和气液相界面积减小,氧气传递量下降,从而导致环己烷氧化反应转化率变化缓慢。
|
图 4 表观液体流速对产物浓度的影响 Fig.4 Effects of superficial liquid velocity on product concentration ‒□‒ cyclohexanol ‒○‒ cyclohexanone ‒△‒ CHHP ‒◇‒ adipic acid |
|
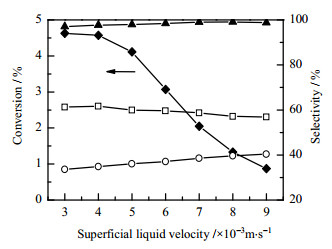
图 5 表观液体流速对转化率和选择性的影响 Fig.5 Effects of superficial liquid velocity on conversion and selectivity ‒▲‒ cyclohexanol + cyclohexanone + CHHP ‒◆‒ cyclohexane ‒□‒ cyclohexanol ‒○‒ cyclohexanone |
图 5表明,环己醇、环己酮及目标产物总选择性分别随环己烷表观液速的降低而缓慢单调上升和下降,即随环己烷转化率的增大而缓慢上升和下降。但醇、酮及CHHP总选择性均大于96.0%。综合考虑环己烷转化率和醇、酮及CHHP总选择性,选择表观液体流速为0.004 m·s-1来进行下一步的研究。
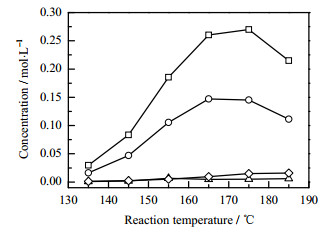
3.3 反应温度的影响环己烷氧化反应是个平行-串联的复合反应体系[2],反应温度对不同反应呈现不同的影响,最终决定氧化反应产物的选择性。实验中固定反应压力为1.4 MPa,液体表观速度为0.004 m·s-1,气体表观速度为1.80 m·s-1,催化剂浓度10 ppm,引发剂浓度0.2 %(wt),考察了反应温度(135 ~ 185℃)对环己烷氧化反应的影响,结果见图 6和图 7。从图中可以看出,在温度较低时,环己烷转化率和各产物浓度都较低。随着反应温度的升高,环己烷氧化反应速度加快,除CHHP外其他产物浓度明显增大,其中环己酮和环己醇分别在170 ~ 175℃达到浓度最高值后逐渐下降,而己二酸浓度却缓慢单调上升。这是因为环己烷氧化为自由基链式反应,反应温度升高加快了自由基引发速率和氧化反应速速率,但反应温度继续升高(大于170℃),则有利于环己烷氧化产物环己醇和环己酮发生深度氧化、生成酸类化合物,因此环己烷氧化与环己醇、环己酮氧化为竞争反应过程,更多的溶解氧被环己醇和环己酮氧化反应所消耗,从而导致环己烷氧化反应速率下降,即环己烷转化率下降,综合结果造成环己醇和环己酮浓度也随之下降。同时,温度升高后期也可能导致沸点相对较低的环己烷气化加剧,从而降低转化率。
|
图 6 反应温度对产物浓度的影响 Fig.6 Effects of reaction temperature on product concentration ‒□‒ cyclohexanol ‒○‒ cyclohexanone ‒△‒ CHHP ‒◇‒ adipic acid |
|
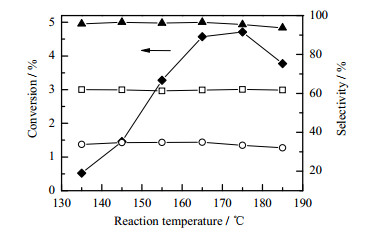
图 7 反应温度对转化率和选择性的影响 Fig.7 Effects of reaction temperature on conversion and selectivity ‒▲‒ cyclohexanol + cyclohexanone + CHHP ‒◆‒ cyclohexane ‒□‒ cyclohexanol ‒○‒ cyclohexanone |
图 7表明,随着反应温度升高,环己烷转化率在175℃达到最大值(4.57%),环己醇选择性基本保持不变,而环己酮及目标产物总选择性在165℃后开始逐渐下降。这可能是环己醇比环己酮更为稳定的缘故。另外,醇、酮及CHHP三者总选择性均大于93.0%,高于文献[2]报道的搅拌釜反应器中环己烷无催化氧化结果(约85%)。另外,在微通道反应器中,环己烷的表观停留时间约83 min(如考虑气流的推动作用、实际停留时间远小于该数值)可达到4.57%转化率;而搅拌釜反应器中达到相同转化率的反应时间约100 min,且难以保持较高的目标产物选择性[2](转化率 > 2%后,选择性 < 92%)。可见,在微通道反应器中进行环己烷液相氧化反应,相同条件下可获得更高的环己烷转化率和目标产物选择性。
综合考虑环己烷转化率和醇、酮及CHHP总选择性两个方面,适宜反应温度为165℃。
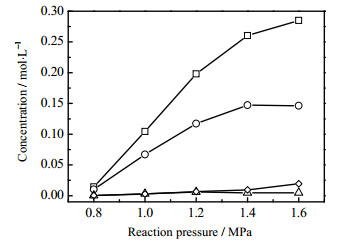
3.4 反应压力的影响环己烷氧化为气液相反应过程,反应压力直接决定了氧气在环己烷中的溶解和液相蒸发量。根据环己烷饱和蒸汽压与温度的对应情况,实验中固定反应温度为165℃,液体表观为0.004 m·s-1,气体表观流量为1.80 m·s-1,催化剂浓度10 ppm,引发剂浓度0.2%(wt),考察了不同反应压力(0.8 ~ 1.6 MPa)对反应的影响,结果见图 8和图 9。从图中可以看出,在反应压力较低时,环己烷转化率和各产物浓度都较低。随着压力升高,氧化反应转化率增大;除CHHP外其它产物浓度也随着反应压力的升高而明显增大,但在反应压力大于1.2MPa时环己烷转化率和环己醇、环己酮浓度的增大趋势逐渐减缓,而己二酸浓度呈现明显的增大趋势。这些结果说明反应压力升高可增大氧气溶解能力,加快了环己烷氧化反应速率,主要产物醇、酮浓度也随之增大;但反应压力升高(即溶解氧浓度升高)更有利于环己酮氧化生成酸类副产物,消耗了部分环己烷氧化生成的环己酮,导致环己酮浓度趋于不变。同时环己酮的竞争氧化反应消耗了更多的溶解氧,从而导致环己烷氧化反应有所减缓。
|
图 8 压力对产物浓度的影响 Fig.8 Effects of reaction pressure on product concentration ‒□‒ cyclohexanol ‒○‒ cyclohexanone ‒△‒ CHHP ‒◇‒ adipic acid |
|
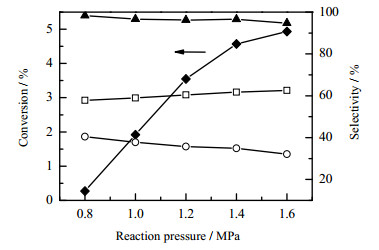
图 9 压力对转化率和选择性的影响 Fig.9 Effects of reaction pressure on conversion and selectivity ‒▲‒ cyclohexanol + cyclohexanone + CHHP ‒◆‒ cyclohexane ‒□‒ cyclohexanol ‒○‒ cyclohexanone |
图 9表明,随着反应压力升高,环己醇和环己酮的选择性分别呈现缓慢增大和下降,目标产物总选择性也逐渐下降。其原因可能是环己醇比环己酮更为稳定,对溶解氧浓度变化不敏感。该结果与文献[2]报道的结果一致。综合考虑环己烷转化率和醇、酮及CHHP总选择性两个方面,选择反应压力为1.2 ~ 1.4 MPa比较适宜。
3.5 催化剂用量的影响环己烷液相氧化是一个典型的自由基链式反应,添加催化剂有利于活性自由基的生成,从而加快氧化反应速度。二价有机酸钴盐(环烷酸钴、硬脂酸钴或辛酸钴)常用于催化有机物氧化,其催化作用表现为二价钴遇氧或过氧化物被氧化为三价钴的同时,伴随了活性自由基的生成,从而加快了反应进程[1]。实验中采用环烷酸钴(Ⅱ)为催化剂,固定表观液体流速为0.004 m·s-1,表观气体流速为1.80 m·s-1,反应温度165℃,反应压力1.4 MPa,引发剂浓度0.2%(wt),考察了催化剂浓度(0 ppm ~ 25 ppm)对反应的影响,结果见图 10和图 11。
|
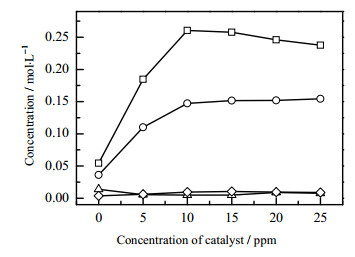
图 10 催化剂用量对产物浓度的影响 Fig.10 Effects of catalyst amount on product concentration ‒□‒ cyclohexanol ‒○‒ cyclohexanone ‒△‒ CHHP ‒◇‒ adipic acid |
|
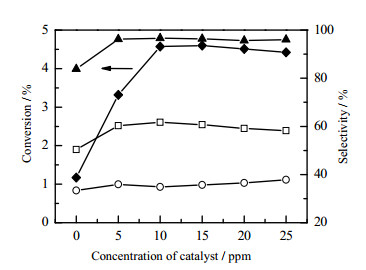
图 11 催化剂用量对转化率和选择性的影响 Fig.11 Effects of catalyst amount on conversion and selectivity ‒▲‒ cyclohexanol + cyclohexanone + CHHP ‒◆‒ cyclohexane ‒□‒ cyclohexanol ‒○‒cyclohexanone |
从图中可以看出,在实验条件下不添加催化剂时环己烷也能发生氧化反应(无催化氧化),但环己烷转化率和各产物浓度均很低。添加催化剂后,环己烷氧化反应明显加快,相同反应时间内环己烷转化率及产物环己醇、环己酮浓度有较大的增加,而CHHP浓度则呈现下降趋势,己二酸浓度则一直变化不大。这是因为适量钴离子的加入增加了活性自由基浓度、缩短诱导期、加速氧化反应速率,同时可促进中间产物CHHP分解生成目标产物环己醇和环己酮。但是加入过多的催化剂则可能对氧化反应起抑制作用。因为在二价钴向三价钴转化时,来不及转化的二价钴将会消耗自由基造成其链式反应中断,从而抑制反应进一步进行[18],如式(1)所示。
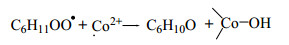
|
(1) |
图 11表明,随着催化剂用量的增加,环己醇、环己酮及目标产物总选择性也逐渐提高。催化剂用量达到10 ppm后,继续增大催化剂用量对氧化反应并无增益,相反环己烷转化率还呈现小幅下降趋势。整个过程醇、酮及CHHP总选择性都在97.0%以上。结果表明,微通道反应器中适当的催化剂加入量可以起到加速反应从而提高环己烷转化率和醇、酮及CHHP总选择性的作用。综合而言,实验中催化剂浓度为10 ppm ~ 15 ppm比较适宜。
4 结论以纯氧作为氧化剂、环烷酸钴(Ⅱ)为催化剂、环己酮为引发剂,在通道内径为0.762 mm、长度为20 m的微通道反应器内进行环己烷液相氧化反应时,表观气体流速对反应的影响较为复杂;表观液体流速对反应结果有直接影响;反应温度、反应压力和催化剂用量适当升高(增大)有利于反应的进行,但过高(大)则会加深副反应程度。在氧气表观流速为1.80 m·s-1、环己烷表观流速为0.004 m·s-1、温度165℃、压力1.4 MPa、环己酮加入量为0.2%(wt)和催化剂钴(Ⅱ)浓度为10 ppm时,环己烷的转化率为4.57%,环己醇、环己酮和环己基过氧化氢(CHHP)的选择性分别为61.72%、34.87%和1.12%,己二酸的选择性小于3.0%。结果表明,微通道反应器用于环己烷液相催化氧化,能有效改善气液相间传质,降低副产物的生成和提高环己烷氧化反应速率。
| [1] | Van de Vyver S, Leshkov Y R. Emerging catalytic processes for the production of adipic acid[J]. Catalysis Science & Technology , 2013, 3(6): 1465-1479. |
| [2] | CHEN Ji-zhong(陈纪忠), FEI Li-min(费黎明), FAN Zhen(范镇), et al. A study on the kinetics of liquid phase oxidation of cyclohexane without catalyst(环己烷液相无催化剂的氧化动力学研究)[J]. Chemical Reaction Engineering and Technology(化学反应工程与工艺) , 1992, 9(3): 237-245. |
| [3] | Ishii Y. A novel catalysis of N-hydroxyphthalimide (NHPI) combined with Co (acac) n (n=2 or 3) in the oxidation of organic substrates with molecular oxygen[J]. Journal of Molecular Catalysis A: Chemical , 1997, 117(1-3): 123-137. DOI:10.1016/S1381-1169(96)00265-8. |
| [4] | XU Li-xin(许立信), HE Chao-hong(何潮洪), ZHU Ming-qiao(朱明乔), et al. Cyclohexane oxidation over nano gold catalysts supported on zirconia-modified alumina(锆改性氧化铝负载的纳米金催化剂上环己烷氧化研究)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报) , 2009, 23(2): 309-313. |
| [5] | Zhang Z Q, Huang J, Zhang L, et al. Facile synthesis of Cu-Pd bimetallic multipods for application in cyclohexane oxidation[J]. Nanotechnology , 2014, 25(43): 435602. DOI:10.1088/0957-4484/25/43/435602. |
| [6] | Herskowits D, Herskowits V, Stephan K, et al. Characterization of a two-phase impinging jet absorber-Ⅱ. Absorption with chemical reaction of CO2 in NaOH solutions[J]. Chemical Engineering Science , 1990, 45(5): 1281-1287. DOI:10.1016/0009-2509(90)87120-H. |
| [7] | Janicke M T, Kestenbaum H, Hagendorf U, et al. The Controlled oxidation of hydrogen from an explosive mixture of gases using a microstructured reactor/heat exchanger and Pt/Al2O3catalyst[J]. Journal of Catalysis , 2000, 191(2): 282-293. DOI:10.1006/jcat.2000.2819. |
| [8] | YUE Jun(乐军), CHEN Guang-wen(陈光文), YUAN Quan(袁权), et al. Mass transfer in gas-liquid flow in microchannels(微通道内气-液传质研究)[J]. Journal of Chemical Industry and Engineering(China)(化工学报) , 2006, 57(6): 1296-1303. |
| [9] | Shao N, Gavriilidis A, Angeli P. Mass transfer during Taylor flow in microchannels with and without chemical reaction[J]. Chemical Engineering Journal , 2010, 160(3): 873-881. DOI:10.1016/j.cej.2010.02.049. |
| [10] | Hallett J P, Welton T. Room-temperature ionic liquids: solvents for synthesis and catalysis. 2[J]. Chemical Review , 2011, 111(5): 3508-3576. DOI:10.1021/cr1003248. |
| [11] | GE Hao(葛皓), CHEN Guang-wen(陈光文), YUAN Quan(袁权), et al. Kinetics of gas phase catalytic oxidation of toluene in microreactor(微反应器内甲苯气相催化氧化反应动力学)[J]. Journal of Chemical Industry and Engineering (China)(化工学报) , 2007, 58(8): 1967-1972. |
| [12] | Mason B P, Price K E, Steinbacher J L, et al. Greener approaches to organic synthesis using microreactor technology[J]. Chemical Reviews , 2007, 107(6): 2300-2318. DOI:10.1021/cr050944c. |
| [13] | Jevtic R, Ramachandran PA, Dudukovic M P. Capillary reactor for cyclohexane oxidation with oxygen[J]. Chemical Engineering Research and Design , 2010, 88(3): 255-262. DOI:10.1016/j.cherd.2009.12.008. |
| [14] | Fischer J, Lange T, Boehling R, et al. Uncatalyzed selective oxidation of liquid cyclohexane with air in a microcapillary reactor[J]. Chemical Engineering Science , 2010, 65(16): 4866-4872. DOI:10.1016/j.ces.2010.05.028. |
| [15] | ZHANG Hai-guang(张海广). Gas-liquid two-phase flow characteristic and liquid phase oxidation of cyclohexane in a mini-channel reactor (小通道反应器中气液两相流动特性及环己烷液相氧化的研究)[D]. Chengdu (成都): Sichuan University (四川大学), 2012. |
| [16] | Wang L, Zhu M Q, Lu J G, et al. Uncatalyzed oxidation of cyclohexane in the microchannels[J]. Key Engineering Materials , 2013, 562-565: 1542-1547. DOI:10.4028/www.scientific.net/KEM.562-565. |
| [17] | DAI Li (戴莉). Study on gas-liquid flow and mass transfer in microchannels (微通道内的气液两相流动与传质研究)[D]. Tianjin (天津): Tianjin University (天津大学), 2010. http://cdmd.cnki.com.cn/Article/CDMD-10056-2010209272.htm |
| [18] | The production and application of caprolactam (己内酰胺生产及应用)[M]. Beijing (北京): Hydrocarbon Processing Press (烃加工出版社), 1986. |




