近年来,随着化石能源的日益消耗以及大众对环境问题的重视,将生物质及其衍生物转化为化学品或者燃料吸引了越来越多的关注[1]。甘油是一种重要的生物质衍生物,在植物油或动物油脂通过酯转移反应生产生物柴油的工艺过程中,平均每生产9吨生物柴油就有1吨甘油生成[2]。甘油选择性氢解制备高附加值的1, 3-丙二醇是具有工业应用潜力的工艺,有助于增加生物柴油产业的经济效益。1, 3-丙二醇作为重要的化学品和化学中间体,可以用于增塑剂、洗涤剂、防腐剂和乳化剂的合成,它最主要的用途是作为单体合成高性能可降解聚酯材料如聚对苯二甲酸丙二醇酯(PTT)[2]。
一般情况下,Pt、Ru、Cu等单金属催化剂催化甘油氢解反应的主要产物为1, 2-丙二醇,而1, 3-丙二醇的选择性通常低于5%[3~5]。研究表明,向Pt、Ir、Rh等贵金属催化剂中加入Re或者W物种作为助剂,能够显著提高催化活性和1, 3-丙二醇的选择性[6~11],其中双金属Ir-Re催化剂是目前报道最有效的甘油氢解制备1, 3-丙二醇的催化剂之一。日本的Tomishige研究小组[7]采用常规的浸渍、干燥、焙烧和还原的方法制备的Ir-Re双金属催化剂,在加入固体酸作为反应助剂的条件下最高可以得到30%的1, 3-PD收率,但甘油氢解24 h的平均速率仅为15.4 mol1, 3-PD molIr-1·h-1。该双金属催化剂通过EXAFS、TPR、XRD和XPS等一系列表征发现其结构为Ir-ReOx,即Ir金属粒子表面覆盖有部分低价Re氧化物。本课题组在前期的研究工作中[9]提出了一种浸渍干燥后直接还原的方法制备的Ir-Re双金属催化剂,其具有Ir-Re合金结构,能显著提高甘油的反应速率,24 h的平均速率在同样的反应条件下可达25.6 mol1, 3-PDmolIr-1·h-1,遗憾的是甘油转化率达到63%时,1, 3-PD选择性下降到了30%左右。显然,焙烧与否改变了Ir-Re双金属催化剂的微观结构,并显著影响它们在甘油氢解反应中的催化性能。
通常情况下,双金属催化剂的结构及性能较单金属更易受到热处理条件如焙烧温度的影响[9, 12, 13]。比如,Epron等人[12]的研究表明,双金属Pt-Cu催化剂经过高温焙烧处理后,由于Cu迁移到Al2O3载体上,破坏了Pt和Cu之间的相互作用,从而降低其催化硝酸盐还原反应的性能。另一方面,由于Re具有很强的亲氧性[14],极易与载体表面的羟基或氧化物种形成Re-O键,使其铺展在载体表面并显示出特殊的还原性质。研究表明[15]单金属Re催化剂前驱体的焙烧温度、负载量等都可影响Re的还原程度。因此,本论文针对Ir-Re双金属催化剂,系统考察催化剂前驱体的焙烧温度对Ir-Re双金属结构的影响,以期探索调控Ir-Re双金属催化剂结构和性能的关键因素,为甘油选择性氢解高效催化剂的优化和理性设计提供指导,进一步提高1, 3-PD选择性和收率。
2 实验方法 2.1 催化剂制备以氯铱酸及高铼酸铵水溶液为前驱体,采用分步-等体积浸渍法制备双金属Ir-Re/KIT-6催化剂,具有三维有序介孔孔道的二氧化硅载体KIT-6(比表面积812 m2·g-1,孔径7 nm)的合成如文献[16]所示。将一定量氯铱酸滴加到KIT-6上,充分搅拌并在室温下老化12 h,随后在120℃下干燥12 h。用相同的方法将活性组分Re负载到Ir/KIT-6催化剂上,静置过夜并于120℃烘干12 h。将浸渍干燥后的样品在空气气氛中进行高温焙烧3 h,焙烧温度分别为350、500和650℃。焙烧后的催化剂命名为“Ir-Re/KIT-6-Ct”,其中“C”表示焙烧处理,“t”表示焙烧温度。随后,将焙烧后的Ir-Re/KIT-6-Ct于500℃的氢气气氛中(70 mL·min-1)还原3 h,并通入1%的O2/Ar混合气钝化20 min。还原后的催化剂命名为“Ir-Re/KIT-6-CtR”。催化剂中金属Ir和Re的名义负载量分别为4.0%(wt)和3.8%(wt),Re/Ir比(mol/mol)为1.0。作为参照,采用相同的制备方法制备相同负载量的单金属Ir和Re催化剂,命名的方式如上述。
2.2 甘油氢解反应甘油氢解反应在高压间歇釜式反应器(100 mL,Parr 4575A)中进行。将20 g浓度为20%(wt)甘油水溶液,150 mg Ir-Re/KIT-6催化剂和50 mg的固体酸助剂(Amberlyst-15)加入反应釜密封后,通入H2(2.0MPa)吹扫3次,设定搅拌转速为500 r·min-1,升温至120℃后,通入氢气至8 MPa,反应12 h后,冷却至室温并取样以超高效液相色谱(UPLC,Waters 2414)进行定性定量分析,采用RID检测器以及C18色谱柱。
2.3 催化剂的表征XRD表征在Rigaku D/Max2550VB/PC衍射仪(Rigaku公司)上完成;采用透射电子显微镜(TEM,JEM-2100F)表征Ir-Re/KIT-6催化剂的颗粒尺寸大小,加速电压为200 kV;用配有原位池的傅里叶变换红外光谱仪(FT-IR,Nicolet 6700)测试样品的CO吸附的红外光谱,催化剂均预先进行上述还原处理并钝化,原位还原温度为350℃;NH3-TPD和H2-TPR测试均在AutoChem 2920 (Micromeritics)仪器上进行,升温速率为10℃·min-1。
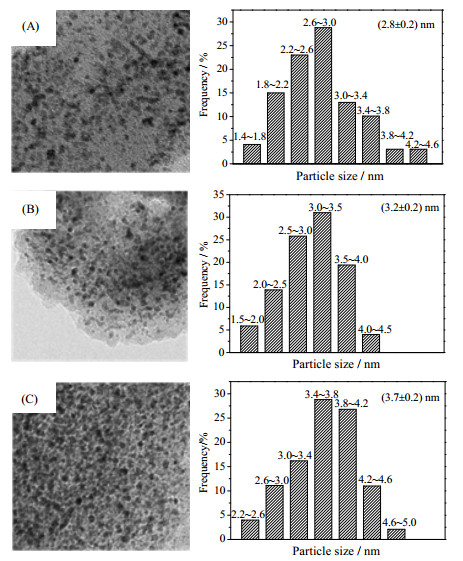
3 结果与讨论 3.1 焙烧温度对催化剂性质和结构的影响采用TEM考察了不同焙烧温度对金属颗粒的粒径大小及分布的影响,如图 1所示。从图中可以看出,所有样品中金属颗粒均高度分散于KIT-6载体表面,粒径显示出单峰分布,没有观测到明显的烧结现象。随着焙烧温度从350提高到500和650℃,平均粒径从2.8 nm逐渐增大到3.2和3.7 nm(表 1)。采用CO化学吸附定量分析了双金属Ir-Re催化剂的CO吸附能力,如表 1所示,随着焙烧温度的升高其CO吸附能力逐渐下降。由于Re金属对CO的吸附能力极弱,CO吸附主要发生在催化剂表面的Ir原子簇上,因此,这一CO吸附的减弱也表明Ir的分散度逐渐降低。这与TEM观察到的催化剂表面颗粒大小随焙烧温度上升逐渐增加的事实一致。
|
图 1 不同焙烧温度下Ir-Re双金属催化剂的TEM图及相应的粒径分布图 Fig.1 TEM images and corresponding size distribution of Ir-Re/KIT-6 catalysts with different pretreatments (A) Ir-Re/KIT-6-C350R (B) Ir-Re/KIT-6-C500R (C) Ir-Re/KIT-6-C650R |
| 表 1 焙烧温度对催化剂性质的影响 Table 1 Effects of calcination temperature on the properties of the bimetallic Ir-Re/KIT-6 catalysts |
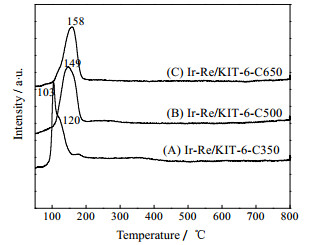
图 2给出了经过不同焙烧温度处理的Ir-Re催化剂的H2-TPR图谱。从图中可以看出,Ir-Re/KIT-6-C350的TPR图谱中存在103℃主还原峰和120℃附近的肩峰,这可能是由于在低温焙烧后还有一部分活性组分前体以盐的形式高度分散在载体上,2个还原峰分别对应于高分散的前体和活性组分氧化物晶相(IrO2和Re2O7)的还原。而随着焙烧温度提高到500和650℃,活性组分均形成氧化物晶相,同时Ir和Re物种之间相互作用较强,在TPR图谱中分别显示了位于149和158℃的单一还原峰,较单Ir和单Re催化剂的还原峰(分别为192和320℃[9])显著降低。同时,随着焙烧温度的提高,还原峰的温度逐渐向高温区域移动,这一方面由于焙烧温度提高增大了金属颗粒的平均粒径,另一方面也是由于焙烧温度升高增加了金属颗粒和载体之间的相互作用。
|
图 2 双金属Ir-Re催化剂经过不同温度焙烧处理后的TPR图谱 Fig.2 TPR profiles of Ir-Re/KIT-6 after different calcination treatments:(A) Ir-Re/KIT-6-C350 (B) Ir-Re/KIT-6-C500 (C) Ir-Re/KIT-6-C650 |
通过对H2-TPR过程中的耗氢量做定量分析,进一步确定活性组分的还原程度。已有的研究表明IrO2极易完全还原为金属态,因此Re的平均价态可以通过扣除IrO2还原所消耗的氢气量进行计算,结果如表 1所示。从表中可以看出,Ir-Re/KIT-6-C350样品的Re物种能够完全还原为金属态;Ir-Re/KIT-6-C500中Re的平均价态为+2.4,表明形成了低价氧化铼(ReOx)物种[7];而焙烧温度进一步提高制备的Ir-Re/KIT-C650中Re的平均价态进一步增大到+4.4,说明有更多高价态的氧化铼物种生成。显然,随着预处理焙烧温度的升高,Ir-Re双金属催化剂中的Re物种的还原能力显著降低。这可能是由于Re具有高度亲氧性,高温焙烧显著增强了Re物种和载体表面的Si-OH之间的相互作用,生成了Re7+-O-载体的化学键[17]。一方面,Re物种和载体间作用力的增强直接降低了它的还原能力;另一方面,由于Ir和Re的相互作用能够促进Ir和Re的共同还原[7],而Re7+-O-载体化学键的形成降低Re物种在载体表面的移动性能,不利于Ir和Re物种之间相互作用,因此降低其还原能力。
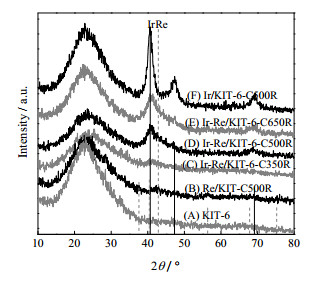
图 3给出了不同焙烧温度处理后的双金属Ir-Re催化剂以及对应的500℃焙烧还原的单金属Ir、Re催化剂和载体的XRD图谱。从中可以看出,单金属Ir/KIT-6-C500R的XRD图谱中可以在40.7,47.3和69.1°观测到尖锐的金属Ir的衍射峰,而Re/KIT-6-C500R的XRD图谱仅能在42.8°观测到微弱的Re金属的衍射峰,这表明单金属Re可以在KIT-6载体表面高度分散,而单金属Ir则容易在KIT-6表面生成结晶度高的较大粒子。焙烧还原处理的Ir-Re双金属催化剂,可以明显看到其晶体结构的演变。Ir-Re/KIT-6-C350R催化剂仅在位于Ir和Re的最强峰之间的41.2°显示出很弱的Ir(111)衍射峰,说明金属的晶粒较小,和TEM表征结果一致(其平均粒径为2.8 nm)。而Ir-Re/KIT-6-C500R和Ir-Re/KIT-6-C650R则在40.8°显示出明显的归属于Ir(111)晶面的衍射峰,但峰强度远远低于单金属Ir的衍射峰,同时没有观测到归属于Re金属或者Re氧化物的衍射峰,这说明Ir金属形成较大晶粒,而Re物种则在催化剂上高度分散。
|
图 3 双金属Ir-Re催化剂的XRD图谱 Fig.3 XRD patterns of bimetallic Ir-Re catalysts upon different calcination treatments |
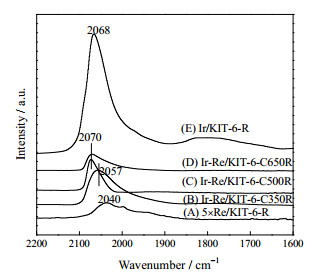
前期的研究表明CO-DRIFTS是用于研究Ir-Re双金属催化剂的合金结构和程度的有力手段[7, 9],不同焙烧温度制备的催化剂的CO-DRIFTS图谱如图 4所示。单金属Ir/KIT-6-R的2068和1800 cm-1附近的CO吸附峰分别归属于CO在Ir表面的线式吸附和桥式吸附,而Re/KIT-6-R的2040 cm-1附近的CO吸附峰则归属于CO在Re表面的线式吸附。需要指出的是,Re对于CO的吸附强度远远小于Ir。Ir-Re/KIT-6-C350R的CO吸附峰位于2057 cm-1附近,介于单金属Ir和Re的CO吸附峰之间,这是Ir-Re合金形成的有力证明:Ir和Re合金化后,由于Ir的电负性更强,电子由Re原子转移至Ir原子上,从而导致电子在Ir表面富集,造成Ir-CO峰的红移;相应的,Re-CO峰因此发生蓝移现象,最终形成的Ir-Re合金的CO吸附峰介于中间。此外,Ir-Re/KIT-6-C350R的CO吸附峰强度显著低于Ir/KIT-6-R,这可能是由于Re原子稀释了表面Ir的原子数,从而降低了催化剂对CO的吸附能力。同时,Ir和Re合金化造成的金属电子状态的变化也可能导致CO吸附能力的下降。
|
图 4 双金属Ir-Re以及单金属Ir、Re催化剂的CO-DRIFT图谱 Fig.4 DRIFT spectra of CO adsorbed onto Re/KIT-6-R, Ir/KIT-6-R and Ir-Re/KIT-6 upon different calcination treatments Note : The signal intensity of Re/KIT-6 is artificially multiplied by 5 for easy comparison |
Ir-Re/KIT-6-C500R和Ir-Re/KIT-6-C650R的CO吸附峰均位于2070 cm-1附近,和单金属Ir/KIT-6-R的CO吸附峰位置基本一致,可以归结为CO在表面Ir金属上的线式吸附。而Ir-CO吸附峰没有出现红移现象,说明其表面Ir中心的电子状态没有发生明显的改变,即Ir和Re没有发生强相互作用,不存在Ir-Re合金结构。此外,相较于Ir/KIT-6-R,Ir-Re/KIT-6-C500R和Ir-Re/KIT-6-C650R的吸附强度明显更低。这是由两方面原因造成,一是由于高温焙烧制备的Ir-Re合金催化剂中的Re以ReOx的氧化态形式存在覆盖在催化剂的表面,ReOx物种不吸附CO,因而导致催化剂CO吸附能力的降低;二是由于高温焙烧使得金属的分散度降低,从而降低CO吸附。
为了进一步确定Ir-Re双金属催化剂中Ir和Re之间的作用和结构,采用STEM-HAADF-EDX测定了Ir-Re/KIT-6-C500R催化剂中单个金属纳米粒子的化学组成,结果如图 5所示。从单颗粒的EDX图谱可以观测到Re和Ir,这表明单个金属纳米粒子上同时存在Ir和Re,两者紧密接触并相互作用。结合前述TPR、XRD和CO-DRIFTS结果可以认为:Ir-Re/KIT-6-C350R催化剂上Ir和Re均以金属态存在,且CO红外吸附峰存在明显的位移,因此存在Ir-Re合金结构;而Ir-Re/KIT-6-C500R和Ir-Re/KIT-6-C650R中,Ir物种完全还原为Ir0,并形成一定大小的晶粒,而Re物种则处于氧化态。高温焙烧的Ir-Re双金属催化剂上的金属为Ir-ReOx的结构,即高度分散的ReOx附着于Ir晶粒表面,这一结构与Tomishige采用相同的方法在另一种氧化硅(G-6,Fuji Silysia Chemical)载体上负载得到的核壳结构的Ir-Re双金属催化剂的结构非常类似。

|
图 5 Ir-Re/KIT-6-C500R的STEM-HAADF图片及单个颗粒金属颗粒(图左的圆圈内)的EDX图谱 Fig.5 A STEM-HAADF image of Ir-Re/KIT-6-C500R and its EDX spectra of an individual metal particle (marked by a circle in the left picture) |
对不同温度焙烧后制备的Ir-Re双金属催化剂的一系列表征结果表明双金属Ir-Re的结构随前驱体焙烧温度的变化而发生了显著的改变,在低温350℃焙烧后还原所得的Ir-Re/KIT-6-C350R具有Ir-Re合金结构,而500和650℃焙烧还原所得的催化剂具有Ir-ReOx结构。甘油氢解反应是典型的结构敏感性反应[8]。显然,双金属Ir-Re催化剂结构的变化将导致其甘油氢解反应性能发生相应的改变。
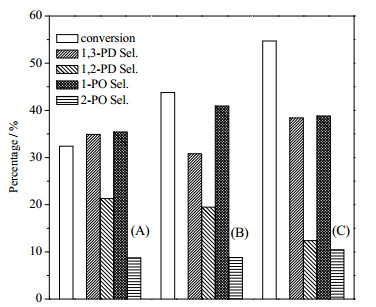
图 6给出了不同温度焙烧制备双金属Ir-Re催化剂的甘油氢解反应性能,可以看到催化活性呈如下趋势Ir-Re/KIT-6-C350 R > Ir-Re/KIT-6-C500R > Ir-Re/ KIT-6-C650 R,即甘油氢解反应活性随着催化剂焙烧温度的升高而逐渐降低,这一结果并不意外。虽然常规的催化剂制备过程中均采用焙烧后还原处理,但我们之前的研究表明直接还原得到的Ir-Re双金属催化剂为合金结构,其甘油氢解反应活性远高于Tomishige研究组采用类似本文的高温焙烧并还原方式得到的催化剂。有意思的是(由于单金属催化剂几乎没有活性,因此未在图 6标注具体数值),焙烧并还原后的单金属Ir和Re催化剂的活性非常低,Ir/KIT-6在同样的反应条件下得到的甘油转化率仅为0.5%,而Re/KIT-6则无法检测到反应活性。可见,Ir和Re之间的相互协同作用是其催化甘油氢解的必要条件。
|
图 6 Ir-Re/KIT-6催化剂的甘油氢解性能 Fig.6 Glycerol hydrogenolysis performance of Ir-Re/KIT-6 upon different calcination treatments (A) Ir-Re/KIT-6-C650R (B) Ir-Re/KIT-6-C500R (C) Ir-Re/KIT-6-C350R PD: propanediol, PO: propanol |
已有的研究认为[7, 9],Ir-Re双金属催化甘油氢解过程中金属Ir作为H2的活化中心,而Re-OH则作为甘油的吸附位,甘油氢解反应的活性中心为金属Ir和酸性位Re-OH之间的界面。由此可见,双金属Ir-Re催化剂的催化性能取决于酸位Re-OH的数量以及Ir的分散度的大小,以及两者之间的协同作用。从上述TEM及CO-化学吸附表征结果可知,随着催化剂焙烧温度的降低,双金属Ir-Re纳米粒子的粒径逐渐减小,表面Ir的分散度增大。同时,如表 1所示的NH3-TPD结果所示双金属Ir-Re催化剂的表面酸量随着前驱体焙烧温度的降低也逐渐增大。需要说明的是,载体KIT-6本身没有酸性[18],双金属Ir-Re的表面酸性由铼羟基(Re-OH)产生[9, 14, 19]。因此,酸量的大小直接反应了催化剂表面Re-OH的数量。此外,由于Ir-Re合金表面Ir和Re的相互作用更强,电子由Re中心转移到Ir中心上,由此导致了Re中心更为缺电子,从而提高了Ir-Re/KIT-6-C350R上Re-OH脱质子能力以及相应的酸强度。因此,催化剂前驱体焙烧温度改变Ir-Re双金属结构的同时,增大了表面Re-OH以及Ir的分散度,最终导致了催化活性随催化剂焙烧温度的降低而增大。
从图 6中还可以看到,三种催化剂催化甘油氢解反应的主要产物为1, 3-丙二醇和正丙醇,选择性均超过30%,其中Ir-Re/KIT-6-C350R显示出最高的1, 3-丙二醇选择性和收率,分别达到38.4%和21.1%。此外,1, 2-丙二醇选择性随着催化剂焙烧温度的降低而逐渐减小,这是由于催化剂活性的提高会促进丙二醇过度氢解反应的发生,从而导致丙二醇的选择性随着反应活性的提高而降低,生成了更多的丙醇。有趣的是,Ir-Re/KIT-6-C350R不仅显示出最高的活性,其1, 3-丙二醇选择性也高于Ir-Re/KIT-6-C500R和Ir-Re/KIT-6-C650R催化剂,这表明Ir-Re合金结构催化剂的性能较Ir-ReOx结构的催化剂优越。这是由于Ir-Re合金催化剂中的Ir原子簇和Re原子簇之间的接触更为密切,存在更为显著的协同相互作用,由于Re在氧化物载体表面的高分散能力也进一步提高了Ir的分散度,同时也生成了更多的Ir-Re-OH的酸性位,充分发挥了双功能催化性能。
4 结论双金属Ir-Re催化剂的结构随着焙烧温度的改变而变化。高温焙烧(≥500℃)降低了Re物种的还原能力,在还原过程中形成了Re的低价氧化物并部分覆盖于Ir金属颗粒的表面,形成Ir-ReOx的结构;而低温焙烧( < 350℃)有利于保持Re物种的高度还原性,在还原后得到Ir-Re合金结构的催化剂。甘油氢解反应结果显示,相比于具有Ir-ReOx结构的催化剂,具有Ir-Re合金结构的催化剂显示出更高的甘油转化活性和1, 3-丙二醇选择性,这是由于催化剂焙烧温度的降低同时提高了Ir的分散度和酸位Re-OH的数量,增加了活性中心的数目,并促进了两者之间的协同作用。
| [1] | Corma A, Iborra S, Velty A . Chemical routes for the transformation of biomass into chemicals[J]. Chem Rev , 2007, 107 (6) : 2411-2502 DOI:10.1021/cr050989d |
| [2] | Nakagawa Y, Tomishige K . Heterogeneous catalysis of the glycerol hydrogenolysis[J]. Catal Sci Technol , 2011, 1 (2) : 179-190 DOI:10.1039/c0cy00054j |
| [3] | Bolado S, Treviño R E, García-Cubero M T . Glycerol hydrogenolysis to 1, 2-propanediol over Ru/C catalyst[J]. Catal Commun , 2010, 12 (2) : 122-126 DOI:10.1016/j.catcom.2010.08.016 |
| [4] | Maris E P, Davis R J . Hydrogenolysis of glycerol over carbon-supported Ru and Pt catalysts[J]. J Catal , 2007, 249 (2) : 328-337 DOI:10.1016/j.jcat.2007.05.008 |
| [5] | Vasiliadou E S, Eggenhuisen T M, Munnik P . Synthesis and performance of highly dispersed Cu/SiO2 catalysts for the hydrogenolysis of glycerol[J]. Appl Catal B:Environ , 2014, 145 : 108-119 DOI:10.1016/j.apcatb.2012.12.044 |
| [6] | Shimao A, Koso S, Ueda N . Promoting effect of Re addition to Rh/SiO2 on glycerol hydrogenolysis[J]. Chem Lett , 2009, 38 (6) : 540-541 DOI:10.1246/cl.2009.540 |
| [7] | Nakagawa Y, Shinmi Y, Koso S . Direct hydrogenolysis of glycerol into 1, 3-propanediol over rhenium-modified iridium catalyst[J]. J Catal , 2010, 272 (2) : 191-194 DOI:10.1016/j.jcat.2010.04.009 |
| [8] | Deng C H, Duan X Z, Zhou J H . Size effects of Pt-Re bimetallic catalysts for glycerol hydrogenolysis[J]. Catal Today , 2014, 234 : 208-214 DOI:10.1016/j.cattod.2014.02.023 |
| [9] | Deng C H, Duan X Z, Zhou J H . Ir-Re Alloy as a highly active catalyst for the hydrogenolysis of glycerol to 1, 3-propanediol[J]. Catal Sci Technol , 2015, 5 : 1540-1547 DOI:10.1039/C4CY01285B |
| [10] | Liu L, Zhang Y, Wang A . Mesoporous WO3 supported Pt catalyst for hydrogenolysis of glycerol to 1, 3-propanediol[J]. Chin J Catal , 2012, 33 (7) : 1257-1261 |
| [11] | Zhu S, Gao X, Zhu Y . Alkaline metals modified Pt-H4SiW12O40/ZrO2 catalysts for the selective hydrogenolysis of glycerol to 1, 3-propanediol[J]. Appl Catal B:Environ , 2013, 140-141 : 60-67 DOI:10.1016/j.apcatb.2013.03.041 |
| [12] | Epron F, Gauthard F, Barbier J . Influence of oxidizing and reducing treatments on the metal-metal interactions and on the activity for nitrate reduction of a Pt-Cu bimetallic catalyst[J]. Appl Catal A:Gen , 2002, 237 (1) : 253-261 |
| [13] | Daniel O M, DeLaRiva A, Kunkels E L . X-ray absorption spectroscopy of bimetallic Pt-Re catalysts for hydrogenolysis of glycerol to propanediols[J]. Chem Cat Chem , 2010, 2 (9) : 1107-1114 |
| [14] | Zhang L, Karim A M, Engelhard M H . Correlation of Pt-Re surface properties with reaction pathways for the aqueous-phase reforming of glycerol[J]. J Catal , 2012, 287 : 37-43 DOI:10.1016/j.jcat.2011.11.015 |
| [15] | Bare S R, Kelly S D, Vila S D . Experimental(XAS, STEM, TPR, and XPS) and theoretical(DFT) characterization of supported rhenium catalysts[J]. J Phy Chem C , 2011, 115 (13) : 5740-5755 DOI:10.1021/jp1105218 |
| [16] | Kleitz F, Choi S H, Ryoo R . Cubic Ia3d large mesoporous silica:synthesis and replication to platinum nanowires, carbon nanorods and carbon nanotubes[J]. Chem Commun , 2003, 17 (17) : 2136-2137 |
| [17] | Kim D S, Wachs I E . Surface rhenium oxide-support interaction for supported Re2O7 catalysts[J]. J Catal , 1993, 141 (2) : 419-429 DOI:10.1006/jcat.1993.1151 |
| [18] | Karthikeyan G, Pandurangan A . Post synthesis alumination of KIT-6 materials with Ia3d symmetry and their catalytic efficiency towards multicomponent synthesis of 1H-pyrazolo[1, 2-] phthalazine-5, 10-dione carbonitriles and carboxylates[J]. J Mol Catal A:Chem , 2012, 361 : 58-67 |
| [19] | Ma L, He D H . Hydrogenolysis of glycerol to propanediols over highly active Ru-Re bimetallic catalysts[J]. Top Catal , 2009, 52 (6-7) : 834-844 DOI:10.1007/s11244-009-9231-3 |




