2. 浙江大学衢州研究院, 浙江 衢州 324000
2. Institute of Zhejiang University-Quzhou, Quzhou 324000, China
近年来水体中频繁检测出微量的新污染物,尤以药物和个人护理产品(PPCPs)为代表。PPCPs在环境中具有较强的生物活性和持久性[1],使用传统的生物处理法无法将其有效去除,使用现有的高级氧化技术(如Fenton氧化[2-3]、超声氧化[4-5]、光催化氧化[6-8]等)也存在着降解效率低、能耗高以及二次污染等问题。低温等离子体近几年被用于去除水中的PPCPs[9-10],主要是利用放电过程中产生的化学和物理效应去除水中的污染物[11-12]。根据放电类型的不同,可分为脉冲和非脉冲电晕放电[13-14]、介质阻挡放电(DBD)[15]、滑动弧光放电、直流辉光放电、直流弧光放电。
DBD是一种在放电空间插入固体绝缘介质的气体放电形式[16]。由于一个或多个介质的存在,DBD利用覆盖在电极上或悬挂在放电空间里的介质阻挡层阻止了电流的流通,阻抑了因放电电流无限增长而形成的极间火花或弧光,使放电更均匀,同时有利于高能电子(电荷)在整个电极表面上均匀分布,增加沿着阳极表面的微放电密度,可显著提高DBD反应器中反应性物质的产率,从而提升污染物的降解速率。
由于具有耦合多种高级氧化法的特点,DBD技术理论上具有更高的氧化物降解能力[17-19],其为处理水体中的PPCPs提供了高效、绿色、经济的可能。当前采用DBD技术作为单一手段处理PPCPs的研究较少,尤其在污染物降解机理与反应动力学方面。双氯芬酸(DCF)是一种广泛使用的非甾体类抗炎药,也是常见的水环境中药物残留物之一。它具有难以降解的特点,容易在水环境中积累并对环境造成危害。因此,研究基于平板式循环DBD反应器在等离子体条件下DCF的降解宏观动力学,并建立平板式循环DBD系统中DCF和活性物质的传质-反应模型,有助于深入了解该药物在废水处理过程中的降解机理,进一步指导废水处理技术的优化和改进。
2 实验装置与方法 2.1 实验装置采用平板式循环反应器进行水中DCF的降解实验,详细实验装置见本课题组前期的研究论文[20]。半径为3 mm的圆柱形不锈钢高压电极固定于聚四氟乙烯板上,置于水平导轨上方,并与低温等离子体发生器连接。聚四氟乙烯板的两端嵌于垂直金属杆上,上下滑动调节高压电极与水平导轨距离。距进水口4 cm处设置溢流挡板,与水平面轨道成45°。DCF水溶液置于夹套烧杯中,通过蠕动泵与反应器形成循环回路。
2.2 DCF浓度测定采用高效液相色谱仪(Agilent 1260)测定溶液中DCF浓度,带有反相C18柱(Eclipse XDB C18,250 mm×5 µm×4.6 mm,Agilent)和紫外检测器(G1314F,Agilent)。流动相由50% 乙腈和50% 水溶液(质量分数为1%的乙酸溶液)组成,流量为0.2 mL·min−1。进样体积为10 µL,紫外检测波长为280 nm。
2.3 放电参数测量反应器两端的电压和电荷信号均用泰克P6015A探头连接在等离子体电源的输出电压与电荷端口上进行采集,其中电荷端口内部是电流取样电容,电容为0.45 µF;反应器中的电流信号通过泰克TCP0150钳口式探头接在反应器接地线上进行采集。所有采集的信号均可在泰克DPO3014示波器上记录和处理。
2.4 实验方法配制1 g·L−1的双氯芬酸钠标准溶液作为储备液,置于棕色广口瓶中并存放在阴凉避光处。每次量取适量的储备液稀释到一定浓度用于实验,单次实验处理量固定为300 mL。在DBD处理过程中,每隔2 min进行取样,取处理时间前14 min的样品,每次取样量为1.5 mL,取样后迅速加入15 µL的1 mol·L−1碳酸钠溶液,淬灭溶液中可能残留的羟基自由基。将样品用0.45 µm的水系膜过滤后置于棕色液相小瓶中,用于液相测定。
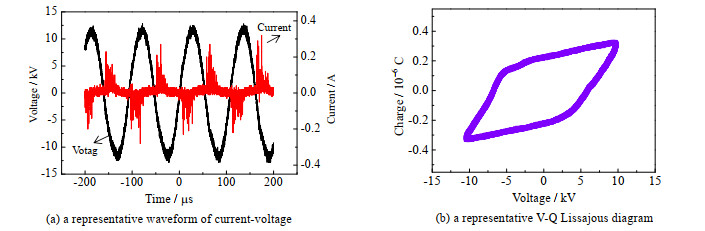
3 结果与讨论 3.1 DBD放电特性如图 1(a)所示,DBD输出电压为典型的正弦波形,实验中周期固定为0.1 ms。输出电流的波形类似正弦波,但波峰和波谷附近叠加了高振幅的脉冲式波动。由于DBD的电流、电压间存在的相位差及介质损耗,有效放电功率难以直接测量。介质表面电荷量可通过串联一个合适的电容来准确测量,因此通常通过表面电荷-放电电压的利萨如(Lissajous)图形来分析DBD放电功率。图 1(b)为典型的V-Q lissajous图形,其形状大致为一个平行四边形,其面积的大小代表了有效放电功率的大小,其值为33 kW。
|
图 1 DBD电压电流功率图 Fig.1 DBD representative waveform of current-voltage |
为研究实验条件参数(输入电压、电极间距、初始质量浓度)对DCF降解的影响并进行系统分析,采用式(1)一阶动力学模型拟合DCF的降解过程:
| $ C = {C_0}{e^{ - kt}} $ | (1) |
式中:C0表示溶液中DCF的初始质量浓度,mg·L−1;t表示反应时间,min;C表示反应时间后溶液中DCF的剩余质量浓度,mg·L−1;k表示DCF的宏观反应速率常数,min−1。
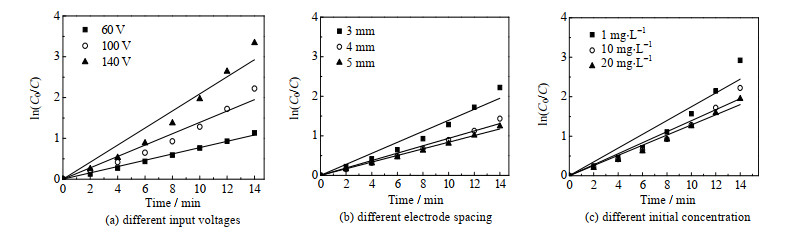
分别对不同输入电压、电极间隙、初始质量浓度等条件下DCF的降解曲线进行了拟合,结果如表 1和图 2所示。初始质量浓度的选择是影响实验结果的一个重要因素,本研究中选取初始质量浓度为1、10、20 mg·L−1进行研究。因取样间隔为2 min、处理时间为14 min时降解率已达96.45% 以上,故选用14 min作为处理时间的终点。
|
|
表 1 基于拟一级动力学的DCF降解模型参数 Table 1 Model parameters for DCF degradation based on pseudo-first-order kinetics |
|
图 2 DCF一级降解动力学回归曲线 Fig.2 Fitting curves of first order kinetics of DCF degradation |
研究结果表明一阶动力学模型与实验数据吻合较好,相关系数均大于0.95,表明DCF的降解符合拟一级反应。当输入电压从60 V增加到140 V时,DCF的降解速率常数从0.077 min−1增加到0.209 min−1。当放电间距从5 mm减小到3 mm时,DCF的降解速率常数也从0.084 min−1增加到了0.139 min−1。此外,随着DCF的初始质量浓度变化,降解速率常数也会有所改变,当初始质量浓度分别为1、10、20 mg·L−1时,所对应的降解速率常数为0.175、0.139、0.129 min−1,即DCF的宏观反应速率常数会随着初始质量浓度的升高而降低。其原因是DCF的降解主要是通过与DBD过程中在液相或气液界面上所产生的活性物质反应,如·OH、·O、NO·、NO2·、·O −、O3、H2O2等,其中O3等活性物质可能选择性地与有机物上的某些官能团反应,而像·OH会无选择性地与污染物反应。因此在降解过程中,除了DCF外,DCF降解后产生的中间产物也会参与和活性物质的反应,从而增加了某时刻反应物的初始质量浓度,并且DCF的浓度越高,其降解后所产生的中间产物也越多,与活性物质反应的竞争越激烈,从而降低了与DCF反应的活性物质浓度,这便是高浓度会导致DCF降解宏观速率降低的主要原因。因此,为了排除DCF中间产物的干扰,需要建立液膜单次流过放电区域的传质-反应模型来单一地研究DCF降解的本征反应级数。值得注意的是,在酸性条件下活性氧更容易存在,溶液中的氢离子会中和水合电子反应生成氢自由基,氢自由基进一步与水发生一系列反应生成更多的活性氧分子,但这部分作用对降解贡献较小。
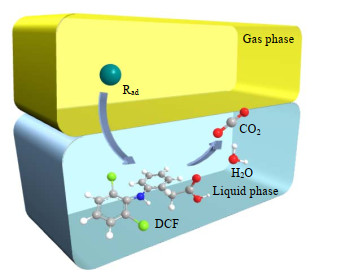
3.3 本征动力学研究结合本课题组前期对等离子体技术降解有机污染物的研究[21],可将DBD放电条件下DCF降解反应过程分为3个部分,分别为气相活性物质的产生、活性物质的吸收和液相活性物质与DCF的反应。根据上述反应过程建立DCF降解的气相活性物质产生模型、液相活性物质吸收模型和液相反应模型。同时,为了简化各种活性物质在DCF降解过程中的作用,借鉴Yan等[22]的实验结论,将可与DCF反应的活性物质用一种虚拟的有效自由基来代替,且活性物质的浓度由输入反应中的功率密度所决定。所以DCF与各种活性物质的复杂反应可简化为与一种单一的虚拟自由基之间的反应,如图 3所示。
|
图 3 DCF与自由基反应示意图 Fig.3 Schematic diagram of reaction between DCF and free radicals |
根据上述假设,将气相主体成分设为M,自由基设为Rad,则气相中自由基的产生模型可由式(2)~(4)来表示。
| $自由基的产生:~~~~ \mathrm{M} \xrightarrow{k_1} \mathrm{R}_{\mathrm{ad}} $ | (2) |
| $自由基与气相物质反应的线性湮灭:~~~~ \mathrm{R}_{\mathrm{ad}}+\mathrm{M} \xrightarrow{k_2} \mathrm{R}_{\mathrm{B}} $ | (3) |
| $自由基互相反应的非线性湮灭:~~~~~ \mathrm{R}_{\mathrm{ad}}+\mathrm{R}_{\mathrm{ad}} \xrightarrow{k_3} \mathrm{R}_{\mathrm{C}} $ | (4) |
式中:RB、RC表示自由基湮灭所形成的产物;k1、k2、k3分别表示自由基产生、自由基线性湮灭、自由基非线性湮灭的系数。由于气相中自由基的浓度等于产生的减去湮灭和被液膜所吸收的,若假设液膜对自由基的吸收系数为k4,则可以得出如式(5)所示的气相自由基动力学方程。
| $ \frac{\mathrm{d} C_{\mathrm{R}_{\mathrm{ad}}, \mathrm{~g}}}{\mathrm{~d} t}=k_1 P_{\mathrm{g}}-k_2 C_{\mathrm{R}_{\mathrm{ad}}, \mathrm{~g}} C_{\mathrm{M}}-k_3 C_{\mathrm{R}_{\mathrm{ad}}, \mathrm{~g}}^2-k_4 C_{\mathrm{R}_{\mathrm{ad}}, \mathrm{~g}}$ | (5) |
式中:CRad, g表示气相中自由基的浓度,mol·L−1;CM表示气相主体成分的浓度,mol·L−1;Pg表示平均放电间隙的功率密度,W·m−3。而在DBD过程中反应处于平衡状态时,可以认为气相中的活性物质也处于平衡状态,即气相中自由基的浓度基本保持不变,则有:
| $ \frac{\mathrm{d} C_{\mathrm{R}_{\mathrm{ad}}, \mathrm{~g}}}{\mathrm{~d} t}=0$ | (6) |
通常情况下,可以认为自由基浓度CRad, g远小于气相主体成分的浓度CM,因此可以忽略自由基互相反应后非线性湮灭所减少的自由基,结合式(6)可将式(5)简化为:
| $ \frac{\mathrm{d} C_{\mathrm{R}_{\mathrm{ad}}, \mathrm{~g}}}{\mathrm{~d} t}=k_1 P_{\mathrm{g}}-k_2 C_{\mathrm{R}_{\mathrm{ad}}, \mathrm{~g}} C_{\mathrm{M}}-k_4 C_{\mathrm{R}_{\mathrm{ad}}, \mathrm{~g}}^2=0$ | (7) |
由式(7)可以解得气相中自由基的浓度关于功率密度和气相主体成分浓度的函数,如式(8)所示。
| $ \mathrm{d} C_{\mathrm{R}_{\mathrm{ad}}, \mathrm{~g}}=\frac{k_1 P_{\mathrm{g}}}{k_2 C_{\mathrm{M}}+k_4}$ | (8) |
根据本次实验中DBD装置的结构特征,放电过程中的平均功率密度可由式(9)得到:
| $ P_{\mathrm{g}}=\frac{P}{\pi R^2(h-\delta)} $ | (9) |
式中:P表示放电功率,W·m−3;R表示圆形高压电极半径(即放电区域的半径),m;h表示介质距离水平轨道的距离,m;δ表示液膜的厚度,m。综上所述,结合式(8)和(9)可以得到气相自由基浓度的计算式:
| $ C_{\mathrm{R}_{\mathrm{ad}}, \mathrm{~g}}=\frac{k_1}{k_2 C_{\mathrm{M}}+k_4} \cdot \frac{P}{\pi R^2(h-\delta)} $ | (10) |
由于DCF与虚拟自由基的反应比例未知,为了得到液相中DCF的本征反应速率方程,假设DCF与虚拟自由基之间的反应比例为1:1,可得:
| $ -r_{\mathrm{DCF}}=k_{\mathrm{DCF}} C_{\mathrm{DCF}}^a C_{\mathrm{R}_{\mathrm{ad}, 1}}^b$ | (11) |
式中:CDCF表示液相中DCF的浓度,mol·L−1;CRad, l表示液相中自由基的浓度,mol·L−1;kDCF表示DCF的反应速率常数;a和b分别表示DCF和自由基的反应级数。结合双膜理论可建立反应器内的传质-反应方程,如式(12)所示。
| $ \frac{D_{\mathrm{R}_{\mathrm{ad}}} \mathrm{~d}^2 C_{\mathrm{R}_{\mathrm{ad}}}, 1}{\mathrm{~d} x^2}=K_{\mathrm{DCF}} C_{\mathrm{DCF}}^a C_{\mathrm{R}_{\mathrm{ad}}, 1}^b $ | (12) |
边界条件为
式中:DRad表示自由基在液相中的扩散系数;CRad, i表示自由基在气-液界面处的浓度,mol·L−1;δl表示自由基在液相的传质边界层厚度,m;CDCF, l表示液相中DCF的浓度,mol·L−1。其中,边界条件是基于在双膜理论中膜层以外的气、液两相主体区无传质阻力,即浓度梯度或分压梯度为零,并且液相中的DCF不会挥发到气相中的假设所建立的。因此,可近似认为自由基进入液膜的传质速率等于自由基在气液界面处的反应速率,得到自由基进入液膜的宏观反应传质速率rRad为:
| $ r_{\mathrm{R}_{\mathrm{ad}}}=-D_{\mathrm{R}_{\mathrm{ad}}}\left(\frac{\mathrm{~d} C_{\mathrm{R}_{\mathrm{ad}}, 1}}{\mathrm{d}x}\right)$ | (13) |
但传至液相中的自由基并非均与DCF发生反应,往往只有部分自由基与DCF进行有效反应。因此,设传入液相当中的自由基有效利用率为k5,则液相中DCF与自由基的反应速率rDCF为:
| $ r_{\mathrm{DCF}}=k_5 r_{\mathrm{R}_{\mathrm{ad}}}=-k_5 D_{\mathrm{R}_{\mathrm{ad}}}\left(\frac{\mathrm{~d} C_{\mathrm{R}_{\mathrm{ad}}, 1}}{\mathrm{~d} x}\right)_{x=0} $ | (14) |
通常情况下,传质反应方程式(12)没有解析解,为了得到任意级数的近似解,假设液相反应物在液膜内的浓度等于其在气液界面的浓度,即CDCF = CDCF, i,则原方程可转化为:
| $\frac{D_{\mathrm{R}_{\mathrm{ad}}} \mathrm{~d}^2 C_{\mathrm{R}_{\mathrm{ad}}, 1}}{\mathrm{~d} x^2}=k_{\mathrm{DCF}} C_{\mathrm{DCF}, \mathrm{C}}^a C_{\mathrm{R}_{\mathrm{ad}, \mathrm{i}}}^b$ | (15) |
由于液相中DCF的浓度已知,因此
| $ r_{\mathrm{DCF}}=k_5 r_{\mathrm{R}_{\mathrm{ad}}}=-k_5 D_{\mathrm{R}_{\mathrm{ad}}}\left(\frac{\mathrm{~d} C_{\mathrm{R}_{\mathrm{ad}}, 1}}{\mathrm{~d} x}\right)_{x=0}=k_5\left(\frac{2}{1+b} D_{\mathrm{R}_{\mathrm{ad}}} k_{\mathrm{DCF}}\right)^{\frac{1}{2}} C_{\mathrm{DCF}, \mathrm{i}}^{\frac{a}{2}} C_{\mathrm{R}_{\mathrm{ad}, \mathrm{i}}}^{\frac{1+b}{2}}$ | (16) |
根据双膜理论,一般认为气膜内的传质阻力可以忽略不计,认为CRad, i = kRadCRad, g,所以将气相自由基的浓度计算式(10)代入式(16)中,可得到DCF的宏观反应速率方程:
| $ r_{\mathrm{DCF}}=k_5\left(\frac{2}{1+b} D_{\mathrm{R}_{\mathrm{ad}}} k_{\mathrm{DCF}}\right)^{\frac{1}{2}} C_{\mathrm{DCF}, \mathrm{i}}^{\frac{a}{2}}\left(\frac{k_1}{k_2 C_{\mathrm{M}}+k_4} \cdot \frac{k_{\mathrm{R}_{\mathrm{ad}}} P}{\pi R^2(h-\delta)}\right)^{\frac{1+b}{2}} $ | (17) |
式中:kRad表示自由基的亨利系数。所以,单次经过放电区后液膜中DCF的反应量即等于DCF宏观反应速率与液膜经放电处理的平均时间的乘积,如式(18)所示:
| $ {r_\text{DCF}}T = \Delta {C_\text{DCF}}{V_\text{unit}} \approx \Delta {C_\text{DCF}}{S_\text{unit}}\delta $ | (18) |
式中:T表示液膜经放电处理的平均时间,s;
| $ {\gamma _\text{DCF}} = \frac{{\Delta {C_\text{DCF}}}}{{\Delta {C_\text{DCF, 0}}}} $ | (19) |
式中:CDCF, 0表示放电区域入口处DCF的浓度,mol· L−1。将式(18)代入式(19)中,可得到:
| $ {\gamma _\text{DCF}} = \frac{{\Delta {C_\text{DCF}}}}{{\Delta {C_\text{DCF, 0}}}} = \frac{{{r_\text{DCF}}T/{S_\text{unit}}\delta }}{{\Delta {C_\text{DCF, 0}}}} = \frac{{{r_\text{DCF}}T}}{{{S_\text{unit}}\delta {C_\text{DCF, 0}}}} $ | (20) |
假设液膜为牛顿流体,且液膜在流动方向截面上流速均匀,则液膜的平均停留时间可通过单次处理液膜的体积与液膜流量的比值得出,如式(21)所示:
| $ T = \frac{{\pi R{'^2}\delta }}{Q} $ | (21) |
式中:R′表示圆柱形高压电极的半径,m;Q表示反应体系中液膜的流量,m3·s−1。由于液膜单次流过放电区域时DCF的转化率较小,可以近似认为液相中DCF的浓度等于反应器入口处DCF的浓度,即:
| $ {C_\text{DCF}} = {C_\text{DCF, 0}} $ | (22) |
将DCF的宏观反应速率方程式(17)和液膜的平均停留时间方程(21)代入式(20)中,便可得到单次流过放电区域的DCF的转化率:
| $ {\gamma _\text{DCF}} = \frac{{K{\text{π }}R{'^2}}}{{{S_\text{unit}}Q}}{\left( {\frac{2}{{1 + b}}} \right)^{\frac{1}{2}}}{\left( {\frac{P}{{{\text{π }}{R^2}(h - \delta )}}} \right)^{\frac{{1 + b}}{2}}}C_\text{DCF}^{\frac{{a - 2}}{2}} $ | (23) |
式中:
从式(23)可以看出,DCF单次转化的反应级数
|
|
表 2 DBD降解DCF的模型参数 Table 2 Model parameters of DCF degradation by DBD |
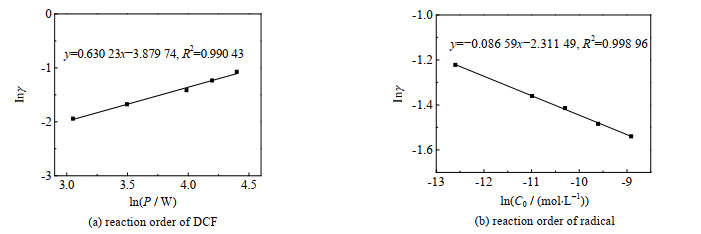
因此,本实验分别测量了在其他条件保持一致的情况下,不同浓度下DCF的单次转化率以及在不同输入电压下(即不同输入功率下)DCF的单次转化率。通过计算lnγDCF~lnCDCF和lnγDCF~lnP的斜率,求得
|
图 4 DCF与自由基反应级数的求取 Fig.4 Evaluation of reaction orders between DCF and free radicals |
通过计算图 4中的斜率可以得到
| $ {\gamma _\text{DCF}} = \frac{{8.533\pi {R^2}}}{{{S_\text{unit}}Q}}{\left( {\frac{8}{5}} \right)^{\frac{1}{2}}}{\left( {\frac{P}{{\pi {R^2}(h - \delta )}}} \right)^{\frac{5}{8}}} $ | (24) |
|
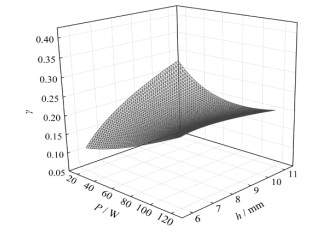
图 5 DCF单次流过放电区域的降解模型 Fig.5 Degradation model of DCF passing through the discharge region in a single flow |
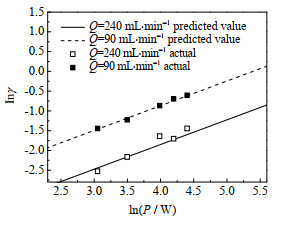
从式(24)可以看出,DCF单次流过放电区域的转化率不仅与输入功率和电极间隙有关,还受到溶液流速的影响。为验证模型的准确度,保持其他条件不变,在不同流速下(Q=90 mg·min−1和240 mL·min−1),改变输入功率,通过式(24)计算得到预测值,与实验值进行对比,结果如图 6所示。
|
图 6 DCF单次通过放电区域转化率的实验值与预测值的比较 Fig.6 Comparison of experimental and predicted values of DCF conversion rates in a single pass discharge area |
结果表明,在溶液流速为90 mg·min−1和240 mL·min−1时,DCF单次转化率的实验值和预测值的平均相对偏差(AARD)绝对值分别为2.984% 和5.348%,表明模型的可信度较高。另外,从实验结果和预测结果均可以发现,随着溶液流速的增加,DCF单次流过放电区域的转化率有所下降。这主要是因为单次放电处理不同于循环模式,溶液流速越大,通过放电区域的时间便越短,导致单位体积的液膜与气相活性成分的接触时间变短,从而造成转换率的下降。
4 结论通过对DCF降解的宏观动力学研究以及平板式循环DBD系统中DCF和活性物质的传质-反应模型的建立,得出了如下结论:
(1) 在平板式循环DBD反应器中,DCF的降解符合一级动力学反应,当初始质量浓度为1 mg·L−1时,降解速率常数为0.175 min−1。由于中间产物会与DCF竞争与活性物质的反应,宏观动力学反应常数受到输入电压、电极间距、初始质量浓度等因素的影响。
(2) DCF单次流过放电区域的转化率受到输入功率、电极间距和溶液流速的影响,其常数K=8.533 mol·min−1·mm3.25·W−0.75,并且DCF在DBD系统中的本征动力学反应为二级反应。
动力学的深入研究有助于阐释DBD技术在水处理领域的应用前景,可以进一步探究和预测不同废水中DCF的降解效率以及DBD系统对其他污染物的处理效果,为实际工程应用提供更为科学的依据。
| [1] |
YE B, WU Q Y, WANG W L, et al. PPCP degradation by ammonia/chlorine: Efficiency, radical species, and byproducts formation[J]. Water Research, 2023, 235: 119862. DOI:10.1016/j.watres.2023.119862 |
| [2] |
METIN S, ÇIFÇI D I. Chemical industry wastewater treatment by coagulation combined with Fenton and photo-Fenton processes[J]. Journal of Chemical Technology & Biotechnology, 2023, 98(5): 1158-1165. |
| [3] |
CONDE J J, ABELLEIRA S, ESTÉVEZ S, et al. Improving the sustainability of heterogeneous Fenton-based methods for micropollutant abatement by electrochemical coupling[J]. Journal of Environmental Management, 2023, 332: 117308. DOI:10.1016/j.jenvman.2023.117308 |
| [4] |
AL-HAMADANI Y A J, LEE G, KIM S, et al. Sonocatalytic degradation of carbamazepine and diclofenac in the presence of graphene oxides in aqueous solution[J]. Chemosphere, 2018, 205: 719-727. DOI:10.1016/j.chemosphere.2018.04.129 |
| [5] |
NIE E, YANG M, WANG D, et al. Degradation of diclofenac by ultrasonic irradiation: Kinetic studies and degradation pathways[J]. Chemosphere, 2014, 113: 165-170. DOI:10.1016/j.chemosphere.2014.05.031 |
| [6] |
LIU W, LI Y Y, LIU F Y, et al. WITHDRAWN: Visible-light-driven photocatalytic degradation of diclofenac by carbon quantum dots modified porous g-C3N4: Mechanisms, degradation pathway and DFT calculation[J]. Water Research, 2019, 150: 431-441. DOI:10.1016/j.watres.2018.12.001 |
| [7] |
LIU F Y, LIANG J L, CHEN L, et al. Photocatalytic removal of diclofenac by Ti doped BiOI microspheres under visible light irradiation: Kinetics, mechanism, and pathways[J]. Journal of Molecular Liquids, 2019, 275: 807-814. DOI:10.1016/j.molliq.2018.11.119 |
| [8] |
LI S, WANG Z R, ZHANG X L, et al. Preparation of magnetic nanosphere/nanorod/nanosheet-like Fe3O4/Bi2S3/BiOBr with enhanced (001) and (110) facets to photodegrade diclofenac and ibuprofen under visible LED light irradiation[J]. Chemical Engineering Journal, 2019, 378: 122169. DOI:10.1016/j.cej.2019.122169 |
| [9] |
CUBAS A L V, DUTRA A R D A, ALVES T C, et al. Evaluation of antimicrobial sensitivity to tetracycline exposed to non-thermal plasma[J]. Química Nova, 2023, 46(3): 236-240. |
| [10] |
MAGUREANU M, PIROI D, MANDACHE N B, et al. Degradation of pharmaceutical compound pentoxifylline in water by non-thermal plasma treatment[J]. Water Research, 2010, 44(11): 3445-3453. DOI:10.1016/j.watres.2010.03.020 |
| [11] |
BRUGGEMAN P, LEYS C. Non-thermal plasmas in and in contact with liquids[J]. Journal of Physics D: Applied Physics, 2009, 42(5): 053001. DOI:10.1088/0022-3727/42/5/053001 |
| [12] |
侯浩, 党小庆, 李世杰, 等. 低温等离子体耦合Co-Mn双金属催化剂降解三氯乙烯[J]. 环境化学, 2023, 42(4): 1185-1195. HOU H, DANG X Q, LI S J, et al. Removal of trichloroethylene by non-thermal plasma combined with Co-Mn bimetallic catalyst[J]. Environmental Chemistry, 2023, 42(4): 1185-1195. |
| [13] |
ZENG J H, YANG B, WANG X P, et al. Degradation of pharmaceutical contaminant ibuprofen in aqueous solution by cylindrical wetted-wall corona discharge[J]. Chemical Engineering Journal, 2015, 267: 282-288. DOI:10.1016/j.cej.2015.01.030 |
| [14] |
DOBRIN D, BRADU C, MAGUREANU M, et al. Degradation of diclofenac in water using a pulsed corona discharge[J]. Chemical Engineering Journal, 2013, 234: 389-396. DOI:10.1016/j.cej.2013.08.114 |
| [15] |
RONG S P, SUN Y B, ZHAO Z H. Degradation of sulfadiazine antibiotics by water falling film dielectric barrier discharge[J]. Chinese Chemical Letters, 2014, 25(1): 187-192. DOI:10.1016/j.cclet.2013.11.003 |
| [16] |
CAL M P, SCHLUEP M. Destruction of benzene with non-thermal plasma in dielectric barrier discharge reactors[J]. Environmental Progress, 2001, 20(3): 151-156. DOI:10.1002/ep.670200310 |
| [17] |
HIJOSA-VALSERO M, MOLINA R, SCHIKORA H, et al. Removal of priority pollutants from water by means of dielectric barrier discharge atmospheric plasma[J]. Journal of Hazardous Materials, 2013, 262: 664-673. DOI:10.1016/j.jhazmat.2013.09.022 |
| [18] |
MAGUREANU M, DOBRIN D, MANDACHE N B, et al. The mechanism of plasma destruction of Enalapril and related metabolites in water[J]. Plasma Processes and Polymers, 2013, 10(5): 459-468. DOI:10.1002/ppap.201200146 |
| [19] |
KRAUSE H, SCHWEIGER B, PRINZ E, et al. Degradation of persistent pharmaceuticals in aqueous solutions by a positive dielectric barrier discharge treatment[J]. Journal of Electrostatics, 2011, 69(4): 333-338. DOI:10.1016/j.elstat.2011.04.011 |
| [20] |
ZHAO X S, YANG Y H, CHEN Q, et al. Insights into catalyst-free, highly effective degradation of pharmaceutical contaminant in aqueous solution by a dielectric barrier discharge system[J]. Separation and Purification Technology, 2023, 320: 124211. DOI:10.1016/j.seppur.2023.124211 |
| [21] |
WANG X P, LI Z J, LEI L C. Model study of sulfite oxidation in seawater flue gas desulfurization by cylindrical wetted-wall corona-streamer discharge[J]. Chemical Engineering Science, 2013, 97: 7-15. DOI:10.1016/j.ces.2013.04.011 |
| [22] |
YAN K, VAN HEESCH E J M, PEMEN A J M, et al. From chemical kinetics to streamer corona reactor and voltage pulse generator[J]. Plasma Chemistry and Plasma Processing, 2001, 21(1): 107-137. DOI:10.1023/A:1007045529652 |




