1-甲基-2, 4-环己二胺(2, 4-MCHD)是重要的有机化工和精细化工中间体,可应用于生产涂层硬化剂、陈化阻聚剂、涂层树脂、环氧树脂固化剂,也可作为染料、洗涤剂和医药中间体的原料[1]。最重要的用途是作为制备甲基环己烷二异氰酸酯(HDI)的原料,HDI可继续用于制备应用广泛的重要功能材料——脂肪族聚氨酯[1~3]。
2, 4-MCHD可用脂环族的硝基还原或羟基氨化和芳香二胺直接催化加氢等方法制备,考虑到原料的来源、成本、工艺简便性和产率等方面,目前多采用直接催化加氢法[2],该方法生产工艺简单、环境友好、符合原子经济性原则。但是在2, 4-甲苯二胺(2, 4-TDA)催化加氢反应过程中,苯环上其中的一个氨基(-NH2)容易脱去生成对甲基环己胺(MCHA)副产物,造成2, 4-MCHD选择性的下降[4, 5]。国外对2, 4-TDA催化加氢的研究多见于上世纪90年代专利,Vedage等[6]以3%~8%的Rh/Al2O3催化剂,在140~195℃、5.5~17 MPa、THF为溶剂条件下,转化率为83.5%,选择性为86.4%,但是目标产物收率并不高。Nichlas等[7]用Pd,Pt/AC为催化剂,以H2SO4和H2O为助剂,在50℃、0.3 MPa下反应0.75 h,2, 4-MCHD选择性可达97%,但是液体强酸会对反应容器造成腐蚀,工业生产成本较高。Gerhard Darson等[8]以Ce、Mn等金属改性Al2O3为载体,负载活性金属Ru为催化剂在215℃、30 MPa条件下2, 4-TDA转化率97.6%,但2, 4-MCHD选择性较低,最高时仅为62.8%。Weissel O等[9]以Mn和Cr的氧化物或氢氧化物作载体,负载Ru为催化剂进行TDA加氢反应,在180~300℃,1~7 MPa,0.01~0.1 g催化剂/kg TDA及无溶剂的条件下,2, 4-TDA加氢活性为84.2%,2, 4-MCHD选择性可达87.5%,该催化剂制备过程复杂且资源消耗很高,不利于广泛使用。Kiel W等[10]用共沉淀法制备Ru、Ce、Mn复合催化剂催化TDA加氢,在220~240℃,15~18 MPa下反应,2, 4-TDA转化率和2, 4-MCHD选择性最高分别可达88%和94%,但过高的反应温度和压力限制了该催化剂的工业应用。国内对2, 4-TDA催化加氢研究很少,郭迎秋[2]以浸渍法制备5% Ru/Al2O3为催化剂,在170℃、9.0 MPa及溶剂THF条件下,2, 4-MCHD选择性为71.3%,但是2, 4-TDA转化率只有31.1%。综上研究成果可知,Ru/Al2O3是较为适合催化2, 4-TDA加氢同时也是研究最多的催化体系,但单金属的Ru/Al2O3为了提高转化率大多需要较高的反应温度(> 200℃)和压力(> 10MPa),而且载体也需进行一定改性以提高2, 4-MCHD的选择性。
本研究是在Ru/γ-Al2O3催化剂的基础上,通过添加Rh金属形成Ru-Rh合金,利用Ru-Rh之间的协同作用,在相对较低的反应条件下(温度180℃,压力8.0 MPa)提高2, 4-TDA加氢催化活性,并以LiOH修饰γ-Al2O3表面碱性来提高2, 4-MCHD选择性,最后考察该催化剂的稳定性。通过BET、TEM、XRD、H2-TPR、XPS及CO2-TPD等表征手段分析催化剂物理结构和表面化学性质,建立催化剂性质与性能之间的联系,探究LiOH修饰的Ru-Rh/γ-Al2O3双金属催化剂的协同催化作用机理。
2 实验部分 2.1 催化剂的制备采用浸渍-沉淀法制备Ru-Rh/γ-Al2O3双金属负载催化剂。所需原材料有:RuCl3溶液(0.05 g·mL-1 Ru)、RhCl3溶液(0.05 g·mL-1 Rh)、γ-Al2O3(比表面积247.3 m2·g-1,250目筛分)、NaOH(AR,≥99%)。将一定量的γ-Al2O3和过量蒸馏水加入三口烧瓶中,开启搅拌水浴加热至80℃,再将RhCl3和RuCl3溶液混合后缓慢滴加到烧瓶中,保持80℃浸渍4 h后,降至室温并添加NaOH溶液(15%(wt))调节浸渍液pH值至8~9,0.5 h后过滤、洗涤催化剂,110℃真空干燥后,经在400℃空气焙烧4h和250℃ H2气氛下还原4 h活化,得到不同Ru和Rh负载量比例的Ru-Rh/γ-Al2O3催化剂。
将还原后的Ru-Rh/γ-Al2O3催化剂置于一定浓度的LiOH水溶液中,静置24 h后,滤去剩余溶液后于100℃真空烘干,得到经LiOH修饰的Ru-Rh/γ-Al2O3催化剂。
2.2 催化剂的表征采用Micromeritics ASAP 2020 N2吸附脱附仪在脱气温度300℃进行5 h,根据BET法测定催化剂比表面积、孔容和孔径等物理结构性质。采用荷兰Philip-FEI 300 kV场发射透射电子显微镜(TEM)表征催化剂表面Ru和Rh颗粒形貌、粒径尺寸及X射线能谱仪(EDX)测定金属颗粒分布。采用荷兰PNAlytical公司X’Pert PRO型X-射线衍射仪(XRD)进行催化剂物相结构分析,测定参数为Cu Kα靶辐射,电压45 kV,电流40 mA,扫描范围2θ=10 ~80 ,扫描速度5 ·min-1。通过H2程序升温还原实验(H2-TPR)测定Ru与Rh双金属的化学状态,将未经还原的样品于石英衬管中Ar/H2混合气流条件下以10℃·min-1程序升温至600℃,用气相色谱检测流出气流中H2含量。采用日本岛津KRATOS公司AXIS Ultra DLD型X射线光电子能谱仪(XPS)表征催化剂金属电子状态,X射线源为单色化Al靶,功率300W,结合能以C1s为284.6 eV校正。通过CO2程序升温脱附实验(CO2-TPD)测定经LiOH处理前后催化剂的碱性强度和数量变化。实验步骤是先将样品置于石英衬管中,在400℃ He气吹扫下除去表面杂质,然后在室温下通过CO2气流吸附1 h,再在100℃保持1 h以脱去样品表面物理吸附的CO2,最后以10℃·min-1升温至700℃,同时用TCD检测CO2脱附速率。
2.3 催化加氢反应2, 4-TDA催化加氢反应在600 mL不锈钢高压釜中进行。依次向釜中加入原料2, 4-TDA 5.0 g、助剂NaNO2 0.20 g和H2O 1.0 mL[11, 12]、溶剂THF 50 mL以及催化剂0.50 g,密封反应釜后,先在室温下用H2置换釜内空气3次,再开启搅拌,将温度升至反应温度180℃,同时通入H2至初始压力8.0 MPa。反应开始后,每当H2压力下降0.5 MPa,便重新补充H2至8.0 MPa,直至当釜内H2压力不再下降时反应结束,停止搅拌,降温,卸去H2压力,取出反应釜后过滤催化剂,将反应溶液送至Agilent GC 7890A气相色谱仪进行分析。气相色谱分析条件:毛细管色谱柱(30 m×320 μm×3 μm),FID检测,柱温80℃~280℃,进样口温度250℃,检测器温度300℃,统一归化法定量计算峰面积。
3 结果与讨论 3.1 催化剂的物理化学性质表征 3.1.1 催化剂的物理结构性质由表 1的BET数据可知,γ-Al2O3具有较大的比表面积A(247.3 m2·g-1)和孔容V(0.818 mL·g-1),随金属Ru和Rh负载量的增加,催化剂的比表面积和孔容逐渐减小至5%Ru-5%Rh/γ-Al2O3时的193 m2·g-1和0.740 mL·g-1。20%和40%浓度的LiOH水溶液浸渍对催化剂的比表面积和孔结构影响不大。在金属总负载量均为10%的情况下,10%Ru/γ-Al2O3比5%Ru-5%Rh/γ-Al2O3的比表面积更小。
| 表 1 催化剂的物理结构性质 Table 1 Physical properties of the catalysts |
从图 1的TEM和颗粒尺寸分布图可知,单金属5%Ru/γ-Al2O3(a)的Ru纳米颗粒存在较多的聚集,Ru颗粒尺寸在3~15 nm,平均颗粒尺寸为8.3 nm。提高Ru负载量对金属颗粒聚集更为严重,10%Ru/ γ-Al2O3(e)的平均颗粒尺寸增大为11.8 nm。添加Rh形成Ru-Rh双金属催化剂后,由于Ru和Rh金属外层电子结构不同,造成金属间以化学键结合形成合金,抑制了Ru金属小颗粒间发生相互熔聚,难以形成金属簇,使得金属在载体上更为分散[13~15],金属颗粒尺寸减小到1~6 nm。随Rh含量的增加,金属颗粒平均尺寸逐渐减小,在5%Rh含量时,5%Ru-5%Rh/γ-Al2O3(c)金属颗粒平均尺寸减小到2.6 nm左右。浸渍LiOH后,5%Ru-5%Rh/γ-Al2O3(40%LiOH)(d)的颗粒平均尺寸继续减小至2.2 nm左右,分散度得到进一步提高。

|
图 1 催化剂的TEM图和金属颗粒尺寸分布图 Fig.1 TEM micrographs of the catalysts and PSD histograms of Ru-Rh NPs (a) 5%Ru/γ-Al2O3 (b) 5%Ru-2%Rh/γ-Al2O3 (c) 5%Ru-5%Rh/γ-Al2O3 (d) 5%Ru-5%Rh/γ-Al2O3(40%LiOH) (e) 10%Ru/γ-Al2O3 |
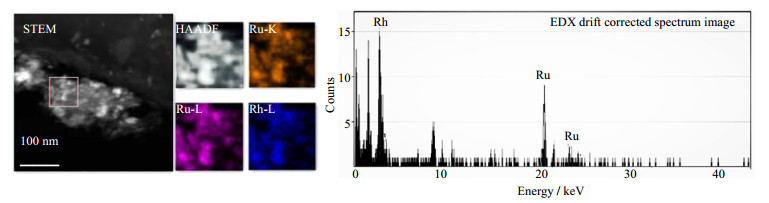
从图 2所示5%Ru-5%Rh/γ-Al2O3的金属颗粒分布情况显示,Ru和Rh元素在催化剂表面出现的位置基本重合,由EDX能谱测定的金属颗粒中Ru和Rh的质量比为1:0.87,说明金属Ru与Rh形成了合金。
|
图 2 5%Ru-5%Rh/γ-Al2O3催化剂的HAADF及EDX图 Fig.2 HAADF and EDX spectrum of 5%Ru-5%Rh/γ-Al2O3 catalyst |
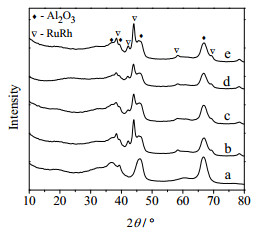
图 3所示的是不同Rh/Ru比催化剂的XRD图,(a)为γ-Al2O3,在单金属5%Ru/γ-Al2O3(b)和10%Ru/γ-Al2O3(e)中2θ=38.3 ,42.2 ,43.9 ,58.3 ,69.3 处均出现了Ru金属衍射峰[16~18]。在双金属催化体系中,5%Ru-2%Rh/γ-Al2O3(c)和5%Ru-5%Rh/γ-Al2O3(d)双金属催化剂中没有出现Rh衍射峰,在2θ=38.2 , 42.2 , 43.8 , 58.2 , 69.1 处出现的衍射峰为Ru-Rh合金,与单金属Ru的衍射峰相比,衍射峰位置没有改变,只是对应的特征衍射峰随Rh含量的增加而趋于弥散,说明Rh与Ru所形成的合金使金属分散得更为均匀[14~18],与图 1所示的TEM表征结果相吻合。
|
图 3 不同Rh/Ru比5%Ru-Rh/γ-Al2O3的XRD图谱 Fig.3 XRD patterns of 5%Ru-Rh/γ-Al2O3 with different Rh/Ru ratios (a) γ-Al2O3 (b) 5%Ru/γ-Al2O3 (c) 5%Ru-2%Rh/γ-Al2O3 (d) 5%Ru-5%Rh/γ-Al2O3 (e) 10%/γ-Al2O3 |
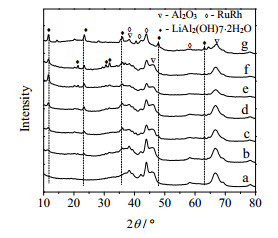
图 4所示的是未浸渍LiOH和不同浓度LiOH修饰后的5%Ru-5%Rh/γ-Al2O3 XRD图,发现经LiOH修饰后的催化剂中均在2θ=11.7 ,20.8 ,23.7 ,36.2 ,64.3 出现了新的晶相,且随LiOH浓度增大,对应的特征衍射峰逐渐变得尖锐。通过比照标准卡片(PDF#40-0710)可知,新晶体物种为LiAl2(OH)7·2H2O,该物种可由LiOH与Al2O3在室温条件下反应形成,呈现[LiAl2(OH)6]+OH- ·2H2O层状结构,具有较强的碱性[19~22]。由此可见,LiOH的修饰改变了载体的晶体结构,进而影响载体的碱性以及活性金属与载体间的相互作用。
|
图 4 不同浓度LiOH修饰的5%Ru-5%Rh/γ-Al2O3的XRD图谱 Fig.4 XRD patterns of 5%Ru-5%Rh/γ-Al2O3 modified by various concentrations of LiOH (a) 0% (b) 5% (c) 10% (d) 20% (e) 30% (f) 40% (g) 50% |
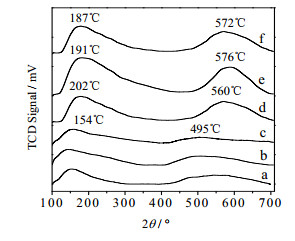
从图 5所示的不同催化剂CO2-TPD图可以看出,经LiOH浸渍修饰的催化剂(d)、(e)、(f)与未经LiOH修饰的催化剂(a)、(b)、(c)相比,CO2脱附峰温度更高,脱附峰面积也更大。(a)、(b)、(c)在温度150℃和500℃左右存在两个CO2脱附峰,分别对应Al2O3载体上的弱碱性位和强碱性位。(d)、(e)、(f)在190℃和570℃左右分别有两个CO2脱附峰,脱附温度均向高温移动,40%LiOH浸渍催化剂(e)的CO2脱附峰温度和峰面积最大。由脱附峰的温度和面积可知,LiOH的修饰显著增强了Al2O3载体上的弱碱性位和强碱性位的强度和数量。该结果与图 4中LiOH对5%Ru-5%Rh/γ-Al2O3催化剂的晶体结构的影响结果相吻合,进一步说明LiOH所起的作用是在Al2O3载体表面形成新晶相LiAl2(OH)7·2H2O,提高催化剂碱性位的强度和数量。
|
图 5 不同催化剂的CO2-TPD图 Fig.5 CO2-TPD profiles of the catalysts (a) 5%Ru/γ-Al2O3 (b) 5%Ru-2%Rh/γ-Al2O3 (c) 5%Ru-5%Rh/γ-Al2O3 (d) 5%Ru-5%Rh/γ-Al2O3(10%LiOH) (e) 5%Ru-5%Rh/γ-Al2O3(40%LiOH) (f) 5%Ru-5%Rh/γ-Al2O3(50%LiOH) |
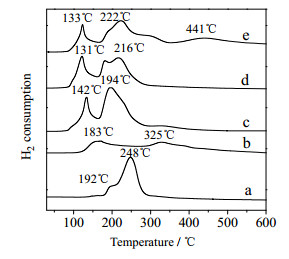
从图 6的H2-TPR可以看出,RuO-RhO双金属负载催化剂(c)、(d)、(e)的H2还原峰位置相对于单金属RuO和RhO负载催化剂(a)、(b)明显地向低温移动,可归因于加入Rh后所形成的Ru-Rh合金具有的氢溢流作用[13~17],使Ru和Rh金属更容易被还原。(a)在192和248℃出现的H2还原峰分别对应催化剂上游离态的RuO物种和与Al2O3相互作用的RuO物种。(b)中138和325℃的H2还原峰为游离态的RhO和与Al2O3相互作用的RhO。随着Rh的加入,(c)和(d)在142、194℃和131、182、216℃出现的还原峰分别属于分散状态的和与载体Al2O3结合RuO-RhO混合氧化物。(d)和(e)还原峰相对于(c)向高温偏移,(e)在441℃出现高温还原峰,结合TEM表征结果,可归因于(d)和(e)中金属颗粒尺寸显著减小,导致金属与载体间结合力随之增强,使金属更难被还原。
|
图 6 金属氧化态的催化剂的H2-TPR图 Fig.6 H2-TPR profiles of the oxidized catalysts (a)5%RuO/γ-Al2O3 (b)5%RhO/γ-Al2O3 (c) 5%RuO-2%RhO/γ-Al2O3 (d) 5%RuO-5%RhO/γ-Al2O3 (e) 5%RuO-5%RhO/γ-Al2O3(40%LiOH) |
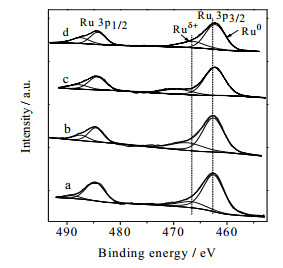
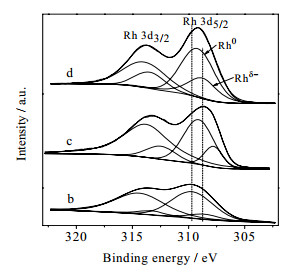
由图 7、图 8和表 2所示的Ru3p和Rh3d的XPS电子结合能数据可知,与Ru/γ-Al2O3(a)相比,加入Rh形成双金属Ru-Rh/γ-Al2O3(b)和(c)的Ru金属呈现更多缺电子的Ruδ+状态,而Rh金属形成富电子的Rhδ-状态,电子从Ru金属转移到Rh金属上[13~15, 23~25]。随着Rh金属负载量的增加,5%Ru-5%Rh/γ-Al2O3(c)的Ruδ+结合能(469.2eV)相对于5%Ru-2%Rh/γ-Al2O3(b)的Ruδ+结合能(467.4eV)向高结合能偏移量更大,Ruδ+占比由20.6%提升至23.0%,(c)的Rhδ-结合能(307.7 eV)相较于(b)的Rhδ-(308.6 eV)向低结合能偏移量也更多,Rhδ-占比由14.3%增加到22.4%。经LiOH修饰后的5%Ru-5%Rh/γ-Al2O3(d)的Ruδ+和Rhδ-占比分别继续增加到27.5%和30.9%。由此可见,Ru-Rh合金之间Ru易失去电子,将电子转移至Rh上面,使Ru呈缺电子状态,Rh呈现富电子状态。
|
图 7 不同催化剂的Ru 3p XPS谱图 Fig.7 Ru 3p XPS spectra of the catalysts (a) 5%Ru/γ-Al2O3 (b)5%Ru-2%Rh/γ-Al2O3 (c) 5%Ru-5%Rh/γ-Al2O3 (d) 5%Ru-5%Rh/γ-Al2O3(40%LiOH) |
|
图 8 不同催化剂的Rh 3d XPS谱图 Fig.8 Rh 3d XPS spectra of the catalysts (b) 5%Ru-2%Rh/γ-Al2O3 (c)5%Ru-5%Rh/γ-Al2O3 (d) 5%Ru-5%Rh/γ-Al2O3(40%LiOH) |
| 表 2 催化剂的Ru 3p3/2和Rh 3d5/2结合能 Table 2 Binding energy of Ru 3p3/2 and Rh 3d5/2 |
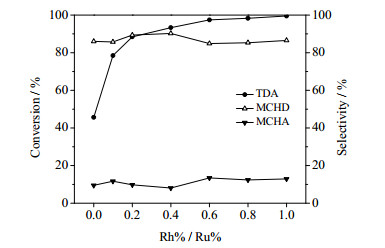
5%Ru-x%Rh/γ-Al2O3随Rh%含量变化(即Rh/Ru比)对2, 4-TDA加氢反应的影响见表 3和图 9。从表 3和图 9中可看出,随催化剂中Rh含量的增加,2, 4-TDA的转化率由Rh%为0时的45.62%显著增大到Rh%为4.0时的93.32%,Rh%为5.0时达到最高的99.55%。Rh含量的增加对2, 4-MCHD的选择性没有明显的影响,基本维持在84%以上,在5%Ru-2%Rh/γ-Al2O3时可达最高的90.23%。当Rh%为5.0,即催化剂为5%Ru-5%Rh/γ-Al2O3时,2, 4-MCHD的收率达到最高的86.14%。而单金属的10%Ru/γ-Al2O3催化剂的加氢活性仅为34.88%,由此可见,Ru-Rh/γ-Al2O3双金属催化剂具有高加氢活性的原因不是因为金属负载量的提升,而是因为Ru-Rh双金属之间的相互促进作用。
| 表 3 Rh/Ru比对5%Ru-x%Rh/γ-Al2O3上2, 4-TDA加氢反应的影响 Table 3 Effects of Rh/Ru ratios in 5%Ru-x%Rh/γ-Al2O3 on 2, 4-TDA hydrogenation |
|
图 9 Rh/Ru比对5%Ru-x%Rh/γ-Al2O3上2, 4-TDA加氢反应的影响
Fig.9 Effects of Rh/Ru ratios in 5%Ru-x%Rh/γ-Al2O3 on 2, 4-TDA hydrogenation
TDA: 2, 4-toluenediamine; MCHD: 1-methyl-2, 4-cyclohexanediamine; MCHA: methylcyclohexylamine Reaction conditions: 2, 4-TDA 5.0 g, Catalyst 0.50 g, NaNO2 0.20 g, H2O 1.0 mL, THF 50 mL, 180℃, 8.0 MPa, 8 h. |
不同LiOH浓度修饰的5%Ru-5%Rh/γ-Al2O3对2, 4-TDA加氢反应的性能如表 4和图 10所示。
| 表 4 LiOH浓度对5%Ru-5%Rh/γ-Al2O3的2, 4-TDA加氢反应的影响 Table 4 Effects of LiOH concentrations in 5%Ru-5%Rh/γ-Al2O3 on 2, 4-TDA hydrogenation |
|
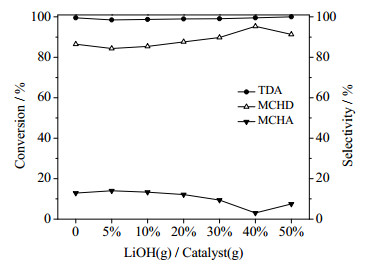
图 10 LiOH浓度对5%Ru-5%Rh/γ-Al2O3的2, 4-TDA加氢反应性能的影响 Fig.10 Effects of LiOH concentrations in 5%Ru-5%Rh/γ-Al2O3 on 2, 4-TDA hydrogenation Reaction conditions: 2, 4-TDA 5.0 g, catalyst 0.50 g, NaNO2 0.20g, H2O 1.0 mL, THF 50 mL, 180℃, 8.0 MPa, 8 h |
表 4和图 10结果显示,LiOH修饰前后的5%Ru-5%Rh/γ-Al2O3的2, 4-TDA转化率维持在98%以上,即LiOH不影响催化剂对2, 4-TDA的加氢活性。在较低LiOH浓度下(5%~10%),2, 4-MCHD选择性有轻微的降低,但仍然保持在84%以上。继续增大LiOH浓度对2, 4-MCHD选择性有所提升,在LiOH(g)/Cat(g)为40%时,催化剂可达到95.36%的最高选择性和94.92%的最大收率。50%LiOH浓度下反而不利于2, 4-MCHD的生成,使选择性略有下降。
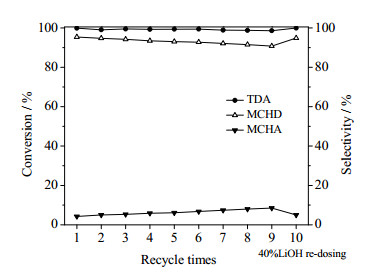
3.3 催化剂的稳定性在相同反应条件下考察了5%Ru-5%Rh/γ-Al2O3(40%LiOH)催化剂循环套用10次的反应活性和选择性。反应后的催化剂经过滤和蒸馏水简单清洗后,每次再补充0.025 g(初始催化剂用量的5%)新鲜催化剂重新投入加氢反应,实验结果见图 11。
|
图 11 5%Ru-5%Rh/γ-Al2O3(40%LiOH)在2, 4-TDA加氢反应中的稳定性 Fig.11 Stability of 5%Ru-5%Rh/γ-Al2O3(40%LiOH) in 2, 4-TDA hydrogenation Reaction conditions: 2, 4-TDA 5.0 g, catalyst 0.50 g, NaNO2 0.20 g, H2O 1.0 mL, THF 50 mL, 180℃, 8.0 MPa, 8 h. |
由图 11中可知,随催化剂循环使用次数的增加,2, 4-TDA转化率基本维持在99%左右,2, 4-MCHD选择性呈缓慢下降的趋势,但循环使用9次时选择性仍然保持在90%以上。在第10次对催化剂重新浸渍40%LiOH(g)/Cat(g)的LiOH后,2, 4-MCHD选择性返回到初次使用时的95.28%的高选择性。说明随催化剂使用次数的增加,催化剂表面金属活性中心未受到破坏和流失,显示出Ru-Rh合金在Al2O3载体上的稳固。2, 4-MCHD选择性的缓慢下降说明催化剂表面碱性物种存在少量流失,但通过加入LiOH可补充流失的碱性以再次提高选择性。
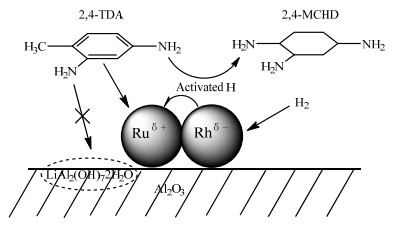
3.4 催化剂作用机理讨论从TEM和XRD数据可知,与单金属5%Ru/γ-Al2O3相比,双金属5%Ru-x%Rh/γ-Al2O3中随Rh含量的增加,金属颗粒尺寸显著减小,金属分散度明显提高,暴露了更多的活性中心;另一方面,从EDX、XRD、H2-TPR和XPS结果可知,Ru-Rh双金属形成了合金并存在金属间的电子转移,改变了Ru和Rh的外层电子状态,使Ru呈现缺电子状态。2, 4-TDA苯环上的两个供电子氨基(-NH2)使苯环呈现富电子状态,富电子态的苯环更容易在缺电子态的Ru上发生化学吸附,显著降低苯环催化加氢反应的吸附活化性能垒;与此同时,富电子状态的Rh容易将H2吸附活化分解为活化氢,并通过氢溢流作用将活化氢转移至Ru上参与苯环加氢反应。通过以上的协同催化作用,使Ru-Rh/γ-Al2O3催化活性得到显著提升,催化作用机理如图 12所示。
|
图 12 Ru-Rh/γ-Al2O3(LiOH)催化作用机理 Fig.12 Catalytic mechanism of Ru-Rh/γ-Al2O3(LiOH) |
同时,由LiOH修饰的Ru-Rh/γ-Al2O3的XRD图可知,LiOH可与Al2O3载体在表面反应生成LiAl2(OH)7·2H2O碱式铝锂盐,从BET结果可知在LiOH浓度较低的时(20%,40%),催化剂的比表面积和孔容没有明显下降,并不会引起Al2O3骨架结构的坍塌。且根据图 5的CO2-TPD可知,随LiOH浓度的增加,碱式铝锂盐含量逐渐增大,导致催化剂碱性逐渐加强,进而增强了催化剂对苯环上氨基(-NH2)吸附的抑制作用,防止氨基在催化剂表面吸附并进一步发生断键反应,减小副产物MCHA的生成,提高了2, 4-MCHD选择性。过高的LiOH浓度(50%)使Al2O3孔道骨架结构发生部分坍缩,从而导致暴露在Al2O3表面的碱性中心减少,使2, 4-MCHD的选择性有所降低。同理,在多次循环使用后出现催化剂选择性下降的原因是LiAl2(OH)7·2H2O碱式铝锂盐的破坏和流失,再次加入LiOH形成的LiAl2(OH)7·2H2O可以恢复原有的高选择性。
4 结论(1) 在Ru/γ-Al2O3基础上加入Rh形成Ru-Rh双金属负载催化剂可显著地提高2, 4-TDA的加氢活性,在180℃,8.0 MPa条件下反应8h,2, 4-TDA转化率由5%Ru/γ-Al2O3的45.62%提升至5%Ru-5%Rh/γ-Al2O3的99.55%。其原因在于Ru-Rh合金的协同催化作用:Rh金属一方面阻止了Ru纳米颗粒的自聚,降低了金属颗粒尺寸,提高活性金属的分散度;另一方面,Ru和Rh金属间的电子转移使Ru呈现更多缺电子状态,增强了对2, 4-TDA的化学吸附作用,同时富电子态的Rh将吸附活性的氢通过氢溢流作用转移至Ru上参与苯环加氢反应,两者相互促进使该催化剂加氢活性显著提升。
(2) 在5%Ru-5%Rh/γ-Al2O3基础上浸渍LiOH可进一步将2, 4-MCHD选择性由86.53%提升至95.36%。其原因在于LiOH与γ-Al2O3形成LiAl2(OH)7新的晶相,增加了γ-Al2O3表面碱性,抑制苯环上氨基在催化剂表面上的吸附,促进2, 4-MCHD选择性的提升。
(3) 经LiOH修饰的Ru-Rh/γ-Al2O3催化剂在循环使用10次后仍保持较高的活性和选择性,显示Ru-Rh合金催化中心和碱性LiAl2(OH)7·2H2O物相的稳固,重新浸渍LiOH可补充因碱性少量流失造成的选择性下降,说明该催化剂具有较高的稳定性。
| [1] | ZHU Chang-chun(朱长春). China's polyurethane industry status quo and planning for the development of " much starker choices-and graver consequences-in"(中国聚氨酯产业现状及"十三五"发展规划建议)[J]. Polyurethane Industry(聚氨酯工业) , 2015, 30(3): 1-25. |
| [2] | GUO Ying-qiu (郭迎秋). Study on synthesis of cycloaliphatic amides from aromatic amides hydrogenation over supported Ru catalyst (负载Ru催化剂上芳香胺加氢制脂环胺的研究)[D]. Tianjin (天津): Hebei University of Technology (河北工业大学), 2007. http://cdmd.cnki.com.cn/Article/CDMD-10080-2007190346.htm |
| [3] | MA Hong-xian (麻洪先). Catalytic hydrogenation of 1, 4-phenylenediamine to 1, 4-cyclohexanediamine (对苯二胺催化加氢合成1, 4-环己二胺)[D]. Shanghai (上海): East China University of Science and Technology (华东理工大学), 2014. http://cdmd.cnki.com.cn/Article/CDMD-10251-1014255885.htm |
| [4] | SU Wen-ting (苏文庭). Experimental study on catalytic hydrogenation of MDA to prepare PACM containing lower trans-trans isomer (MDA催化加氢制备含低反-反异构PACM的实验研究)[D]. Hangzhou (杭州): Zhejiang University (浙江大学), 2004. http://cdmd.cnki.com.cn/Article/CDMD-10335-2004042944.htm |
| [5] | WANG Tao(王涛), DING Yun-jie(丁云杰), CHEN Wei-maio(陈维苗), et al. Hydrogenation of o-phenylenediamine to 1, 2-diaminocyclohexane over Ru/AC catalyst(Ru/AC催化邻苯二胺加氢制1, 2-环己二胺)[J]. Petrochemical Technology(石油化工) , 2015, 44(2): 192-197. |
| [6] | Vedage, Gamini A. Hydrogenation of meta-toluenediamine: EP, 0645367[P]. 1994-09-24. |
| [7] | Greco N P, Pittsburgh. Hydrogenation of phenyl primary amines to cyclohexyl amines: US, 3520928[P]. 1970-03-21. |
| [8] | Gerhard Darson, Michael Petrack E. Preparation of a mixture of aminomethylcyclohexanes and diaminomethylcyclohexanes by hydrogenation of diaminotoluenes: US, 5741929[P]. 1998-04-21. |
| [9] | Weissel O. Process for the hydrogenation of an aromatic amine and the supported ruthenium catalyst used in the process: US, 4186145[P]. 1980-06-29. |
| [10] | Kiel W, Zirngiebl E, Jentsch J D, et al. Ruthenium catalysts, their preparation and a process for preparing cycloaliphatic polyamines using these catalysts: US, 5663443[P]. 1997-09-02. |
| [11] | Kim H S, Park K Y, Kwon Y S, et al. Method for preparing cycloaliphatic diamines from aromatic diamines: US, 0675167[P]. 2000-01-13. |
| [12] | Kim H S, Seob S H, Leea H, et al. Ru-catalyzed hydrogenation of aromatic diamines: the effect of alkali metal salts[J]. Journal of Molecular Catalysis A: Chemical , 1998, 132: 267-276. DOI:10.1016/S1381-1169(97)00246-X. |
| [13] | André V H S, Joyce B S, Derek D F, et al. A study of glycerol hydrogenolysis over Ru–Cu/Al2O3 and Ru–Cu/ZrO2 catalysts[J]. Journal of Molecular Catalysis A: Chemical , 2016, 415: 27-36. DOI:10.1016/j.molcata.2016.01.027. |
| [14] | Parnian M J, Khodadadi A A, Najafabadi A T, et al. Preferential chemical vapor deposition of ruthenium on cobalt with highly enhanced activity and selectivity for Fischer–Tropsch synthesis[J]. Applied Catalysis A: General , 2014, 470: 221-231. DOI:10.1016/j.apcata.2013.11.004. |
| [15] | Parnian M J, Najafabadi A T, Mortazavi Y, et al. Ru promoted cobalt catalyst on γ-Al2O3: influence of different catalyst preparation method and Ru loadings on Fischer-Tropsch reaction and kinetics[J]. Applied Surface Science , 2014, 313: 183-195. DOI:10.1016/j.apsusc.2014.05.183. |
| [16] | Murat Rakap. PVP-stabilized Ru-Rh nanoparticles as highly efficient catalysts for hydrogen generation from hydrolysis of ammonia borane[J]. Journal of Alloys and Compounds , 2015, 649: 1025-1030. DOI:10.1016/j.jallcom.2015.07.249. |
| [17] | Baranowska K, Okal J. Bimetallic Ru-Re/γ-Al2O3 catalysts for the catalytic combustion of propane: Effect of the Re addition[J]. Applied Catalysis A: General , 2015, 499: 158-167. DOI:10.1016/j.apcata.2015.04.023. |
| [18] | Baranowska K, Okal J, Tylus W. Microwave-assisted polyol synthesis of bimetallic Ru-Re nanoparticles stabilized by PVP or oxide supports (γ-alumina and silica)[J]. Applied Catalysis A: General , 2016, 511: 117-130. DOI:10.1016/j.apcata.2015.11.045. |
| [19] | Thiel J P, Chiang C K, Poeppelmeier K R. Structure of LiA12(OH)7·H2O[J]. Chemistry of Materials , 1993, 5: 297-304. DOI:10.1021/cm00027a011. |
| [20] | Besserguenev A V, Fogg A M, Francis R J, et al. Synthesis and structure of the gibbsite intercalation compounds[LiAl2(OH)6]X{X=Cl, Br, NO3}and[LiAl2(OH)6]Cl·H2O using synchrotron X-ray and neutron powder diffraction[J]. Chemistry of Materials , 1997, 9: 241-247. DOI:10.1021/cm960316z. |
| [21] | Nayak M T, Kutty R N, Jayaraman V, et al. Preparation of the layered double hydroxide (LDH) LiAl2(OH)7·2H2O by gel to crystallite conversion and a hydrothermal method, and its conversion to lithium aluminates[J]. Journal of Materials Chemistry , 1997, 7(10): 2131-2137. DOI:10.1039/a702065a. |
| [22] | Bajus S A, Agel F A, Kusche M, et al. Alkali hydroxide-modified Ru/γ-Al2O3 catalysts for ammonia decomposition[J]. Applied Catalysis A: General , 2016, 510: 189-195. DOI:10.1016/j.apcata.2015.11.024. |
| [23] | LI Chen(李晨), ZHANG Hai-tao(张海涛), YING Wei-yong(应卫勇), et al. The hydrocarbon products distributions and stability of cobalt-based catalyst for Fischer-Tropsch synthesis(钴基催化剂F-T合成的产物分布及稳定性研究)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报) , 2006, 20(6): 920-924. |
| [24] | ZHU Yi-feng(祝一锋), LI Xiao-nian(李小年), LIU Lian-qing(刘连庆), et al. Agent on the role of ruthenium based ammonia synthesis catalyst activity research(助剂对钌基氨合成催化剂活性的作用研究)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报) , 2003, 17(2): 162-165. |
| [25] | Nelly H, Lilian O, Laurence P R, et al. Controlled preparation and characterization of Pt-Rh/Al2O3 bimetallic catalysts for reactions in reducing conditions[J]. Applied Catalysis A: General , 2016, 517: 81-90. DOI:10.1016/j.apcata.2016.02.024. |




