2. 安徽大学 化学化工学院, 安徽 合肥 230601
2. School of Chemistry & Chemical Engineering, Anhui University, Hefei 230601, China
N, N’-二(2-羟丙基)哌嗪(HPP)作为一种新型烟气脱硫剂,具有可循环使用、脱硫效率高、吸收的SO2能通过热解吸方法回收利用等优点[1, 2],在某炼化厂应用于年产120万吨铁球团烧结烟气综合处理系统,已稳定运行2年以上。在脱硫过程中,由SO2转化生成的硫酸盐含量高,无法通过热解吸作用脱除,且含量过高时会使有机胺以离子型铵盐的形式存在,导致吸收剂脱硫效率降低和设备腐蚀等问题[3]。目前国内外热稳定性盐净化处理的主要方法有电渗析法[4~6]、反渗透法[7, 8]、电吸附分离法[9, 10]和离子交换等方法[11~13]。但这些方法存在设备工艺复杂、膜件易受污染、再生周期长、易产生大量废水及经济成本高等问题。相关专利提供了一种通过相分离从酸性气体吸收剂中脱除热稳定性盐的方法[14],明显减少了液体废物的产生,对吸收剂中较高浓度的热稳定性盐处理效果较优。但对该方法相关理论、基础参数等研究未见文献报道。
本课题组在相关课题研究过程中发现HPP和Na2SO4共存的水溶液会出现双水相的现象。所谓双水相,当两种聚合物[15]、一种聚合物或小分子有机物与一种亲液盐[16~18]或是两种盐在适当的浓度或特定温度下相混合而形成互不相溶的两个水相。作为一种高效而温和的分离技术,双水相萃取技术具有设备投资费用少、操作简单、体系含水量高、不易引起生物活性物质变性失活、易放大等优点,近几年国内外科研人员在细胞器[19]、蛋白质与DNA[20, 21]、金属离子[22, 23]、有机物[24, 25]等分离提纯方面都进行了大量研究。
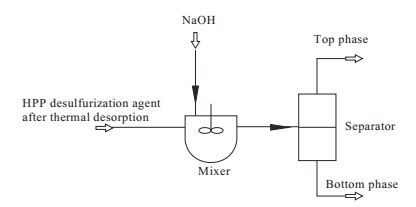
根据HPP与Na2SO4可以形成双水相,在分离烟气脱硫剂中的热稳定性盐过程中可采用如图 1所示的方法。热解吸后的部分HPP烟气脱硫剂通过加入NaOH调节pH值形成双水相,上水相含有大量的HPP和很少量的硫酸钠及其他杂质离子,而下水相含有大量的硫酸钠和少量的HPP及杂质离子,有效地将烟气脱硫剂HPP中的热稳定性盐,尤其是硫酸盐以硫酸钠的形式进行去除。本文在测定303.15~323.15 K下HPP-H2O-Na2SO4双水相系统相平衡数据的基础上,通过NRTL方程对相平衡数据进行关联,所得的NRTL模型二元交互参数可为该体系的工艺计算和化工流程模拟提供有效数据。
|
图 1 HPP烟气脱硫剂中硫酸根脱除示意图 Fig.1 Scheme of sulfate removal from HPP flue gas desulfurization agents |
HPP为自制,纯度大于99%;其它试剂均购于国药集团化学试剂有限公司,除指示剂外均为分析纯;实验所用水为二次蒸馏水。
2.2 实验仪器KAICC超级恒温水浴槽,艾卡仪器设备有限公司(德国独资);AL104电子分析天平、FE20数显pH计(梅特勒-托利多仪器上海有限公司)。
2.3 实验方案设计实验温度上限选取323.15 K。Na2SO4和HPP在水中溶解度随温度降低而降低[26],形成双水相的浓度范围会收窄或不能形成双水相,故本文实验温度下限选取303.15 K。此温度范围能满足双水相法除热稳定性盐实际生产需要。
萃取工艺计算和流程模拟过程中,常用活度系数模型表示相平衡关系。通过测定液液相平衡数据,依据热力学模型,回归得到活度系数模型参数,从而计算各组分的活度系数和热力学平衡常数[27, 28]。两相中以摩尔分数之比表示的分配系数可用该物质在两相中活度系数之比计算得到。用活度系数模拟的方法来描述相平衡关系,不仅可以表示相平衡关系,还可以表示多溶质体系的相平衡分配关系。目前本体系适用的相平衡活度系数模型为NRTL模型。
2.4 实验方法 2.4.1 相平衡数据的测定将Na2SO4、水和HPP以一定配比加入带有夹套恒温的玻璃装置中,搅拌1 h后静置3 h。用注射器分别抽取上下两相溶液进行Na2SO4和HPP含量测定。其中,上水相中硫酸钠含量的测定采用容量法[29],下水相中硫酸钠含量的测定采用重量法[29];电位滴定法测定HPP含量[30];水含量由差减法计算得出。
2.4.2 实验值与计算值误差计算实验采用Aspen Plus8.4对常压303.15~323.15 K下测定的HPP-H2O-Na2SO4相平衡实验值进行NRTL模型关联。实验值和计算值之间的误差采用相对均方根误差(RMSD)和平均相对误差(AAD)进行计算,表达式如下:
| ${\text{RMSD}} = \sqrt {\frac{{\sum {\sum {\sum {{{\left( {({x_{\exp ,i}} -{x_{{\text{cal}},i}})/{x_{\exp ,i}}} \right)}^2}} } } }}{{6k}}} $ | (1) |
| ${\text{AAD}} = \frac{{\sum {\sum {\sum {\left( {\left| {{x_{\exp ,i}} -{x_{{\text{cal}},i}}} \right|/{x_{\exp ,i}}} \right)} } } }}{{6k}}$ | (2) |
不同温度下的相平衡数据如表 1所示。为了验证实验结果的准确性,采用Othmer–Tobias方程[31]进行验证,如式(3)所示:
| $\ln \left( {\frac{{1 -w_3^{\text{b}}}}{{w_3^{\text{b}}}}} \right) = n + k\ln \left( {\frac{{1 -w_1^{\text{t}}}}{{w_1^{\text{t}}}}} \right)$ | (3) |
| 表 1 双水相系统相平衡组成和计算值 Table 1 Equilibrium and calculated compositions for aqueous two-phase system |
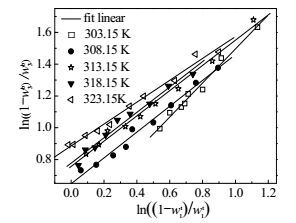
实验温度下HPP-H2O-Na2SO4双水相系统的液液相平衡数据的Othmer-Tobias图如图 2所示。经线性拟合得出不同温度下对应的参数n、k及拟合度R2,如表 2所示。通过拟合结果可以看出,拟合度均接近于1,实验结果可靠。
|
图 2 Othmer-Tobias图 Fig.2 Othmer-Tobias plot |
| 表 2 Othmer-Tobias方程参数和拟合度 Table 2 Fitting results of the Othmer-Tobias equation |
根据热力学原理,如果液体混合物在一定温度下形成两相并达到平衡,两相中的各组分有如下关系:
| $x_i^{\text{t}}\gamma _i^{\text{t}} = x_i^{\text{b}}\gamma _i^{\text{b}}$ | (4) |
| $\sum\limits_i {x_i^{\text{t}}} = 1$ | (5) |
| $\sum\limits_i {x_i^{\text{b}}} = 1$ | (6) |
由此可见,液液相平衡关系可以通过组分在两相中的活度系数来描述。活度系数则可以由活度系数模型及其二元交互作用参数来计算。目前适用于该体系的描述液液相平衡活度系数模型为NRTL模型。
NRTL模型认为组分数为m的混合物的过量Gibbs自由能gE可以用下式表示:
| $\frac{{{g^{\text{E}}}}}{{RT}} = \sum\limits_{i = 1}^m {{x_i}} \frac{{\sum\limits_{j = 1}^m {{\tau _{ji}}{G_{ji}}{x_j}} }}{{\sum\limits_{l = 1}^m {{G_{li}}{x_l}} }}$ | (7) |
其中
| ${\tau _{ji}} = ({g_{ji}} -{g_{ii}})/RT$ |
| ${\tau _{ii}} = 0$ |
| ${G_{ji}} = \exp ( -{\alpha _{ji}}{\tau _{ji}})$ |
| ${\alpha _{ij}} = {\alpha _{ji}}$ |
相应组分i的活度系数方程为:
| $\ln {\gamma _i} = \frac{{\sum\limits_{j = 1}^m {{\tau _{ji}}{G_{ji}}{x_j}} }}{{\sum\limits_{l = 1}^m {{G_{li}}{x_l}} }} + \sum\limits_{j = 1}^m {\frac{{{x_j}G{}_{ij}}}{{\sum\limits_{l = 1}^m {{G_{lj}}{x_l}} }}} \left[ {{\tau _{ij}} -\frac{{\sum\limits_{r = 1}^m {x{}_r{\tau _{rj}}{G_{rj}}} }}{{\sum\limits_{l = 1}^m {{G_{lj}}{x_l}} }}} \right]$ | (8) |
其中gji是组分j和组分i之间的交互作用能量参数,且gji= gij。αij是与混合物非自由度相关的可调特性常数,且αij=αji,可取固定值或根据实验数据进行拟合计算[32]。τji或(gji-gii)即为NRTL方程的二元交互作用参数。
对该双水相体系在303.15~323.15 K的相平衡数据采用Aspen Plus 8.4进行NRTL方程拟合计算,在该软件中方程中相关参数的表达形式如下:
| ${\tau _{ji}} = {a_{ji}} + \frac{{{b_{ji}}}}{T} + {e_{ji}}\ln T + {f_{ji}}T$ | (9) |
| ${\alpha _{ji}} = {c_{ji}} + {d_{ji}}(T -273.15K)$ | (10) |
其中aji、bji, 、eij和fij是非对称参数,cij和dij为对称参数,一般计算时式(9)后两项和式(10)第二项的影响可以忽略[33],此时式(9)可表示成式(11)。
| ${\tau _{ji}} = {a_{ji}} + \frac{{{b_{ji}}}}{T}$ | (11) |
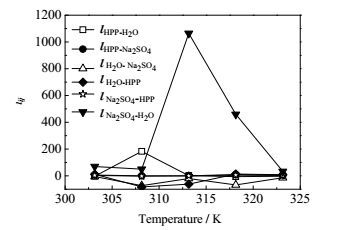
经计算,各参数结果在表 3中列出。HPP为新型的烟气脱硫剂,与其他物质的NRTL方程相关参数的计算未见报道。Na2SO4与H2O之间的NRTL方程参数aji与bji在相同温度不同物系中的值略有差别[34],303.15与308.15 K时计算结果与Miran Milosevic等[34]在聚丙二醇、聚环氧乙烷与Na2SO4、H2O形成的双水相体系在298.15 K时的计算结果比较接近,但温度差别较大时计算结果与文献中差别较大。可见,NRTL方程参数aji、bji除与体系相关以外还受温度的影响。因aji、bji和αij不是NRTL方程的二元交互作用参数,故没有与温度变化的规律可循。NRTL方程的二元交互作用参数τji随温度的变化经计算如图 3所示。
| 表 3 NRTL方程参数 Table 3 The NRTL equation parameters |
|
图 3 NRTL参数随温度的变化 Fig.3 NRTL parameters as a function of temperature |
从图 3中可以看出,二元交互作用参数τNa2SO4-H2O随温度的变化较大,且在313.15 K时出现一个最大值,这是因为在实验温度范围内,Na2SO4对H2O的交互能量参数gNa2SO4-H2O与H2O自身的交互能量参数gH2O-H2O相比较大,且其差值在313.15 K时最大。而Na2SO4对HPP的交互能量参数gNa2SO4-HPP与HPP自身的交互能量参数gHPP-HPP和Na2SO4自身的交互能量参数gNa2SO4-Na2SO4的值相差无几,且随着温度的变化率近似相等,故τNa2SO4-HPP和τHPP-Na2SO4的值在实验温度范围内都接近于0。同理,τHPP-H2O和τH2O-HPP在308.15 K时分别出现最大值和最小值。从图 3中可以看出,在实验温度范围内τHPP-Na2SO4均小于0,这说明H2O对Na2SO4的交互能量参数gH2O-Na2SO4较Na2SO4自身的交互能量参数gNa2SO4-Na2SO4小。τH2O-Na2SO4在308.15和318.15 K时分别出现两个较低值,这是因为gH2O-Na2SO4与gNa2SO4-Na2SO4值都随着温度发生变化,而在303.15~313.15和313.15~323.15 K这两个温度段内gNa2SO4-Na2SO4随温度的变化程度较gH2O-Na2SO4缓和,而在303.15、313.15和323.15 K时两者差值较小,因此两者相减,就会得到图 3中这种趋势。
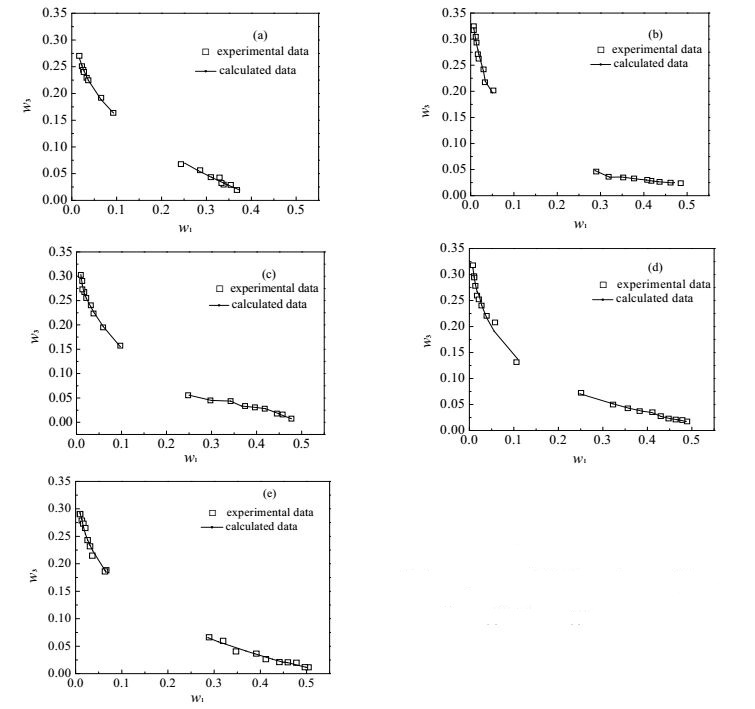
将计算值和实验值进行对比,如表 1和图 4所示。实验值与计算值的误差如表 4所示。
|
图 4 实验值和计算值的对比图 Fig.4 Comparison of calculated data and experimental data (a) 303.15 K (b) 308.15 K (c) 313.15 K (d) 318.15 K (e) 323.15 K |
| 表 4 实验值和计算值的误差 Table 4 Residual deviations between calculated and experimental values |
从表 1、图 4和表 4中可以很好的看出计算结果与实验值可以很好的吻合,相对均方根误差和平均相对误差分别小于2%和1.5%,说明通过液液相平衡数据关联的NRTL方程参数计算出相平衡结果和实际情况符合程度较好,实验温度范围内关联的NRTL方程参数能满足实际计算和工程应用。
4 结论测定了常压条件下303.15~323.15K HPP-H2O-Na2SO4双水相体系的相平衡组成,并对该体系下NRTL活度系数模型的二元交互作用参数τji进行了拟合,结果表明:NRTL模型能很好的关联该三元两相物系的相平衡数据,计算值与实验值的相对均方根误差(RMSD)和平均相对误差(AAD)分别低于2%和1.5%;在实验温度范围内,除HPP与Na2SO4之间的NRTL方程二元交互作用参数外,其他二元交互作用参数均会随着温度发生变化,其中Na2SO4对H2O二元交互作用参数受温度的影响最明显,313.15 K时达到最大值为1063.9。
符号说明:
| AAD | -平均相对误差 | γ | -活度系数 |
| a, b, e, f | -NRTL方程非对称参数 | τ | -NRTL方程二元交互作用参数 |
| c, d | -NRTL方程对称参数 | 上标 | |
| g | -NRTL方程交互作用参数 | b | -下水相 |
| k, n | -Othmer−Tobias方程参数 | E | -过量 |
| m | -组分 | t | -上水相 |
| RMSD | -相对均方根误差 | 下标 | |
| w | -质量分数 | cal | -计算值 |
| x | -摩尔分数 | exp | -实验值 |
| α | -NRTL方程可调特性常数 | 1, 2, 3, i, j | -组分 |
| [1] | Cui P, Wang T, Chen Y, et al. Density, viscosity, and surface tension of aqueous solution of 1, 4-bis-(2-hydroxypropyl)-piperazine sulfate[J]. Journal of Chemical and Engineering Data , 2013, 58(12): 3327-3331. DOI:10.1021/je400405m. |
| [2] | Wei F, He Y, Xue P, et al. Mass transfer performance for low SO2 absorption into aqueous N, N'-Bis-(2-hydroxypropyl) piperazine solution in a θ-ring packed column[J]. Industrial and Engineering Chemistry Research , 2014, 53(11): 4462-4468. DOI:10.1021/ie404000w. |
| [3] | LIU Cui-qiang(刘翠强), ZHU Jian-hua(朱建华), WU Ben-cheng(武本成), et al. Analysis and removal of TSS accumulated in amine absorption solution for removing SO2 from flue gas(烟气脱硫用胺液中热稳定盐的分析及脱除)[J]. Petroleum Refinery Engineering(炼油技术与工程) , 2010, 40(1): 49-54. |
| [4] | Huang C, Xu T, Jacobs M L. Regenerating flue-gas desulfurizing agents by bipolar membrane electrodialysis[J]. Aiche Journal , 2006, 52(l): 393-401. |
| [5] | Bazhenov S, Vasilevsky V, Rieder A, et al. Heat stable salts (HSS) removal by electrodialysis:reclaiming of MEA used in post-combustion CO2 capture[J]. Energy Procedia , 2014, 63(63): 6349-6356. |
| [6] | Meng H, Zhang S, Li C, et al. Removal of heat stable salts from aqueous solutions of N-methyldiethanolamine using a specially designed three-compartment configuration electrodialyzer[J]. Journal of Membrane Science , 2008, 322(2): 436-440. DOI:10.1016/j.memsci.2008.05.072. |
| [7] | Güler E, van Baak W, Saakes M, et al. Monovalent-ion-selective membranes for reverse electrodialysis[J]. Journal of Membrane Science , 2014, 455(4): 254-270. |
| [8] | WANG Huan-zhi(王焕志), MA Xun(马勋), ZHANG Kai(张凯). Study of the utmost ion removal ratio by reverse osmosis membrane(反渗透膜理论离子去除率的研究)[J]. Membrane Science and Technology(膜科学与技术) , 2013, 33(6): 53-57. |
| [9] | Kong Y, Li W, Wang Z, et al. Heat electrosorption behavior of copper ions with poly(m-phenylenediamine) paper electrode[J]. Electrochemistry Communications , 2013, 26(3): 59-62. |
| [10] | Sharma K, Mayes R T, Kiggans J O, et al. Enhancement of electrosorption rates using low-amplitude, high-frequency, pulsed electrical potentiall[J]. Separation and Purification Technology , 2014, 129(129): 18-24. |
| [11] | Pal P, Banat F, AlShoaibi A. Adsorptive removal of heat stable salt anions from industrial lean amine solvent using anion exchange resins from gas sweetening unit[J]. Journal of Natural Gas Science and Engineering , 2013, 15(15): 14-21. |
| [12] | Matthew C, John S, Bhambhani G V, et al. Method for treating a diamine absorbent stream:US, 8, 097, 068[P]. 2012-01-17. |
| [13] | Sarlis J N. Regeneration of ion exchangers that are used for salt removal from acid gas capture plants:US, 7, 776, 296[P]. 2010-08-17. |
| [14] | Vijay B G, John N S. Process for the removal of heat stable salts from acid gas absorbents:US, 0, 193, 375, A1[P]. 2013-08-01. |
| [15] | Silva L M D, Meirelles A A. Phase equilibrium in polyethylene glycol/maltodextrin aqueous two-phase system[J]. Carbohydrate Polymers , 2000, 42(3): 273-278. DOI:10.1016/S0144-8617(99)00178-2. |
| [16] | Daniela A S, Luciana I M, Carlos I Y, et al. Aqueous two-phase (polyethylene glycol + sodium sulfate) system for caffeine extraction:equilibrium diagrams and partitioning study[J]. Journal of Chemical Thermodynamics , 2016, 98(7): 86-94. |
| [17] | Yecid P J, Hector R G, Martha C. Liquid-liquid partition of perchlorate ion in the aqueous two-phase system formed by NaNO3 + poly(ethylene glycol) + H2O[J]. Fluid Phase Equilibria , 2016, 421(15): 93-103. |
| [18] | Cheng Z, Cheng L, Song H, et al. Aqueous two-phase system for preliminary purification of lignans from fruits of Schisandra chinensis Baill[J]. Separation and Purification Technology , 2016, 166(22): 16-25. |
| [19] | Santesson S, Ramirez I B R, Viberg P, et al. Affinity two-phase partitioning in acoustically levitated drops[J]. Analytical Chemistry , 2004, 76(2): 303-308. DOI:10.1021/ac034951h. |
| [20] | Xu K, Wang Y, Huang Y, et al. A green deep eutectic solvent-based aqueous two-phase system for protein extracting[J]. Analytica Chimica Acta , 2015, 864(3): 9-20. |
| [21] | Everberg H, Clough J, Henderson P, et al. Isolation of escherichia coli inner membranes by metal affinity two-phase partitioning[J]. Journal of Chromatography A , 2006, 1118(2): 244-252. DOI:10.1016/j.chroma.2006.03.123. |
| [22] | Chen Y, Deng Y, Meng Y, et al. Partitioning equilibria and thermodynamics of gallium, indium, and thallium in aqueous two-phase systems[J]. Journal of Chemical and Engineering Data , 2015, 60(5): 1464-1468. DOI:10.1021/acs.jced.5b00010. |
| [23] | Zhang Y, Sun T, Hou Q, et al. A green method for extracting molybdenum (VI) from aqueous solution with aqueous two-phase system without any extractant[J]. Separation and Purification Technology , 2016, 169(1): 151-157. |
| [24] | Burcu T, Berna K, Leman T. Partitioning and purification of menadione induced NAD(P)H oxidase from phanerochaete chrysosporium in aqueous two-phase systems[J]. Separation and Purification Technology , 2016, 163(2): 275-281. |
| [25] | Carlos E A P, Paulo V F D, Francisco C S J, et al. Recovery and concentration of o-phenylphenol from biodesulfurization of 4-methyl dibenzothiophene by aqueous two-phase flotation[J]. Separation and Purification Technology , 2017, 176(4): 306-312. |
| [26] | 王婷婷. SO2-HPP/H2SO4-H2O多元吸收体系基础物化参数的测定与研究[D]. 合肥: 合肥工业大学, 2013. WANG Ting-ting. Physicochemical properties for the multicomponent system sulfur dioxide-HPP/sulfuric acid-water [D]. Hefei :Hefei University of Technology, 2013. http://cdmd.cnki.com.cn/Article/CDMD-10359-1013250968.htm |
| [27] | Ghanadzaheh H, Ghanadzadeh A, Altitvoli M. LLE of ternary mixtures of water/acetone/2-ethyl-l-hexanol at different temperatures[J]. Fluid Phase Equilibria , 2004, 219(2): 165-169. DOI:10.1016/j.fluid.2004.02.006. |
| [28] | Arce A, Blanco M, Soto A. Quaternary liquid-liquid equilibria of systems with two partially miscible solvent pairs:1-otctanol +2-methoxy-2-methylpropane + water + ethanol at 25℃[J]. Fluid Phase Equilibria , 1998, 146(1): 161-173. |
| [29] | 制盐工业通用试验方法硫酸根的测定: 北京: 中国标准出版社, 2012. General test method in salt industry-determination of sulfate ion :GB/T 13025.8-2012[S]. Beijing :China Standards Press, 2012. |
| [30] | 程浩. 无机离子对HPP-SO2吸收体系的影响与分离研究[D]. 合肥: 合肥工业大学, 2016. CHENG Hao. The relationship between the weight of a plant part and total weight as affected by plant density [D]. Hefei :Hefei University of Technology, 2016. http://cdmd.cnki.com.cn/Article/CDMD-10359-1016112577.htm |
| [31] | Othmer D F, Tobias P E. Tie-line correlation[J]. Industrial and Engineering Chemistry , 1942, 34(6): 693-696. DOI:10.1021/ie50390a600. |
| [32] | Renon H, Prausnitz J M. Local compositions in thermodynamic excess function for liquid mixtures[J]. Aiche Journal , 1968, 14(1): 135-144. DOI:10.1002/(ISSN)1547-5905. |
| [33] | BAO Zong-hong(包宗宏), WU Wen-liang(武文良). Chemical calculation and software application(化工计算与软件应用)[M].Beijing(北京): Chemical industry press(化学工业出版社), 2013. |
| [34] | Miran M, Koen J J S, Boelo S, et al. Experimental data and thermodynamic modeling of ternary aqueousbiphasic systems of EO/PO polymers-Na2SO4-H2O[J]. Fluid Phase Equilibria , 2014, 366(2): 45-56. |




