在化工生产和设计过程中,非水二元液体混合物的物化性质具有重要的指导作用。含醇体系由于醇分子可以通过氢键发生自缔合,也可以和其它极性分子发生交联缔合,因而导致高度的非理想性[1~4]。其中醇-醇二元系由于强烈的氢键作用,往往呈现出许多特殊的热力学性质。相关的密度和黏度数据在萃取分离、流体力学、传热和传质计算中必不可少。在有限的实验数据情况下,依赖可靠的计算模型,可以大大节省试验投资费用和时间。因而,此类体系的相关物性常数和热力学数据的研究受到普遍关注[5~9]。
1, 2-丙二醇(12PD)、丁醇、戊醇和己醇都是重要的基础化工原料。Rodrigues等[10, 11]研究了12PD水溶液中离子液体的体积效应,Moosavi[5]研究了含12PD的几个二元醇-醇体系的密度和黏度等物性数据及热力学性质,Dubey等[6]报道了1-丁氧基-2-丙醇与丙醇、丁醇非水混合体系的密度等物化性质。含丁醇、戊醇或己醇二元或三元混合系的超额性质已有很多的研究工作[12~19],但未见与12PD形成二元系的密度和黏度文献报道。
本文在常压下测定了1, 2-丙二醇分别与丁醇、戊醇和己醇形成的二元系在293.15~318.15 K全浓度范围内的密度和黏度,计算了过量摩尔体积、黏度偏差和过量流动活化自由能,建立了混合溶液的密度和黏度随温度和组成变化的计算方程。利用Redlich-Kister方程进行了关联。分析和探讨了过量性质的变化及分子间相互作用。
2 实验部分 2.1 试剂1, 2-丙二醇,AR,含量≥99%(如皋市金陵试剂厂);丁醇,AR,含量≥99.5%(杭州双林化工试剂厂);戊醇,AR,含量≥98.5%(天津市化学试剂研究所);己醇,AR,含量≥98%(上海凌峰化学试剂有限公司)。样品均未进一步提纯,开瓶即用。实验用水为石英亚沸蒸馏水。
2.2 密度和黏度测定密度用25 mL的比重瓶在恒温条件下称重测量。比重瓶在不同温度下的空瓶体积用蒸馏水校正。循环式超级恒温槽,控温精度为±0.05 K。电子天平(称量精度±1×10-4g),上海精密仪器仪表有限公司生产。密度测量精度为±0.05%。
黏度利用乌氏黏度计垂直置于恒温槽中测定,毛细管内径0.57 mm,控温精度±0.05 K,秒表计时精度0.01 s。计算公式为η=η0ρt/ρ0t0,其中η、ρ和t分别为待测液体黏度、密度和流经毛细管时间,η0、ρ0和t0分别代表蒸馏水的相应变量。重复读数5次以上,每次相差不超过0.05 s,取平均值。黏度测量精度为±0.2%。
利用上述方法常压下测定了样品在298.15 K时的密度和黏度,与文献值进行了比较,两者吻合甚好,见表 1。
| 表 1 1, 2-丙二醇、丁醇、戊醇和己醇在298.15K时的密度和黏度 Table 1 Densities and viscosities of 1, 2-propanediol, butanol, pentanol and hexanol at 298.15 K |
在293.15~318.15 K下,测定了12PD(1)+丁醇(2)、12PD(1)+戊醇(2)和12PD(1)+己醇(2)二元系的密度和黏度,实验数据分别列于表 2和表 3。
| 表 2 12PD与丁醇、戊醇和己醇二元系在不同温度下的密度 Table 2 Densities of binary mixtures consisting of butanol, pentanol or hexanol with 1, 2-propanediol from 293.15 K to 318.15 K |
| 表 3 12PD与丁醇、戊醇和己醇二元系在不同温度下的黏度 Table 3 Viscosities of binary mixtures consisting of butanol, pentanol or hexanol with 1, 2-propanediol from 293.15 K to 318.15 K |
二元系的密度ρ或黏度的对数值lnη与组成x1的关系可以用下面多项式拟合:
| $ Y={{A}_{0}}+{{A}_{1}}{{x}_{1}}+{{A}_{2}}x_{1}^{2} $ | (1) |
式中Y表示混合液密度ρ或黏度的对数lnη, x1为混合液中12PD的摩尔分数,A0、A1和A2为方程参数,与温度T有关;A0=a1+a2T+a3T2,A1=a4+a5T+a6T2,A2=a7+a8T+a9T2,利用最小二乘法确定各参数,分别列于表 4。相关系数达到0.999以上。
| 表 4 方程(1)的拟合参数 Table 4 Fitting parameters for equation (1) |
二元系过量摩尔体积VE、黏度偏差△η和过量流动活化自由能△G*E分别按下列(2)~(4)式计算:
| $ {{V}^{E}}=({{x}_{1}}{{M}_{1}}+{{x}_{2}}{{M}_{2}})/\rho -x{}_{1}{{M}_{1}}/{{\rho }_{1}}-{{x}_{2}}{{M}_{2}}/{{\rho }_{2}} $ | (2) |
| $ \Delta \eta =\eta -{{x}_{1}}{{\eta }_{1}}-{{x}_{2}}{{\eta }_{2}} $ | (3) |
| $ \Delta {{G}^{*E}}=RT\left[ \ln \left( \eta V \right)-{{x}_{1}}\ln ({{\eta }_{1}}{{V}_{1}})-{{x}_{2}}\ln ({{\eta }_{2}}{{V}_{2}}) \right] $ | (4) |
式中ρ和η分别为混合液密度和黏度,x为摩尔分数,M为摩尔质量,V为混合液摩尔体积,下标1和2分别表示组分1和组分2的相应性质。R为气体常数。过量摩尔体积计算结果见图 1~图 3,黏度偏差见图 4,过量流动活化自由能见图 5。
|
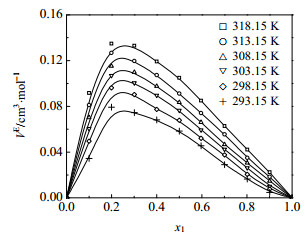
图 1 不同温度下12PD(1)+丁醇(2)二元系的VE~x1图 Fig.1 Profiles of VE against x1 for 12PD(1) + butanol(2) binary mixture at different temperatures Solidlines represent values fitted from eq.(5) |
|
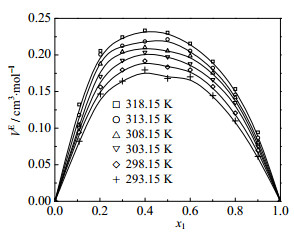
图 2 不同温度下12PD(1)+戊醇(2)二元系的VE~x1图 Fig.2 Profiles of VE against x1 for the 12PD(1) + pentanol(2) binary mixture at different temperatures Solidlines represent values fitted from eq.(5) |
|
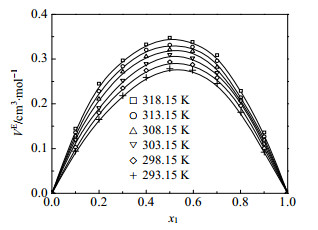
图 3 不同温度下12PD(1)+己醇(2)二元系的VE~x1图 Fig.3 Profiles of VE against x1 for the 12PD(1) + hexanol(2) binary mixture at different temperatures Solidlines represent values fitted from eq.(5) |
|
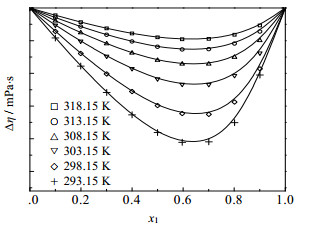
图 4 不同温度下12PD(1)+丁醇(2)二元系的△η~x1图 Fig.4 Profiles of △η against x1 for the 12PD(1) + buntanol(2) binary mixture at different temperatures Solidlines represent values from fitted eq.(5) |
|
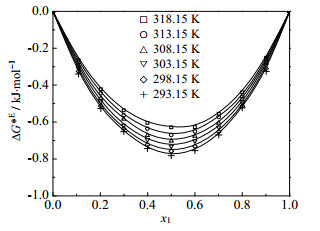
图 5 不同温度下12PD(1)+戊醇(2)二元系的△G*E~x1图 Fig.5 Profiles of △G*E against x1 for the 12PD(1) + pentanol(2) binary mixture at different temperatures Solidlines represent values fitted from eq.(5) |
三个体系的VE在实验温度范围均为正值, 都随温度升高而偏差增大。醇-醇混合体系的过量摩尔体积大多为负值,如Moosavi等[5]发现12PD+乙二醇,12PD+13PD在298.15 K时,过量体积均为负值,认为氢键在体积压缩和膨胀两个对立效应中起主导作用。而Almasi[7]等在研究13PD+甲醇/乙醇/丙醇/丁醇/戊醇二元系的过量摩尔体积时发现,13PD+甲醇/乙醇/丙醇/丁醇的VE为负值,但13PD+戊醇的VE为正值,而且VE值随烷醇链长的增加而逐渐增大。通常来说,引起体积膨胀的原因有[13, 20, 22]:(1)重组引起的氢键破坏;(2)组份分子间的位阻现象;(3)不利的几何填充;(4)色散力和静电斥力等。12PD与丁醇、戊醇和己醇的二元系VE都为正值,说明混合体系分子间存在疏松填充。12PD与烷基醇的不同的分子大小和形状,以及位阻现象都起着重要作用,同时,由于混合过程,氢键结构的破坏也是考虑的因素。显然,上述体系VE的正值说明在混合过程中膨胀效应起了主导作用。由图 1~图 3可以看出,过量摩尔体积值按丁醇-戊醇-己醇顺序逐渐增大,这个变化规律与文献[7]结论相一致。Uddin等[13]认为烷基醇单体内部可以形成环状或链状的复合物,随着-CH2基团的增加,环状复合物的比例也增加,分子间结合度随之下降,因而体积膨胀效应更为突出。另外,随温度升高,体系中分子热运动加剧,基团间距离增大,氢键进一步弱化,体积堆积效应降低,因而导致偏差随温度升高而变得更大。
同时注意到三个体系发生最大偏差时的组成是不同的,12PD(1)+丁醇(2)约在x1=0.25处,12PD(1)+戊醇(2)约在x1=0.4处,而12PD(1)+己醇(2)约在x1=0.5处。这与烷基醇的碳链长度有关,随丁醇-戊醇-己醇顺序,碳链长度逐渐增大,其空间位阻效应增强;反之,碳链越短,其有效填充效应越显著。
图 4是12PD(1)+丁醇(2)的黏度偏差。各温度下均为负值。随温度降低偏差增大。η是液体流动时分子层之间的黏滞力,是分子间作用力的反映。△η为负值,表明混合组份间存在结构破坏效应,即混合过程降低了单体醇结构的高度有序性,导致流动性增强,从而黏度下降。12PD和丁醇都是极性分子,两者之间存在偶极-偶极作用,这种作用与混合时形成溶剂-助溶剂加合物有关,随温度的升高,这种特殊的分子间相互作用变得松弛和减弱,因为参与形成加合物的每个分子的振动频率加快[23]。因此,高温时,偏离理想的程度有所下降。12PD+戊醇和12PD+己醇体系的黏度偏差也均为负值(图略),随组成变化与图 4非常类似,体系最大偏差均发生在x1=0.65处。
图 5是12PD(1)+戊醇(2)的过量流动活化自由能△GE随组成变化。△GE为负值。这是由于单体醇分子的偶极序因混合过程而被打破。温度越低,偏差越大。另两个体系的过量流动活化自由能△GE随组成、温度的变化与12PD+戊醇体系十分相似(图略),自由能最大偏差均发生在x1=0.5处。
二元系的过量性质采用Redlich-Kister[24]方程进行关联:
| $ \Delta Y={{x}_{1}}(1-{{x}_{1}})\sum\limits_{i=0}^{j}{{{B}_{j}}(2{{x}_{1}}}-1{{)}^{j}} $ | (5) |
式中j代表关联方程阶数,Bj为相应的方程参数,△Y分别代表过量摩尔体积VE、黏度偏差△η和过量流动活化自由能△G*E。
关联结果的标准偏差δ用下式计算:
| $ \delta ={{\left[ \sum{{{(\Delta {{Y}_{\exp }}-\Delta {{Y}_{\text{cal}}})}^{2}}/({{N}_{\exp }}-m)} \right]}^{\frac{1}{2}}} $ | (6) |
上式中△Yexp和△Ycal分别代表过量性质的实验值和按式(5)的计算值,Nexp为实验点个数,m为Redlich-Kister方程拟合参数个数。方程参数和标准偏差均列于表 5。
| 表 5 Redlich-Kister方程参数及标准偏差 Table 5 Redlich-Kister equation parameters and standard deviations |
(1)常压下测定了1, 2-丙二醇分别与丁醇、戊醇和己醇形成的二元系在293.15~318.15 K温度之间全浓度范围内的密度和黏度, 建立了混合溶液的密度和黏度随组成和温度变化的计算方程。
(2)三个体系的VE在实验温度范围均为正值。随温度升高偏差增大。但发生最大偏差时的溶液组成不同,12PD(1)+丁醇(2)约在x1=0.25处,12PD(1)+戊醇(2)约在x1=0.4处,而12PD(1)+己醇(2)约在x1=0.5处。过量摩尔体积值按丁醇-戊醇-己醇顺序逐渐增大。
(3)三个体系的黏度偏差和过量流动活化自由能都是负值,其偏差程度也十分相近,并都随温度降低而偏差增大。其中黏度偏差最大值发生在x1=0.65处,过量流动活化自由能最大值发生在x1=0.5处。
(4)对不同温度下的过量性质与组成的关系利用Redlich-Kister方程进行了关联,得出关联系数与标准偏差。
符号说明:| [1] | Kumar D S, Srikanth K, Rao D K . Molecular interactions in the mixture of 2-chloroaniline with equimolar mixture of methanol and isopropanol/isobutanol[J]. Journal of Molecular Liquids , 2007, 136 : 90-93 DOI:10.1016/j.molliq.2007.01.001 |
| [2] | Yadav A, Trivedi S, Rai R . Densities and dynamic viscosities of(choline chloride+glycerol) deep eutectic solvent and its aqueous mixtures in the temperature range(283.15-363.15) K[J]. Fluid Phase Equilibria , 2014, 367 : 135-142 DOI:10.1016/j.fluid.2014.01.028 |
| [3] | Zhou Y H, Li S N, Zhai Q G . Compositions, densities, and refractive indices for the ternary systems ethylene glycol+NaCl+H2O, ethylene glycol+KCl+H2O, ethylene glycol+RbCl+H2O, and ethylene+CsCl+H2O at 298.15K[J]. J Chem Eng Data , 2010, 55 (3) : 1289-1294 DOI:10.1021/je900630n |
| [4] | LING Jin-long(凌锦龙), CAO Feng(曹枫), XU Min-hong(徐敏虹) . Densities, refractive index and viscosity of binary mixture of ethyl acetate and 1, 2-propanediol(乙酸乙酯-1, 2-丙二醇二元系的密度、折光率和黏度)[J]. Journal of Chemical Industry and Engineering(化工学报) , 2011, 62 (5) : 1191-1196 |
| [5] | Moosavi M, Motahari A, Omrani A . Thermodynamic study on some alkanediol solutions:measurement and modeling[J]. Thermochimica Acta , 2013, 561 : 1-13 DOI:10.1016/j.tca.2013.03.010 |
| [6] | Dubey G P, Kaur P . Molecular interactions in binary mixtures of 1-butoxy-2-propanol with alcohols at different temperatures:A thermophysical and spectroscopic approach[J]. J Chem Thermodynamics , 2014, 79 : 100-108 DOI:10.1016/j.jct.2014.07.019 |
| [7] | Almasi M, Khosravi L . Excess molar volumes of 1, 3-propanediol+(C1-C5) alkan-1-ols:application of a cubic equation of state[J]. J Serb Chem Soc , 2012, 77 (3) : 363-370 DOI:10.2298/JSC110616194A |
| [8] | YANG De-ling(杨得岭), LIN Xiao(林晓), CAO Hong-bin(曹宏斌) . Excess molar volume and viscosities for binary mixtures of 3-heptanone+ethyl acetate, 3-heptanone+butyl acetate, 3-heptanone+tributyl phosphate, and methyl isobutyl ketone+tributyl phosphate(3-庚酮+乙酸乙酯、3-庚酮+乙酸丁酯、3-庚酮+TBP、MIBK+TBP二元体系的过量摩尔体积和黏度)[J]. Journal of Chemical Industry and Engineering(化工学报) , 2012, 63 (8) : 2327-2340 |
| [9] | ZHENG Bo-yu(郑博予), FANG Sheng(房升), HE Chao-hong(何潮洪) . Measurement and correlation of densities and viscosities for binary mixtures of methyl ethyl ketoxime with methyl ethyl ketone, cylclohexane, and n-hexane(丁酮肟-丁酮、正己烷、环己烷二元体系密度和黏度的测定及关联)[J]. J Chem Eng of Chinese Univ(高校化学工程学报) , 2010, 24 (6) : 911-916 |
| [10] | Zhang H Y, Li S N, Zhai Q G . Solubilities, densities, and refractive indices for the ternary system 1, 2-propylene glycol+MNO3+H2O(M=Na, K, Rb, Cs) at 250C and 35℃[J]. Chem Eng Comm , 2014, 201 : 323-337 DOI:10.1080/00986445.2013.771346 |
| [11] | Rodrigues M, Francesconi A Z . Experimental study of the excess molar volumes of binary and ternary mixtures containing water+(1, 2-ethanediol, or 1, 2-propanediol, or 1, 3-propanediol, or 1, 2-butanediol)+((1-n-butyl-3-methylimidazolium bromide) at 298.15 K and atmospheric pressure[J]. Journal of Solution Chemistry , 2011, 40 (11) : 1863-1873 DOI:10.1007/s10953-011-9756-5 |
| [12] | Domanska U, Krolikowska M . Effect of temperature and composition on the surface tension and thermodynamic properties of binary mixtures of 1-butyl-3-methylimidazolium thiocyanate with alcohols[J]. Journal of Colloid and Interface Science , 2010, 348 (2) : 661-667 DOI:10.1016/j.jcis.2010.04.060 |
| [13] | Uddin M H, Khan M Z H, Rahman M H . Volumetric and viscometric properties observed for the mixtures of DMF (N, N-dimethyl formamide) and other alcohols(butanol and 1-propanol)[J]. Physics and Chemistry of Liquids , 2014, 52 (2) : 251-261 DOI:10.1080/00319104.2013.812021 |
| [14] | Pradhan P, Roy M N . Studies on solution properties of ternary mixture of acetophenone+n-amyl alcohol+dichloromethane and its corresponding binaries at 298.15 K[J]. Physics and Chemistry of Liquids , 2014, 52 (1) : 100-112 DOI:10.1080/00319104.2011.604779 |
| [15] | Silva J L D, Aznar M . Thermophysical properties of 2, 5-dimethyfuran and liquid-liquid equilibria of ternary systems water+2, 5-dimethylfuran+alcohols(1-butanol or 2-butanol or 1-hexanol)[J]. Fuel , 2014, 136 : 316-325 DOI:10.1016/j.fuel.2014.07.039 |
| [16] | Maharolkar A P, Sudke Y, Kamble S . Densities, viscosities and refractive indices of n-butanol+allyl chloride mixture at 298 K[J]. International Journal of Chemistry , 2010, 2 (2) : 250-260 |
| [17] | Radovic I R, Kijevcanin M L, Tasic A Z . Densities and excess molar volumes of alcohol+cyclohexylamine mixtures[J]. J Serb Chem Soc , 2009, 74 (11) : 1303-1318 DOI:10.2298/JSC0911303R |
| [18] | Verdes P V, Mato M M, Salgado J . Excess molar volumes for methyl tert-butyl ether+1-pentanol+heptane at 298.15 K[J]. Journal of Thermal Analysis and Calorimetry , 2005, 80 (2) : 333-337 DOI:10.1007/s10973-005-0656-z |
| [19] | XIAO Juan(肖娟), GUO Yong-sheng(郭永胜), YANG Yu-zhong(杨玉忠) . Volumetric properties of binary systems of n-butanol or n-pentanol+JP-10(正丁醇/正戊醇+JP-10二元体系的体积性质)[J]. Chemical Journal of Chinese University(高等学校化学学报) , 2012, 33 (7) : 1523-1527 |
| [20] | Saleh M A, Akhtar S, Ahmed M S . Density, excess molar volume, viscosity and thermodynamic activation of viscous flow of water+ethylenecarbonate[J]. Physics and Chemistry of Liquids , 2005, 43 (4) : 367-377 DOI:10.1080/00319100500130194 |
| [21] | Saleh M A, Ahmed M S, Begum S K . Density, viscosity and thermodynamic activation for viscous flow of water+sulfolane[J]. Physics and Chemistry of Liquids , 2006, 44 (2) : 153-165 DOI:10.1080/00319100500217819 |
| [22] | SUN Yi(孙义), MA Pei-sheng(马沛生) . Densities and viscosities for binary mixture of the ethyl crotonate with ethanol at different temperatures(巴豆酸乙酯与乙醇混合液密度和黏度的测定及关联)[J]. J Chem Eng of Chinese Univ(高校化学工程学报) , 2007, 21 (3) : 511-515 |
| [23] | Manfredini M, Marchetti A, Sighinolfi S . Kinematic viscosities of binary liquid mixtures of 2-butanone with 1, 2-propanediol[J]. Journal of Solution Chemistry , 2002, 31 (3) : 235-252 DOI:10.1023/A:1015872926433 |
| [24] | Redlich O, Kister A T . Thermodynamics of nonelectrolyte solutions -x-y-t relations in a binary system[J]. Ind Eng Chem , 1948, 40 (2) : 341-345 DOI:10.1021/ie50458a035 |




