2. 浙江农林大学 工程学院, 浙江 杭州 311300;
3. 浙江农林大学 环资学院, 浙江 杭州 311300
2. College of Engineering, Zhejiang Agriculture and Forestry University, Hangzhou 311300, China;
3. School of Environmental Management, Zhejiang Agriculture and Forestry University, Hangzhou 311300, China
当前,空气污染带来的环境问题已成为关注的热点。致癌物多环芳烃(polcyclic aromatic hydrocarbons, PAHs)是最引人注目的危害物,超过90% 的致癌PAHs存在于PM 2.5的颗粒相中,PAHs中苯并α芘(BaP)来源广泛、降解难、致癌性强[1-2],被认为是一类影响很大的环境污染物。BaP具有多环芳烃的亲脂性,通过口腔呼吸或与皮肤接触能够快速进入人体,其代谢产物与机体蛋白、核酸共价结合,对包括呼吸系统在内的机体各部位造成永久性损伤,致使人体免疫力降低。此外,BaP还对生殖有不利影响,破坏甲状腺功能,可引发高血压、心血管疾病和代谢综合症等[3-4]。因此研究去除空气中的BaP具有重要意义。
目前,除去环境中BaP的方法有微生物降解法[5-6]、光催化降解法[7]、吸附法[8-9]等,其中吸附法因成本低、操作简单、通用性强,一直被广泛关注[10],是目前去除BaP最有效的办法。Costa等[11-12]研究了改性吸附剂对BaP的吸附效果,杨岚[13]研究了氧化石墨烯对有机物的催化降解,但是还没有有效的方法降解多环芳烃,现有吸附材料只能无选择性地吸附BaP,而不能彻底将其转化成无害物,且存在回收或分离困难等限制。因此,迫切需要一种容量大、吸附速度快、分离方便、可降解BaP的复合吸附降解新材料,以便高效、经济地去除BaP污染物。
近几年复合吸附降解材料中,石墨烯是一种有巨大开发潜能的二维新型炭吸附材料。石墨烯基气凝胶具有超高孔隙率和比表面积,有良好的吸附效果[14-15]。但石墨烯基气凝胶仅具有高吸附性能,尚不具备高选择富集性和吸附-降解一体化功效,同时从吸附环境中分离吸附材料以防止二次污染也是亟待解决的问题。本文以氧化石墨烯为分子骨架,负载纳米氧化铁(γ-Fe2O3)和TiO2,并利用苯并α芘为模板合成具有识别、吸附、光催化降解BaP性能的石墨烯基磁性分子印迹气凝胶(GMIA),GMIA不但提高了石墨烯基负载光催化剂的活性和光稳定性[16],具有的磁分离性能也更易被循环利用[17-18]。这种多功效新型吸附降解材料的制备及对多环烷烃的吸附降解具有重要的参考价值。
2 实验部分 2.1 材料与仪器鳞片石墨(AR,99.5%)、4-乙烯吡啶(AR,96.0%)购于阿拉丁生化科技股份有限公司。硫酸氧钛(AR,93.0%)、萘(AR,≥99.7%)、二乙烯苯(AR,80.0%)、3,4-苯并芘(BaP,AR,96.0%)、偶氮二异丁腈(AR,98.0%),购于萨恩化学技术(上海)有限公司。硼氢化钠(AR,96.0%)、聚乙烯醇(AR,≥99.0%)、聚乙烯吡咯烷酮(AR,≥95.0%)、尿素(AR,≥99.0%)、氢氧化钠(AR,≥96.0%)、七水合硫酸亚铁(AR,99.0%~101.0%)、无水乙醇(AR,≥99.7%)、双氧水(AR,≥30.0%)、高锰酸钾(AR,≥99.5%)、苯(AR,≥99.5%)、环己烷(AR,≥99.5%)、二氯甲烷(AR,≥99.5%)、乙腈(AR,≥99.5%)均购于国药集团化学有限公司。盐酸(AR,36.0%~38.0%)、浓硫酸(AR,95.0%~98.0%)、浓硝酸(AR,65.0%~68.0%),购于衢州巨化试剂有限公司。
DF-101S型集热式磁力加热搅拌器(上海凌科实业发展有限公司);KQ-500DE型数控超声波清洗器(杭州大卫科教仪器有限公司);SJ双嘉冷冻干燥机(宁波市双嘉仪器有限公司);AB104-14型电子天平(Mettler Toledo,瑞士);IR Prestige-21型傅里叶变换红外光谱仪(Shimadzu,日本);Phenom Pro PW-100-011型扫描电镜(SEM,Hitachi,日本);XRD-6000型X射线衍射仪(Shimadzu,日本);DQ-I大气采样机及自制香烟气体收集装置;GCMS-QP201PLUS型气相质谱联用仪(Shimadzu,日本);TF20,Jeol 2100F透射电镜(TEM,Shimadzu,日本)。
2.2 氧化石墨烯(GO)的合成与γ-Fe2O3/rGO的制备Hummers法[19]制备GO悬浮液,冷冻干燥制得GO基气凝胶。量取30 mL GO悬浮液液250 mL超纯水中,超声2 h,质量分数为5%的NaOH溶液(pH=7.0)。将8.36 g聚乙烯吡咯烷酮加入150 mL质量浓度为0.15 mg·L-1的硫酸亚铁乙醇溶液中(水与乙醇体积分数φ=7/3)制得溶液。N2 氛围下,先将溶液加入GO溶液中,搅拌15 min,再缓慢加入50 mL浓度为0.30 mol·L-1的硼氢化钠溶液,搅拌反应4 h后过滤,将产物用无水乙醇洗涤3次以上,60 ℃真空干燥2 d,得到磁性负载纳米氧化铁的还原氧化石墨烯γ-Fe2O3/rGO固体。
2.3 TiO2-γ-Fe2O3/rGO的合成与石墨烯基分子印迹气凝胶的制备水热法制备TiO2-γ-Fe2O3/rGO:称取0.8 g γ-Fe2O3/rGO加入150 mL去离子水中,15 ℃超声30 min后,称取0.96 g硫酸氧钛、0.48 g尿素,搅拌下缓慢加入γ-Fe2O3/rGO水溶液中,搅拌反应0.5 ~1 h。将混合液装入反应釜,180 ℃水热反应12 h,沉淀物用去离子水洗涤后冷冻干燥,制得TiO2-γ-Fe2O3/rGO。
悬浮聚合法和分子印迹法制备GMIA/石墨烯基非分子印迹气凝胶(GNMIA):称取2.0 g聚乙烯醇加入100 mL去离子水中,加热至90 ℃使其完全溶解,冷却至室温得到黏稠状透明溶液。向该溶液中加入0.6 g TiO2-γ-Fe2O3/rGO,超声30 min后,转至250 mL三口烧瓶。取0.025 g BaP(模板分子)和0.25 g 4-乙烯吡啶(4VP)(功能单体)于锥形瓶,加入15 mL乙腈(致孔剂),于0 ℃冰冻30 min。再加入3 mL二乙烯苯(DVB)交联剂和0.06 g偶氮二异丁腈(引发剂),超声溶解。将锥形瓶中混合物缓慢加入三口烧瓶中,60 ℃ N2氛围中搅拌1 d。聚合反应完成后,用注射器吸取0.2 mL产物于0.5 mL乙腈中静置4 h,冷冻干燥1 d,将所制得的胶状GMIA于50 mL乙腈中超声清洗30 min,GC-MS检测洗脱液直至去除全部BaP模板分子。将GMIA分散于20 mL乙腈中置于4 ℃冷藏待用。GNMIA的制备方法类似,区别为不加入BaP模板分子。
2.4 GO中间产物及最终产物GMIA的表征傅里叶红外光谱仪(FT-IR)表征产物结构,KBr压片法制样,波数扫描范围4 000~400 cm-1。X射线衍分析仪分析产物物相组成,扫描方式:步进扫描;电压/电流:35 kV/30 mA;扫描速度:2°·min-1;步长:0.02°;Cu靶,K0辐射(λ=0.154 06 nm),扫描范围:2θ=5°~85°。扫描电镜(SEM)表征中间产物和最终产物的表观形貌,工作电压15 kV。透射电镜((TEM)表征中间产物和最终产物的表观形貌,工作电压200 kV,使用铜网过滤。X射线能谱分析(EDS)检测中间产物和最终产物的元素含量,工作电压0~20 kV。气相质谱联用仪(GC-MC)检测BaP,色谱柱从80 ℃程序升温至280 ℃,保持20 min,进样口温度为280 ℃,分流进样,内标法检测系列标准溶液和GMIA/GNMIA降解液中的BaP含量。
2.5 GMIA/GNMIA吸附实验制作工作曲线:配制20、95、150、300、600 ng·mL-1 BaP标准溶液,每份标准溶液中加入150 ng·mL-1的萘内标溶液。GC-MS检测系列标准溶液中BaP。分别以BaP标准溶液浓度为横坐标,BaP峰面积/内标峰面积为纵坐标制作工作曲线。
BaP废弃气体收集及纯化:以600 mL苯为吸收液,用大气采样机吸收600根香烟烟气。吸收液减压浓缩,固体上样法上样,于环己烷浸润的硅胶固相萃取柱上进行萃取,分8次加入100 mL洗脱液(氯乙烷/环已烷 (φ=1))洗脱,收集洗脱液,减压浓缩至100 mL。以此香烟浓缩液模拟BaP废气吸收液,准确移取1.0 mL香烟浓缩液GC-MS检测香烟浓缩液中BaP、3-甲氧基-2, 4, 5-三氟苯甲酸(2, 4, 5-Trifluoro-3-methoxybenzoic acid,PAHs1)、1, 2-苯二甲酸(1, 2-phthalic acid,PAHs2)的出峰位置,记录初始峰面积。
吸附试验:取6份5 mL香烟浓缩液于锥形瓶中,分别加入0.4 g GMIA和GNMIA。25 ℃恒温振荡6、8、12 h后,用磁铁将GMIA(GNMIA)粒子吸在底部,准确移取1.0 mL上层清液和150 ng·mL-1的内标物溶液于进样瓶,GC-MS自动进样检测BaP、PAHs1、PAHs2,记录BaP平衡吸附时BaP、PAHs1、PAHs2的峰面积,计算吸附效率。采用内标法(以萘为内标物) [20]定量BaP,计算GMIA和GNMIA对BaP的饱和吸附容量,计算GMIA的印迹因子α。通过对比平衡吸附前后GC-MS峰面积比测定BaP、PAHs1、PAHs2的吸附率。
2.6 GMIA/GNMIA吸附动力学实验取20组5 mL香烟浓缩液于锥形瓶中,分别加入0.4 g GMIA和GNMIA。25 ℃恒温避光振荡不同时间(5、10、20、30、45、60、120、240、480和720 min)后,用磁铁将GMIA(GNMIA)粒子吸于锥形瓶底部,准确移取1.0 mL上层清液和150 ng·mL-1的内标物溶液于进样瓶,GC-MS自动进样检测BaP,BaP的定量采用内标法(萘为内标物)[20]。计算不同时间内的吸附容量,绘制吸附动力曲线。
2.7 GMIA/GNMIA降解实验取10组5.0 mL香烟浓缩液于锥形瓶中,分别加入0.4 g GMIA和GNMIA。暗处理8 h后,将10组样品置于紫外灯下分别照射1、2、4、8、12 h并静置,准确移取1.0 mL上层清液和150 ng·mL-1的萘内标物溶液于进样瓶[19-20],GC-MS自动进样定量检测BaP,计算BaP降解率。在BaP降解率最大的辐射条件下,以相同的实验条件检测GO对BaP吸附降解效率。
2.8 重复利用实验取5 mL香烟浓缩液于锥形瓶中,加入0.4 g GMIA,25 ℃恒温避光振荡480 min后,将其置于紫外灯下辐射8 h,准确移取1.0 mL上层清液和150 ng·mL-1的萘内标物溶液于进样瓶,GC-MS自动进样定量检测BaP,计算BaP降解率。重复吸附和降解实验各5次,计算吸附量和降解率。
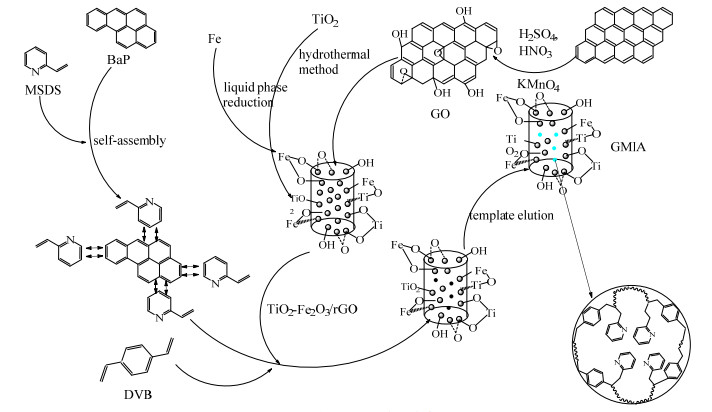
3 结果与讨论 3.1 GMIA的合成GMIA合成路线如图 1所示。
|
图 1 GMIA合成路线 Fig.1 Synthetic route of GMIA |
利用Hummers法制备GO,硼氢化钠将GO还原成rGO,增加GO表面的─O─C─键,减少C═O键,液相还原法负载γ-Fe2O3时,与rGO形成─Fe─O─C─键,达到稳定负载γ-Fe2O3于rGO表面的目的。通过水热法将纳米TiO2包裹于Fe2O3表面,反应釜内高压环境有利于TiO2与γ-Fe2O3形成─Ti─O─Fe─O─键,得到稳定的TiO2-γ-Fe2O3。以BaP为分子模板、4-乙烯吡啶为功能单体通过聚合作用形成分子印迹,再通过二乙烯苯与其他功能单体交联使分子印迹稳定镶嵌于TiO2-γ-Fe2O3/rGO和rGO表面,得到具有磁性和光催化性能的聚合物GMIA。
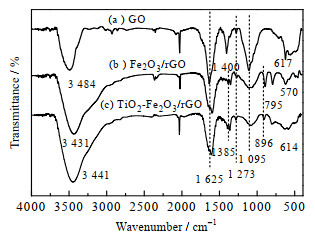
3.2 FT-IR表征原料GO、中间产物γ-Fe2O3/rGO和TiO2-γ-Fe2O3/rGO的FT-IR如图 2所示。
|
图 2 原料GO、中间产物γ-Fe2O3/rGO和TiO2-γ-Fe2O3/rGO的FT-IR图 Fig.2 FT-IR spectra of raw material GO, intermediate feedstock γ-Fe2O3/rGO and TiO2-γ-Fe2O3/rGO |
由图 2可知GO(a)、γ-Fe2O3/rGO(b)和TiO2-γ-Fe2O3/rGO(c)均在3 400 cm-1出现─OH的伸缩振动宽吸收峰,1 625、1 400、1 273、1 095 cm-1分别出现C═O、C─OH、─C─O─C─和─C─O─的伸缩振动峰;图 2(a)中617 cm-1是C═O的面内弯曲振动峰;图 2(b)、(c)中部分峰强度减弱说明GO部分被还原,在1 385、896 cm-1出现Fe2O3的特征吸收峰说明γ-Fe2O3/rGO、TiO2-γ-Fe2O3/rGO均成功负载了γ-Fe2O3;图 2(b)在795、570 cm-1出现γ-Fe2O3的─O─Fe─O─伸缩振动峰,说明成功制备γ-Fe2O3/rGO;图 2(c)在614 cm-1附近出现TiO2的小宽─O─Ti─O─伸缩振动峰,说明成功获得目标产物TiO2-γ-Fe2O3/rGO[21~23]。
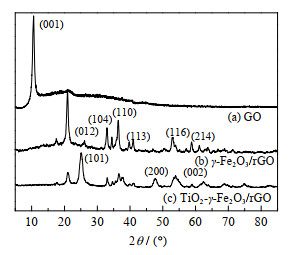
3.3 XRD表征原料GO、中间产物γ-Fe2O3/rGO和TiO2-γ-Fe2O3/rGO的XRD谱如图 3所示。
|
图 3 原料GO、中间产物γ-Fe2O3/rGO和TiO2- γ-Fe2O3/rGO的XRD图 Fig.3 XRD patterns of GO, γ-Fe2O3/rGO and TiO2-γ-Fe2O3/rGO |
由图 3(a)可以看出GO在2θ =10°附近出现了GO层状结构(001)面的特征峰[29]。由图 3(b)和(c)可知γ-Fe2O3/rGO和TiO2-γ-Fe2O3/rGO均在2θ =20°附近出峰,说明复合GO已经被还原成rGO[22],该结果与FT-IR表征相符。由图 3(b)可知,γ-Fe2O3/rGO在2θ =25.601°、33.014°、36.538°、53.116°、53.718°、58.993°出现了γ-Fe2O3 (012)、(104)、(110)、(113)、(116)和 (104)晶面衍射峰[30-31],说明在rGO上成功负载了γ-Fe2O3。由图 3(c)可知TiO2-γ-Fe2O3/rGO在2θ = 25.163°、47.660°、62.410°处出现了TiO2 (101)、(200)和(002)晶面衍射峰,说明成功制得目标产物TiO2-γ-Fe2O3/rGO[20-21]。
3.4 SEM和TEM表征原料GO及终产物GMIA的SEM如图 4所示。

|
图 4 GO及GMIA的SEM图 Fig.4 SEM micrographs of GO and GMIA |
由图 4(a)可以看出GO整体呈三维絮状分布,三维分布可提高GO的吸附比表面积。由图 4(b)看出γ-Fe2O3、TiO2和分子印迹以大小不等的颗粒分散地镶嵌于终产物GMIA表面。
中间产物γ-Fe2O3/rGO和TiO2- γ-Fe2O3/rGO及终产物GMIA的TEM如图 5所示。

|
图 5 γ-Fe2O3/rGO、TiO2- γ-Fe2O3/rGO和GMIA的TEM图 Fig.5 TEM micrographs of γ-Fe2O3/rGO, TiO2-γ-Fe2O3/rGO and GMIA |
由图 5(a)可以看出负载在rGO的纳米Fe2O3呈棒状和球状,与参考文献[21]纳米氧化铁符合。由图 5(b)可以看出TiO2主要包裹于纳米氧化铁表面,少量TiO2和纳米Fe2O3负载于rGO表面。包裹在纳米Fe2O3的TiO2,可利用纳米Fe2O3优异的导电性[23]在光催化时进行快速电子传输,抑制电子空穴的复合,提高光催化降解率。由图 5(c)可知引入的椭球状分子印迹均匀接枝于TiO2-γ-Fe2O3/rGO表面,该结果与SEM表征相符。
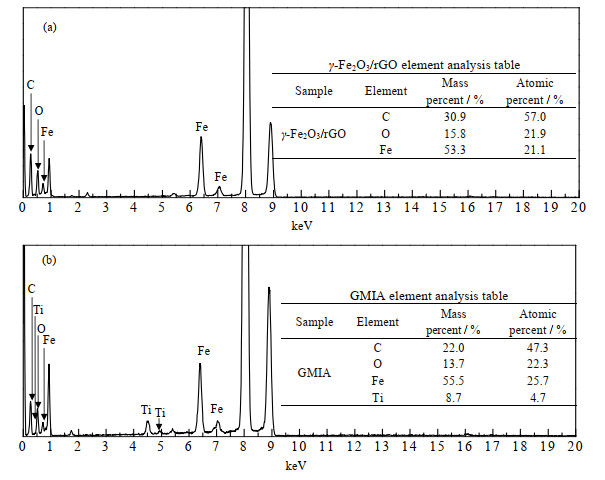
3.5 EDS表征GMIA中间产物γ-Fe2O3/rGO及终产物GMIA的EDS如图 6所示。
|
图 6 γ-Fe2O3/rGO(a)和GMIA(b)的EDS图 Fig.6 EDS spectra of γ-Fe2O3/rGO(a) and GMIA(b) |
图 6(a)、(b)分别是γ-Fe2O3/rGO和GMIA的EDS图,铁元素与氧化铁[23]的标准EDS谱图相符,钛元素的DES图与锐钛型TiO2[25]谱图完全相符。由图 6(a)、(b)可以看出在γ-Fe2O3/rGO上负载TiO2前后Fe的含量相近,说明纳米铁可以稳定负载在rGO上。用磁铁吸取相同质量的γ-Fe2O3/rGO、TiO2-γ-Fe2O3/rGO、GMIA时,TiO2-γ-Fe2O3/rGO、GMIA的吸引量小于γ-Fe2O3/rGO,是因为TiO2包裹纳米氧化铁后减小了纳米氧化铁的磁性。
3.6 GMIA/GNMIA吸附性能分析BaP的工作曲线如图 7所示。
|
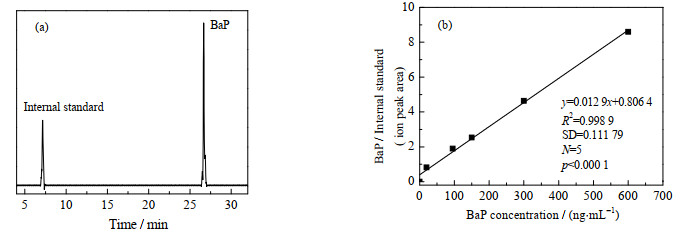
图 7 BaP的工作曲线 Fig.7 Standard working curve of BaP |
由图 7(a)可见,内标物萘和BaP能显著分离,BaP在26.6 min左右出现尖峰。BaP的工作曲线方程为y=0.012 9 x+0.806 4。y代表BaP峰面积与内标峰面积的比值;x代表BaP标准物质浓度。工作曲线的相关系数为0.998 9,线性范围为2~800 ng·mL-1。
用GC-MS测得未处理烟气吸收液中BaP峰面积/内标峰面积比值为4.628 3,代入工作曲线的方程,获得模拟BaP吸收液中BaP的质量浓度为296.273 ng·mL-1。同样利用工作曲线结合GC-MS检测结果获得GMIA和GNMIA对BaP的吸附效果,如图 8所示。
|
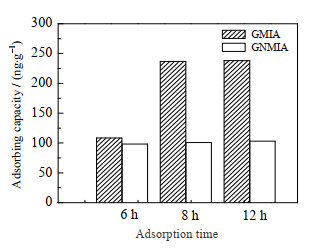
图 8 GMIA和GNMIA对BaP的吸附效果图 Fig.8 Adsorption results of BaP on GMIA and GNMIA |
由图 8可见,当吸附8 h后GMIA对BaP的吸附效果远高于GNMIA。利用式(1)[19]计算处理液中BaP的浓度:
| $\frac{{{S_{\rm{S}}}}}{{{S_1}}} = \frac{{{\rho _{\rm{S}}}}}{{{\rho _1}}}$ | (1) |
式中:SS、S1、
| $Q = \frac{{\left( {{\rho _0} - {\rho _2}} \right)V}}{m}$ | (2) |
式中:Q为不同吸附时间GMIA和GNMIA对BaP的吸附量(ng·g-1);V为香烟收集液的体积(mL);ρ0,ρ2为吸附前后溶液中BaP的质量浓度(mg·L-1);m为GMIA、GNMIA的质量(g)。GMIA对BaP吸附6、8、12 h的吸附数据如表 1所示。
|
|
表 1 GMIA和GNMIA对BaP的吸附数据 Table 1 Adsorption results of BaP on GMIA and GNMIA |
由表 1可知,吸附初期GMIA和GNMIA对BaP的吸附量相近,随着吸附时间的增加GMIA和GNMIA对BaP逐渐达到饱和吸附,根据式(3)计算得8 h时GMIA的印迹因子α=2.35[26],说明GMIA对BaP的吸附能力远高于GNMIA。
| $\alpha = \frac{{{Q_{\rm{GMIA}}}}}{{{Q_{\rm{GNMIA}}}}}$ | (3) |
由表 2可知,未引入分子印迹前GNMIA对BaP的吸附率仅为34.03%,引入分子印迹后GMIA对BaP的吸附率变为79.96%,吸附率明显提升,引入分子印记后GMIA对其他两种PHAs的吸附率明显下降,由此说明引入分子印迹可以有效提升GMIA对BaP的吸附率,实现GMIA对BaP的特异吸附。
|
|
表 2 GMIA和GNMIA对PHAs的吸附数据 Table 2 Adsorption results of PHAs on GMIA and GNMIA |
判断吸附材料的优劣与吸附的速度有关,可以通过建立动力学模型比较GMIA/GNMIA的吸附效能。GMIA和GNMIA的吸附动力学曲线如图 9所示。
|
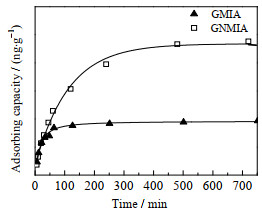
图 9 GMIA和GNMIA的吸附动力学曲线 Fig.9 Adsorption kinetic curves of GMIA and GNMIA |
由图 9可见,240 min之前GMIA和GNMIA的吸附速率较高,在240 min以后几乎没有变化,达到吸附平衡。
对GMIA和GNMIA吸附动力学结果进行准一级和准二级动力学模型拟合,表达式如下[27]:
一级动力学:
| $ {\ln _{}}({Q_{\rm{e}}} - {Q_t}) = - {k_1}t + \ln {Q_{\rm{e}}} $ | (4) |
二级动力学:
| $ \frac{t}{{{Q_t}}} = \frac{t}{{{Q_{\rm{e}}}}} + \frac{t}{{{k_2}Q_{\rm{e}}^2}} $ | (5) |
式中:t为吸附时间(min);Qe、Qt分别为吸附平衡时和t时刻GMIA和GNMIA对BaP的吸附量(ng·g-1);k1和k2分别为准一级和准二级吸附速率常数。GMIA和GNMIA的准一级和准二级反应动力学拟合结果如表 3。
|
|
表 3 吸附动力学模型拟合参数 Table 3 Fitting parameters of adsorption kinetic models |
由表 3可知,与一级吸附动力学拟合结果相比,二级吸附动力学模型拟合结果与实测得到的平衡吸附量Qe更接近,且相关性系数优于准一级吸附动力学模型(R2 < 0.999 8)。因此,GMIA和GNMIA对BaP的吸附动力学过程可用准二级吸附动力学模型描述。
由吸附量及吸附模型,结合相关文献,以及GMIA和BaP的分子特征推断吸附机理为:所制备的GMIA,以氧化石墨烯为分子骨架通过还原反应成为rGO。通过rGO表面的C─C和C─O键与烟气中PAHs的苯环及其他极性取代基间的π-π、p-π共轭作用及相互作用力将其吸附在表面[28]。石墨烯基气凝胶中引入BaP分子印迹,使其对BaP具有特异选择性,吸附烟气中各种物质时,BaP可被优先大量吸附,同时分子印记的特异吸附特性使BaP的平衡吸附量增加,特异吸附的同时吸附能力也随之提升。
3.8 GMIA降解性能及降解机理根据2.7节GMIA/GNMIA降解实验,利用式(1)计算紫外照射处理液中BaP的浓度,利用式(6) 计算降解率,降解数据如表 4所示。
| $w = \frac{{{\rho _0} - {\rho _2}}}{{{\rho _0}}} \times 100\% $ | (6) |
|
|
表 4 制备样品降解测定结果 Table 4 Degradation results of prepared samples |
式中:w为降解率。
从表 4见,随着紫外照射时间的延长,GMIA对BaP降解率在8 h时达到最大,为100%,同样条件下GNMIA对BaP的降解率为90.24%。即使继续紫外照射4 h,GNMIA也未能实现对BaP完全降解。外加磁场回收GMIA,在乙腈中充分超声洗涤,GC-MC检测洗涤液中无BaP,说明BaP已完全被GMIA降解。在2.7节的测定条件下测定紫外照射8 h GO对BaP的降解率,紫外照射后直接取出,降解液中BaP的质量浓度变为原香烟浓缩液的63%,充分超声清洗回收的GO,测得清洗液中BaP的质量浓度为原香烟浓缩液的34%,由此说明普通的吸附材料GO只能吸附BaP,但不能使其降解。
由吸附实验及降解实验,结合相关文献,以及GMIA和BaP的分子特征推断降解机制为:负载于GMIA表面的TiO2通过紫外照射形成的强氧化─OH [29]进攻吸附在GMIA分子印迹中的BaP使其被光催化降解。光催化降解过程中rGO[30]和纳米氧化铁[24]优良的导电性促进TiO2光电子的运输,抑制电子-空穴的复合,有效提高了TiO2的光催化降解率。BaP分子长时间被强氧化─OH进攻,稳定的多环共轭结构被破坏,被降解成其他链状化合物。而GMIA降解效率高于GNMIA,是因为GMIA和GNMIA吸附降解BaP时,含有GMIA溶液中的BaP逐一对应进入分子印迹中,减少了BaP在TiO2表面的堆积,有利于TiO2光催化时电子的运输,从而表现出优于GNMIA的降解性能。通过引入不同多环芳烃分子印迹,负载不同物质,赋予GMIA吸附光催化降解、电降解、磁性回收等性能,丰富GMIA的性能,扩展应用前景。
3.9 重复利用性应用性是新型吸附材料的重要研究价值所在,其重要的衡量指标之一即是能否重复利用。为此,针对本工作制备的GMIA进行重复利用实验。重复利用GMIA吸附降解效率如图 10所示。
|
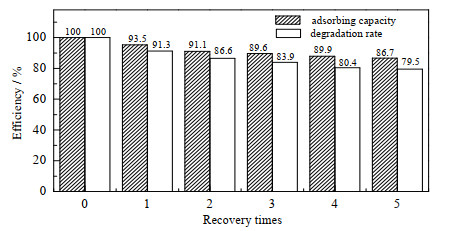
图 10 GMIA回收利用吸附和降解率 Fig.10 Recovery performance and degradation rates of GMIA |
由图 10可知,经过5次重复吸附降解循环,GMIA对BaP平衡吸附量仍保持在86% 以上,降解率也在79% 以上。说明GMIA具有优良的循环性能,便于重复吸附降解BaP,有广阔的应用前景。
4 结论所制备的GMIA兼具还原氧化石墨烯(rGO)的吸附性能和分子印迹聚合物的特异选择性能,可优先吸附BaP分子,并通过负载的TiO2光催化降解,达到特异吸附降解BaP的目的,最后利用纳米γ-Fe2O3的磁性将其回收;实验测得GMIA对BaP的平衡吸附量为236.891 ng·g-1,印迹因子α=2.35,吸附量远高于GNMIA,吸附动力学满足二级动力学模型;紫外照射8 h后GMIA可将BaP完全降解,吸附降解后的GMIA可通过外部磁场完全回收;GMIA重复5次吸附降解后,吸附量和降解率均保持在未重复利用的79% 以上,循环利用性能优异。本工作所制得的GMIA不仅能特异吸附BaP还可将其彻底降解,效果显著,弥补了现有吸附材料只能吸附不能降解BaP这一缺陷,减少了二次污染,为特异吸附降解空气中的BaP提供了一种优良的新型材料,为空气中多环芳烃的吸附降解研究提供参考。
| [1] |
LUCIA P, AVIO C G, GIULIANI M E, et al. Microplastics as vehicles of environmental PAHs to marine organisms: Combined chemical and physical hazards to the mediterranean mussels, mytilus galloprovincialis[J]. Frontiers in Marine Science, 2018, 5: 103-103. DOI:10.3389/fmars.2018.00103 |
| [2] |
SARKAR S, KHILLARE P S. Profile of PAHs in the inhalable particulate fraction: Source apportionment and associated health risks in a tropical megacity[J]. Environmental Monitoring and Assessment, 2013, 185(2): 1199-1213. DOI:10.1007/s10661-012-2626-9 |
| [3] |
AHSAN M A, JABBARI V, ISLAM M T, et al. Sustainable synthesis and remarkable adsorption capacity of MOF/graphene oxide and MOF/CNT based hybrid nanocomposites for the removal of Bisphenol A from water[J]. Science of the Total Environment, 2019, 673: 306-317. DOI:10.1016/j.scitotenv.2019.03.219 |
| [4] |
CUI Q, CHEN F Y, CHEN H Y. Benzo[a] pyrene (BaP) exposure generates persistent reactive oxygen species (ROS) to inhibit the NF-k B pathway in medaka (Oryzias melas tigma)[J]. Environmental Pollution, 2019, 251: 502-509. DOI:10.1016/j.envpol.2019.04.063 |
| [5] |
GRECO G, DI PIAZZA S, CECCHI G, et al. Mycoremediation of oily slime containing a polycyclic aromatic hydrocarbon mixture[J]. Waste and Biomass Valorization, 2019, 10: 3821-3831. DOI:10.1007/s12649-019-00802-x |
| [6] |
BELLINO A, BALDANTONI D, PICARIELLO E, et al. Role of different microorganisms in remediating PAH-contaminated soils treated with compost or fungi[J]. Journal of Environmental, 2019, 252: 109675.1-109675.8. |
| [7] |
KUDLEK E, DUDZIAK M. Degradation pathways of pentachlorophenol and benzo[a] pyrene during heterogeneous photocatalysis[J]. Water Science & Technology, 2018. DOI:10.2166/wst.2018.192 |
| [8] |
LAMICHHANE S, KRISHNA K C B, SARUKKALIGE R. Poly-cyclic aromatic hydrocarbons (PAHs) removal by sorption: A review[J]. Chemosphere, 2016, 148: 336-353. DOI:10.1016/j.chemosphere.2016.01.036 |
| [9] |
ZHOU Q X, WANG Y Q, XIAO J, et al. Preparation and characterization of magnetic nanomaterial and its application for removal of polycyclic aromatic hydrocarbons[J]. Journal of Hazardous Materials, 2019, 371: 323-331. DOI:10.1016/j.jhazmat.2019.03.027 |
| [10] |
SUN Z, WU Z, LIU D, et al. Microwave-assisted modification of activated carbon with cationic surfactants for enhancement of naphthalene adsorption[J]. Korean Journal of Chemical Engineering, 2017, 35: 203-210. |
| [11] |
COSTA J A S, SARMENTO V H V, ROMAO L P C, et al. Synthesis of functionalized mesoporous material from rice husk ash and its application in the removal of the polycyclic aromatic hydrocarbons[J]. Environmental Science and Pollution Research, 2019, 26: 25476-25490. DOI:10.1007/s11356-019-05852-1 |
| [12] |
YANG D Z, TAMMINA S K, LI X, et al. Enhanced removal and detection of benzo[a] pyrene in environmental water samples using carbon dots-modified magnetic nanocomposites[J]. Ecotoxicology and Environmental Safety, 2019, 170: 383-390. DOI:10.1016/j.ecoenv.2018.11.138 |
| [13] |
杨岚. 聚苯乙烯-石墨烯微球制备及其对有机污染物的吸附[D]. 天津: 天津大学, 2018. YANG L. Preparation of polystyrene-graphene microspheres and their adsorption of organic pollutants[D]. Tianjin: Tianjin University, 2018. |
| [14] |
HUANGFU Y M, RUAN K P, QIU H, et al. Fabrication and investigation on the PANI/MWCNT/thermally annealed graphene aerogel/epoxy electromagnetic interference shielding nanocomposites[J]. Applied Science and Manufacturing, 2019, 121: 265-272. DOI:10.1016/j.compositesa.2019.03.041 |
| [15] |
刘会娥, 黄扬帆, 马雁冰, 等. 石墨烯基气凝胶对有机物的饱和吸附能力[J]. 化工学报, 2018, 70(1): 280-289. LIU H E, HUANG Y F, MA Y B, et al. Saturation adsorption capacity of graphene-based aerogel on organic compounds[J]. CIESC Journal, 2018, 70(1): 280-289. |
| [16] |
AZAR F, ROBERT L, AVNEET K, et al. Photocatalytic degradation using TiO2-graphene nanocomposite under UV-LED illumination: Optimization using response surface methodology[J]. Journal of Environmental Chemical Engineering, 2019, 7(5): 103366. DOI:10.1016/j.jece.2019.103366 |
| [17] |
YAKOUT A A, SHAKER M A, ELWAKEEL K Z, et al. Lauryl sulfate@magnetic graphene oxide nanosorbent for fast methylene blue recovery from aqueous solutions[J]. Journal of Dispersion Science & Technology, 2019, 40(5): 707-715. |
| [18] |
王文霞. 银基及氧化铁基纳米材料的制备与催化性能研究[D]. 广州: 华南理工大学, 2019. WANG W X. Preparation and catalytic properties of silver and iron oxide based nanomaterials[D]. Guangzhou: South China University of Technology, 2019. |
| [19] |
LI J, CHEN C L, ZHANG R, et al. Nanoscale zero-valent iron particles supported on reduced graphene oxides by using a plasma technique and their application for removal of heavy-metal ions[J]. Chemistry, an Asian Journal, 2015, 10(6): 1410-1417. DOI:10.1002/asia.201500242 |
| [20] |
WANG S W, HSU K H, HUANG S C, et al. Determination of polycyclic aromatic hydrocarbons (PAHs) in cosmetic products by gas chromatography-tandem mass spectrometry[J]. Journal of Food and Drug Analysis, 2019, 27: 851-824. |
| [21] |
WANG Q J, TANG A D, ZHONG L F, et al. Amino-modified γ-Fe2O3/sepiolite composite with rod-like morphology for magnetic separation removal of Congo red dye from aqueous solution[J]. Powder Technology, 2018, 339: 872-811. DOI:10.1016/j.powtec.2018.08.055 |
| [22] |
KAMAL S, IONOV A, MOZHCHIL R N, et al. Simple synthesis of graphene nanocomposites MgO-rGO and Fe2O3-rGO for multifunctional applications[J]. Applied Physics A, 2018, 124: 365. DOI:10.1007/s00339-018-1748-5 |
| [23] |
KEPPELER M, SHEN N, NAGESWARAN S, et al. Synthesis of α-Fe2O3/carbon nanocomposites as high capacity electrodes for next generation lithium ion batteries: a review[J]. Journal of Materials Chemistry A, 2016, 4: 18223-18239. DOI:10.1039/C6TA08456G |
| [24] |
LI J J, GUO R N, MA Q L, et al. Efficient removal of organic contaminant via activation of potassium persulfate by γ-Fe2O3/α-MnO2 nanocomposite[J]. Separation and Purification Technology, 2019, 227: 115-669. |
| [25] |
陈永珍, 韩颖, 陈金发, 等. 二氧化钛的制备及以其为载体的脱硝催化性能研究[J]. 材料导报, 2016, 30(S1): 264-265, 273. CHEN Y Z, HAN Y, CHEN J F, et al. Preparation of titanium dioxide and its catalytic denitrification[J]. Materials review, 2016, 30(S1): 264-265, 273. |
| [26] |
MIN F, LV Z, HU Z, et al. A molecularly imprinted polymers/carbon dots-grafted paper sensor for 3-monochloropropane-1, 2-diol determination[J]. Food Chemistry, 2019, 274: 156-161. DOI:10.1016/j.foodchem.2018.08.133 |
| [27] |
MUSSA Z H, AI-QAIM F F, OTHMAN M R, et al. Pseudo first order kinetics and proposed transformation products pathway for the degradation of diclofenac using graphite-PVC composite as anode[J]. Journal of the Taiwan Institute of Chemical Engineers, 2017, 72: 37-44. DOI:10.1016/j.jtice.2016.12.031 |
| [28] |
CHENG C L, CAI Y Q, GUAN G J, et al. Hydrophobic-force-driven removal of organic compounds from water by reduced graphene oxides generated in agarose hydrogels[J]. Angewandte Chemie, 2018, 57: 11177-11181. DOI:10.1002/anie.201803834 |
| [29] |
VALERIE L E S, CHIN W L, JOON C J, et al. One-step solvothermal synthesis of rGO/TiO2 nanocomposite for efficient solar photocatalytic degradation of methylene blue dye[J]. Current Nanoscience, 2019, 15: 157-162. |
| [30] |
彭璐. 二氧化钛/还原石墨烯基复合纳米催化剂的制备及其催化性能研究[D]. 合肥: 合肥工业大学, 2019. PENG L. Preparation and catalytic performance of titanium dioxide/reduced graphene-based composite nano-catalysts[D]. Hefei: Hefei University of Technology, 2019. |




