2. 深圳清华大学研究院 生态与环境保护实验室, 广东 深圳 518057
2. Laboratory of Ecology and Environmental Protection, Research Institute of Tsinghua University in Shenzhen, Shenzhen 518057, China
紫外线应用于水消毒具有无药物残留、操作简单安全等优点,特别是作用于耐氯的“两虫”灭活效果好[1],在水消毒领域得到了广泛应用。它还可和其他消毒技术组合成为高级氧化技术来分解水中的难氧化物质[2-3]。紫外线应用的核心是到达目标物质的光子数量与被照射物质的生物或化学变化之间的关系。因此,对于研发、设计和运行紫外线反应器,准确测量紫外线光子数量非常重要[4]。紫外线测量方法分为仪器物理测量和化学曝光剂测量2种方法。紫外辐照计对测量环境要求低,且测量过程简单,但需要标准量值传递的校准、对入射光束的面积和角度要求高。化学曝光剂是通过检测光线照射前后液体中化学物质浓度的变化,计算出接收到的光子数量。作为一种测量手段,它可直接获得光子数量的绝对值,无需依赖标准数据传递的校准过程。据统计,文献报道的化学曝光剂有90余种,而且仍不断有新型化学曝光剂的报道[5-16]。在紫外线测量领域,研究和应用最多的是碘离子/碘酸根(KI/KIO3)化学曝光剂[17-20]和草酸铁(ferrioxalate)化学曝光剂[7, 21]。虽然后者的历史更长[22-23],但其感应波长上限达490 nm[22]。而KI/KIO3的敏感波长范围在330 nm以下[24],在操作和受可见光干扰方面具有优势。由于测量的是进入液体的光子数量,其与光子的入射角无关;但入射角有关的反射量,可应用菲涅尔方程进行计算而排除影响。这避免了电子紫外辐照计接收窗的响应角度的问题[25-26],从而使化学曝光剂适用于测量点光源、大入射角光线。例如,新型紫外光源紫外发光二极管(UV-LED)近似点光源,足够面积的化学曝光剂可充分捕捉其光子总量,化学曝光剂是有效准确的测量手段。由于化学曝光剂具有可以直接测量光子数量的特性,故还可应用于校准电子紫外辐照计。世界知名紫外线学者Jim Bolton教授测量并报道了准确的量子收率数值。KI/KIO3化学曝光剂目前是领域内最重要的化学曝光剂。在文献中,一般在使用KI/KIO3化学曝光剂时,都是以“当天配制”控制/描述测量精度。显然,影响测量精度的不只时间一个因素,并且“当天”也不是一个准确的时间概念。为了保证测量的准确性,必须了解各种影响因素对测量数值的影响。然而,目前还没有关于KI/KIO3化学曝光剂的测量误差、影响因素的报道。本文考察了准确测量所需要控制的因素,为在应用KI/KIO3化学曝光剂进行测量时,减小误差提供理论基础。
2 实验部分 2.1 试剂与仪器化学试剂均为分析纯,使用前未进行任何预处理。溶液配制均使用在实验室制备的纯水(Arium comfort,德国赛多利斯)。用分光光度计(Cary 60 UV-Vis,安捷伦)测量溶液的吸光度。紫外线仪器测量使用的是254 nm辐射照度计(UV-B,北师大光学仪器厂)。紫外线光源为低压汞灯(ZW14D15W-Z287,柯维)。为避免电压波动的影响,设置了电压调节器(T18124258,德力西),并用功率仪(WT333E,横河)连续监测电压。
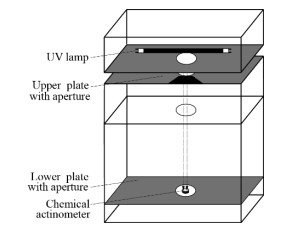
2.2 实验过程曝光剂的照射主要是在平行光设备中进行。采用的是孔式平行光设备[26-28]。如图 1所示,照射距离和投光孔径是可调节的。为减少温度和空气流动对紫外线灯的影响,紫外线灯设置在水下[28-29]。
|
图 1 孔式平行光设备 Fig.1 Aperture collimated beam apparatus |
碘离子接受波长小于330 nm的光子后,会发生电子向溶液转移的化学反应[23-24]:
| $4{{\rm{I}}^ - } + 2h\nu \to {\rm{I}}_3^ - + {{\rm{I}}^ - } + 2{{\rm{e}}^ - }_{{\rm{aq}}}$ | (1) |
式中:h为普朗克常数,6.626 070 15×10-34 J·s;
| ${{\rm{I}}^ - } + 4{{\rm{e}}^ - }_{{\rm{aq}}} + {\rm{IO}}_3^ - + 3{{\rm{H}}_{\rm{2}}}{\rm{O}} \to {\rm{I}}_3^ - + 6{\rm{O}}{{\rm{H}}^ - }$ | (2) |
最终产物I3-在352 nm具有特征峰,可用分光光度计测量其浓度。根据其浓度及量子收率即可确定光子的数量。KI/KIO3化学曝光剂的量子收率的最新数据为[30]
| $ \varphi = (0.71 \pm 0.02) + (0.0099 \pm 0.000\;4) \times (t - 24) $ | (3) |
式中:t为温度,℃
根据化学反应式(1)和(2),4个光子可以产生3个I3-,理论量子收率是0.75。该值高于式(3)的值,说明有一定数量光子进入液体后没有诱发光化学反应。相同的光子通量照射下,I3-的产率与KI/KIO3化学曝光剂溶液的浓度关联[20, 24]。经典的KI/KIO3化学曝光剂溶液浓度是0.6 mol·L-1碘化钾、0.1 mol·L-1碘酸钾、0.01 mol·L-1四硼酸钠。四硼酸钠的作用是缓冲溶液的pH值。式(3)和以前报道的量子收率[31]都是在此浓度下测量的。Rahn对I3-的摩尔吸收系数ε352有研究报道,并进行了2次修订,26 400[24]、27 600[31],27 636 mol-1·L·cm-1[32]。根据量子收率和摩尔吸收系数即可获得光子总量的计算公式[19, 24]:
| $E = \frac{{\Delta {A_{352}} \times V \times {U_{253.7}}}}{{\varphi \times {\varepsilon _{352}} \times (1 - R)}}$ | (4) |
式中:E为光子能量总和,mJ;ΔA352为化学曝光剂在紫外线照射前后在352 nm、1 cm光程的吸光度变化;V为溶液的有效体积,mL;U253.7为波长253.7 nm的光子能量,J·mol-1;R为光线射入水体时的反射系数。
| ${U_{253.7}} = h \times \nu = \frac{{h \times c}}{{{\rm{253}}{\rm{.7}}}}$ | (5) |
式中:c为光速,2.997 924 58×108 m·s-1。
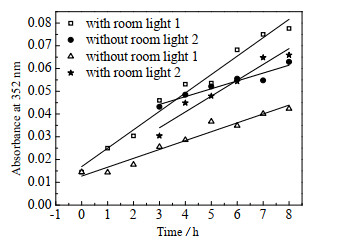
3 实验结果与讨论 3.1 溶液的稳定性 3.1.1 时间与可见光在室内,将窗帘放下避免太阳光直射并且照明灯关闭的情况下,将配制的曝光剂溶液放入2个透明瓶子中,一个置于桌面不避光保存(标记为:有光1),一个放入遮光盒避光(标记为:无光1)。3 h后,从“有光1”样品中取出部分液体转入透明瓶中并避光保存(标记为:无光2),从“无光1”样品中取出部分液体转入透明瓶置于桌面不避光保存(标记为:有光2)。各样品的352 nm吸光度随时间变化曲线见图 2。
|
图 2 KI/KIO3曝光剂吸光度随时间的变化曲线(22.4 ℃) Fig.2 Absorbance curve of KI/KIO3 actinometer with time (22.4 ℃) |
在无光的情况下,曝光剂溶液也有可能产生分子碘[33],
| ${\rm{IO}}_3^ - + 5{{\rm{I}}^ - } + 6{{\rm{H}}^{\rm{ + }}} \to 3{{\rm{H}}_{\rm{2}}}{\rm{O + 3}}{{\rm{I}}_{\rm{2}}}$ | (6) |
| ${\rm{I}}_3^ - \leftrightarrow {{\rm{I}}^ - }{\rm{ + }}{{\rm{I}}_{\rm{2}}}$ | (7) |
由于式(6)和(7)并无任何波长的光子参与,也产生了I3-。因此,本文可以观察到在完全避光的情况下(见图 2中的曲线无光1),溶液的352 nm吸光度也在随时间上升。图 2显示化学反应式(6)和(7)的反应速度很慢,所以KI/KIO3可以作为化学曝光剂使用。一般文献中都以“当天配制”间接表示化学曝光剂测量的准确性。事实上,时间因素会导致一定的测量误差。实验中,记录测量时间,可根据图 2的线性关系计算消除这一误差。
观察图 2,可以看到不但“有光1”的上升速度(斜率)大于“无光1”,而且“有光1”平行于“有光2”,“无光1”平行于“无光2”。有光时,352 nm吸光度的变化约为0.007 7 Abs·h-1。如果用56 mm直径的小玻璃皿加5 mL溶液进行测量,0.007 7 Abs·h-1导致的辐射剂量误差是0.03 J·(m2·h)-1。说明室内可见光对测量的影响非常小。这符合Rahn[23]报道的碘化钾在可见光区域的400、425、450 nm仍有吸光系数,但比在352 nm的吸光系数低了一个数量级。Rahn[24]认为这些吸收可忽略。另一方面,尽管误差很小,根据图 2的实验数据,实际操作时,待使用的曝光剂应避光保存。
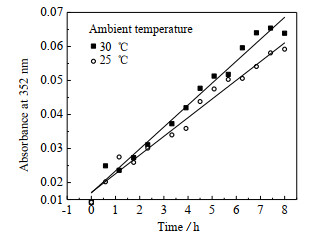
3.1.2 温度在无紫外线照射情况下,曝光剂液体内仍有化学反应(见式(6)和(7))。图 3是不同温度下溶液在352 nm吸光度随时间的变化曲线(放置在室内,未进行特别的避光处理)。在25和30 ℃时的352 nm吸光度的变化分别为0.005 6和0.006 2 Abs·h-1。温度升高加剧了吸光度的上升速度。这是因为温度增强了分子的活泼性,会增加I3-的浓度。
|
图 3 KI/KIO3曝光剂吸光度在不同环境温度下随时间变化曲线 Fig.3 Absorbance curve of KI/KIO3 actinometer with time at different ambient temperatures |
吸光度随时间的变化与室内光线强弱、置放地点与灯的相对距离和角度有关。图 2和3的实验是在不同房间进行的,对比吸光度的时间变化值(Abs·h-1),显然,进行图 2实验的房间光线相对强一些。为消除溶液不稳定性可能造成的测量误差,在实验过程中,可设置全程伴随的空白试样:每次实验都设置2个样品,一个接受紫外线照射,一个不照射,两者的吸光度之差为照射样的真实吸光度。
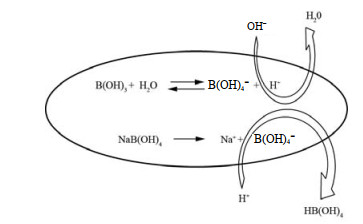
3.2 溶液的配制曝光剂是由3种化学药剂溶解配制而成的溶液。本文考察了曝光剂配制过程中,四硼酸钠的溶解顺序及浓度对液体吸光度的影响。实验结果显示:(1)碘化钾、碘酸钾和四硼酸钠同时加入水中,溶解后,溶液无色,352 nm吸光度为0.043 5;(2)先将碘化钾和碘酸钾同时加入水中,溶解后,溶液呈淡黄色;随后分别加入不同浓度(0.01、0.064 mol·L-1)的四硼酸钠并溶解,溶液仍维持淡黄色,352 nm吸光度分别为0.430 1、0.438 8;(3)先配制0.01 mol·L-1的四硼酸钠。然后加入碘化钾,充分溶解后,再加入碘酸钾,充分溶解,溶液无色,352 nm吸光度为0.040 3。说明在配制曝光剂时,四硼酸钠的浓度对吸光度影响不大,但其添加顺序影响非常大。这说明pH对液体内部KI和KIO3之间的反应有非常大的影响。化学反应式(6)显示低pH有利于I2的形成,而溶液中有大量I-存在,最后导致低pH促进了化学反应式(7),即促进了I3-的形成。四硼酸钠缓冲pH的机理是水解产生
|
图 4 四硼酸钠缓冲pH的机理 Fig.4 Mechanism of buffering pH in sodium tetraborate |
(1) 搅拌
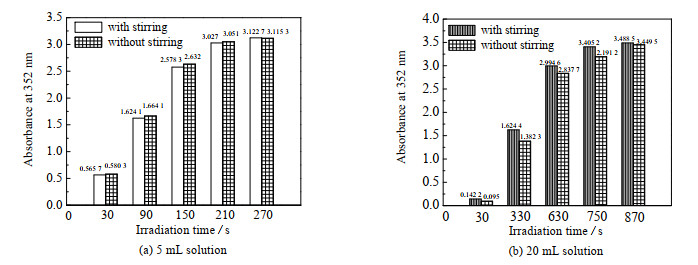
用内直径为56 mm的玻璃容器进行搅拌和不搅拌的对比实验,搅拌子直径3 mm,长15 mm。被照射液体表面距灯中心的距离是428 mm。分别进行了5和20 mL 2组液体的实验,水深分别为2.0和8.1 mm。照射时,准平行光束的投影面积大于液体面积。实验结果见图 5,由图 5(a)可知水量少、水浅时搅拌和不搅拌情况下,照射后溶液的吸光度没有区别,而根据图 5(b)可知水量多、水深时,有无搅拌有明显差异。经实测,KI/KIO3化学曝光剂在253.7 nm的吸光度约为4.5,即5 mm的透光率仅为0.56%。因此,光化学反应主要发生在液体表面,在液体表面生成的I3-需要扩散离开表面、碘离子需要扩散至表面,这些扩散的速度有限,导致在水深较大、不搅拌的情况下,扩散不充分会使测量值偏低。
|
图 5 搅拌对吸光度的影响 Fig.5 Influence of stirring on absorbance |
(2) 转子与照射面积
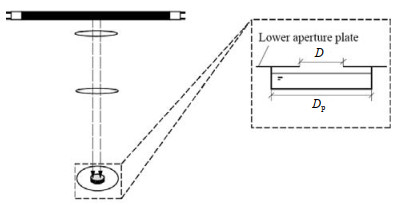
磁力搅拌转子对测量体积和面积都可能有影响。化学曝光剂计量的是进入液体的光子数量(光子总能量),见式(4)。光子总能量除以这些光子“光束通过的面积”就是辐射剂量。实际测量时,照射面积示意图见图 6,当调节平行光设备的下孔板的直径时,会有2种情况(Dp为容器内溶液的上表面直径;D为下孔板上孔的直径):D < Dp,“光束通过的面积”实际是下孔板上孔径的面积;D≥Dp,“光束通过的面积”实际是容器内溶液的上表面积。实验中的转子直径为3 mm,长为15 mm,体积为0.106 mL,旋转时占面积为1.766 cm2。D≥Dp,转子和液体的体积和面积比值分别为0.021 2(液体体积为5 mL)和0.071 7。根据图 5,在这些比率下,转子的体积和面积对测量的影响很小。为考察D < Dp的情况,将下孔径板上的孔径D调节到14 mm,用5 mL液体对比2种情况:转子在下孔板上的孔正中心的下方,入射光可照射到转子;转子不在下孔板上的孔正中心的下方(偏离孔中心),入射光照射不到转子。共进行了6组实验(3组对照实验),结果表明转子被照射时的辐射照度平均值E(1.125 W·m-2)低于转子不被照射时的平均值(1.364 W·m-2),存在17.5 % 的误差。因此,实际照射时,应避免搅拌转子被紫外光直接照射。
|
图 6 照射面积示意图 Fig.6 Schematic diagram of irradiation area |
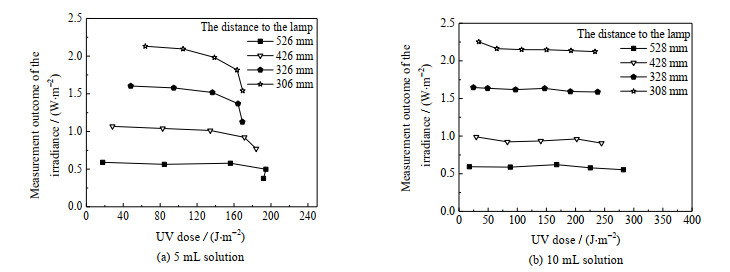
溶液接受到的辐射剂量越大,产生的I3-越多,过高的I3-浓度可能会干扰光子和碘离子的反应。造成干扰的最小I3-浓度是一个临界阈值浓度,可认为在该浓度下I3-已达“饱和”状态,浓度再高时会导致曝光剂测量不准确。为了考察I3-的“饱和”现象,进行了不同剂量下测量到的辐射照度值的实验。由图 7(a)知,辐射照度值在一定的剂量值范围内呈稳定状态,在超出了一定的剂量后,呈现突然下降,说明了I3-的“饱和”现象的存在,饱和阈值出现在150~200 J·m-2。保守地取160 J·m-2作为剂量的饱和阈值,可根据液体表面积和公式(4)计算出I3-浓度的饱和阈值浓度为0.001 672 mol·L-1。而图 7(b),由于I3-浓度尚未到达I3-的“饱和”阈值浓度,I3-没有干扰光子和碘离子的反应,所以曲线都呈稳定态。因此,为确保化学曝光剂测量的准确性,测量时需控制I3-浓度不高于阈值浓度。
|
图 7 辐射剂量对曝光剂液体测得的辐射照度的影响 Fig.7 Influence of UV dose on the measured irradiance by chemical actinometer |
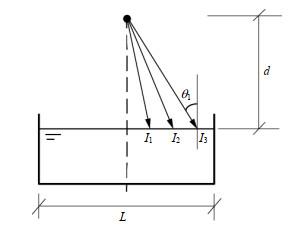
紫外线从空气入射曝光剂时,有部分光子被反射而没有进入曝光剂。在平行光设备中,入射角度很小,因此取反射系数R为0.025。但当化学曝光剂测定点光源的紫外辐射照度时,需要将点光源设置在化学曝光剂液面的近距离处。这样的情况下,入射角度对反射系数的影响不能忽略。点光源近距离、多角度入射化学曝光剂的示意图见图 8,图中,d为点光源距化学曝光剂液面的距离,mm;L为接收点光源照射面的直径,mm。反射系数遵循菲涅耳方程(Fresnel Equation),
| $ R = \frac{1}{2} \times {\left( {\frac{{{n_1} \times \cos {\theta _1} - {n_2} \times \cos {\theta _2}}}{{{n_1} \times \cos {\theta _1} + {n_2} \times \cos {\theta _2}}}} \right)^2} + \frac{1}{2} \times {\left( {\frac{{{n_2} \times \cos {\theta _1} - {n_1} \times \cos {\theta _2}}}{{{n_1} \times \cos {\theta _2} + {n_2} \times \cos {\theta _1}}}} \right)^2} $ | (8) |
|
图 8 曝光剂点光源入射 Fig.8 Radiation beams from a point light source to the actinometer |
式中:n1为紫外线在空气的折射率,1.0;n2为紫外线在水的折射率,1.372;θ1为空气侧的入射角,度;θ2为水侧的出射角,度。
平均反射系数为
| ${R_{{\rm{av}}e}} = \frac{{\sum\nolimits_{i = 1}^n {{I_i} \times {R_i}} }}{{\sum\nolimits_{i = 1}^n {{I_i}} }}$ | (9) |
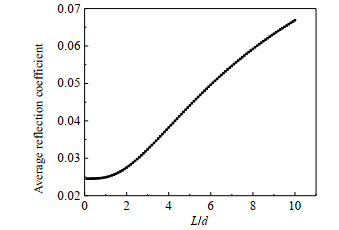
式中:Ri、Ii分别为不同入射角时所对应的反射系数、入射光的辐射照度值。反射系数的平均值Rave与L/d的关系见图 9。当L/d < 1时,Rave为0.025。当L/d > 1时,Rave随L/d增大。
|
图 9 平均反射因子随L/d的变化 Fig.9 Variation of the average reflection coefficient with L/d |
孔式平行光设备最主要的特点是移除了管式平行光设备的“管”,这就消除了管内壁的反射导致的测量误差。但是,因为孔式平行光设备采取了在板上开孔的方法,而板具有厚度,开孔后,实际构成了一个高度为板厚、直径为孔径的管,依然有可能反射光线。对比了厚度为5 mm的带孔板和几乎无厚度板(用开孔纸调节了孔边缘)的读数,因“短管”的反射,测量值增加了4.58% (4次测量的标准偏差是0.021 7)。
3.4.3 容器残留水应用于平行光设备的化学曝光剂液体放置在小玻璃皿中。清洗后烘干使用不会有残留水等问题。但在实际操作中,一般都是清洗后立刻使用。如用擦拭纸吸附玻璃皿中残留水,会有纸巾残留物的担忧。通过多次甩动,可清除残留水,但去除不彻底。用直径56 mm、深15 mm的玻璃皿进行5 mL液体的10次重复实验,残留水导致的相对误差平均值为0.23% (标准偏差为0.082 4%)。
4 结论本文对KI/KIO3化学曝光剂测量影响因素的研究显示:传统以“当天配制”的方式无法确保测量精度。为保证测量的准确性,需要对主要影响因素进行控制:
(1) 曝光剂自身的稳定性受室内可见光和温度的影响,分别为0.03 J·(m2·h)-1、0.005 6 Abs·h-1(25 ℃)。设立全程伴随空白试样是消除这2个因素影响的有效方法;
(2) 曝光剂药品添加和溶解顺序可导致352 nm吸光度相差1个数量级。因此,溶液的配制应按四硼酸钠、碘化钾、碘酸钾的顺序依次添加、溶解后再添加另一种药品;
(3) 曝光剂接收到的辐射剂量不能过高,否则I3-浓度超过饱和阈值,会导致测量失准。
| [1] |
李梦凯, 王琛, 陈鹏, 等. 饮用水紫外消毒器辐射剂量验证和在线监控[J]. 中国给水排水, 2013, 29(7): 48-51. LI M K, WANG C, CHEN P, et al. Dose validation and online monitoring of UV disinfection reactor for drinking water treatment[J]. China Water & Wastewater, 2013, 29(7): 48-51. DOI:10.3969/j.issn.1000-4602.2013.07.012 |
| [2] |
张晖, 陈焕钦. 紫外光辐射下臭氧在水中的分解动力学[J]. 高校化学工程学报, 2002, 16(1): 28-32. ZHANG H, CHEN H Q. Decomposition kinetics of ozone in water with ultraviolet radiation[J]. Journal of Chemical Engineering of Chinese Universities, 2002, 16(1): 28-32. DOI:10.3321/j.issn:1003-9015.2002.01.006 |
| [3] |
翁棣. 动态紫外光辐射下臭氧协同循环流动降解磺基水杨酸的研究[J]. 高校化学工程学报, 2003, 17(4): 471-475. WENG D. Studies on degradation of sulfosalicylic acid by dynamic O3/UV process[J]. Journal of Chemical Engineering of Chinese Universities, 2003, 17(4): 471-475. DOI:10.3321/j.issn:1003-9015.2003.04.022 |
| [4] |
宋叶叶, 张连峰, 张金松, 等. 环境反射光导致紫外线辐射照度测量误差的分析与消除方法[J]. 辐射研究与辐射工艺学报, 2020, 38(2): 64-72. SONG Y Y, ZHANG L F, ZHANG J S, et al. Analysis and countermeasure of the error evoked by the reflective light from the measurement of UV irradiance[J]. Journal of Radiance Research and Radiation Processing, 2020, 38(2): 64-72. |
| [5] |
KUHN H J, BRASLAVSKY S E, SCHMIDT R. Chemical actinometry[J]. Pure and Applied Chemistry, 2004, 76(12): 2105-2146. DOI:10.1351/pac200476122105 |
| [6] |
EL ACHI N, BAKKOUR Y, CHAUSSET-BOISSARIE L, et al. Rapid and facile chemical actinometric protocol for photo-microfluidic systems using azobenzene and NMR spectroscopy[J]. The Royal Society of Chemistry Advances, 2017, 7(47): 29815-29820. |
| [7] |
ASENATH-SMITH E, AMBROGI E K, MOORES L C, et al. Leveraging chemical actinometry and optical radiometry to reduce uncertainty in photochemical research[J]. Journal of Photochemistry and Photobiology A- Chemistry, 2019, 372: 279-287. DOI:10.1016/j.jphotochem.2018.12.024 |
| [8] |
REINFELDS M, HERMANNS V, HALBRITTER T, et al. A robustly absorbing fulgide derivative as a universal chemical actinometer for the UV to NIR region[J]. Chemphotochem, 2019, 3(6): 441-449. DOI:10.1002/cptc.201900010 |
| [9] |
PENCONI M, LOBRY E, JASINSKI F, et al. The use of chemical actinometry for the evaluation of the light absorption efficiency in scattering photopolymerizable miniemulsions[J]. Photochemical & Photobiological Sciences, 2015, 14(2): 308-319. |
| [10] |
MAAFI M, MAAFI W. Montelukast photodegradation: elucidation of Ф-order kinetics, determination of quantum yields and application to actinometry[J]. International Journal of Pharmaceutics, 2014, 471(1/2): 544-552. |
| [11] |
MAAFI M, MAAFI W. Quantification of unimolecular photoreaction kinetics: Determination of quantum yields and development of actinometers-the photodegradation case of cardiovascular drug nisoldipine[J]. International Journal of Photoenergy, 2015, 2015: 1-12. |
| [12] |
MAAFI M, MAAFI W. Quantitative assessment of photostability and photostabilisation of fluvoxamine and its design for actinometry[J]. Photochemical & Photobiological Sciences, 2015, 14(5): 982-994. |
| [13] |
LI H, BETTERTON E A, ARNOLD R G, et al. Convenient new chemical actinometer based on aqueous acetone, 2-propanol, and carbon tetrachloride[J]. Environmental Science & Technology, 2005, 39(7): 2262-2266. |
| [14] |
LEE J, KIM J, CHOI W. Ferrioxalate-polyoxometalate system as a new chemical actinometer[J]. Environmental Science & Technology, 2007, 41(15): 5433-5438. |
| [15] |
SANTOS A R, BALLARDINI R, BELSER P, et al. Photochemical investigation of a photochromic diarylethene compound that can be used as a wide range actinometer[J]. Photochemical & photobiological Sciences, 2009, 8(12): 1734-1742. |
| [16] |
BLATCHLEY E R, SHEN C Y, NAUNOVIC Z, et al. Dyed microspheres for quantification of UV dose distributions: photochemical reactor characterization by lagrangian actinometry[J]. Journal of Environmental Engineering, 2006, 132(11): 1390-1403. DOI:10.1061/(ASCE)0733-9372(2006)132:11(1390) |
| [17] |
RAHN R O, BOLTON J, STEFAN M. The iodide/iodate actinometer in UV disinfection: Determination of the fluence rate distribution in UV reactors[J]. Photochemistry and Photobiology, 2006, 82(2): 611-615. DOI:10.1562/2005-06-10-RN-570 |
| [18] |
RAHN R O, ECHOLS S. Iodide/Iodate chemical actinometry using spherical vessels for radiation exposure as well as for monitoring absorbance changes[J]. Photochemistry and Photobiology, 2010, 86(4): 990-993. DOI:10.1111/j.1751-1097.2010.00747.x |
| [19] |
QIANG Z M, LI W T, LI M K, et al. Inspection of feasible calibration conditions for UV radiometer detectors with the KI/KIO3 actinometer[J]. Photochemistry & Photobiology, 2015, 91(1): 68-73. |
| [20] |
陈钰, 张连峰, 刘淑杰, 等. 低压单波长紫外灯在水下时紫外线输出量的测量[J]. 中国给水排水, 2018, 34(21): 47-52. CHEN Y, ZHANG L F, LIU S J, et al. Measurement of UV output of monochromatic (254 nm) low pressure UV lamp in water[J]. China Water & Wastewater, 2018, 34(21): 47-52. |
| [21] |
AILLET T, LOUBIERE K, DECHY-CABARET O, et al. Accurate measurement of the photon flux received inside two continuous flow microphotoreactors by actinometry[J]. International Journal of Chemical Reactor Engineering, 2014, 12(1): 1-13. DOI:10.1515/ijcre-2013-0071 |
| [22] |
PARKER C A. A new sensitive chemical actinometer Ⅰ. Some trials with potassium ferrioxalate[J]. Mathematical and Physical Sciences, 1953, 220(1140): 104-116. |
| [23] |
RAHN R O. Use of potassium iodide as a chemical actinometer[J]. Photochemistry and Photobiology, 1993, 58(6): 874-880. DOI:10.1111/j.1751-1097.1993.tb04986.x |
| [24] |
RAHN R O. Potassium iodide as a chemical actinometer for 254 nm radiation: use of iodate as an electron scavenger[J]. Photochemistry and Photobiology, 1997, 66(4): 450-455. DOI:10.1111/j.1751-1097.1997.tb03172.x |
| [25] |
MARTIN C J, CURRIE G D, PYE S D. The importance of radiometer angular response for ultraviolet phototherapy dosimetry[J]. Physics in Medicine and Biology, 1999, 44(4): 843-855. DOI:10.1088/0031-9155/44/4/003 |
| [26] |
BOLTON J R, LINDEN K G. Standardization of methods for fluence (UV dose) determination in bench-scale UV experiments[J]. Journal of Environmental Engineering, 2003, 129(3): 209-215. DOI:10.1061/(ASCE)0733-9372(2003)129:3(209) |
| [27] |
BOLTON J R, BECK S E, LINDEN K G. Protocol for the determination of fluence (UV dose) using a low-pressure or low-pressure high-output UV lamp in bench-scale collimated beam ultraviolet experiments[J]. IUVA News, 2015, 17(1): 11-16. |
| [28] |
ZHANG L F, SONG Y Y, ZHANG J S, et al. Mathematical modeling and application of aperture type of collimated beam apparatus for fluence measurement and radiometer calibration[J]. Journal of Environmental Engineering, 2020, 146(12): 04020129. DOI:10.1061/(ASCE)EE.1943-7870.0001811 |
| [29] |
张连峰, 张金松. 箱式紫外线平行光设备及紫外线辐射照度计的校准方法: CN, 201910791304.7[P]. 2019-12-10. ZHANG L F, ZHANG J S. Box-type ultraviolet collimated beam apparatus and the calibration method of an ultraviolet radiometer: CN, 201910791304.7[P]. 2019-12-10. |
| [30] |
BOLTON J R, STEFAN M I, SHAW P S, et al. Determination of the quantum yields of the potassium ferrioxalate and potassium iodide-iodate actinometers and a method for the calibration of radiometer detectors[J]. Journal of Photochemistry and Photobiology A: Chemistry, 2011, 222(1): 166-169. DOI:10.1016/j.jphotochem.2011.05.017 |
| [31] |
RAHN R O, STEFAN M I, BOLTON J R, et al. Quantum yield of the iodide-iodate chemical actinometer: dependence on wavelength and concentration[J]. Photochemistry and Photobiology, 2003, 78(2): 146-152. DOI:10.1562/0031-8655(2003)078<0146:QYOTIC>2.0.CO;2 |
| [32] |
RAHN R O. Fluence measurements employing iodide/iodate chemical actinometry as applied to upper-room germicidal radiation[J]. Photochemistry and Photobiology, 2013, 89(4): 816-818. DOI:10.1111/php.12094 |
| [33] |
NOYES R M, KALACHEV L V, FIELD R J. Mathematical model of the bray-liebhafsky oscillations[J]. Journal of Physical Chemistry, 1995, 99(11): 3514-3520. DOI:10.1021/j100011a018 |
| [34] |
RUASSE M F, AUBARD J, GALLAND B, et al. Kinetic study of the fast halogen-trihalide ion equilibria in protic media by the raman-laser temperature-jump technique. A non-diffusion-controlled ion-molecule reaction[J]. Journal of Physical Chemistry, 1986, 90(18): 4382-4388. DOI:10.1021/j100409a034 |




