X-连锁显性低血磷性佝偻病/骨软化症(X-linked dominant hypophosphatemic rickets/osteomalacia,XLH)是一种罕见的骨骼矿化异常性疾病,其发病率约为(3.9~5.0)/10万[1],是遗传性低血磷性佝偻病/骨软化症中最常见的一型。该疾病临床表现存在一定轻重差异,典型临床表现:患儿常于幼年起病,自学步期逐渐出现双下肢弯曲畸形,身高生长缓慢、身高低于同龄儿童,可伴有骨骼疼痛,以双下肢为著,牙齿发育异常,常伴发牙周脓肿;成年患者则会进一步出现骨软化表现,关节退行性变及关节炎、肌腱韧带钙化(附着点病)、假骨折等,同时伴有显著身材矮小、骨痛及活动能力受限,严重影响患者的生活质量。XLH患者主要生化特点为低磷血症、1,25双羟维生素D3 [1,25-dihydroxyvitamin D, 1, 25(OH)2D3]水平偏低或不恰当的正常、PTH可在正常范围或轻度升高,儿童患者常伴有骨碱性磷酸酶水平升高。
XLH的致病机制是PHEX (phosphate-regulat-ing gene with homology to endopeptidases on the X chromosome)基因的失活突变[2]。PHEX蛋白是M13金属蛋白酶家族成员,其编码基因包含22个外显子,编码蛋白含749个氨基酸。PHEX的主要功能域是位于17和19外显子的锌离子结合区,该区域在M13家族各成员间高度保守,在蛋白发挥其催化作用的过程中起关键作用[3]。目前已有超过400个PHEX基因突变位点被报道,包括错义突变、无义突变、插入/缺失突变或剪切位点突变等不同突变类型,均可影响PHEX蛋白功能,导致疾病的发生。该基因功能缺陷导致XLH发生的机制为成纤维细胞生长因子23(fibroblast growth factor-23, FGF-23)在体内堆积,FGF-23是XLH发生过程中的关键因子。
FGF-23主要由成骨细胞及骨细胞分泌,在体内磷稳态维持及维生素D调节方面发挥十分重要的作用。其活性形式为全段FGF-23(intact FGF-23, iFGF-23),被降解为N端和C端片段后则失去活性。iFGF-23主要经由肾脏发挥作用,通过抑制肾近端小管钠-磷共转运体蛋白(NaPi-2a和NaPi-2c)表达,直接抑制肾脏磷的重吸收,导致经肾脏磷丢失增多;另一方面,iFGF-23可以通过抑制1α羟化酶同时促进24羟化酶作用,抑制活性维生素D 1, 25(OH)2D3的生成,进而抑制肠道对磷的吸收[4]。综上,iFGF-23通过促进肾脏磷排出及抑制肠道磷吸收,共同发挥下调血磷的作用。因此,除低磷血症外,XLH患者另一显著特征为血iFGF-23水平升高。因此,iFGF-23因子水平与XLH疾病的严重程度是否存在一定相关性,成为值得关注的问题。
据国外文献报道,XLH患者血iFGF-23水平通常为正常人群的3~5倍[5-6],亦有研究初步探讨了XLH患者iFGF-23水平与PHEX基因突变类型或疾病严重程度的相关性[7],但样本量均较小。既往文献报道,不同PHEX基因突变类型(截短或非截短突变)或不同突变位置(N端或C端突变)可能对PHEX蛋白功能的影响程度不同[8-9]。然而,尚未有研究探索XLH患者PHEX基因不同突变类型或突变位点对其iFGF-23水平的影响,是否可能引起iFGF-23水平差异。本研究首次提出假设,PHEX基因突变位点如果位于其重要功能域(锌离子结合区),对蛋白功能及iFGF-23表达水平的影响可能会更显著。
由于XLH疾病的罕见性,现有关于XLH患者iFGF-23水平特征的研究样本量有限,仍缺少大样本量研究进一步描述XLH患者群体iFGF-23水平升高的特点,以及iFGF-23水平与疾病严重程度的相关分析。且目前关于XLH的研究多源于欧美人群及少数日本患者人群,对于中国XLH患者iFGF-23水平的研究十分有限,其中大多仅为个例研究。本研究中心在中国最早开展XLH遗传及临床研究,于2007年最早报告了中国3个XLH家系[10],并在19例较小样本低血磷性佝偻病/骨软化症患者中进行了iFGF-23水平的测定及初步分析[11]。
本研究纳入233例已明确PHEX基因突变的XLH患者,收集患者血清进行iFGF-23水平测定,分析了iFGF-23水平升高特点、不同PHEX基因突变类型或突变位置的XLH患者血iFGF-23水平差异,以及iFGF-23水平与疾病严重程度(包括起病年龄、身高、血磷水平及佝偻病严重程度)的相关性。
对象与方法研究对象
收集2005至2017年就诊于北京协和医院内分泌科的XLH患者中已明确PHEX基因突变者,最终共233例XLH患者纳入本研究。本研究获北京协和医院伦理委员会批准。所有成年患者均已签署知情同意书,未成年患者均由父母代为签署知情同意书。
临床资料及实验室检查
回顾性收集患者相关临床资料,包括起病年龄、身高、血磷等反映患者疾病严重程度的指标及X线影像学资料。为排除治疗对患者生化指标及疾病严重程度评估可能带来的影响,以及为更好地描述疾病自然状态,仅纳入未接受中性磷治疗患者的临床资料。
生化指标血磷(Pi)测定采用全自动生化分析仪(Beckman Coulter, 美国)。因不同年龄段患者血磷的正常参考范围存在差异[12],为方便对不同年龄段患者进行比较,本研究采用“血磷/正常上限比”这一指标,其计算方法为将每一位患者实际血磷测量值除以该患者所在年龄组正常血磷上限值,从而得到该比值。同样,为方便比较,所有患者身高测量值均依照中国0~18岁儿童青少年身高体重标准化曲线转换为SD值[13]。
影像学方面,收集了47例骨骺尚未闭合的XLH患儿双侧腕关节及膝关节X线正位片,根据Thacher等[14]提出的佝偻病严重程度评分(rickets severity score, RSS)方法对患儿佝偻病严重程度进行评估。该方法为0~10分的量化评估体系,0分代表正常,10分代表佝偻病骨骼病变最为严重。
血清iFGF-23测定
233例XLH患者血清样本均于第一次于北京协和医院就诊时采集,所有血清样本均于-80 ℃冻存备用。采用双抗夹心酶联免疫吸附法(Elisa)进行iFGF-23测定,试剂盒购于Kainos公司(日本)。该试剂盒iFGF-23测定范围为3~800 ng/L。iFGF-23正常参考范围参照于本实验室进行的8例正常青年志愿者的空腹iFGF-23水平测定(16.1~42.2 ng/L)[15]。
测定步骤:准备试剂及标准品,所有待测患者血清,提前1晚置于4 ℃冰箱解冻;取50 μL缓冲液加入每个微孔中;取50 μL FGF-23标准品稀释液或待测血清分别加入相应微孔,覆铝膜以避光,置于摇床上室温孵育2 h;移去覆膜,洗板4次,每次每孔加入300 μL洗液,最后完全移除洗液;每微孔中加入100 μL HRP标记的FGF-23抗体,覆膜,室温摇床孵育1 h;移去覆膜,洗板4次,最后完全移除洗液;取100 μL底物加入每孔,覆膜,置于铝箔避光室温孵育30 min;移除铝箔和覆膜,每孔立即加入100 μL反应终止液,覆膜轻摇1 min;10 min内使用酶标仪吸光度波长450 nm读取数值,计算各孔iFGF-23浓度。
XLH患者iFGF-23水平与PHEX基因突变分析
本研究纳入的所有XLH患者均已行PHEX基因突变检测,明确PHEX基因突变位点。
首先,为探究PHEX基因突变类型对iFGF-23水平的影响,将XLH患者分为PHEX基因截短突变(无义突变、造成移码的插入/缺失突变、剪切位点突变)或非截短突变(错义突变及非移码插入/缺失突变)组,分析各组患者iFGF-23水平表达的差异。
其次,对于PHEX突变位置对蛋白功能和iFGF-23水平的影响,由于无义突变、插入或缺失突变均会导致蛋白截短和大片段的缺失。为了更好地分析不同位置局部突变对于整体蛋白功能造成的影响,本研究仅选取导致单氨基酸改变的错义突变进行分析。以PHEX蛋白中位氨基酸(第375位异亮氨酸)为界,将XLH患者分为PHEX错义突变发生于PHEX蛋白N端(氨基酸1~375)或C端(氨基酸376~749)组,以及按照突变是否位于PHEX重要的功能域(17和19外显子的锌离子结合区)组,分析各组患者iFGF-23水平表达的差异。
XLH患者iFGF-23水平与疾病严重程度相关性分析
分析XLH患者疾病严重程度是否与iFGF-23水平相关。反映XLH患者疾病严重程度的主要指标包括起病年龄、身高(SD值)、血磷正常上限比以及RSS。分析以上指标与iFGF-23的相关性。
统计学方法
采用SPSS 19.0软件进行统计学分析。正态分布计量资料采用均数±标准差(x±s)表示,非正态分布计量数据采用中位数(四分位数间距)表示。正态分布数据两组间比较采用独立样本t检验,非正态分布数据采用秩和检验。简单相关分析采用Spearman相关。以P<0.05为差异有统计学意义。
结果一般资料
本研究纳入的233例XLH患者,其中男性患者73例,女性患者160例; 年龄中位数10.5(0.58~58.00)岁。233例患者中,97.9%患者(228例)表现为显著低磷血症,血磷水平低于该年龄组血磷水平参考范围,余5例患者血磷水平位于正常范围低限。
233例XLH患者共检测出147种PHEX基因突变,包括错义突变(21种)、无义突变(33种)、插入突变(20种)、缺失突变(30种)、剪切位点突变(22种)及大片段插入/缺失突变(cnv, 21种)等。
XLH患者iFGF-23水平特征
本研究233例XLH患者血清iFGF-23中位数为101.9 (71.37, 143.81)ng/L,普遍升高,约为正常人群的2.5~5.0倍(XLH患者iFGF-23水平除以正常人群参考均值),但个体差异较大(范围6.46~542.57 ng/L)。91.9%患者iFGF-23水平高于正常参考范围上限(42.2 ng/L)。
73例男性患者iFGF-23中位数为109.05 (74.16, 148.52)ng/L,160例女性iFGF-23中位数97.29(69.53, 140.23)ng/L, XLH患者iFGF-23水平性别差异无统计学意义(P=0.668)(图 1)。此外,XLH患者iFGF-23水平与患者年龄亦无显著相关性(r=-0.082,P=0.254)(图 2)。

|
| 图 1 XLH患者iFGF-23水平性别差异分析 Figure 1 Gender difference of iFGF-23 levels in XLH patients 虚线及阴影:iFGF-23正常参考范围(16.1~42.2 ng/L); iFGF-23:全段成纤维细胞生长因子23 |

|
| 图 2 XLH患者iFGF-23水平与年龄的相关性 Figure 2 Correlation of iFGF-23 levels and age in XLH patients 虚线及阴影:iFGF-23正常参考范围(16.1~42.2 ng/L); iFGF-23:全段成纤维细胞生长因子23 |
PHEX基因突变类型/突变位置对iFGF-23水平的影响
比较不同PHEX基因突变类型(截短/非截短突变)或不同错义突变位置(N端/C端突变, 锌离子结合域/非锌离子结合域突变)XLH患者血iFGF-23水平,组间比较差异均无统计学意义(P>0.05)(表 1)。表明XLH患者血清iFGF-23水平并不受PHEX基因突变类型或突变位置的影响。
| PHEX基因突变类型/位置 | n | iFGF-23(ng/L) | P |
| 截短突变 | 184 | 102.41(74.55, 140.23) | 0.777 |
| 非截短突变 | 49 | 96.18(63.33, 171.26) | |
| 错义突变(N端,氨基酸1~375) | 12 | 114.00±84.10 | 0.635 |
| 错义突变(C端,氨基酸376~749) | 34 | 96.65(69.71, 175.21) | |
| 错义突变(锌离子结合域*) | 10 | 105.82±45.75 | 0.522 |
| 错义突变(非锌离子结合域) | 36 | 122.13±75.79 | |
| iFGF-23:全段成纤维细胞生长因子23; XLH:X-连锁显性低血磷性佝偻病/骨软化症; *锌离子结合域:位于PHEX基因17和19外显子 | |||
iFGF-23水平与XLH患者疾病严重程度的相关性
XLH患者起病年龄中位数为1.25(1, 2)岁,平均身高SD值为-2.7±1.6,显著低于正常人。对骨骺尚未闭合的未成年患者,通过对其双侧腕关节及膝关节X线平片分析,RSS评分中位数为6(5, 7)分,绝大多数XLH患儿均有显著佝偻病骨骼表现。
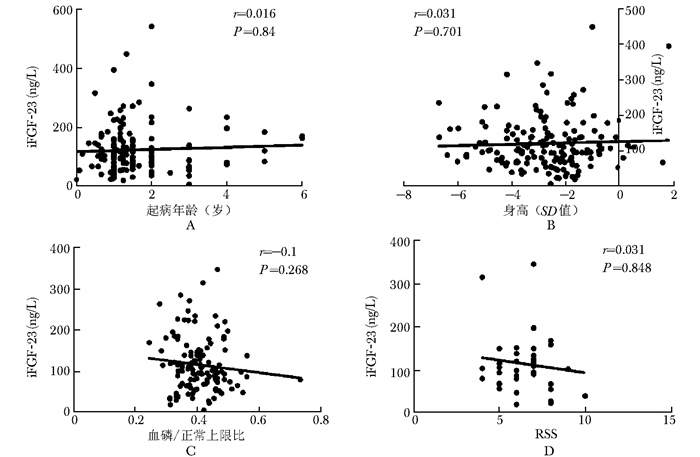
Spearman相关分析结果显示,XLH患者iFGF-23水平与患者起病年龄(n=157)、身高(SD值)(n=153)、血磷/正常上限比(n=125)及患儿佝偻病RSS(n=41)均无显著相关性(图 3)。
|
| 图 3 XLH患者血iFGF-23水平与患者表型严重程度相关性分析 Figure 3 Correlation between iFGF-23 levels and severity of XLH A:患者起病年龄与iFGF-23水平无显著相关性;B:身高(SD值)与iFGF-23水平无显著相关性;C:血磷/正常上限比与iFGF-23水平无显著相关性;D:RSS(佝偻病评分)与iFGF-23水平无显著相关性 |
XLH疾病的发生是由于PHEX基因失活突变引起iFGF-23水平升高,进而导致磷过量丢失所致。虽然PHEX功能缺失导致iFGF-23升高的机制目前尚不明确,但是iFGF-23在XLH疾病发生过程中的关键作用已明确。国外研究已经证实,除低磷血症外,iFGF-23可作为明确XLH诊断的另一重要临床指标[7]。由于XLH发病非常罕见,此前国外关于XLH患者iFGF-23水平的研究样本量均有限,且国内该方面研究鲜见报道。
本研究作为目前国内外最大样本量XLH病例研究(233例),使用Elisa方法在大样本中国XLH患者群体中明确了患者iFGF-23水平显著升高,约为正常人群的2.5~5.0倍,但是存在较大个体差异(6.46~542.57 ng/L)。该发现与国外研究结果一致,XLH患者iFGF-23水平升高约为正常人群的3~5倍[5, 16],且个体异质性大[7]。值得注意的是,本研究发现并非所有XLH患者iFGF-23水平都显著高于正常人群,仍有约8.1%患者iFGF-23水平在正常参考范围内。由于本研究样本量群体较大,可排除测定偶然性可能;本研究建立的正常值参考范围亦与Yamazaki等[5]在104例大样本正常人群中建立的iFGF-23参考值(10~50 ng/L)十分接近,排除正常参考范围偏差。两项日本关于XLH患者iFGF-23水平的研究亦有类似的发现,XLH患者iFGF-23水平升高程度并不完全一致,大多数而非全部XLH患者iFGF-23水平高于正常范围,XLH患者与正常人群iFGF-23水平存在部分重叠[7, 17]。分析可能的原因:(1)iFGF-23水平存在一定个体差异,不仅在正常人群,在XLH患者群体中更为显著,不同个体对于iFGF-23的敏感及耐受程度可能存在较大差异;(2)iFGF-23受血磷水平调节,低磷状态下iFGF-23水平应下调,而XLH患者在低磷状态下iFGF-23仍在正常范围可以被认为是“不恰当的正常”;(3)iFGF-23水平可能受多项因素的共同调控,诸如甲状旁腺素、循环中α-Klotho、血清铁及部分炎性因子的影响(如肿瘤坏死因子及白介素1β)[18];(4)在部分血标本的长期存贮过程中,可能存在少量iFGF-23降解现象。
由于XLH为X连锁显性遗传疾病,男性为半合子,因此是否存在剂量效应而导致XLH患者iFGF-23水平存在性别差异,本研究对该问题进行了进一步探究,结果证实XLH患者iFGF-23水平并无性别差异,且与患者年龄无明显相关性。本研究结果与Yamazaki等[5]和Carpenter等[16]分别在日本及美国较小XLH患者群体iFGF-23的研究发现一致。
本研究探究了XLH患者iFGF-23水平与其致病基因PHEX突变类型及突变位点的相关性,研究结果证实了XLH患者iFGF-23水平在PHEX截短/非截短突变、N端/C端突变、PHEX重要功能域(锌离子结合区)/非重要功能域突变患者间差异均无统计学意义。说明PHEX基因功能的正常行使需要其蛋白的完整性,不论突变导致蛋白的大片段缺失截短,还是单个氨基酸替换均会引起疾病的发生,且对iFGF-23升高程度的影响无显著差异。
本研究的另一重要发现为在此大样本XLH群体中分析了iFGF-23水平与患者疾病严重程度的相关性,包括起病年龄、血磷/正常上限比、身高(SD值)及儿童RSS评分。结果发现,XLH患者血清iFGF-23水平与以上反映疾病严重程度的指标均无明显相关性。与2011年Igaki等[7]对3个XLH家系(共6例患者)的研究结果一致,该研究发现iFGF-23水平和XLH疾病严重程度(起病年龄、骨骼畸形、血磷水平、血碱性磷酸酶水平等)均无显著相关性,但由于样本量小,仅纳入了3个家系共6例患者,存在明显局限性。iFGF-23是XLH疾病发生过程中最为关键的因子,然而本研究及以往研究均证实,XLH患者的iFGF-23水平与患者疾病严重程度并无直接明确的相关性。考虑可能与讨论中提及的iFGF-23的个体异质性较大及多因素共同复杂调控机制相关;且除FGF-23外,在XLH疾病发生过程中可能还有其他因子,如细胞外基质磷酸化糖蛋白(matrix extracellular phosphoglycoprotein,MEPE)、分泌型卷曲相关蛋白4(secreted frizzled-related protein-4,sFRP-4)等对疾病的发生发展具有一定调控作用[7]。
本研究是目前国内外样本量最大的XLH患者群体研究,全部233例患者均已明确致病PHEX基因突变,并进行了iFGF-23水平测定,分析了iFGF-23与患者PHEX基因突变类型/位置及疾病表型严重程度的相关性。本研究弥补了XLH患者iFGF-23水平研究小样本量的缺陷,填补了XLH患者不同PHEX基因突变类型及突变位置对iFGF-23水平影响研究的空白,明确了中国XLH人群患者iFGF-23水平的特征。
综上,中国XLH患者人群血清iFGF-23水平较正常人群显著升高,个体差异较大,与国外研究结果一致。且iFGF-23水平与患者年龄、PHEX基因突变类型或位置、患者疾病严重程度并无显著相关性。iFGF-23可以作为明确诊断XLH疾病的一项重要指标,然而其升高程度并不能预测及代表患者疾病严重程度。
| [1] | Beck-Nielsen SS, Brock-Jacobsen B, Gram J, et al. Incidence and prevalence of nutritional and hereditary rickets in southern Denmark[J]. Eur J Endocrinol, 2009, 160: 491–497. DOI:10.1530/EJE-08-0818 |
| [2] | Francis F, Hennig S, Korn B, et al. A gene (PEX) with homologies to endopeptidases is mutated in patients with X-linked hypophosphatemic rickets[J]. Nature Genetics, 1995, 11: 130–136. DOI:10.1038/ng1095-130 |
| [3] | Rowe PS, Oudet CL, Francis F, et al. Distribution of mutations in the PEX gene in families with X-linked hypophosphataemic rickets (HYP)[J]. Hum Mol Genet, 1997, 6: 539–549. DOI:10.1093/hmg/6.4.539 |
| [4] | Shimada T, Hasegawa H, Yamazaki Y, et al. FGF-23 is a potent regulator of vitamin D metabolism and phosphate homeostasis[J]. J Bone Miner Res, 2004, 19: 429–435. |
| [5] | Yamazaki Y Okazaki R, Shibata M, et al. Increased circulatory level of biologically active full-length FGF-23 in patients with hypophosphatemic rickets/osteomalacia[J]. J Clin Endocrinol Metab, 2002, 87: 4957–4960. DOI:10.1210/jc.2002-021105 |
| [6] | Pavone V, Testa G, Gioitta IS, et al. Hypophosphatemic rickets: etiology, clinical features and treatment[J]. Eur J Orthop Surg Traumatol, 2015, 25: 221–226. DOI:10.1007/s00590-014-1496-y |
| [7] | Igaki JM, Yamada M, Yamazaki Y, et al. High iFGF23 level despite hypophosphatemia is one of the clinical indicators to make diagnosis of XLH[J]. Endocr J, 2011, 58: 647–655. DOI:10.1507/endocrj.K10E-257 |
| [8] | Holm IA, Nelson AE, Robinson BG, et al. Mutational analysis and genotype-phenotype correlation of the PHEX gene in X-linked hypophosphatemic rickets[J]. J Clin Endocrinol Metab, 2001, 86: 3889–3899. DOI:10.1210/jcem.86.8.7761 |
| [9] | Song HR, Park JW, Cho DY, et al. PHEX gene mutations and genotype-phenotype analysis of Korean patients with hypophosphatemic rickets[J]. J Korean Med Sci, 2007, 22: 981–986. DOI:10.3346/jkms.2007.22.6.981 |
| [10] | Xia W, Meng X, Jiang Y, et al. Three novel mutations of the PHEX gene in three Chinese families with X-linked dominant hypophosphatemic rickets[J]. Calcif Tissue Int, 2007, 81: 415–420. DOI:10.1007/s00223-007-9067-4 |
| [11] | Xia WB, Jiang Y, Li M, et al. Levels and dynamic changes of serum fibroblast growth factor 23 in hypophosphatemic rickets/osteomalacia[J]. Chin Med J (Engl), 2010, 123: 1158–1162. |
| [12] | Mary DR.2012 X-linked hypophosphatemia[M]. Seattle(WA): University of Washington, 2017. |
| [13] | Li H, Ji CY, Zong XN, et al. Height and weight standardized growth charts for Chinese children and adolescents aged 0 to 18 years[J]. Zhonghua Er Ke Za Zhi, 2009, 47: 487–892. |
| [14] | Thacher TD, Fischer PR, Pettifor JM, et al. Radiographic scoring method for the assessment of the severity of nutritional rickets[J]. J Trop Pediatr, 2000, 46: 132–139. DOI:10.1093/tropej/46.3.132 |
| [15] | Chi Y, Zhao Z, He X, et al. A compound heterozy-gous mutation in SLC34A3 causes hereditary hypophosphatemic rickets with hypercalciuria in a Chinese patient[J]. Bone, 2014, 59: 114–121. DOI:10.1016/j.bone.2013.11.008 |
| [16] | Carpenter TO, Insogna KL, Zhang JH, et al. Circulating levels of soluble klotho and FGF23 in X-linked hypophosphatemia: circadian variance, effects of treatment, and relationship to parathyroid status[J]. J Clin Endocrinol Metab, 2010, 95: E352–E357. DOI:10.1210/jc.2010-0589 |
| [17] | Ito N, Fukumoto S, Takeuchi Y, et al. Comparison of two assays for fibroblast growth factor (FGF)-23[J]. J Bone Miner Metab, 2005, 23: 435–440. DOI:10.1007/s00774-005-0625-4 |
| [18] | Courbebaisse M, Lanske B. Biology of fibroblast growth factor 23: from physiology to pathology[J]. Cold Spring Harb Perspect Med, 2018, 8: pii. |
| (收稿日期:2018-12-15) |

